что такое кожные реакции ссд и тэн
Синдром Стивенса–Джонсона
Синдром Стивенса–Джонсона относится к тяжелым системным аллергическим реакциям замедленного типа (иммунокомплексным) и представляет собой тяжелый вариант течения многоформной эритемы ( рис. 1 ), при которой наряду с поражением кожи отмечается поражение
Синдром Стивенса–Джонсона относится к тяжелым системным аллергическим реакциям замедленного типа (иммунокомплексным) и представляет собой тяжелый вариант течения многоформной эритемы (рис. 1), при которой наряду с поражением кожи отмечается поражение слизистых оболочек как минимум двух органов [1].
Причины развития синдрома Стивенса–Джонсона подразделяют на четыре категории [2].
Клиническая картина
Синдром Стивенса–Джонсона чаще возникает в возрасте 20–40 лет, однако описаны случаи его развития и у трехмесячных детей. Мужчины заболевают в 2 раза чаще женщин. Как правило (в 85% случаев), заболевание начинается с проявлений инфекции верхних дыхательных путей. Продромальный гриппоподобный период длится от 1 до 14 дней и характеризуется лихорадкой, общей слабостью, кашлем, болью в горле, головной болью, артралгией. Иногда отмечается рвота и диарея. Поражение кожи и слизистых развивается стремительно, обычно через 4–6 дней, может локализоваться где угодно, но более характерны симметричные высыпания на разгибательных поверхностях предплечий, голеней, тыла кистей и стоп, лице, половых органах, на слизистых оболочках. Появляются отечные, четко отграниченные, уплощенные папулы розово-красного цвета округлой формы, диаметром от нескольких миллиметров до 2–5 см, имеющие две зоны: внутреннюю (серовато-синюшного цвета, иногда с пузырем в центре, наполненным серозным или геморрагическим содержимым) и наружную (красного цвета). На губах, щеках, небе возникают разлитая эритема, пузыри, эрозивные участки, покрытые желтовато-серым налетом. После вскрытия крупных пузырей на коже и слизистых оболочках образуются сплошные кровоточащие болезненные очаги, при этом губы и десны становятся опухшими, болезненными, с геморрагическими корками (рис. 2, 3). Высыпания сопровождаются жжением и зудом. Эрозивное поражение слизистых оболочек мочеполовой системы может осложняться стриктурами уретры у мужчин, кровотечениями из мочевого пузыря и вульвовагинитами у женщин. При поражении глаз наблюдаются блефароконъюнктивит, иридоциклит, которые могут привести к потере зрения. Редко развиваются бронхиолиты, колиты, проктиты. Из общих симптомов характерны лихорадка, головная боль и боль в суставах [5].
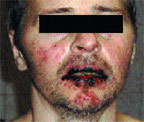 |
| Рисунок 2. Поражение губ и слизистых ротовой полости при синдроме Стивенса–Джонсона у больного 42 лет |
К прогностически неблагоприятным факторам при синдроме Стивенса–Джонсона и синдроме Лайелла относятся: возраст старше 40 лет, быстро прогрессирующее течение, тахикардия с частотой сердечных сокращений (ЧСС) более 120 уд./мин, начальная площадь эпидермального поражения более 10%, гипергликемия более 14 ммоль/л [6].
Летальность при синдроме Стивенса-Джонсона составляет 3–15%. При поражении слизистых оболочек внутренних органов могут формироваться стеноз пищевода, сужение мочевыводящих путей. Слепота вследствие вторичного тяжелого кератита регистрируется у 3–10% больных.
Дифференциальную диагностику следует проводить между многоформной эритемой, синдромом Стивенса–Джонсона и синдромом Лайелла (табл. 1). Следует помнить, что похожие поражения кожи могут встречаться при первичных системных васкулитах (геморрагический васкулит, узелковый полиартериит, микроскопический полиартериит и др.).
Диагностика
При сборе анамнеза больному необходимо задать следующие вопросы:
Обязательна запись о наличии лекарственной аллергии в медицинской документации.
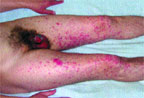 |
| Рисунок 3. Симметричные поражения кистей, нижних конечностей и слизистых половых органов у того же больного |
При начальном осмотре обращают внимание на наличие изменений кожных покровов и видимых слизистых, отмечают характер высыпаний, локализацию, указывают процент поражения кожи, наличие пузырей, эпидермального некроза; стридора, диспноэ, свистящего дыхания, одышки или апноэ; гипотензии или резкого снижения обычного артериального давления (АД); гастроинтестинальных симптомов (тошнота, боль в животе, диарея); болезненность при глотании, мочеиспускании; изменение сознания.
Объективное обследование включает измерение ЧСС, АД, температуры тела, пальпаторное исследование лимфатических узлов и брюшной полости.
С целью верификации кожных высыпаний и поражения слизистых показана консультация дерматолога. При наличии признаков поражения других органов и систем целесообразна консультация других узких специалистов (отоларинголога, окулиста, уролога и др.).
Неотложная помощь на догоспитальном этапе
При развитии синдрома Стивенса–Джонсона основное направление неотложной терапии — это восполнение потери жидкости, как у ожоговых больных (даже при стабильном состоянии пациента на момент осмотра). Проводится катетеризация периферической вены и начинается переливание жидкостей (коллоидные и солевые растворы 1–2 л), по возможности — пероральная регидратация.
Применяют внутривенное струйное введение глюкокортикостероидов (в перерасчете на преднизолон внутривенно 60–150 мг). Однако эффективность назначения системных гормонов вызывает сомнения. Целесообразным считается применение пульс-терапии в высоких дозах в ранние сроки с момента начала острой токсико-аллергической реакции, потому что плановое их назначение увеличивает риск септических осложнений и может привести к росту числа летальных исходов [5].
Должна быть готовность к искусственной вентиляции легких (ИВЛ), трахеотомии при развитии асфиксии и немедленная госпитализация в реанимационное отделение [9].
Принципы терапии в стационаре
Основные мероприятия направлены на коррекцию гиповолемии, проведение неспецифической дезинтоксикации, предотвращение развития осложнений, в первую очередь инфекций, а также исключение повторного воздействия аллергена.
Необходимо отменить все лекарственные препараты, за исключением тех, которые необходимы пациенту по жизненным показаниям.
В качестве гипоаллергенной назначается общая неспецифическая гипоаллергенная диета по А. Д. Адо. Она предполагает исключение из рациона следующих продуктов: цитрусовые (апельсины, мандарины, лимоны, грейпфруты и др.); орехи (арахис, фундук, миндаль и др.); рыба и рыбные продукты (свежая и соленая рыба, рыбные бульоны, консервы из рыб, икра и др.); мясо птицы (гусь, утка, индейка, курица и др.) и изделия из него; шоколад и шоколадные изделия; кофе; копченые изделия; уксус, горчица, майонез и прочие специи; хрен, редис, редька; томаты, баклажаны; грибы; яйца; молоко пресное; клубника, дыня, ананас; сдобное тесто; мед; алкогольные напитки.
– на вторичном говяжьем бульоне;
– вегетарианские с добавлением масла сливочного, оливкового, подсолнечного;
Пищевой рацион включает около 2800 ккал (15 г белков, 200 г углеводов, 150 г жиров).
– использование низких доз глюкокортикостероидов в начале заболевания и длительная глюкокортикостероидная терапия после стабилизации состояния больного;
– профилактическое назначение антибактериальных препаратов при отсутствии инфекционных осложнений.
Еще раз подчеркнем, что категорически противопоказаны препараты пенициллинового ряда и противопоказано назначение витаминов (группы В, аскорбиновой кислоты и др.), так как они являются сильными аллергенами.
Применение препаратов кальция (глюконат кальция, хлористый кальций) патогенетически необоснованно и может непредсказуемо повлиять на дальнейшее течение заболевания.
Дальнейшие рекомендации
Пациенту постоянно напоминают, что принимать лекарственные средства следует только по назначению врача. Больному выдают памятку по непереносимости лекарственных средств, направляют на консультацию к аллергологу или клиническому иммунологу, рекомендуют обучение в аллергошколе. Пациента обучают правильному применению средств неотложной помощи, технике инъекции на случай повторного контакта с аллергеном и возникновения тяжелых острых токсико-аллергических реакций (анафилактического шока). В домашней аптечке следует иметь адреналин, глюкокортикостероиды (преднизолон) для парентерального введения, шприцы, иглы и антигистаминные препараты.
Профилактика развития лекарственной аллергии включает соблюдение следующих правил.
Таким образом, синдром Стивенса–Джонсона является серьезным заболеванием, требующим ранней диагностики, госпитализации больного, тщательного ухода и наблюдения, рациональной медикаментозной терапии.
Литература
А. Л. Верткин, доктор медицинских наук, профессор
А. В. Дадыкина, кандидат медицинских наук
ННПОС МП, МГМСУ, ЦПК и ППС НижГМА, Москва, Нижний Новгород
Синдром Стивенса — Джонсона — иммунная катастрофа
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Синдром Стивенса — Джонсона (ССД) и токсический эпидермальный некролиз (ТЭН) относятся к редким острым жизнеугрожающим заболеваниям кожи и слизистых, индуцированным у детей преимущественно инфекциями и/или лекарственными средствами (ЛС). Согласно современной концепции ССД представляет «малую форму» ТЭН, когда общая площадь отслойки эпидермиса занимает не более 10%, однако при этом у пациента могут быть и глубокие поражения слизистых оболочек (как минимум двух органов): гортани, трахеи, бронхов, желудочно-кишечного тракта, мочевого пузыря или уретры. Собственно ТЭН сопровождается массивным эпидермолизом на площади более 30% поверхности тела. Полипрагмазия затрудняет распознавание индуктора заболевания, тяжесть синдрома зависит от скорости его отмены и элиминации. Болезнь редко встречается в практике педиатра. Верификация диагноза базируется преимущественно на клинической картине. Дебют ССД похож на ОРЗ и «сыпные» инфекции. Поздняя диагностика ухудшает прогноз. Алгоритмы лечения не унифицированы, требуется индивидуальный подбор лечебных схем. Представленный клинический случай подтверждает необходимость своевременной диагностики и ранней терапии.
Ключевые слова: синдром Стивенса — Джонсона, дети, триггер, маска, дебют, клиника, алгоритм лечения.
Stevens-Johnson syndrome (SJS) and toxic epidermal necrolysis (TEN) are rare acute life-threatening skin and mucosal disorders provoked in children mainly by infections and/or medications. According to the modern concept, SJS is a minor variant of TEN characterized by a total area of epidermal detachment less than 10% of the body surface area. However, a patient may present with deep mucosal lesions of at least two organs, e.g., larynx, trachea, bronchi, gastrointestinal tract, bladder or urethra. TEN is characterized by massive epidermolysis which involves more than 30% of the body surface area. Polypragmasia make difficulties for trigger identification while the severity depends on trigger withdrawal and elimination. This disorder is uncommon in paediatrics. Diagnosis is verified mainly by clinical manifestations. SJS debut is similar to acute respiratory infections and rash infections. Late diagnosis is associated with poor outcomes. There are no uniform treatment algorithms, individual treatment choice is required. Clinical case demonstrates that early diagnosis and treatment are vital.
Key words: Stevens-Johnson syndrome, toxic epidermal necrolysis, epidermolysis, life-threatening condition, apoptosis, children, trigger, mask, treatment algorithm.
For citation: Bardenikova S.I., Pentkovskaya O.S., Isaeva E.K. Stevens-Johnson syndrome is an immune catastrophe. Russian Journal of Woman and Child Health. 2019;2(1):66–72.
Представлен клинический случай синдрома Стивенса — Джонсона, относящегося к редким острым жизнеугрожающим заболеваниям кожи и слизистых, индуцированным у детей преимущественно инфекциями и/или лекарственными средствами. Представленный случай подтверждает необходимость своевременной диагностики и ранней терапии.
Актуальность
Патогенез апоптоза кератиноцитов
Триггерные факторы ССД
Клиническая картина ССД и ТЭН
Диагностика
Клиническая картина
Обсуждение
Заключение
Синдром Стивенса–Джонсона (ССД) и токсический эпидермальный некролиз (ТЭН)
, MD, University of Miami Miller School of Medicine
Синдром Стивена-Джонса и токсический эпидермальный некролиз клинически сходны, за исключением распространенности высыпаний. Согласно одному широко используемому определению, поражение 10% площади поверхности тела наблюдается при CДС и > 30% поверхности тела – при ТЭН; поражение от 15 до 30% поверхности тела рассматривается как перекрестный синдром CДC/ТЭН.
Это заболевание поражает от 1 до 5 чаловек на миллион населения. Частота развития, степень тяжести или оба эти показателя могут быть повышены у реципиентов трансплантата костного мозга, у инфицированных Pneumocystis jirovecii больных с ВИЧ-инфекцией, у пациентов с системной красной волчанкой и у больных с другими хроническими ревматологическими заболеваниями.
Этиология
Прием лекарственных препаратов обусловливает более 50% случаев CДC и до 95% случаев ТЭН. Чаще всего развитие заболевания обусловлено приемом следующих препаратов:
Препараты, содержащие сульфо-группу (например, котримоксазол, сульфасалазин)
Другие антибиотики (например, аминопенициллины [обычно ампициллин или амоксициллин], фторхинолоны, цефалоспорины)
Противоэпилептические препараты (например, фенитоин, карбамазепин, фенобарбитал, вальпроат, ламотриджин)
Различные другие препараты (например, пироксикам, аллопуринол, хлормезанон)
Случаи заболевания, не связанные с приемом лекарственных препаратов, рассматриваются как обусловленные:
Инфекционным процессом (главным образом при инфицировании Mycoplasma pneumoniae)
Реакцией ТПХ («трансплантат против хозяина»)
Изредка причину не могут выявить.
Патофизиология
Точный механизм развития синдрома Стивенса-Джонсона и токсического эпидермального некролиза неизвестен; однако, согласно одной из теорий считается, что измененный метаболизм лекарственного препарата (например, неспособность выводить реактивные метаболиты) у некоторых пациентов является триггером цитотоксической реакции в кератиноцитах на антигены лекарственных средств, опосредованной Т-клетами. CD8 + T-клетки были идентифицированы как важные медиаторы в образовании волдырей.
Недавно полученные данные указывают на то, что гранулизин, высвобождаемый цитотоксическими Т-клетками и натуральными киллерными клетками, может играть роль в гибели кератиноцитов; концентрация гранулизина в жидкости волдыря коррелирует с тяжестью заболевания. Другая теория состоит в том, что взаимодействие между Fas (рецептор на поверхности клеток, участвующий в апоптозе) и его лигандами, в частности растворимой формой Fas-лиганда, высвобождаемой мононуклеарными клетками, ведет к гибели клеток и формированию волдырей. Предполагается возможность наличия генетической предрасположенности к СШД/TЭН.
Клинические проявления
В течение 1–3 недель после начала приема препарата, вызывающего заболевание, у больных начинается продромальный период в виде недомогания, лихорадки, головной боли, кашля и кератоконъюнктивита. Затем внезапно на коже лица, шеи и верхней части туловища появляются пятна, часто мишеневидные. Эти пятна одновременно появляются на разных участках тела, сливаются с образованием крупных плоских пузырей, покрышка которых отторгается в течение 1–3 дней. Ногти и брови могут отторгаться вместе с эпителием. Могут быть вовлечены ладони и ступни. Характерны болезненность кожи, слизистых оболочек и глаз. В некоторых случаях диффузная эритема является первым патологическим состоянием кожи при токсическом эпидермальном некролизе.
При тяжелом токсическом эпидермальном некролизе крупные пласты эпителия отслаиваются со всей поверхности тела в местах давления (симптом Никольского), обнажая влажные болезненные участки кожи красного цвета. У почти 90% больных, помимо отслаивающегося эпидермиса отмечаются болезненные корки и эрозии в ротовой полости, кератоконъюнктивит и высыпания на гениталиях (например, уретрит, фимоз, синехии влагалища). Эпителий бронхов может также отслаиваться, вызывая кашель, диспноэ, пневмонию, отек легких и гипоксию. Могут развиваться гломерулонефрит и гепатит.
Диагностика
Часто биопсия кожи
Диагноз часто очевиден по внешнему виду высыпаний и быстрому прогрессированию симптомов. При гистологическом исследовании отслоившейся кожи выявляется характерный признак – некротические изменения эпителия.
Синдромом токсического шока Синдром токсического шока (СТШ) Синдром токсического шока обусловлен экзотоксинами стафилококков или стрептококков. Симптомы включают высокую температуру, гипотонию, диффузную эритематозную сыпь и полиорганную недостаточность. Прочитайте дополнительные сведения 
Эксфолиативной эритродермией Эксфолиативный дерматит Эксфолиативный дерматит – это распространенная эритема и шелушение кожи, вызванные перенесенными заболеваниями кожи, приемом лекарственных препаратов, раком или неизвестными причинами. Симптомы. Прочитайте дополнительные сведения 
Паранеопластической пузырчаткой Вульгарная пузырчатка Вульгарная пузырчатка – это редко встречающееся потенциально смертельное аутоиммунное заболевание, характеризующееся образованием внутриэпидермальных пузырей и обширных эрозий на видимо непораженной. Прочитайте дополнительные сведения 
Прогноз
Тяжелый токсический эпидермальный некролиз сходен с обширными ожогами; пациенты остро больны, могут быть не способны открыть глаза или принять пищу и страдают от массивной потери жидкости и электролитов. Они подвержены высокому риску присоединения вторичной инфекции, развития мультиорганной недостаточности и смерти. При раннем начале терапии выживаемость достигает 90%. Шкала оценки степени тяжести токсического эпидермального некролиза ( Шкала оценки степени тяжести токсического эпидермального некролиза (SCORTEN) Шкала оценки степени тяжести токсического эпидермального некролиза (SCORTEN) Синдром Стивенса–Джонсона (СДС) и токсический эпидермальный некролиз (ТЭН) – это тяжелые кожные реакции гиперчувствительности. Наиболее частой причиной является прием лекарственных препаратов. Прочитайте дополнительные сведения 
Лечение
Возможно использование плазмафереза или внутривенного введения иммуноглобулинов (ВВИГ)
Медикаментозное лечение синдрома Стивенса-Джонсона и токсического эпидермального некролиза является спорным. Циклоспорин (3–5 мг/кг перорально 1 раз/день) подавляет CD8-клетки и продемонстрировал способность уменьшать длительность активной фазы заболевания на 2–3 дня при некоторых условиях и, возможно, снижает уровень смертности. Использование системных кортикостероидов является дискутабельным, поскольку, как полагают многие эксперты, они увеличивают смертность из-за повышения риска инфицирования и маскировки сепсиса. Тем не менее, недавние отчеты показали улучшение исхода со стороны зрения при ранней пульс-терапии кортикостероидами.
Замещение плазмы Терапевтический аферез Аферез – это процесс разделения клеточных и растворимых компонентов крови с помощью прибора. Аферез часто проводится на донорах, цельная кровь которых центрифугируется для получения отдельных. Прочитайте дополнительные сведения может удалить реактивные метаболиты или антитела и может рассматриваться как вариант лечения. Раннее лечение высокими дозами ВВИГ в дозе 2,7 г/кг в течение 3 дней блокирует антитела и Fas-лиганды. Тем не менее, несмотря на некоторые впечатляющие начальные результаты, полученные при использование высоких доз ВВИГ при ТЭН, дальнейшие клинические испытания с участием небольших когорт продемонстрировали противоречивые результаты, при этом ретроспективный анализ показал отсутствие улучшений и даже более высокую смертность, чем ожидалось (1 Справочные материалы по лечению Синдром Стивенса–Джонсона (СДС) и токсический эпидермальный некролиз (ТЭН) – это тяжелые кожные реакции гиперчувствительности. Наиболее частой причиной является прием лекарственных препаратов. Прочитайте дополнительные сведения 
Справочные материалы по лечению
Kirchhof MG, Miliszewski MA, Sikora S, et al: Retrospective review of Stevens-Johnson syndrome/toxic epidermal necrolysis treatment comparing intravenous immunoglobulin with cyclosporine. J Am Acad Dermatol 71(5):941-947, 2014. doi: 10.1016/j.jaad.2014.07.016.
Основные положения
Лекарственные средства вызывают > 50% случаев СДС и до 95% случаев ТЭН, однако инфекция, вакцинация и реакция «трансплантат против хозяина» также являются потенциальными причинами.
Подтверждают диагноз с помощью биопсии (обнаружение некротического эпителия), если клинические характеристики (например, кольцевидные поражения прогрессируют в буллы, вовлечение глаз и слизистых оболочек, положительный симптом Никольского, шелушение кожи) не являются убедительными.
Раннее лечение позволяет снизить высокий уровень смертности, о котором часто сообщают в литературе.
За исключением легких случаев лечение СДC/ТЭН проводится в ожоговом отделении и отделении интенсивной терапии.
Если поражены глаза, требуется консультация офтальмолога.
В тяжелых случаях рассматривают возможность использования циклоспорина и замещения плазмы.
Синдром Стивенса-Джонсона
Общая информация
Краткое описание
РОССИЙСКОЕ ОБЩЕСТВО ДЕРМАТОВЕНЕРОЛОГОВ И КОСМЕТОЛОГОВ
ФЕДЕРАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ВЕДЕНИЮ БОЛЬНЫХ СИНДРОМОМ СТИВЕНСА-ДЖОНСОНА / ТОКСИЧЕСКИМ ЭПИДЕРМАЛЬНЫМ НЕКРОЛИЗОМ
Шифр по Международной классификации болезней МКБ-10
Синдром Стивенса-Джонсона – L51.1
Токсический эпидермальный некролиз – L51.2
ОПРЕДЕЛЕНИЕ
Синдром Стивенса-Джонсона / токсический эпидермальный некролиз – эпидермолитические лекарственные реакции (ЭЛР) – острые тяжелые аллергические реакции, характеризующиеся обширными поражениями кожи и слизистых оболочек, индуцированные приемом лекарственных препаратов.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
В зависимости от площади пораженной кожи выделяют следующие формы ЭЛР:
— синдром Стивенса-Джонсона (ССД) – менее 10% поверхности тела;
— токсический эпидермальный некролиз (ТЭН, синдром Лайелла) – более 30% поверхности тела;
— промежуточная форма ССД/ТЭН (поражение 10–30% кожи).
Этиология и патогенез
Наиболее часто синдром Стивенса-Джонсона развивается при приеме лекарственных препаратов, однако в некоторых случаях причину заболевания выяснить не удается. Среди лекарственных препаратов, при приеме которых чаще развивается синдром Стивенса-Джонсона, выделяют: сульфаниламиды, аллопуринол, фенитонин, карбамазепин, фенибутазол, пироксикам, хлормазанон, пенициллины. Реже развитию синдрома способствует прием цефалоспоринов, фторхинолонов, ванкомицина, рифампицина, этамбутола, теноксикама, тиапрофеновой кислоты, диклофенака, сулиндака, ибупрофена, кетопрофена, напроксена, тиабендазола.
Заболеваемость ЭЛР оценивается как 1–6 случаев на миллион человек. ЭЛР могут возникать в любом возрасте, риск развития заболеваний возрастает у лиц в возрасте старше 40 лет, у ВИЧ-позитивных лиц (в 1000 раз), больных системной красной волчанкой и онкологическими заболеваниями. Чем старше возраст пациента, серьезнее сопутствующее заболевание и обширнее поражение кожи, тем хуже прогноз заболевания. Смертность от ЭЛР составляет 5–12%.
Для заболеваний характерен скрытый период между приемом препарата и развитием клинической картины (от 2 до 8 недель), необходимый для формирования иммунного ответа. Патогенез ЭЛР связан с массовой гибелью базальных кератиноцитов кожи и эпителия слизистых оболочек, вызванных Fas-индуцированным и перфорин/гранзим-опосредованным апоптозом клеток. Программируемая гибель клеток происходит в результате иммуноопосредованного воспаления, важную роль в развитии которого играют цитотоксические Т-клетки.
Клиническая картина
Cимптомы, течение
При синдроме Стивенса-Джонсона отмечается поражение слизистых оболочек как минимум двух органов, площадь поражения достигает не более 10% всего кожного покрова.
Синдром Стивенса-Джонсона развивается остро, поражение кожи и слизистых оболочек сопровождается тяжелыми общими расстройствами: высокой температурой тела (38. 40°С), головной болью, коматозным состоянием, диспепсическими явлениями и др. Высыпания локализуются преимущественно на коже лица и туловища. Клиническая картина характеризуется появлением множественных полиморфных высыпаний в виде багрово-красных пятен с синюшным оттенком, папул, пузырьков, мишеневидных очагов. Очень быстро (в течение нескольких часов) на этих местах формируются пузыри размером до ладони взрослого и больше; сливаясь, они могут достигать гигантских размеров. Покрышки пузырей сравнительно легко разрушаются (положительный симптом Никольского), образуя обширные ярко-красные эрозированные мокнущие поверхности, окаймленные обрывками покрышек пузырей («эпидермальный воротник»).
Иногда на коже ладоней и стоп появляются округлые темно-красные пятна с геморрагическим компонентом.
Наиболее тяжелое поражение наблюдается на слизистых оболочках полости рта, носа, половых органов, коже красной кайме губ и в перианальной области, где появляются пузыри, которые быстро вскрываются, обнажая обширные, резко болезненные эрозии, покрытые сероватым фибринозным налетом. На красной кайме губ часто образуются толстые буро-коричневые геморрагические корки. При поражении глаз наблюдается блефароконъюнктивит, возникает риск развития язвы роговицы и увеита. Пациенты отказываются от приема пищи, предъявляют жалобы на боль, жжение, повышенную чувствительность при глотании, парестезии, светобоязнь, болезненное мочеиспускание.
Диагностика
Диагноз синдрома Стивенса-Джонсона основывается на результатах анамнеза заболевания и характерной клинической картине.
При проведении клинического анализа крови выявляется анемия, лимфопения, эозинофилия (редко); нейтропения является неблагоприятным прогностическим признаком.
При необходимости проводят гистологическое исследование биоптата кожи. При гистологическом исследовании наблюдаются некроз всех слоев эпидермиса, образование щели над базальной мембраной, отслойка эпидермиса, в дерме воспалительная инфильтрация выражена незначительно или отсутствует.
Дифференциальный диагноз
Синдром Стивенса–Джонсона следует дифференцировать с вульгарной пузырчаткой, синдромом стафилококковой ошпаренной кожи, токсическим эпидермальным некролизом (синдромом Лайелла), для которого характерна отслойка эпидермиса более чем 30% поверхности тела; реакцией «трансплантат против хозяина», многоформной экссудативной эритемой, скарлатиной, термическим ожогом, фототоксической реакцией, эксфолиативной эритродермией, фиксированной токсидермией.
Лечение
— улучшение общего состояния пациента;
— регресс высыпаний;
— предупреждение развития системных осложнений и рецидивов заболевания.
Общие замечания по терапии
Лечение синдрома Стивенса-Джонсона проводит врач-дерматовенеролог, терапию более тяжелых форм ЭЛР осуществляют другие специалисты, врач-дерматовенеролог привлекается в качестве консультанта.
При выявлении эпидермолитической лекарственной реакции, врач, независимо от его специализации, обязан оказать больному неотложную медицинскую помощь и обеспечить его транспортировку в ожоговый центр (отделение) либо в реанимационное отделение.
Немедленная отмена приема препарата, спровоцировавшего развитие ЭЛР, увеличивает выживаемость при коротком периоде его полувыведения. В сомнительных случаях следует отменить прием всех препаратов, не являющихся жизненно необходимыми, и в особенности тех, прием которых был начат в течение последних 8 недель.
Необходимо учитывать неблагоприятные прогностические факторы течения ЭЛР:
1. Возраст > 40 лет – 1 балл.
2. ЧСС > 120 в мин. – 1 балл.
3. Поражение > 10% поверхности кожи – 1 балл.
4. Злокачественные новообразования (в т.ч. в анамнезе) – 1 балл.
5. В биохимическом анализе крови:
— уровень глюкозы > 14 ммоль/л – 1 балл;
— уровень мочевины > 10 ммоль/л – 1 балл;
— бикарбонаты 5 баллов (90%).
Показания к госпитализации
Установленный диагноз Синдрома Стивенса-Джонсона / токсического эпидермального некролиза.
Схемы лечения
Системная терапия
1. Глюкокортикостероидные препараты системного действия:
— преднизолон (В) 90–150 мг в сутки внутримышечно или внутривенно [1]
или
— дексаметазон (В) 12–20 мг в сутки внутримышечно или внутривенно [2].
2. Инфузионная терапия (допустимо чередование различных схем):
— калия хлорид + натрия хлорид + магния хлорид (C) 400,0 мл внутривенно капельно, на курс 5–10 вливаний
или
— натрия хлорид 0,9% (C) 400 мл внутривенно капельно на курс 5–10 вливаний
или
— кальция глюконат 10% (C) 10 мл 1 раз в сутки внутримышечно в течение 8–10 дней;
— тиосульфат натрия 30% (C) 10 мл 1 раз в сутки внутривенно на курс 8–10 вливаний.
Также является оправданным проведение процедур гемосорбции, плазмафереза (C) [3].
3. При возникновении инфекционных осложнений назначают антибактериальные препараты с учетом выделенного возбудителя, его чувствительности к антибактериальным препаратам и тяжести клинических проявлений.
Наружная терапия
заключается в тщательном уходе и обработке кожных покровов путем очищения, удаления некротической ткани. Не следует проводить обширное и агрессивное удаление некротически измененного эпидермиса, поскольку поверхностный некроз не является преградой для реэпителизации и может ускорять пролиферацию стволовых клеток посредством воспалительных цитокинов.
Для наружной терапии используют растворы антисептических препаратов (D): раствор перекиси водорода 1%, раствор хлоргексидина 0,06%, раствор перманганата калия (D).
Для обработки эрозий применяют раневые покрытия, анилиновые красители (D): метиленовый синий, фукорцин, бриллиантовый зеленый.
При поражении глаз требуется консультация офтальмолога. Не рекомендуется использовать глазные капли с антибактериальными препаратами в связи с частым развитием синдрома «сухого глаза». Целесообразно использовать глазные капли с глюкокортикостероидными препаратами (дексаметазоном), препараты искусственной слезы. Требуется механическая деструкция ранних синехий в случае их формирования.
При поражении слизистой оболочки полости рта проводят полоскания несколько раз в день антисептическими (хлоргексидин, мирамистин) или противогрибковыми (клотримазол) растворами.
Особые ситуации
Лечение детей
Требует интенсивного междисциплинарного взаимодействия педиатров, дерматологов, офтальмологов, хирургов:
— контроль за жидкостным балансом, электролитами, температурой и артериальным давлением;
— асептическое вскрытие еще упругих пузырей (покрышку оставляют на месте);
— микробиологический мониторинг очагов на коже и слизистых оболочках;
— уход за глазами и полостью рта;
— антисептические мероприятия, для обработки эрозий у детей применяют анилиновые красители без спирта: метиленовый синий, бриллиантовый зеленый;
— неадгезивные раневые повязки;
— помещение больного на специальный матрац;
— адекватная обезболивающая терапия;
— осторожная лечебная гимнастика для предупреждения контрактур.
Требования к результатам лечения
— клиническое выздоровление;
— предупреждение развития рецидивов.
ПРОФИЛАКТИКА
Профилактика рецидивов синдрома Стивенса–Джонсона заключается в исключении препаратов, вызвавших данное заболевание. Рекомендуется носить опознавательный браслет с указанием препаратов, вызвавших синдром Стивенса–Джонсона.
Информация
Источники и литература
Информация
Персональный состав рабочей группы по подготовке федеральных клинических рекомендаций по профилю «Дерматовенерология», раздел «Синдром Стивена-Джонсона»:
1. Заславский Денис Владимирович – профессор кафедры дерматовенерологии ГБОУ ВПО «Санкт-Петербургский государственный педиатрический университет» Минздрава России, профессор, доктор медицинских наук, г. Санкт-Петербург.
2. Горланов Игорь Александрович заведующий кафедрой дерматовенерологии ГБОУ ВПО «Санкт-Петербургский государственный педиатрический университет» Минздрава России, профессор, доктор медицинских наук, г. Санкт-Петербург.
3. Самцов Алексей Викторович – заведующий кафедрой кожных и венерических болезней ФГБВОУ ВПО «Военно-медицинская академия им С.М. Кирова», доктор медицинских наук, профессор, г. Санкт-Петербург.
4. Хайрутдинов Владислав Ринатович – ассистент кафедры кожных и венерических болезней ФГБВОУ ВПО «Военно-медицинская академия им С.М. Кирова», доктор медицинских наук, г. Санкт-Петербург.
МЕТОДОЛОГИЯ
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций являются публикации, вошедшие в Кокрановскую библиотеку, базы данных EMBASE и MEDLINE.
Методы, использованные для оценки качества и силы доказательств:
· Консенсус экспертов;
· Оценка значимости в соответствии с рейтинговой схемой (схема прилагается).
Рейтинговая схема для оценки силы рекомендаций:
| Уровни доказательств | Описание |
| 1++ | Мета-анализы высокого качества, систематические обзоры рандомизированных контролируемых исследований (РКИ) или РКИ с очень низким риском систематических ошибок |
| 1+ | Качественно проведенные мета-анализы, систематические, или РКИ с низким риском систематических ошибок |
| 1- | Мета-анализы, систематические, или РКИ с высоким риском систематических ошибок |
| 2++ | Высококачественные систематические обзоры исследований случай-контроль или когортных исследований. Высококачественные обзоры исследований случай-контроль или когортных исследований с очень низким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 2+ | Хорошо проведенные исследования случай-контроль или когортные исследования со средним риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 2- | Исследования случай-контроль или когортные исследования с высоким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи |
| 3 | Неаналитические исследования (например: описания случаев, серий случаев) |
| 4 | Мнение экспертов |
Методы, использованные для анализа доказательств:
· Обзоры опубликованных мета-анализов;
· Систематические обзоры с таблицами доказательств.
Методы, использованные для формулирования рекомендаций:
Консенсус экспертов.
Рейтинговая схема для оценки силы рекомендаций:
Индикаторы доброкачественной практики (Good Practice Points – GPPs):
Рекомендуемая доброкачественная практика базируется на клиническом опыте членов рабочей группы по разработке рекомендаций.
Экономический анализ:
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
· Внешняя экспертная оценка;
· Внутренняя экспертная оценка.
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами.
Комментарии, полученные от экспертов, систематизированы и обсуждены членами рабочей группы. Вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не были внесены, то зарегистрированы причины отказа от внесения изменений.
Консультация и экспертная оценка:
Предварительная версия была выставлена для обсуждения на сайте ФГБУ «Государственный научный центр дерматовенерологии и косметологии» Минздрава России для того, чтобы лица, не участвующие в разработке рекомендаций, имели возможность принять участие в обсуждении и совершенствовании рекомендаций.
Рабочая группа:
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы.
Основные рекомендации:
Сила рекомендаций (A–D) приводится при изложении текста рекомендаций.

