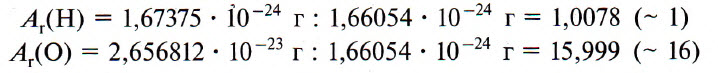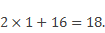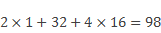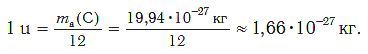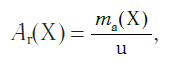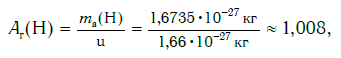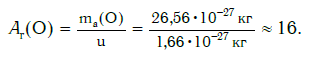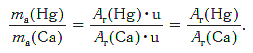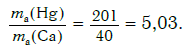что такое атомная масса относительная молекулярная масса
Что такое атомная масса относительная молекулярная масса
Ключевые слова конспекта: атомная единица массы, относительная атомная масса химических элементов, относительная молекулярная масса.
Атомная единица массы — это 1/12 массы атома углерода, масса которого равна 12 а.е.м.
Обратите внимание! На Земле встречаются три разновидности атомов углерода, различающиеся только массой. Такие разновидности атомов одного и того же элемента называют изотопами. В данном случае речь идёт о разновидности, масса атомов которой в атомных единицах массы равна 12.
Разделив массу атома какого-либо химического элемента на 1/12 массы атома углерода, получают величину, которую называют относительной атомной массой и обозначают Аr (А — от слова «атом», r — от латинского слова relativus — относительный).
Например, относительную атомную массу водорода и кислорода вычисляют следующим образом:
Относительная атомная масса элемента (Аr) показывает, во сколько раз масса его атома больше 1/12 массы атома углерода, масса которого равна 12 а. е. м.
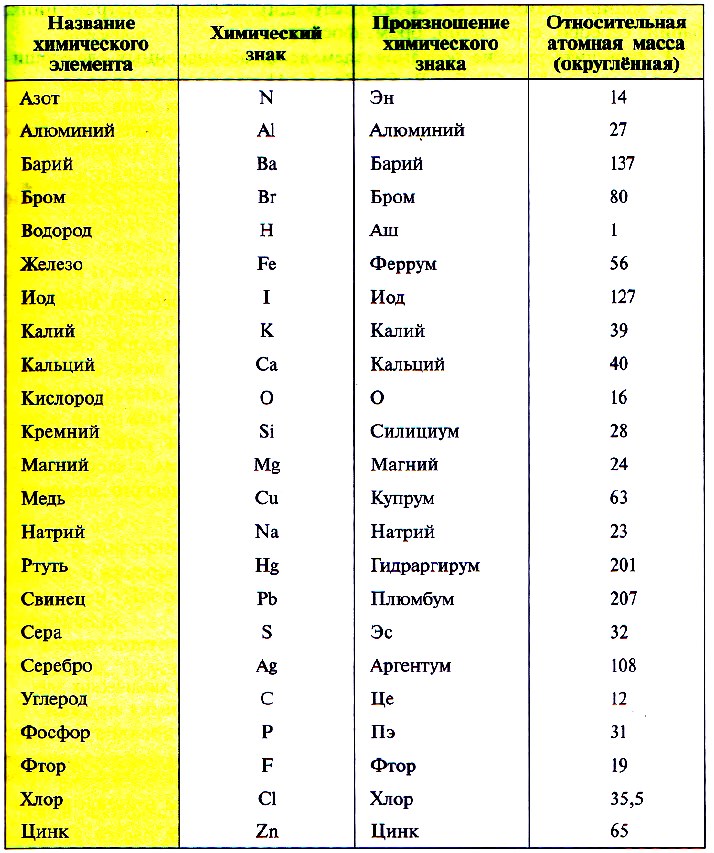
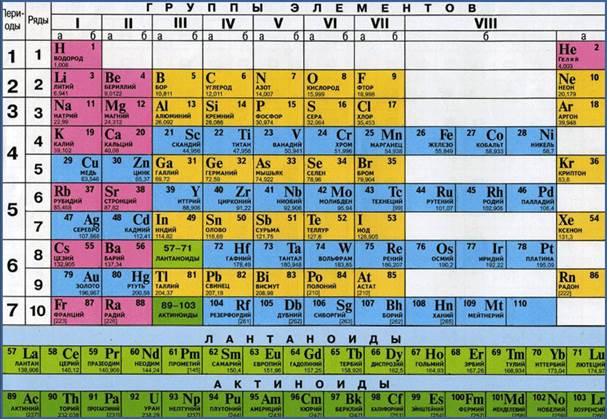
Так как первую таблицу относительных атомных масс ряда элементов составил английский учёный Джон Дальтон в 1803 г, то в память о его трудах химики иногда называют атомную единицу массы дальтоном (сокращённо Da). Значение относительной атомной массы каждого химического элемента приведено в периодической таблице Д. И. Менделеева. На практике эти значения обычно округляют до целых чисел.
Относительная молекулярная масса
Массу молекул, так же как массу атомов, принято выражать в атомных единицах массы. Разделив массу молекулы какого-либо вещества на 1/12 массы атома углерода, получают величину, которую называют относительной молекулярной массой вещества.
Относительная молекулярная масса вещества показывает, во сколько раз масса молекулы данного вещества больше 1/12 массы атома углерода, масса которого равна 12 а.е.м.
Относительная молекулярная масса Мr — безразмерная величина. Она складывается из относительных атомных масс элементов, составляющих молекулу, например:
Конец конспекта «Относительная атомная масса. Относительная молекулярная масса».
Что такое атомная масса относительная молекулярная масса
Письмо с инструкцией по восстановлению пароля
будет отправлено на вашу почту
Любое тело имеет массу. Возьмем такое тело как, например, мешок яблок. Это тело имеет массу. Его масса будет складываться из массы каждого яблока в мешке. Мешок риса тоже имеет свою массу, которая определяется путем сложения массы всех рисовых зернышек, хотя они очень маленькие и легкие.
Все тела состоят из веществ. Масса тела складывается из массы составляющих его веществ. Вещества, в свою очередь, состоят из частиц, молекул или атомов, следовательно, частицы вещества тоже имеют массу.
Если выразить массу самого легкого атома водорода в граммах, то получим очень сложное для дальнейшей работы число
Масса атома кислорода примерно в шестнадцать раз больше и составляет 2,66∙10-23г, масса атома углерода 1,99∙10-23г. Масса атома обозначается – ma.
Производить расчеты с такими числами неудобно.
Для измерения атомных (и молекулярных) масс применяют атомную единицу массы (а.е.м.).
Атомная единица массы – это 1/12 массы атома углерода.
В таком случае, масса атома водорода будет равна 1 а.е.м., масса атома кислорода – 16 а.е.м., а масса атома углерода – 12 а.е.м.
Химики долгое время не имели ни малейшего представления о том, сколько весит один атом какого-либо элемента в привычных и удобных для нас единицах измерения массы (грамм, килограмм и т. д.).
Поэтому первоначально задача определения атомных масс была изменена.
Были предприняты попытки определить, во сколько раз атомы одних элементов тяжелее других. Таким образом, учёные стремились сопоставить массу атома одного элемента с массой атома другого элемента.
Решение этой задачи также было сопряжено с большими трудностями, и прежде всего с выбором эталона, т. е. того химического элемента, относительно которого следовало проводить сравнение атомных масс остальных элементов.
Учёные XIX столетия решили эту проблему на основании экспериментальных данных по определению состава веществ. В качестве эталона был взят самый лёгкий атом – атом водорода. Экспериментально, было установлено, что атом кислорода в 16 раз тяжелее атома водорода, т. е. его относительная масса (относительно массы атома водорода) равна 16.
Эту величину условились обозначать буквами Ar (индекс «r» – от начальной буквы английского слова «relative» –относительный). Таким образом, запись значения относительных атомных масс химических элементов должна выглядеть следующим образом: относительная атомная масса водорода равна 1, относительная атомная масса кислорода равна 16, относительная атомная масса углерода равна 12.
Относительная атомная масса показывает, во сколько раз масса атома одного химического элемента больше массы атома, являющегося эталоном, поэтому данная величина не имеет размерности.
Как уже говорилось, первоначально значения атомных масс определяли по отношению к массе атома водорода. Позже эталоном для определения атомных масс стала 1/12 часть массы атома углерода (атом углерода в 12 раз тяжелее атома водорода).
Относительная атомная масса элемента (Ar) – это отношение массы атома химического элемента к 1/12 массы атома углерода.
Значения атомных масс химических элементов приведены в Периодической системе химических элементов Д.И. Менделеева. Взгляните на периодическую таблицу и рассмотрите любую ее клетку, например, под номером 8.
Под химическим знаком и названием в нижней строке указывается значение атомной массы химического элемента: относительная атомная масса кислорода равна 15,9994. Обратите внимание: относительные атомные массы почти всех химических элементов имеют дробное значение. Причиной этого является существование изотопов. Напомню, что изотопами называют атомы одного и того же химического элемента, незначительно отличающиеся по массе.
В школе в расчётах обычно используют значения относительных атомных масс, округленные до целых чисел. Но в нескольких случаях пользуются дробными величинами, например: относительная атомная масса хлора равна 35,5.
Из масс атомов складывается масса молекулы.
Относительной молекулярной массой вещества называется число, показывающее, во сколько раз масса молекулы этого вещества больше 1/12 массы атома углерода.
Относительная молекулярная масса обозначается – Mr
Относительную молекулярную массу веществ рассчитывают по химическим формулам, выражающим состав веществ. Для нахождения относительной молекулярной массы надо суммировать значения относительных атомных масс элементов, входящих в состав молекулы вещества, с учётом количественного состава, т. е. числа атомов каждого элемента (в химических формулах оно выражается с помощью индексов). Например, относительная молекулярная масса воды, имеющей формулу H2O, равна сумме двух значений относительной
атомной массы водорода и одного значения относительной атомной массы кислорода:
Относительная молекулярная масса серной кислоты, имеющей формулу H2SO4, равна сумме
Относительная молекулярная масса – величина безразмерная. Ее не следует путать с истинной массой молекул, выражаемой в атомных единицах массы.
Определение абсолютной и относительной массы вещества
Абсолютная и относительная масса атомов и молекул
Массу относят к фундаментальным характеристикам атома. Поскольку ее абсолютное значение очень мало, в химии вводится понятие относительной, т.е. условной, атомной массы.
Ничтожный размер атома не исключает наличия у него атомной массы. Вся масса атома сосредоточена в ядре (протон и нейтрон практически в 2000 раз тяжелее, чем электрон). В результате почти вся масса атома приходится на общую массу нейтронов и протонов. К примеру, атомная масса кислорода равняется 2,667·10-23 г. Это его абсолютная атомная масса. Работать с таким числом неудобно. Поэтому было предложено ввести еще одну величину – относительную атомную массу.
В начале XIX века Дж. Дальтон предложил, вычисляя атомную массу, использовать в качестве эталона массу атома водорода, поскольку он является самым легким элементом. Именно по отношению к нему выражались массы атомов прочих элементов.
Однако с учетом того, что на практике чаще использовались кислородные соединения для вычисления атомных масс многих элементов, в качестве эталона удобнее стало использовать атомную массу кислорода. При этом известно, что соотношение атомных масс кислорода и водорода равно 16:1. Так возникло понятие кислородной единицы – 1/16 части его атомной массы.
Таким образом, относительная атомная масса показывает, во сколько раз масса атома конкретного элемента больше массы атома, который принимается за единицу. Сегодня это 1/12 часть массы атома углерода. Это и есть атомная единица массы, которую иногда обозначают как «дальтон».
Относительная атомная масса – отношение массы атома определенного элемента к 1/12 массы атома изотопа углерода-12. По сути относительная атомная масса является безразмерной величиной (при ее расчете единицы измерения сокращаются), но иногда ее значение выражают в атомных единицах массы (а.е.м.).
Абсолютная масса атома углерода составляет 1,993·10-23 г, согласно Периодической таблице Д.И. Менделеева. Его относительная атомная масса равна 12. Следовательно, 1/12 часть массы атома углерода составляет:
Масса одного кислородного атома приблизительно в 16 раз превышает 1/12-ю массы углеродного атома 12С.
Чтобы вычислить относительную молекулярную массу вещества, нужно сложить суммы относительных атомных масс элементов, входящих в состав молекулы, с учетом индексов, которые показывают количество атомов элемента в молекуле. Абсолютная масса одной молекулы равна относительной, умноженной на одну атомную единицу массы (1 а.е.м.).
Относительная атомная масса химического элемента
Например, определение относительной массы атома водорода выглядит так:
Элемент кислород имеет следующую относительную атомную массу:
Из формул следует, что относительная атомная масса является величиной, равной отношению абсолютной атомной массы к единице массы u (или 1 а.е.м.).
Относительная молекулярная масса вещества
Если молекула состоит из атомов нескольких химических элементов, то ее относительная молекулярная масса равна сумме их относительных атомных масс с учетом индексов в формуле вещества.
Рассмотрим пример. Молекула воды имеет в своем составе два атома водорода и один – кислорода. Чтобы определить относительную молекулярную массу, нужно сложить произведения относительной атомной массы каждого элемента на соответствующее количество атомов:
Знание относительной молекулярной массы веществ в газообразном состоянии помогает в решении задач по сравнению их плотности. Для этого высчитывается относительная плотность газов друг по другу, которая равна соотношению их относительных молекулярных масс:
Поскольку закон Авогадро применим исключительно к газообразным веществам, а ученым-химикам часто необходимо знать, сколько молекул, атомов или ионов заключено в определенных порциях твердых веществ или жидкостей, введено понятие молярной массы. Ее значение численно равно относительной молекулярной массе.
Как вычислить абсолютную массу, формулы, примеры
Найти молекулярную массу серной кислоты, используя таблицу Менделеева.
Известно, что молекулярная масса вещества равна сумме атомных масс веществ, входящих в состав молекулы. Поэтому:
M r ( H 2 S O 4 ) = 1 · 2 + 32 + 16 · 4 = 98 г / м о л ь
Решение химических задач по нахождению абсолютной массы может сводиться к использованию следующих методов:
При этом молярную массу можно найти путем сложения атомных масс элементов, входящих в состав соединения. Молярная масса находится также как отношение массы вещества к его соответствующему количеству:
Урок 2. Относительная атомная масса химических элементов
В уроке 2 «Относительная атомная масса химических элементов» из курса «Химия для чайников» рассмотрим разные способы выражения массы химических элементов. Напоминаю, что в прошлом уроке «Атомы и химические элементы» мы рассмотрели, кто и когда высказал идею о том, что все вокруг состоит из атомов; также выяснили, что из себя представляет химический элемент и каким образом обозначается.
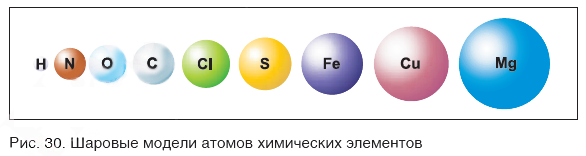
Чем различаются атомы разных элементов между собой? Вы уже знаете: массой, размерами и строением. На рисунке 30 показаны шаровые модели атомов некоторых химических элементов, конечно, не в реальных размерах, а многократно увеличенные. В действительности атомы настолько малы, что их невозможно рассмотреть даже в самые лучшие оптические микроскопы.
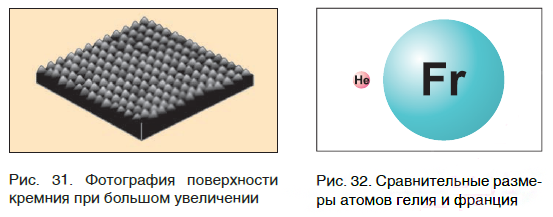
На заметку: В конце XX в. у ученых появились более совершенные микроскопы, позволяющие достигать увеличения в несколько десятков миллионов раз. Они называются туннельными микроскопами. На рисунке 31 показана фотография поверхности кремния. На ней отчетливо видны отдельные атомы, расположенные на поверхности этого вещества.
Размеры и масса атомов
Современная наука обладает методами, позволяющими определять размеры и массы атомов. Так, например, самый легкий атом — атом водорода. Его масса равна 0,0000000000000000000000000016735 кг. Самым маленьким является атом гелия He. Диаметр этого атома равен приблизительно 0,00000000098 м. Записывать и читать такие числа затруднительно, поэтому обычно их представляют в более удобном виде: 1,6735·10 −27 кг и 9,8·10 −10 м. Атомы большинства химических элементов по своим размерам значительно больше атома гелия. Самый большой из них — атом элемента франция Fr. Его диаметр в 7 раз больше диаметра атома гелия (рис. 32).
Еще больше различаются атомы разных элементов по массе. Масса атома обозначается символом ma и выражается в единицах массы СИ (кг). Так, например, масса атома углерода равна: ma(С) = 19,94·10 −27 кг, а атома кислорода — ma(О) = 26,56·10 −27 кг. Масса атома самого тяжелого из существующих на Земле элементов — урана U — почти в 237 раз больше массы атома водорода.
Атомная единица массы
Пользоваться такими маленькими величинами масс атомов при расчетах неудобно. К тому же, когда в XIX в. начало формироваться атомно- молекулярное учение, ученые еще не представляли реальных размеров и масс атомов. Поэтому на практике вместо истинных масс атомов стали применять их относительные значения. Они рассчитывались по массовым отношениям простых веществ в реакциях друг с другом. Химики предположили, что эти отношения пропорциональны массам соответствующих атомов. Именно так в начале XIX в. Дж. Дальтон ввел понятие относительной атомной массы, приняв за единицу сравнения массу самого легкого атома — водорода.
В настоящее время в качестве такой единицы сравнения используется 1/12 часть массы атома углерода (рис. 33). Она получила название атомной единицы массы (а. е. м.). Ее международное обозначение — u (от английского слова «unit» — единица):
Атомная единица массы — это 1/12 часть массы атома углерода, которая равна 1,66·10 −27 кг.
Относительная атомная масса
Сравнивая средние массы атомов различных элементов с атомной единицей массы, получают значения относительных атомных масс химических элементов.
Относительная атомная масса элемента — это физическая величина, которая показывает, во сколько раз масса атома данного химического элемента больше 1/12 части массы атома углерода.
Относительная атомная масса обозначается символами Ar ( А — первая буква английского слова «atomic» —атомный, r — первая буква английского слова «relative», что значит относительный), следовательно:
где Х — символ данного элемента.
Например, относительная атомная масса водорода:
В таблице Менделеева приведены относительные атомные массы всех элементов. В расчетах при решении задач мы будем пользоваться округленными до целых значениями этих величин (см. урок 1).
Внимание! Очень часто относительную атомную массу называют просто атомной массой. Однако следует отличать атомную массу — величину относительную (например, Ar(О) = 16) — от массы атома — величины, выражаемой в единицах массы — килограммах ( ma(O) = 26,56·10 −27 кг) или атомных единицах массы ( ma(O) = 16· u ).
Пример. Во сколько раз атом ртути тяжелее атома кальция?
Решение. Относительные атомные массы элементов равны: Ar(Hg) = 201 и Ar(Ca) = 40.
Масса атома ртути равна: ma(Hg) = Ar(Hg)·u (кг).
Масса атома кальция равна: ma(Са) = Ar(Са)·u (кг).
Другими словами, отношение масс атомов этих элементов равно отношению их относительных атомных масс. Следовательно, отношение масс атомов ртути и кальция равно:
Ответ: в 5,03 раза.
Краткие выводы урока:
Надеюсь урок 2 «Относительная атомная масса химических элементов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Относительная атомная и молекулярная масса
Одной из важнейших характеристик любой молекулы и любого атома является его масса. В химии ее принято измерять не в килограммах, а с помощью так называемой а. е. м. – атомной единицы массы.
Как определить массу молекулы?
Хотя идеи о том, что все вещества состоят из мельчайших частиц, то есть атомов, высказывались ещё Демокритом в Античности, доказать подобные гипотезы было невозможно. Однако в начале XIX в. произошел научный прорыв. Джон Дальтон открыл сразу три важных закона:
Объяснить открытые закономерности можно было только с помощью гипотезы об атомной строении вещества. Эти же законы позволяли Дальтону сравнивать массы атомов и молекул между собой. Ученый принял массу атома водорода за единицу (так как он оказался самым легким атомом), и через нее (то есть через водородную единицу) в 1803 г. выразил массы многих других атомов и молекул. Впрочем, оказалось, что значительная часть вычислений была проведена с ошибками.
На тот момент для определения масс атомов чаще всего использовались реакции образования оксидов, то есть кислородных соединений. По этой причине в ходе опытов фактически в качестве единицы измерения использовалась масса не атома водорода, а атома кислорода. Изначально грубые расчеты показывали, что кислородный атом в 16 раз тяжелее водородного атома, то есть его масса, по системе Дальтона, составляла 16 единиц. Однако потом выяснилось, что всё же атом кислорода тяжелее только в 15,874 раза. Эти данные потребовали пересчета всех атомных масс. Но химики поступили проще – они договорились, что теперь масса кислородного атома принимается в точности равной 16 атомным единицам. Так возникла новая, кислородная единицы атомного веса. В результате пересчитывать пришлось лишь массу водорода – она теперь составляла не единицу, а 16:15,874≈ 1,0079 атомных единиц.
Уже в начале XX в. выяснилось, что в природе могут существовать изотопы – разные по массе атомы одного и того же элемента. В частности, в природе встречается три различных стабильных изотопов кислорода (и ещё 10 – нестабильных). Встал вопрос – масса какого из этих изотопов будет приниматься за единицу? Физики стали использовать массу изотопа кислород-16, а химики – среднюю массу всех изотопов (с учетом их распространенности в природном кислороде). Возникли разночтения, которые были решены лишь в 1960-1961 г. Тогда была принята договоренность, что масса изотопа углерода-12 принимается равной 12 атомным единицам массы (а. е. м.). Таким образом появилась углеродная единица.
Молярная масса
Помимо молекулярной массы существует ещё и молярная масса. Она показывает, сколько грамм весит один моль вещества. Фактически молярная масса совпадает со значением молекулярной массы, но измеряется она в других величинах – в г/моль. Например, если атомная масса углерода-12 равна 12 а. е. м., то его молярная масса составит 12 г/моль.
Какова масса одной а. е. м.?
С помощью атомных масс удобно сравнивать друг с другом массы молекул атомов и соединений. Например, если молекула воды весит 18 а. е. м., в молекула углекислого газа – 44 а. е. м., то это значит, что молекула СО2 тяжелее молекулы воды в 44/18 ≈2,444 раза. Но как определить массу атомов и молекул в привычных для нас килограммах?
Это можно сделать, вычислив число Авогадро, которое показывает, сколько молекул содержится в 1 моле вещества. Первые оценки числа Авогадро были проведены лишь в 1865 г., но тогда ученые ошиблись в 15 раз, через 8 лет ошибка уменьшилась в 10 раз. Сегодняшние измерения показывают, что один атом водорода весит всего лишь 1,66•10 –27 кг.
Подведение итогов
Для определения массы атомов и молекул используется а. е. м. – атомная единица массы. Она составляет 1/12 от массы атома изотопа углерода 12 и примерно равна 1,66•10 –27 кг.