лейкодистрофия это что такое головного мозга
Лейкодистрофия это что такое головного мозга
Лейкодистрофии представляют собой группу генетических заболеваний, поражающих белое вещество головного мозга и при некоторых заболеваниях также периферический миелин. В настоящее время отсутствует классификация, учитывающая все клинические проявления, морфологические нарушения или метаболические или генетические изменения. В широком смысле лейкодистрофии определяются как генетические поражения белого вещества головного мозга.
Лейкодистрофии также относятся к большой группе состояний, преимущественно поражающих белое вещество, называемых лейкоэнцефалопатиями, которые включают многие заболевания, поражающие белое вещество, но имеют скорее негенетическое происхождение. Лейкоэнцефалопатии приводят к формированию выявляемых с помощью визуализации проявлений, напоминающих проявления лейкодистрофий, что является основанием для дифференциальной диагностики.
Первоначально классификация основывалась на морфологических характеристиках; примером являются глобоидно-клеточная лейкодистрофия (болезнь Краббе), метахроматическая лейкодистрофия и суданофильная лейкодистрофия. Последний термин в последнее время употребляется все реже в связи с улучшением понимания генетической этиологии большинства лейкодистрофий. Понятия демиелинизация, дисмиелинизация и гипомиелинизация описывают возможные патофизиологические изменения.
Демиелинизация представляет собой деградацию структурно и биохимически нормального миелина (например, при рассеянном склерозе), дисмиелинизация характеризуется структурно и биохимически аномальным или нестабильным миелином (например, при адренолейкодистрофии), в то время как гипомиелинизация указывает на нарушение и отсрочку формирования миелина (например при болезни Пелицеуса-Мерцбахера). Демиелинизация может встречаться при всех трех состояниях, поражая обычно олигодендроциты и макрофаги как основные клеточные компоненты.
Результаты исследований последних лет свидетельствуют о признаках поражения белков внеклеточного матрикса при стабилизации мембраны миелина (например, при альфа-саркогликанопатиях). Аксонопатии и нарушения нейрофиламентов также могут играть важную роль в поддержании стабильности миелина. Недавно обсуждалась роль дисфункции астроцитов в качестве фактора демиелинизации (Seifert et al., 2006). Несмотря на все диагностические усилия и прогресс современной неврологии, радиологии, биохимии и генетических методик, существенная доля лейкодистрофий детского возраста остается неклассифицированной, а патогенез многих заболеваний белого вещества головного мозга неустановлен.
Несмотря на то, что обычно лейкодистрофия проявляется в раннем детском возрасте, возрастной диапазон начала заболевания варьирует от пренатального периода (врожденное заболевание) до взрослого возраста. Лейкодистрофии представляют собой классический вариант поражения белого вещества. Тем не менее, поражение серого вещества с возрастающей частотой выявляется в качестве проявления многих заболеваний, начинающихся в раннем возрасте.
Классификация лейкодистрофий преимущественно основана на изменениях клеточных органелл (лизосом, пероксисом, митохондрий), структурных элементов (нейрофиламентов, альфа-саркогликана) и метаболических процессов. В таблице ниже приведена классификация лейкодистрофий в соответствии с наличием или отсутствием известных метаболических или генетических дефектов. Большая группа недавно идентифицированных заболеваний белого вещества описана отдельно как «прочие заболевания». Будущая классификация, вероятно, будет основана на индивидуальных генетических дефектах.
С клинической точки зрения лейкодистрофии характеризуются преобладанием моторных нарушений, особенно пирамидных и мозжечковых симптомов, медленной умственной деградацией, низкой частотой припадков, миоклонуса и пароксизмальных ЭЭГ аномалий. При визуализации при всех лейкодистрофиях отмечается поражение белого вещества, лучше всего выявляемое при МРТ, выраженность поражения может быть различной, и в некоторых случаях требуется применение новейших методик визуализации. МРТ признаки поражения белого вещества описаны van der Knaap и Valk (2005), а аномалии, выявляемые при МР-спектроскопии — Hanefeld et al. (2004).
Редактор: Искандер Милевски. Дата публикации: 16.12.2018
Лечение лейкодистрофии в Израиле
О заболевании
Лейкодистрофия – это группа редких неврологических заболеваний (нервной системы). Они влияют на белое вещество головного и спинного мозга. Белое вещество – это ткань, состоящая из изолированных нервных волокон.
Лейкодистрофии нацелены на миелин, который является защитной изоляцией, покрывающей нервные клетки. Без миелина нервы не могут нормально функционировать. Лейкодистрофии приводят к прогрессирующей потере неврологической функции.
Исследователи выделили более 50 видов лейкодистрофии. Некоторые из наиболее распространенных включают:
Каждая форма лейкодистрофии является результатом различных мутаций (изменений) гена и вызывает разные симптомы. Наиболее часто из перечисленных форм встречается метахроматическая лейкодистрофия.
В младенческой форме ребенок страдает прогрессирующим параличом и слабоумием, то есть паралич и слабоумие усугубляются с течением времени. Симптомы этой формы обычно проявляются в возрасте до 4 лет.
В юношеской форме у детей возникают трудности с ходьбой, умственная отсталость, слабость, онемение и боли в руках и ногах. Симптомы этой формы начинаются в возрасте от 4 до 16 лет.
Причины развития заболевания заключаются в мутации генов, контролирующих рост или функцию миелина. Без этого защитного покрытия нервные клетки не работают правильно.
Методы лечения заболевания
Детям, живущим со сложными проблемами лейкодистрофии, в клинике Ихилов предоставляется ультрасовременная медицинская помощь, включающая консервативное лечение и, в отдельных случаях, транстплантацию костного мозга или стволовых клеток.
Консервативное лечение (контроль симптомов)
Лечение большинства лейкодистрофий направлено на устранение симптомов, профилактику и координацию болезненных состояний. Ребенку могут быть назначены лекарства для лечения спастичности или судорог, физиотерапия, эрготерапия, гормональная терапия дисфункции надпочечников и логопедия.
Трансплантация костного мозга или стволовых клеток
Одна из целей терапии лейкодистрофии – раннее выявление пациентов, которые могут получить пользу от трансплантации костного мозга или стволовых клеток. Трансплантация костного мозга считается стандартом лечения некоторых лейкодистрофий, но для этого заболевание необходимо диагностировать на ранней стадии. Процедура не может обратить вспять какие-либо изменения, которые уже произошли в ходе болезни, но может помочь замедлить общее прогрессирование и минимизировать неврологический спад.
Как проходит диагностика
Все диагностические мероприятия в клинике Ихилов проводятся за три дня. Предположительный график получения консультаций и проведения инструментальных исследований согласовывается заранее, еще до приезда пациента в клинику.
Лечащий врач оценит симптомы и признаки заболевания, выполнит физическое и неврологическое обследование, проверит личный и семейный анамнез. Поставить диагноз бывает сложно. Часто врачам приходится использовать несколько видов лабораторного и инструментального тестирования.
Весь второй день обследования посвящен исследованиям. Виды исследований, необходимых для диагностики лейкодистрофии могут включать:
— Анализы крови и мочи.
— Визуализирующие обследования, такие как МРТ или КТ, чтобы проверить белое вещество в головном и спинном мозге.
— Психологические и когнитивные тесты.
Когда результаты обследования готовы, собирается врачебная комиссия. В команду специалистов входят эксперты по заболеваниям нервной системы (неврологи), генетическим заболеваниям (медицинские генетики) и другим нозологиям. Коллегиально они принимают решение о выборе релевантной схемы лечения. Сопровождающий пациента может присутствовать на этом обсуждении и получить информацию о преимуществах и рисках выбранных видов терапии.
Сколько стоит лечение
Цена за курс лечения является одним из наиболее актуальных вопросов. Примерная стоимость сообщается еще до приезда пациента в клинику. Обычно в Ихилов лечение стоит меньше, в среднем на 30%, по сравнению с европейскими и американскими клиниками.
Точная стоимость рассчитывается после проведения диагностического обследования, когда понятен полный объем мер, необходимых пациенту. От случая к случаю выбор терапевтических средств и способов лечения может существенно отличаться, что сказывается и на стоимости.
Преимущества лечения в Ихилов
Своевременное обращение за помощью может существенно улучшить прогноз и общее состояние пациента с лейкодистрофией.
Лейкодистрофии
Лейкодистрофии – это группа генетических заболеваний, связанных с нарушением обмена веществ и сопровождающихся накоплением в белом веществе мозга метаболитов, которые разрушают миелин. Обычно первые симптомы начинают появляться у пациентов в детском возрасте:
Лечение симптоматическое, но при своевременной диагностике и медленном течении заболевания возможна стабилизация состояния после аллогенной (от другого человека) трансплантации костного мозга или стволовых клеток.
Причины лейкодистрофии
Лейкодистрофии возникают в результате поломки генов, отвечающих за метаболизм миелина, после чего возникают метаболические аномалии, приводящие к разрушению белого вещества мозга. В большинстве случаев заболевание наследуется по аутосомно-рецессивному типу, но возможно и наследование, сцепленное с Х-хромосомой, как это случается при адренолейкодистрофии.
Родителям, у которых были дети с лейкодистрофией, необходима консультация генетика при планировании следующей беременности.
Симптомы лейкодистрофии
Дети с лейкодистрофией рождаются клинически здоровыми. Какое-то время они развиваются нормально, но постепенно начинают проявляться признаки поражения ЦНС, которые неумолимо нарастают. Чем раньше началась манифестация, тем выше скорость прогрессирования болезни и тем более неблагоприятный прогноз.
Для каждого вида заболевания характерны свои симптомы и очередность их возникновения, но общие черты все же есть:
Есть ряд симптомов, которые характерны только для определенных видов лейкодистрофии. Например, при адренолейкодистрофии, помимо мозговых нарушений, поражаются надпочечники.
Классификация лейкодистрофий
Существует около 60 видов лейкодистрофий. Они различаются видом генетической поломки и возрастом проявления симптомов. Чаще всего встречаются три вида, соответственно, они наиболее изучены:
Диагностика и лечение лейкодистрофии
Диагностика лейкодистрофии требует комплексного подхода с участием специалистов разного профиля: неврологов, офтальмологов, отоларингологов и др. Одним из главных методов обнаружения болезни является МРТ. Она четко визуализирует очаги демиелинизации еще до начала клинических проявлений. По мере прогрессирования заболевания МРТ-картина также ухудшается. К уточняющим методам диагностики относятся:
Единственным методом лечения лейкодистрофии на сегодняшний день является аллогенная трансплантация костного мозга или стволовых клеток. Она позволяет нормализовать метаболизм миелина, стабилизировать процесс демиелинизации и замедлить или остановить прогрессирование заболевания.
Наилучшие результаты достигаются либо при медленно текущей форме, либо доклиническом назначении трансплантации. В связи с этим большое значение отводится своевременной диагностике в семьях с уже имеющимися больными детьми.
Медико-генетический центр «Геномед» обладает возможностями для молекулярно-генетической диагностики данного заболевания как уже у рожденных пациентов, так и в рамках пренатального скрининга.
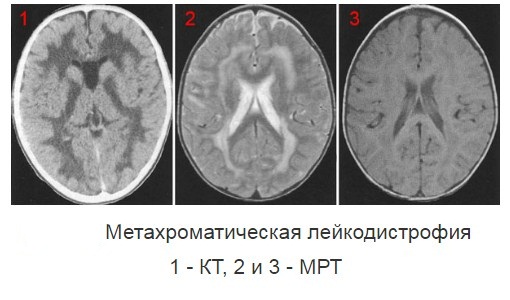
Метахроматическая лейкодистрофия
Метахроматическая лейкодистрофия — аутосомно-рецессивно наследуемая демиелинизирующая патология ЦНС, отличительной особенностью которой является метахроматическое окрашивание зон демиелинизации. В клинике преобладает задержка развития, парезы, судорожные приступы, экстрапирамидные и мозжечковые расстройства, нарушение зрения. В ходе диагностики проводится исследование цереброспинальной жидкости, уровня сульфатидов, активности арилсульфатазы А, КТ/МРТ головного мозга, генетические обследования. Возможна пренатальная диагностика. Лечение симптоматическое, в отдельных случаях проводится трансплантация пуповинной крови или стволовых клеток.
Общие сведения
Метахроматическая лейкодистрофия — один из основных видов лейкодистрофии, характеризующийся, как и другие ее типы, задержкой психомоторного развития, расстройством психики, спастическими парезами, мозжечковым синдромом, экстрапирамидными нарушениями, судорожным синдромом и атрофией зрительных нервов. Встречается в популяции с частотой 1 случай на 40 тыс. Наследуется аутосомно-рецессивно. Впервые выделена как нозологическая форма в 1910 г. Альцгеймером, подробно описана в 1925 г. Шольцем. Время манифестации заболевания существенно варьирует и обуславливает его клиническое течение. В соответствии с этими особенностями выделяют несколько вариантов патологии: врожденную (раннедетскую) форму, позднедетскую форму Гринфилда, ювенильную форму Шольца и взрослую форму. Наиболее часто наблюдается познедетская форма. В виду отсутствия эффективных способов лечения метахроматическая лейкодистрофия является проблемной патологией для современной педиатрии, неврологии и генетики.
Причины
Основным субстратом заболевания выступает дефект расположенного на 22-й хромосоме гена, ответственного за синтез арилсульфатазы А. Результатом дефицита указанного энзима является блокировка метаболизма сульфатида в галактоцереброзид. Сульфатиды откладываются в белом веществе головного и спинного мозга, коже, соматических органах (печени, легких, сердце, почках) и в костях. Однако при этом функция внутренних органов не страдает (исключением является желчный пузырь), а в мозговом веществе происходят прогрессирующие дегенеративные изменения, ведущие к гибели заболевшего.
Отложение сульфатидов в нервной ткани приводит к разрушению миелина и накоплению продуктов его распада. В процесс демиелинизации вовлекаются не только структуры ЦНС, но и периферические нервные стволы. В головном мозге формируются диффузные очаги демиелинизации, дающие при их гистохимическом исследовании метахроматическое окрашивание.
Симптомы метахроматической лейкодистрофии
Врожденная метахроматическая лейкодистрофия дебютирует до 3-месячного возраста задержкой развития и эписиндромом. Быстро присоединяется спастический парез, расстройства глотания. Дети погибают на 1-ом году жизни.
Позднедетская метахроматическая лейкодистрофия (поздняя инфантильная форма) обычно манифестирует на 2-ом году жизни ухудшением моторики и задержкой психического развития. Отмечается неустойчивая походка, понижение мышечного тонуса. В течении позднедетской формы различают 4 периода. Первый характеризуется мышечной гипотонией и слабостью, угасанием сухожильных рефлексов, затруднением ходьбы. Длится от 1-3 мес. до 1 года, иногда и дольше. Второй период знаменуется выраженным отставанием в интеллектуальной сфере, сменой гипотонии на гипертонию мышц. Ребенок утрачивает способность стоять. Наблюдается дизартрия, атрофия зрительных нервов. Период занимает несколько месяцев. В третьем периоде отмечается тетраплегия, тяжелая олигофрения, бульбарный и псевдобульбарный паралич. Четвертый период сопровождается утратой реакций на окружающие события. Ребенок не говорит, не может принимать пищу, развивается полная слепота. При хорошем уходе и кормлении через гастростому или желудочный зонд данный период может продолжаться 1-2 года.
Ювенильная метахроматическая лейкодистрофия начинается после 3-летнего возраста в периоде до 10 лет (чаще в возрасте около 6 лет). Дебютирует эмоциональной лабильностью, изменениями в поведении, снижением когнитивных функций (у школьников происходит резкое ухудшение успеваемости), атаксией, затруднениями при ходьбе. Зачастую отмечаются эпиприступы. Заболевание неуклонно прогрессирует и, в зависимости от начала симптоматики, к 10-15 годам жизни приводит к летальному исходу.
Взрослая метахроматическая лейкодистрофия манифестирует после пубертата, может возникать до 60-летнего возраста. Как правило, имеет начало с психических расстройств шизофреноподобного или психопатического характера, отчего заболевшие первоначально становятся пациентами психиатра. В отдельных случаях дебют происходит с симптомов полиневропатии. Развитие патологических изменений происходит медленнее, чем при других возрастных вариантах заболевания. В позднем периоде развиваются тетрапарез, бульбарные нарушения, деменция. Летальный исход наблюдается спустя 10-20 лет от начала симптоматики.
Диагностика метахроматической лейкодистрофии
Диагностические мероприятия имеют комплексный характер и позволяют отдифференцировать метахроматическую лейкодистрофию от других нейродегенеративных заболеваний и других форм лейкодистрофии. Проводится люмбальная пункция, при исследовании цереброспинальной жидкости определяется повышенная концентрация белка, дефицит арилсульфатазы, белково-клеточная диссоциация. Электромиография выявляет увеличение длительности проведения нервных импульсов. КТ головного мозга визуализирует расширенные желудочки и определяет пониженную плотность белого церебрального вещества. МРТ головного мозга выявляет очаги демиелинизации.
Важное диагностическое значение имеют биохимические исследования: определение сульфатидов в крови и моче, оценка активности арилсульфатазы А в лейкоцитах взятой на анализ крови. Пациентам показана консультация генетика с проведением генеалогического исследования; возможна ДНК-диагностика. Разработан также метод пренатальной диагностики патологии — определение активности арилсульфатазы А в клетках полученной при амниоцентезе амниотической жидкости. Исследования показали, что у носителей патогенного гена также отмечается сниженный уровень арилсульфатазы А. В связи с этим вместо пренатальной диагностики плода предлагается обследовать родителей будущего ребенка, чтобы избежать медаборта плода, являющегося лишь носителем дефектного гена.
Лечение метахроматической лейкодистрофии
Терапия, способная предотвратить летальный исход заболевания, пока не найдена. Осуществляется лечение, направленное на купирование его отдельных симптомов: противосудорожная терапия, борьба с контрактурами суставов; на поздних стадиях — профилактика пролежней, парентеральное питание. Проводится поиск более эффективных способов лечения, особенно в области генной терапии.
Предпринимаются попытки лечения путем трансплантации костного мозга и пуповинной крови. У ряда пациентов пересадка стволовых клеток позволяет добиться временной стабилизации состояния и замедления прогрессирования патологических изменений. Донором стволовых клеток обычно выступает родственник больного, не имеющий лейкодистрофии и тщательно обследованный. Однако следует помнить, что сама трансплантация может повлечь за собой целый ряд осложнений: отторжение, интеркурентные инфекции, реакцию «трансплантат против хозяина». Кроме того, при быстром прогрессировании симптомов летальный исход опережает наступление эффекта трансплантации.
Прогноз
Пока не найдена эффективная терапия лейкодистрофий, она имеет крайне неблагоприятный прогноз. При врожденной форме дети не доживают до 1 года. При позднедетском варианте продолжительность болезни, как правило, не превышает 4 года, при ювенильном — 6 лет. Среди пациентов со взрослой формой известны отдельные случаи, когда продолжительность жизни составила около 50 лет. Пока единственным способом предупреждения лейкодистрофии является недопущение рождения ребенка, имеющего соответствующую генную мутацию. В этом плане основное значение имеет генетическое консультирование пар, планирующих деторождение, а также обследование будущих родителей из группы риска на степень активности арилсульфатазы А.
Лейкодистрофия. Причины, симптоматика, диагностика и лечение лейкодистрофии
1. Общие сведения
Термин «лейкодистрофия» объединяет группу редких (и очень редких) наследственных заболеваний, с развитием которых разрушаются миелиновые оболочки аксонов – связующих проводников между нейронами, функциональными клетками центральной нервной системы. Снижение концентрации миелина, выполняющего функции природного электроизолятора, приводит к «пробоям» и нарушениям в сложнейших электрохимических взаимосвязях, обеспечивающих высшую нервную деятельность, и вызывает ее постепенную общую деградацию вплоть до летального исхода. Название заболевания обусловлено цветом миелина (от греч. «лейкос» – белый). Эпидемиологические данные по лейкодистрофии неодинаковы для разных ее форм и, кроме того, обнаруживают значимую региональную зависимость, однако в среднем частота встречаемости составляет 1 случай на несколько десятков тысяч населения. Известно также, что лейкодистрофии наследуются по аутосомно-рецессивному типу и примерно с равной частотой встречаются у мужчин и женщин. В подавляющем большинстве случаев симптоматика манифестирует уже в раннем детском возрасте (в т.ч. на первом году жизни), причем более раннее начало связано статистической закономерностью с более быстрым и злокачественным течением.
2. Причины
В основе прогрессирующего миелинового дефицита лежит хроническая нехватка в организме лизосомных ферментов, что, в свою очередь, обусловлено наследуемой мутацией определенных генов. При наличии такого сбойного гена у обоих родителей вероятность того, что их ребенок заболеет лейкодистрофией (независимо от очередности и порядкового номера рождения) составляет 25%, или 1/4.
3. Симптоматика, диагностика
Различают несколько более или менее самостоятельных лейкодистрофических процессов, – метахроматическая, суданофильная, адренолейкодистрофия и т.д.; в некоторых из них выделяются, в свою очередь, отдельные возрастные формы. В целом же, симптоматика лейкодистрофий очень многообразна. Так, отмечаются тяжелые нарушения моторики (параличи, тремор, нистагмоидные движения глазных яблок, мышечный гипертонус) и координации движений, атрофия зрительного нерва, судорожные припадки эпилептического типа, при некоторых формах имеет место микроцефалия. Однако наиболее тяжелые нарушения и изменения касаются высшего продукта центральной нервной системы – психики. Если начало заболевания приходится на ранний детский возраст, обнаруживается выраженное отставание интеллектуального и эмоционального развития, некорригируемые поведенческие нарушения, практическое отсутствие обучаемости. Иногда элементарные навыки и автоматизмы не успевают выработаться вообще, и жизнедеятельность больного ребенка приходится поддерживать, фактически, искусственно. Если же заболевание манифестирует в более позднем или зрелом возрасте, начинается своего рода инволюция, т.е. «обратное развитие»: высшие психические функции распадаются и деградируют к предшествующим уровням развития, пока не наступает практически полная беспомощность, вегетативное существование и, в конечном счете, гибель больного.
В диагностике лейкодистрофий ключевое значение имеет изучение анамнеза, в т.ч. семейного; назначается неврологическое, медико-генетическое, биохимическое обследование. Необходим тщательный мониторинг динамики появившихся (и появляющихся) симптомов. В ряде случаев показана спинномозговая пункция с последующим микроскопическим анализом ликвора. Информативны, – и потому широко применяются, – современные визуализирующие методы: МРТ, МСКТ.
4. Лечение
Единственным эффективным, на данный момент, лечением лейкодистрофий является трансплантация костного мозга или пуповинной крови – как правило, от ближайших родственников (что, однако, также не гарантирует от возможных осложнений в виде отторжения донорского материала). Данная процедура позволяет в какой-то степени восполнить дефицит миелина и, по крайней мере, замедлить темпы прогрессирования болезни, но, к сожалению, положительный эффект наступает далеко не сразу (спустя несколько месяцев или даже 1,5-2 лет, в течение которых продолжается психический и неврологический распад) и, кроме того, пересадка не позволяет восстановить уже утраченный функциональный статус. Проводится также поддерживающая симптоматическая терапия, – в частности, для профилактики эпилептиформных приступов.
Исследования этиопатогенетических механизмов и, соответственно, разработка этиопатогенетических терапевтических стратегий (направленных на устранение первопричин) продолжаются. Однако на сегодняшний день лейкодистрофия остается тяжелым инвалидизирующим заболеванием с неблагоприятным прогнозом.