левокарнил или элькар что лучше
Коррекция функциональных изменений сердечно-сосудистой системы препаратом L-карнитина у детей и подростков с сочетанной патологией
В современных условиях недостаточное потребление микронутриентов, воздействие на организм, особенно растущий, гипоксии различного генеза формируют высокий риск нарушений возрастного развития и повышенной заболеваемости у детей
В современных условиях недостаточное потребление микронутриентов, воздействие на организм, особенно растущий, гипоксии различного генеза формируют высокий риск нарушений возрастного развития и повышенной заболеваемости у детей [24]. Особое место среди этих патофизиологических факторов занимает тканевая гипоксия, возникающая в результате нарушения процессов биологического окисления, ключевые этапы которого происходят в митохондриях [1, 14, 15, 19, 20]. Митохондриальные нарушения полиморфны и могут иметь различные варианты и степень клинической выраженности: от минимальных до грубых, угрожающих жизни изменений. Результатом тканевой гипоксии являются нарушения синтеза АТФ, транспорта энергии от места продукции к эффекторным структурам клеток, нарушение утилизации энергии АТФ [8, 11, 20, 21].
Многочисленные клинические исследования, проведенные в последние годы, свидетельствуют о том, что относительная недостаточность энергетического фона может наблюдаться и у практически здоровых лиц. При этом скрытые нарушения клеточной энергетики могут быстро декомпенсироваться, приводя к снижению активности ферментов митохондриальной дыхательной цепи, вследствие чего возникает широкий спектр метаболических функциональных нарушений, в том числе со стороны нервной и сердечно-сосудистой систем [2, 3, 16, 22, 23]. Поэтому в настоящее время в лечении различных патологических состояний у детей большое значение придается метаболической терапии. В связи с этим важен поиск и создание безопасных и эффективных лекарственных средств комплексного воздействия на обмен веществ. К таким препаратам относят карнитин — низкомолекулярное соединение, производное аминомасляной кислоты, содержащееся во всех органах, особенно в больших количествах в тканях с необходимостью высокого энергетического обеспечения — мышцах, миокарде, мозге, печени, почках [1, 2, 6, 10, 11, 20]. Существуют две изомерные формы карнитина: D- и L-изомеры. В тканях млекопитающих присутствует только L-изомер, выполняющий в организме несколько функций: энергетическую (участвует в катаболизме липидов с образованием большого количества АТФ, модулируя внутриклеточный гомеостаз кофермента А с образованием свободного коэнзима А) и дезинтоксикационную (выводит из организма в виде ацилкарнитина соединения, обладающие мембранотоксическим и ингибирующим активность некоторых ферментов действием).
По данным многих клинических исследований, основными клиническими признаками дефицита L-карнитина являются быстрая утомляемость и снижение работоспособности; мышечная слабость, гипотония и гипотрофия, отставание физического развития; задержка психомоторного развития, снижение школьной успеваемости, сонливость или раздражительность; нарушение функции сердца вплоть до кардиомиопатии; увеличение размеров печени и нарушение ее функции [8, 9, 14–19].
Потребность в L-карнитине индивидуальна, а при умственных, физических и эмоциональных нагрузках повышается в 4–20 раз. Обычный пищевой рацион, включающий продукты животного происхождения, покрывает потребность в L-карнитине лишь на 25%, поэтому очевидна необходимость использования дополнительных источников L-карнитина для обеспечения оптимальной физиологической потребности.
В настоящее время появился новый источник L-карнитина — биологически активная добавка к пище Карнитон, зарегистрированная Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека. В состав препарата Карнитон аминокислота карнитин входит в форме L-карнитина тартрата, который наиболее полно усваивается организмом; в 1 мл препарата содержится 500 мг L-карнитина.
Целью данной работы явилась оценка эффективности влияния применения препарата Карнитон на состояние сердечно-сосудистой системы у детей и подростков с сочетанной соматической патологией в период реабилитации после частых респираторных заболеваний.
Работа осуществлялась под руководством сотрудников кафедры педиатрии МГМСУ на базе детского кардиологического санатория «Быково» МВД России.
В несравнительное исследование был включен 71 ребенок от 9 до 14 лет (34 мальчика и 37 девочек), находившийся в санатории в период с ноября 2009 года по январь 2010 года. Критериями отбора явились наличие жалоб вегетативного характера, изменения на стандартной электрокардиограмме (ЭКГ), эхокардиографии (ЭХО-КГ). Всем детям в течение 30 дней в первую половину дня назначался препарат Карнитон в возрастной дозе. В период лечения другие энерготропные и кардиотрофические препараты не назначались. С целью коррекции вегетативных изменений применялась немедикаментозная терапия (режим, прогулки, лечебная физкультура; физиотерапевтическое лечение, включающее массаж и водные процедуры). Нами не было зафиксировано ни одного случая аллергической реакции, непереносимости или отказа от приема препарата Карнитон. Назначение энерготропной терапии в первой половине дня было обусловлено возбуждающим нервную систему действием, что может вызывать трудности засыпания при вечернем приеме [6, 17, 20, 22].
Эффективность терапии препаратом Карнитон оценена по данным опроса детей, результатам стандартной ЭКГ и ЭХО-КГ после курса лечения. Статистический анализ результатов проведен стандартными методами. Степень достоверности количественных показателей оценивалась по t-критерию Стьюдента. Статистически значимыми считали различия при величине p ≤ 0,05.
Обследование включало физикальный осмотр, анализ генеалогического анамнеза, клинико-анамнестических данных, общеклинические исследования, стандартную ЭКГ, ЭХО-КГ с оценкой результатов в соответствии с нормативными показателями, применяемыми в педиатрии [4]. Оценка умственной работоспособности проводилась по методике Э. Крепелина, физическая работоспособность — по пробе с дозированной физической нагрузкой.
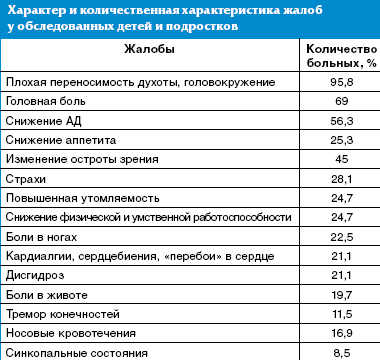
Характер жалоб у детей и подростков носил неспецифический характер, при этом наиболее часто отмечались головокружения и плохая переносимость духоты (95,8% детей), головная боль (69%), снижение артериального давления (АД) — у 56,3% пациентов. У каждого четвертого ребенка отмечались снижение аппетита, повышенная утомляемость со снижением физической и умственной работоспособности, у каждого пятого — или повышенная утомляемость, и/или кардиалгии, и/или дисгидроз, что расценивалось как проявление перманентного течения синдрома вегетативно-сосудистой дистонии (табл.).
Отмечены жалобы на нарушения сна, ночные страхи — у 28,1% пациентов, боли в ногах (22,5%), носовые кровотечения — у 16,9% обследованных. Особое внимание обращалось на детей с вегетативными пароксизмами в анамнезе, симптомами которых были боли в животе, тремор конечностей, синкопальные состояния. Всем детям с синкопальными состояниями ранее проводилось электроэнцефалографическое исследование, и было исключено органическое поражение головного мозга.
При физикальном осмотре патология опорно-двигательного аппарата в виде нарушения осанки, в том числе рахитически измененная (килевидная) грудная клетка (4,2% детей), выявлена у 98,7% больных. Снижение массы тела до 10-го центиля отмечено у 30% детей, избыточная масса — у 7%. При аускультации у 84% пациентов выслушивался низкотембровый систолический шум на верхушке и в V-точке. В процессе обследования исключена органическая патология сердечно-сосудистой, нервной систем. Анализ анамнестических, клинико-инструментальных данных свидетельствовал о том, что изменения сердечно-сосудистой системы носили вторичный характер, обусловленный нарушением вегетативной регуляции, наличием очагов хронической инфекции в носоглотке, полости рта, нарушением двигательного режима, что было выявлено практически у всех обследованных детей. Среди сопутствующих заболеваний наиболее часто встречались миопия (45%), аллергические заболевания, в том числе бронхиальная астма (22,5%), реже отмечались хронический гастродуоденит (6%), хронические запоры (4%).
При стартовом обследовании стандартной ЭКГ изменения зарегистрированы у всех детей. В 71,8% случаев отмечено вертикальное, а в 15,5% — горизонтальное расположение электрической оси сердца. У большинства детей (56,3%) выявлены нарушения автоматизма сердца в виде синусовой брадикардии (45%), эктопического ритма (14%), синусовой тахикардии (9,9%). Нарушения возбудимости сердца зарегистрированы у 45% пациентов, нарушения проводимости в виде атриовентрикулярной блокады (АВБ) I степени отмечены у 4,2%. Эти данные свидетельствуют о выраженных влияниях парасимпатического отдела на сердечно-сосудистую систему у обследованных детей и подростков, что согласуется с характером жалоб, предъявляемых пациентами.
После курса лечения препаратом Карнитон было отмечено статистически значимое (p
Т. И. Рычкова*, кандидат медицинских наук, доцент
И. П. Остроухова*, кандидат медицинских наук
С. А. Яцков**
Л. К. Акулова**
Т. М. Васильева*
* МГМСУ, Москва
** Детский кардиологический санаторий «Быково» МВД России, Московская область
Заботливым мамам
Значение L-карнитина для роста и развития детей

У детей раннего возраста ввиду несовершенства системы биосинтеза собственный синтез л-карнитина покрывает только 1% от его необходимого количества. Только после 15 лет начинает функционировать эндогенный синтез L — карнитина в полной мере.
Суточная норма потребления L-карнитина для детей в зависимости от возраста составляет:
Нормальное обеспечение организма ребенка л-карнитином способствует правильному росту и нормальному развитию жизненно-важных органов: сердца, скелетных мышц, центральной и вегетативной нервных систем, мозга, почек, иммунной системы, при этом для детей, занимающихся спортом, дополнительно берущих уроки у репетитора, находящихся в процессе восстановления после болезни, L-карнитин требуется в гораздо большем количестве.
Симптомы недостатка L-карнитина у детей
Если в организме ребенка наблюдается недостаток л-карнитина, у него отмечаются:
Можно ли устранить недостаток левокарнитина? Ответ однозначный: можно, дополнительным источником L-карнитина для детей является препарат Элькар.
Устранение недостатка L-карнитина: с какого возраста начинать?

Для детей предпочтителен прием л-карнитина в виде раствора, поскольку так препарат лучше усваивается и не вызывает сложностей приема, особенно у маленького ребенка. Таким препаратом является Элькар – раствор для приема внутрь, который выпускается во флаконах по 25, 50 и 100 мл с удобными дозирующими устройствами для детей разных возрастов. В одном миллилитре препарата содержится 300 мг l-карнитина. Элькародин – один из немногих лекарственных препаратов, разрешенных для применения детям с рождения. Препарат отпускается без рецепта врача. Элькар необходим для роста и гармоничного развития ребенка:
Все это связано со свойствами препарата повышать образование энергии в клетках, улучшать усвоение белков, витаминов, жиров.
Эффективность и безопасность препарата Элькар доказана многолетним опытом его клинического применения и положительными отзывами мам, выбирающих Элькар для детей.
Производство препарата на основе L-карнитина Элькар
Копирование материала только с разрешения правообладателей.
Применение карнитина (Элькар) в клинической практике
Камчатнов Павел Рудольфович
доктор медицинских наук, профессор кафедры неврологии и нейрохирургии лечебного факультета ГОУ ВПО Российского Государственного Медицинского Университета им. Н. И. Пирогова
В методическом пособии автор подробно рассказывает об эффектах и механизмах действия L-карнитина, освещает возможности применения L-карнитина (Элькар ® ) в клинической практике.
Пособие предназначено для неврологов, кардиологов, эндокринологов, врачей общей практики и врачей других специальностей.
СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О ФУНКЦИЯХ И МЕХАНИЗМАХ ДЕЙСТВИЯ КАРНИТИНА
Большинство клеток организма млекопитающих обладают способностью синтезировать эндогенный карнитин, который вырабатывается в течение всей жизни в количествах, необходимых для выполнения своих функций, поддержания метаболических процессов на данном уровне развития ткани и её сохранности. Мозговая ткань богата карнитином, причем, концентрация его достаточно высока в различных отделах центральной нервной системы, характеризующихся различной функциональной активностью (гипоталамус, мозжечок, кора, спинной мозг и др.) на фоне его низкого содержания в некоторых других тканях и плазме крови [22, 30].
Существуют два изомера карнитина – право- и левовращающий (D- и L-формы), обладающие различными химическими и биологическими свойствами. Считается, что в организме человека и животных присутствует L-карнитин, который и является биологически активным и безопасным в применении [8].
Одна из основных функций, выполняемая в организме L-карнитином – обеспечение транспорта свободных жирных кислот из цитозоля в митохондрии. По своим химическим свойствам свободные жирные кислоты метаболически инертны и не могут подвергаться никаким биохимическим превращениям до тех пор, пока не будут активированы. Активация свободных жирных кислот происходит на наружной поверхности митохондриальной мембраны при участии коэнзима А в присутствии ионов магния и АТФ. На наружной поверхности мембраны митохондрии находится фермент ацил-коэнзим А-синтетаза, катализирующий реакции, в ходе которых L-карнитин образует промежуточные соединения ацилкарнитина. Именно L-карнитин обеспечивает поступление в митохондрии активированных свободных жирных кислот, обеспечивая их проникновение через внутренний слой мембраны. Считается, что данным путем в митохондрии поступают преимущественно длинноцепочечные жирные кислоты. В последующем, после проникновения в митохондрии, L-карнитин высвобождается из этих соединений на внутренней стороне митохондриальной мембраны; в процессе транспорта принимают участие такие ферменты, как карнитин-транслоказа и карнитин-ацетилтрансферазы [21]. Жирные кислоты, поступающие таким образом в митохондрии, используются в системе бета-окисления, которое по своей эффективности продукции энергии близка к циклу трикарбоновых кислот (цикл Кребса). Одним из основных продуктов бета-окисления жирных кислот является ацетил-коэнзим А, большая часть которого поступает в цикл Кребса, а меньшая транспортируется из митохондрий в цитоплазму, где участвует в ряде пластических процессов. В частности, в цитоплазме клеток мозга ацетил-коэнзим А вовлечен в синтез свободных жирных кислот, образование мембран клеток глии и нейронов [14]. Имеются данные о том, что L-карнитин принимает участие и в транспорте части внутримитохондриального ацетил-коэнзима А в цитозоль клетки.
Результаты многочисленных экспериментальных исследований позволили установить, что L-карнитин абсолютно необходим для осуществления нормальных функций митохондрий и дефицит его может вызывать серьезные негативные последствиями как для клетки, так и для организма в целом [27, 60]. В условиях метаболического стресса в митохондриях накапливается ацил-коэнзим А, баланс которого со свободным коэнзимом поддерживается за счет работы карнитинового челнока [32]. Избыточное накопление в митохондриях ацил-коэнзима А ведет к угнетению скорости фермент-зависимых процессов окислительного метаболизма в различных тканях организма [47]. Повышение концентрации карнитина приводит к уменьшению соотношения ацил-коэнзим А / коэнзим А, обеспечивая возможность для нормального функционирования митохондриальных энзимов [44]. Если активность карнитин-ацетилтрансферазы снижается, в частности, в условиях окислительного стресса, наблюдается снижение мембранного потенциала митохондрий, изменение их структуры с уменьшением содержания некоторых фосфолипидов [41].
Все больший интерес привлекает возможность применения L-карнитина в клинической практике, изучаются различные аспекты его влияния на биохимические процессы, протекающие в организме. Накопленные данные свидетельствуют о том, что разнообразные эффекты L-карнитина не могут быть объяснены только его влиянием на энергетический метаболизм [19]. На протяжении последних 10 лет детально изучается способность L-карнитина уменьшать последствия повреждающего действия на клетку и ее органеллы свободных радикалов, что в значительной степени объясняет протективный эффект препарата при целом ряде заболеваний.
Экспериментальные данные о защитном действии L-карнитина на органеллы, в первую очередь – митохондрии, не ограничивается подавлением процессов перекисного окисления липидов. Оказалось, что L-карнитин предотвращает повреждающее действия такого мощного нейротоксина, как МФТП (1-метил-2фенилпиридин) [72].
Исключительный интерес вызывает способность L-карнитина предотвращать индукцию апоптоза. Ее экспериментальное подтверждение было получено в условиях применения ототоксического препарата гентамицина, при введении которого поражение нервных волокон и развивающаяся глухота обусловлены включением механизмов апоптоза [37]. Введение L-карнитина экспериментальным животным, подвергшимся воздействию гентамицина, предупреждает развитие глухоты. Введение препарата сопровождается угнетением активности проапототического факторы Harakiri (Hrk), экспрессия которого регулируется митоген-активируемой протеинкиназой. Полученные данные позволили авторам рассматривать регуляцию факторов апоптоза как один из ведущих механизмов действия L-карнитина.
Учитывая, что одним из важных продуктов метаболизма L-карнитина является ацетил-L-карнитин, интерес представляет возможность регуляции клеточных функций, осуществляемая этим веществом. В условиях экспериментальной церебральной гипоксии предварительное введение ацетил-L-карнитина значительно ослабляет повреждающее действие дефицита кислорода [12]. Зарегистрированное на фоне введения препарата уменьшение активности каспазы-3, цитохрома С, экспрессии белка Bcl-2 носило дозозависимый характер и было связано с угнетением апоптоза. Предварительное введение ацетил-L-карнитина сопровождалось активацией нейропротекторных механизмов, в частности, повышением синтеза фактора роста нервов и тирозинкиназы А, что обеспечивало увеличение фосфорилирования внеклеточной сигнал-регулируемой киназы и повышало выживаемость клеток. Полученные данные свидетельствуют о том, что нейропротективное действие ацетил-L-карнитина реализуется не только за счет восполнения дефицита субстратов окисления, нормализации синтеза нейротрансмиттеров, но и за счет активации защитных механизмов, связанных с фосфорилированием регуляторных белков.
Нейропротективные свойства присущи не только ацетил-L-карнитину, но и другим эфирам L-карнитина, в частности, пропионил-L-карнитину [10]. Вводимый внутрибрюшинно экспериментальным животным он способствовал сохранности синтеза АТФ, активности глютатиона и поддержанию целостности нейронов. Введение обоих эфиров L-карнитина приводило к значительному угнетению интенсивности перекисного окисления липидов.
Одним из серьезных последствий оксидантного стресса является нарушение функции эндотелия. Даже в тех случаях, когда эндотелиальная дисфункция возникает в силу воздействия другой причины, пути ее реализации во многом опосредованы выработкой высокоактивных свободных радикалов. Способность карнитина улучшать нарушенную функцию эндотелия, продемонстрированная в эксперименте, может быть обусловлена его способностью устранять последствия оксидантного стресса. Применение L-карнитина сопровождается снижением как в тканях, так и в крови концентрации маркеров воспаления. У экспериментальных крыс с артериальной гипертензией определялось содержание некоторых цитокинов, продуктов метаболизма ангиотензиновых рецепторов в миокарде и сыворотке крови на фоне системного введения L-карнитина [52]. При этом регистрировалось снижение артериального давления и достоверное уменьшение концентрации интерлейкина (ИЛ) 1-бета, ИЛ-6 и фактора некроза опухоли альфа. Введение L-карнитина вызывало нормализацию содержания в крови ангиотензинпревращающего фермента и фрагмента рецептора ангиотензина АТ1R, экспрессия которых возрастала у животных с экспериментальной гипертензией. Систематическое применение L-карнитина приводит к ослаблению неспецифических воспалительных процессов в организме больных с артериальной гипертензией и обеспечивает снижение избыточной активности ренин-ангиотензиновой системы.
У животных со стрептозоцин-индуцированным сахарным диабетом с повышенным уровнем холестерина, триглицеридов и продуктов перекисного окисления липидов в крови, применение L-карнитина на протяжении 2 недель привело к нормализации этих показателей [34]. Наряду с этим восстанавливалась эндотелий-зависимая вазодилатация в ответ на введение ацетилхолина. Установлен положительный эффект введения L-карнитина у новорожденных животных, подвергнутых действию ишемии и гипоксии [71]. Выраженный эффект L-карнитина у новорожденных может быть обусловлен отсутствием у них системы его синтеза и зависимостью от поступления L-карнитина извне [25]. В этих условиях возможно развитие карнитиновой недостаточности – увеличение содержания эфиров ацил-коэнзима А при снижении концентрации L-карнитина, состояния, коррегируемое введением L-карнитина [51].
Применение L-карнитина уменьшает выраженность повреждения нервной системы не только при ишемическом поражении, но и при гипергликемии или гипогликемии. Экспериментальным животным на протяжении 1 недели вводили L-карнитин, после чего внутрибрюшинно вводились 20 ЕД инсулина, вызывая гипогликемию [38]. Предварительное применение L-карнитина сопровождалось большей функциональной сохранности головного мозга, о чем свидетельствовали более высокие показатели состояния когнитивных функций. Механизмами защитного действия L-карнитина оказались угнетение процессов перекисного окисления липидов, сохранность митохондрий и нейронов в целом.
КЛИНИЧЕСКОЕ ПРИМЕНЕНИЕ КАРНИТИНА
Сердечно-сосудистые и цереброваскулярные заболевания
Накоплен значительный клинический опыт применения L-карнитина у пациентов с заболеваниями сердечно-сосудистой системы и сосудистым поражением головного мозга. Большой практический интерес вызывает влияние карнитина на функцию эндотелия. Имеются многочисленные сведения о том, что эндотелиальная дисфункция является одной из основных причин ишемического поражения различных органов, в том числе, головного мозга.
Положительные результаты экспериментальных исследований способности карнитина устранять или уменьшать выраженность эндотелиальной дисфункции явились основанием для изучения возможности применения препарата у людей. Так, интересные результаты были получены при изучении поток-зависимой вазодилатации (широко используемый маркер функции эндотелия) у здоровых лиц, получавших с пищей избыточное количество жиров [70]. После рандомизации в две группы, в условиях двойного слепого эксперимента испытуемые получали L-карнитин (2 г в сутки на протяжении 3 недель) или плацебо. Поток-зависимая вазодилатация изучалась на плечевой артерии натощак и после приема унифицированной пищи с высоким содержанием жира. У испытуемых, получавших плацебо, через 1,5 часа после еды регистрировалось достоверное снижение пиковой скорости кровотока, тогда как прием L-карнитина сопровождался значительным приростом скорости кровотока при проведении пробы после приема пищи.
Итогом экспериментальных исследований и клинических испытания на здоровых добровольцах явилось изучение возможности применения L-карнитина у пациентов с артериальной гипертензией. Такое двойное слепое исследование было проведено среди пациентов с ИБС и артериальной гипертензией, основная группа которых получала на протяжении 8 недель комбинацию ацетил-L-карнитина и альфа-липоевой кислоты, а контрольная группа – плацебо [50]. Оказалось, что уровень давления в основной группе больных к окончанию исследования был достоверно ниже, чем в контроле, при этом достоверное снижение регистрировалось как у пациентов с исходно наиболее высоким его уровнем, так и у больных с метаболическим синдромом. Важно также, что применение указанных препаратов сопровождалось дилатацией плечевой артерии и снижением ее тонуса, что отражает уменьшение выраженности явления эндотелиальной дисфункции.
Имеющиеся данные о том, что применение L-карнитина ассоциировано с нарастанием мышечной силы в нижних конечностях и увеличением способности к ходьбе у пациентов со стенозирующим поражением периферических артерий могут быть объяснены именно с учетом восстановления функции эндотелия, хотя не исключены и иные механизмы реализации клинических эффектов препарата [18]. В целом, результаты серии исследований подтверждают эффективность применения L-карнитина у больных со стенозирующим поражением периферических артерий [33].
Накоплен значительный опыт применения L-карнитина у пациентов с различными формами ишемической болезни сердца. В результате проведенного обзора значительного количества исследований было установлено, что применение препарата у пациентов со стабильной стенокардией приводит к уменьшению выраженности депрессии сегмента ST и нормализации конечно-диастолического давления в левом желудочке сердца. Одним из объяснений этого эффекта может служить снижение уровня лактата в миокарде в условиях физической нагрузки [29]. В указанном обзоре приведены данные о рандомизированном мультицентровом исследовании, в которое были включены 472 пациента, перенесших острый инфаркт миокарда или операцию аортокоронарного шунтирования. В острой стадии заболевания на протяжении 5 дней пациенты получали 9 мг/кг в сутки L-карнитина, а в последующем – по 6 г в сутки (per os) на протяжении 12 месяцев. Более выраженный эффект в виде уменьшения выраженности дилатации левого желудочка, предупреждения ремоделирования миокарда имел место у больных, перенесших острый инфаркт. Важно также, что в этой группе уменьшалась частота развития застойной сердечной недостаточности и смерти от заболеваний сердечно-сосудистой системы. Авторы анализа рассматривают возможные механизмы эффективности препарата, в частности, нормализацию энергопродукции, снижение концентрации свободных жирных кислот, являющихся субстратом для образования свободных радикалов, обеспечение сохранности органелл и клеточных мембран. Большое значение имеет предупреждение фатальных аритмий, спровоцированных ишемией миокарда и дисметаболическими нарушениями [40].
Большой интерес исследователей привлекает проблема воздействия на обмен веществ ишемизированной ткани мозга – метаболическая терапия. Имеются сведения о том, что коррекция энергетического метаболизма, подавление процессов перекисного окисления, устранение повреждающего действия возбуждающих нейротрансмиттеров и провоспалительных цитокинов, наряду с восстановлением кровотока, могут обеспечить уменьшение зоны ишемического повреждения, повысить выживаемость пациентов, уменьшить выраженность неврологического дефицита [5]. Перспективным направлением нейрометаболической терапии является применение карнитина, назначение которого обеспечивает уменьшение выраженности последствия тканевой гипоксии, улучшает состояние микроциркуляции, способствует активации энергетического метаболизма [4, 6, 7].
В Российской Федерации накоплен значительный опыт применения карнитина для лечения пациентов с острыми расстройствами мозгового кровообращения [4, 7]. Доказано, что внутривенное применение препарата приводит к значительному уменьшению выраженности очагового неврологического дефицита у пациентов с мозговым инсультом. Положительный эффект наблюдается вне зависимости от локализации очага поражения (каротидная или вертебрально-базилярная системы, глубинное или поверхностное расположение очага поражения). Важным свойством является возможность одновременного применения и других лекарственных препаратов, необходимых для лечения пациента с острым инсультом.
В острой стадии мозгового инсульта карнитин вводится из расчета 15-45 мг/кг массы тела в сутки, т.е., по 10 мл 10% раствора через каждые 8-12 часов [2]. Перед применением препарат разводится в 300-400 мл физиологического или изотонического раствора и вводится внутривенно капельно. Весь курс лечения составляет 10-20 введений. Помимо капельного, возможно внутривенное струйное медленное (на протяжении 2-3 мин.) введение препарата. Показаниями к применению карнитина являются ишемический или геморрагический инсульт, субарахноидальное кровоизлияние. Также препарат продемонстрировал свою эффективность у пациентов, перенесших остановку сердца, массивную кровопотерю, осложненный инфаркт миокарда с постгипоксической энцефалопатией с наличием очагового неврологического дефицита или когнитивного снижения.
Как было продемонстрировано рядом исследований, по миновании острого периода целесообразно повторное введение карнитина через 2-3 месяца. Проведение повторных курсов введения препарата необходимо сочетать с активным проведением реабилитационных мероприятий. Целесообразным представляется введением препарата из расчета 7-15 мг/кг массы тела на протяжении 5-10 дней. Следует, однако, отметить, что и суточная доза, и продолжительность курса лечения могут быть увеличены в зависимости от состояния пациента, выраженности неврологического дефицита, эффективности проводимого лечения.
Имеются убедительные подтверждения эффективности применения карнитина у больных не только с острыми, но и хроническими расстройствами мозгового кровообращения, в частности, дисциркуляторной энцефалопатией, вертебрально-базилярной недостаточностью [4, 6, 9]. Длительность курса лечения и суточные дозы карнитина определяются индивидуально. Одновременно необходимо проведение лечения и обеспечение мероприятий вторичной профилактики цереброваскулярных нарушений, направленные на устранение имеющихся факторов сердечно-сосудистого риска, в частности, коррекцию уровня артериального давления, липидного и углеводного состава крови и пр.
Влияние L-карнитина на состояние когнитивных функций у больных с хроническими расстройствами мозгового кровообращения в рамках дисциркуляторной энцефалопатии, и также лакунарными инфарктами, развившимися на фоне сахарного диабета, изучалось в ходе открытого рандомизированного исследования, наряду с L-карнитином больные получали милдронат [9]. Полученные данные позволили констатировать улучшение на фоне проводимой терапии абстрактного и конкретного мышления, памяти. По мнению авторов, клинические эффекты были обусловлены ингибированием процессов перекисного окисления липидов, а также нормализацией уровня глюкозы крови, наблюдавшейся на фоне применения L-карнитина (у части пациентов оказалось возможным уменьшение дозы принимаемых сахароснижающих препаратов).
Особый интерес вызывает возможность применения карнитина у пациентов, которым предстоит обширное хирургическое вмешательство с высоким риском интароперационной гипоксии, расстройств системной гемодинамики. Целью применения карнитина в данной ситуации является снижение чувствительности головного мозга к гипоксии. Введение препарата начинается за 2-3 суток до операции, ежедневно вводится по 1000 мг карнитина, при необходимости применение препарата может быть продолжено и постоперационном периоде [3].
Имеются сообщения о возможности применения L-карнитина у пациентов с синдромом MELAS (генетически детерминированная митохондриальная миопатия, энцефалопатия, лактатацидоз и инсультоподобные эпизоды) [26]. Применение L-карнитина в комплексе с другими препаратами, оказывающими влияние на тканевой метаболизм и тем самым способствующих устранению имеющегося биохимического дефекта, приводит к регрессу имеющегося неврологического дефицита. К сожалению, небольшое количество наблюдений и относительная редкость синдрома не позволяют обеспечить возможность проведения достаточно большого исследования для определения истиной эффективности L-карнитина.
Когнитивные нарушения и деменция
Когнитивные нарушения и наиболее выраженная их стадия – деменция являются весьма актуальной проблемой неврологии в силу широкого распространения, трудностей и высокой стоимости терапии. Среди широкого спектра лекарственных препаратов, патогенетически обоснованным способом лечения, эффективность которого получила подтверждение в серии клинических испытаний, является применение ингибиторов ацетилхолинэстеразы.
Исходя из указаний на возможную роль L-карнитина в восполнении дефицита ацетилхолина при некоторых патологических состояниях, были предприняты попытки использовать препарат для восстановления пула нейротрансмиттеров и устранения когнитивного дефицита. Так, например, применение L-карнитина у животных с токсической моделью деменции привело к частичному восстановлению когнитивных функций после применения L-карнитина, причем положительный эффект был близок к тому, который достигался при применении ростовых факторов [11].
Было проведено исследование, посвященное определению концентрации в спинномозговой жидкости и в плазме крови у пациентов с болезнью Альцгеймера и здоровых лиц сопоставимого возраста (контрольная группа) свободного карнитина и ацилкарнитина [61]. Оказалось, что в спинномозговой жидкости концентрации указанных веществ существенным образом не отличались, тогда как у пациентов с болезнью Альцгеймера содержание L-карнитина в плазме оказалось существенно ниже. Примечательно, что имелась тенденция к увеличению отношения карнитин/ацилкарнитин у пациентов с болезнью Альцгеймера, что может быть обусловлено низкой активностью карнитин-ацетилтрансферазы. Интересно, что концентрация L-карнитина в спинномозговой жидкости не отличалась у здоровых людей и у пациентов с болезнью Паркинсона, а также не была связана с длительностью заболевания, его тяжестью, приемом противопаркинсонических препаратов [36]. Имеются данные о том, что применение ацетил-L-карнитина способно в определенной степени также отсрочить наступление тяжелой деменции у пациентов с умеренными когнитивными нарушениями [49]
Эффективность применения ацетил-L-карнитина в качестве средства, способного улучшать состояние когнитивных функций, изучена в ходе мета-анализа серии исследований, выполненных двойным слепым способом [53]. Длительность наблюдения составила не менее трех месяцев. Оказалось, что в группе активного лечения имелось достоверно более выраженное улучшение состояния, в частности, по Шкале общего впечатления, а также по комплексу психометрических тестов. Авторы отмечают очень хорошую переносимость препаратов. Проводимая терапия, несомненно, оказывала положительный эффект, который заключался в большей сохранности когнитивных функций, замедлении процессов развития деменции по сравнению с контрольной группой (на протяжении 12 месяцев получали плацебо).
Сходное по своему дизайну исследование возможности применения ацетил-L-карнитина у пациентов с умеренно выраженными когнитивными нарушениями вследствие болезни Альцгеймера позволило ответить на вопрос о том, насколько эффективна терапия в отношении замедления развития тазовых нарушений. Исследование продолжалось на протяжении 12 месяцев, больные контрольной группы получали плацебо. Оказалось, что в обеих группах к концу 12 месяца имело место прогрессирующее когнитивное снижение. Вместе с тем, более выраженный характер оно носило у пациентов, получавших плацебо. Важно также, что своевременное лечения оказалось тесно взаимосвязанным с выраженностью неврологической симптоматики. Имеющиеся данные о положительном эффекте ацетил-L-карнитина у больных с когнитивными расстройствами позволяют предполагать возможность достижения положительного эффекта при назначении L-карнитина пациентам с додементными формами заболевания.
Серьезной клинической проблемой является сочетание сахарного диабета, метаболического синдрома и хронических прогрессирующих поражений головного мозга. На сегодняшний день хорошо установлено, что сахарный диабет является важным фактором риска развития как острых, так и хронических нарушений мозгового кровообращения. У пациентов с нарушениями углеводного обмена значительно раньше дебютируют когнитивные расстройства, и чаще наступает развитие деменции, причем, в ее формировании, помимо собственно сосудистых нарушений, принимает участие и нейродегенеративный процесс.
Учитывая эффективность L-карнитина в отношении угнетения перекисного окисления липидов, положительного влияния на углеводный обмен, со значительным оптимизмом рассматривается возможность его применения у пациентов с сахарным диабетом и метаболическим синдромом с целью предупреждения (или минимизации) поражения головного мозга. В качестве возможных защитных механизмов действия препарата предполагаются нормализация уровня липидов в виде уменьшение концентрации триглицеридов, лептина, снижение массы тела, возможно, некоторые другие факторы [24]. Серьезное значение имеет тот факт, что в некоторых популяциях, в частности, в корейской, нарушение обмена глюкозы тесно ассоциированы с расстройствами липидного обмена и дефицитом L-карнитина. В этой связи большой интерес представляют данные о том, что добавление в пищу L-карнитина и антиоксидантов обеспечивает изменение метаболизма в виде усиления катаболизма липидов, в особенности, в условиях адекватных физических нагрузок [39].
Изучение влияния применения L-карнитина (по 1 г 3 раза в сутки на протяжении 12 недель) проведено в группе больных сахарным диабетом 2 типа [57]. Оказалось, что назначение L-карнитина сопровождалось достоверным снижением концентрации глюкозы крови, притом, что в крови снижалась концентрация триглицеридов, а уровень общего холестерина, холестерина липопротеидов высокой и низкой плотности, гликированного гемоглобина оставался стабильным.
Нейродегенеративные заболевания.
Накоплен определенный опыт изучения нарушений обмена L-карнитина у пациентов с различными нейродегенеративными заболеваниями с преимущественным поражением головного мозга. Одним из наиболее тяжелых нейродегенеративных заболеваний, приводящих к выраженному прогрессирующему поражению головного мозга, является атаксия Фридрейха. Механизмы развития этого генетически детерминированного заболевания достаточно сложны, однако, на сегодняшний день имеются убедительные сведения о том, что ключевую роль в его развитии играют расстройства окислительного фосфорилирования. В проведенном пилотном исследовании, в которое были включены пациенты с установленным диагнозом атаксии Фридрейха, применение L-карнитина на протяжении четырех месяцев сопровождалось увеличением запаса в тканях фосфокреатина (определялся методом МР-спектроскопии), хотя выраженность неврологического дефицита при этом существенно не изменялась [62]. Полученные авторами данные позволяют считать перспективным изучение возможности применения L-карнитина у пациентов с атаксией Фридрейха. Необходимо отметить, что, учитывая роль нарушений энергопродукции в патогенезе заболевания, была предпринята попытка использования в лечебных целях у данной группы больных ацетил-L-карнитина [64]. После проведенного 6-месячного курса применения препарата было установлено, что на фоне лечения уменьшились выраженность атактических расстройств и снизились темпы прогрессирования заболевания.
Печеночная энцефалопатия
Печеночная энцефалопатия, как правило, является следствием цирроза печени и характеризуется прогрессирующими когнитивными нарушениями, расстройствами нервно-мышечной передачи и, в тяжелых стадиях, угнетением сознания. Важную роль в патогенезе печеночной энцефалопатии играет накопление в нервной ткани аммиака, приводящее к нарушению нейротрансмиттерного баланса, нарушению функции гематоэнцефалического барьера, отеку головного мозга [17, 43]. Избыток аммиака ферментативным путем связывается с глутаматом, вследствие чего образуется глутамин, наиболее активно процесс протекает в мышечной ткани и головном мозге [13]. Считается, что ведущей причиной отека клеток является накопление в астроцитах глутамина – продукта детоксикации аммиака [17]. Основным механизмом действия L-карнитина является стимулирование образования мочевины и снижение концентрации аммиака в тканях организма, в том числе, в головном мозга [48]. Определенную роль также может играть способность L-карнитина поддерживать энергетический метаболизм клетки за счет обеспечения образования ацетил-коэнзима А в митохондрии, доставки субстратов окисления в цикл Кребса и активации механизмов бета-окисления. Одним из свидетельств эффективности L-карнитина в условиях гипераммонемии является снижение в спинномозговой жидкости концентрации аланина и лактата, что отражает восстановление митохондриального дыхания и адекватность процессов элиминации аммиака [68].
Результаты серии экспериментальных исследований позволили установить, что введение лабораторным животным L-карнитина приводит к значительному снижению как в крови, так и в твердых тканях организма (в том числе – в мозге) концентрации аммиака [67]. Несколько позже была подтверждена эффективность применения L-карнитина у пациентов с печеночной энцефалопатией, проявляющейся, в частности, когнитивными нарушениями [46]. Клинические исследования подтвердили эффективность L-карнитина в этих условиях, продемонстрировали способность препарата оказывать существенное положительное влияние на когнитивные функции при хорошей переносимости и минимуме побочных эффектов даже при длительном лечении [45].
Несомненный практический интерес представляет тот факт, что L-карнитин может быть использован для коррекции нарушений обмена аммиака ятрогенного характера. Известно, что применение некоторых лекарственных препаратов может сопровождаться гипераммонемией, в частности, таким эффектом обладают препараты вальпроевой кислоты. Применение L-карнитина позволяет нормализовать нарушения обмена мочевины, устраняя, тем самым, нежелательные побочные эффекты терапии [59]. Важным следствием лечения является сохранность функции печени, предположительно, обусловленная предупреждением поражения гепатоцитов [65]. Также представляется важным, что авторы не сообщают о том, что назначение L-карнитина приводит к снижению эффективность препаратов вальпроевой кислоты и ухудшению течения эпилепсии, что предоставляет возможности для клинического применения указанной комбинации препаратов. Имеются данные о том, что применение вальпроатов (как и карбамазепина) может приводить к разнообразным нарушениям метаболизма, в том числе к угнетению синтеза L-карнитина и снижению скорости утилизации имеющихся в организме глюкозы и свободных жирных кислот [35]. В определенной степени это может быть причиной увеличения массы тела у пациентов, длительное время принимающих противоэпилептические препараты. Высказывается предположение о возможной эффективности применения L-карнитина в этой ситуации.
Болевые синдромы
В 2008 году были опубликованы результаты мета-анализа серии из 15 исследований, посвященных применению нетрадиционных методов лечения у пациентов с нейропатическими болевыми синдромами [56]. Оказалось, что на сегодняшний день накоплены сведения о возможности такого эффекта у L-карнитина, что делает целесообразным дальнейшее изучение эффективности и целесообразности его применения у пациентов с нейропатическими болевыми синдромами в комплексе с лекарственными препаратами, применяемых при их купировании.