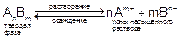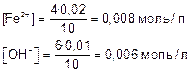что такое произведение растворимости
Произведение растворимости.
Произведение растворимости – величина, количественно характеризующая способность электролита растворяться в насыщенном растворе при данной температуре и произведение концентраций ионов есть величина постоянная.
Растворение твердого вещества в воде останавливается тогда, когда образуется насыщенный раствор, т.е. устанавливается равновесие между твердым веществом и частицами того же вещества, находящимися в растворе. Например, в насыщенном растворе хлорида серебра наблюдается равновесие:
И константа равновесия может быть записана следующим образом:
Скорости 2х противоположных направленных процессов – растворения и кристаллизации – пропорциональны площади поверхности твердого вещества. При достижении равновесия площади поверхности взаимно сокращаются. Поэтому именно эти концентрации записываются в выражении для константы равновесия.
Поэтому произведение растворимости ПР будет выглядеть так:
Произведения растворимости некоторых соединений.
Произведение растворимости для данного соединения можно определить по результатам измерения его растворимости и наоборот.
Рассмотрим пример расчета: необходимо вычислить растворимость AgCl. Обозначим искомую растворимость хлорида серебра через s, тогда разновесные концентрации также будут равны s:
Значение ПР – произведение равновесных концентраций ионов.
Произведение растворимости
Большинство веществ обладают малой растворимостью в воде и других растворителях. В насыщенном растворе малорастворимого электролита устанавливается гетерогенное равновесие между твердой фазой и ионами, образующимися при частичном растворении осадка.
Так, в насыщенном растворе электролита АnBm, находящегося в равновесии с его твердой фазой, будет протекать следующий обратимый процесс:
Этот процесс протекает на поверхности осадка. Состояние этого равновесия по закону действующих масс количественно характеризуется константой, называемой произведением растворимости (ПР):
В насыщенном растворе малорастворимого электролита произведение молярных концентраций ионов, возведенных в степени, равны их стехиометрическим коэффициентам, есть величина постоянная при данной температуре и называется произведением растворимости.
ПР зависит от природы растворителя и растворенного вещества, от температуры и не зависит от концентрации ионов в растворе.
Пример. Са3(РО4)2 « 3Са2+ + 2РО43–
Произведение растворимости и растворимость вещества являются характеристиками малорастворимого вещества, между этими величинами существует тесная связь.
Растворимость (S) – это максимально возможная концентрация вещества в растворе, выражается в г/л, г/100 г Н2О.
Молярная растворимость S совпадает с молярной концентрацией насыщенного раствора, выражается в моль/л и связана с ПР:
Для двухионных электролитов, например AgCl(n=1,m=1):
Для трехионных электролитов, например CaF2(n=1,m=2):
Следовательно, произведение растворимости и растворимость – взаимосвязанные величины, поэтому по известной растворимости вещества можно найти значение произведения растворимости и наоборот.
Вычисление произведения растворимости
малорастворимого электролита
При расчете произведения растворимости необходимо перевести в молярную растворимость (моль/л) растворимость, выраженную в г/л или г/100 г Н2О.
Для перехода растворимости, выраженной в г/100 г Н2О, к молярной концентрации можно принять объем насыщенного раствора »100 мл, учитывая малую растворимость электролита в Н2О.
Пример. Растворимость Mg(OH)2 при 18°С равна 0,012 г/л. Вычислите ПР(Mg(OH)2).
Молярная масса Mg(OH)2: М(Mg(OH)2)=58 г/моль. Рассчитаем молярную растворимость Mg(OH)2
S(Mg(OH)2) = L : M(Mg(OH)2) = 0,012 : 58 = 2,07•10–4 моль/л
Молярная растворимость совпадает с молярной концентрацией соли в растворе:
С(Mg(OH)2) = S(Mg(OH)2) = 2,07•10–4 моль/л
Найдем равновесные молярные концентрации ионов в растворе:
[Mg2+] = S =2,07•10–4 моль/л
[ОН–] = 2S = 2,07•10–4•2 = 4,14•10–4 моль/л
Тогда ПР(Mg(OH)2) = [Mg2+][OH–]2;
ПР(Mg(OH)2) = 2,07•10–4•(4,14•10–4)2 = 3,5•10–11
Вычисление концентрации ионов и растворимости
малорастворимого электролита в его насыщенном
растворе
Пример. Произведение растворимости PbJ2 при 18°С равно 1,4•10–8. Рассчитайте концентрации ионов Pb2+ и J– и молярную растворимость
Обозначим молярную растворимость соли – S моль/л. Тогда концентрации ионов равны:
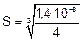
Молярная растворимость соли равна 1,5•10–3 моль/л.
Концентрации ионов равны:
[J–] = 2•1,5•10–3 = 3,0•10–3 моль/л.
Чтобы от молярной растворимости перейти к растворимости в г/л, необходимо молярную растворимость умножить на молярную массу вещества.
L = S•M(PbJ2) = 1,5•10–3•461 = 0,692 г/л.
Условия образования осадков
При проведении реакций в растворе, в результате которых возможно образование осадка, необходимо соблюдать определенные требования к выбору концентраций реагентов.
Условие образования осадка: произведение молярных концентраций ионов, возведенных в степень стехиометрических коэффициентов (ПК), должно быть больше величины произведения растворимости (ПР):
ПК(AnBm) = (CA+m)n•(CB–n)m > ПР(AnBm)
Если ПК(AnBm) Читайте также: Способы получения кислот
Ионно-молекулярное уравнение реакции
Для определения условия образования осадка необходимо рассчитать ПК
Для нахождения ПК нужно найти концентрации Fe2+ и ОН– после смешивания растворов заданной концентрации. Определяем исходные концентрации ионов до сливания растворов:
NaOH « Na+ + OH– [ОН–]=0,01 моль/л
0,01 моль/л 0,01 моль/л
Для определения концентрации ионов Fe2+ нужно перевести нормальную концентрацию FeSO4 в молярную.
fэк(FeSO4) = 1/2 0,04н FeSO4 = 0,02M FeSO4
0,02 моль/л 0,02 моль/л
Определяем концентрацию ионов после смешивания растворов.
Объем раствора после смешивания 4 мл FeSO4 и 6 мл NaOH стал 10 мл.
Концентрация ионов после смешивания растворов
Находим произведение концентраций
ПК(Fe(OH)2) = 0,008 • 0,0062 = 2,88•10–7
Сравниваем ПК с ПР (приложение, табл.3)
Следовательно при сливании 4 мл 0,004н. раствора FeSO4 и 6 мл 0,01М раствора NaOH образуется осадок Fe(OH)2.
Исходные данные и результаты расчета заносим в таблицу.
Произведение растворимости
Определение
Так как данная система находится в состоянии равновесия, то
ПР легко вычислить, зная раcтворимость соединения при данной t°.
Пример 1
Растворимость CaCO3 равна 0,0069 или 6,9
Решение
Выразим растворимость в молях:
SCaCO3 = (6,9
следовательно, ПРCaCO3 = [Ca 2+
Зная величину ПР, можно в свою очередь вычислить растворимость вещества в моль/л или г/л.
Пример 2
Произведение растворимости ПРPbSO4 = 2,2
Чему равна растворимость PbSO4?
Чтобы перейти к растворимости, выраженной в г/л, найденную величину умножим на молекулярную массу, после чего получим:
1,5
Образование осадков
Если
[Ag + ]
Осадок образуется в том случае, когда произведение концентраций ионов малорастворимого электролита превысит величину его произведения растворимости при данной температуре. Когда ионное произведение станет равным величине ПР, выпадение осадка прекращается. Зная объем и концентрацию смешиваемых растворов, можно рассчитать, будет ли выпадать осадок образующейся соли.
Пример 3
Выпадает ли осадок при смешении равных объемов 0,2 M растворов Pb(NO3)2 и NaCl.
ПРPbCl2
Решение
При смешении объем раствора возрастает вдвое и концетрация каждого из веществ уменьшится вдвое, т.е. станет 0,1 M или 1,0
Влияние концентрации растворов
Труднорастворимый электролит с достаточно большой величиной ПР нельзя осадить из разбавленных растворов. Например, осадок PbCl2 не будет выпадать при смешении равных объемов 0,1 M растворов Pb(NO3)2 и NaCl. При смешивании равных объемов концентрации каждого из веществ станут 0,1 / 2 = 0,05 M или 5
Влияние одноименного иона
Растворимость труднорастворимых электролитов понижается в присутствии других сильных электролитов, имеющих одноименные ионы. Если к ненасыщенному раствору BaSO4 понемногу прибавлять раствор Na2SO4, то ионное произведение, которое было сначала меньше ПРBaSO4 (1,1
Влияние температуры
ПР является постоянной величиной при постоянной температуре. С увеличением температуры ПР возрастает, поэтому осаждение лучше проводить из охлажденных растворов.
Растворение осадков
Правило произведения растворимости важно для переведения труднорастворимых осадков в раствор. Предположим, что надо растворить осадок BaСO3. Раствор, соприкасающийся с этим осадком, насыщен относительно BaСO3.
Это означает, что [Ba 2+
Таблица. Произведение растворимости (ПР) и растворимость при 25°С некоторых малорастворимых веществ
Факторы растворимости
Растворимость
Растворимость — это свойство вещества образовывать с различными растворителями гомогенные смеси. Количество растворяемого вещества, необходимое для получения насыщенного раствора и определяет растворимость этого вещества.
В связи с этим растворимость имеет ту же меру, что и состав, например, массовая доля растворенного вещества в его насыщенном растворе или количество растворенного вещества в его насыщенном растворе.
Все вещества с точки зрения его растворимости можно классифицировать на:
Известно, что если полярность растворяемого вещества схожа с полярностью растворителя, то оно скорее всего растворится. Если же полярности разные, то с большой долей вероятности раствора не получится. Почему же так происходит?
Процесс растворения
Полярный растворитель – полярное растворяемое вещество.
Для примера опишем раствор поваренной соли в воде. Как мы уже знаем, молекулы воды имеют полярную природу с частичным положительным зарядом на каждом атоме водорода и частичным отрицательным – на атоме кислорода. А твердые ионные вещества, вроде хлорида натрия, содержат катионы и анионы. Поэтому, когда поваренную соль помещают в воду, частичный положительный заряд на атомах водорода молекул воды притягивается отрицательно заряженным ионом хлора в NaCl. Аналогично, частичный отрицательный заряд на атомах кислорода молекул воды притягивается положительно заряженным ионом натрия в NaCl. И, поскольку притяжение молекул воды для ионов натрия и хлора сильнее взаимодействия, удерживающего их вместе, соль растворяется.
Неполярный растворитель – неполярное растворяемое вещество.
Попробуем растворить кусочек тетрабромида углерода в тетрахлориде углерода. В твердом состоянии молекулы тетрабромида углерода удерживаются вместе благодаря очень слабому дисперсионному взаимодействию. При помещению его в тетрахлорид углерода его молекулы будут располагаться более хаотично, т.е. увеличивается энтропия системы и соединение растворится.
Равновесия при растворении. Произведение растворимости
Рассмотрим раствор малорастворимого соединения. Для того, чтобы между твердым веществом и его раствором установилось равновесие, раствор должен быть насыщенным и соприкасаться с нерастворившейся частью твердого вещества.
Например, предположим, что равновесие установилось в насыщенном растворе хлорида серебра:
AgCl(тв)=Ag + (водн.) + Cl — (водн.)
Рассматриваемое соединение является ионным и в растворенном виде присутствует в виде ионов. Нам уже известно, что в гетерогенных реакциях концентрация твердого вещества остается постоянной, что позволяет включить ее в константу равновесия. Поэтому выражение для константы равновесия будет выглядеть следующим образом:
K = [Ag + ][ Cl — ]
Такая константа называется произведением растворимости ПР, при условии, что концентрации выражаются в моль/л.
ПР = [Ag + ][ Cl — ]
Произведение растворимости равно произведению молярных концентраций ионов, участвующих в равновесии, в степенях, равных соответствующим стехиометрическим коэффициентам в уравнении равновесия.
Следует отличать понятие растворимости и произведения растворимости.
Растворимость вещества может меняться при добавлении в раствор еще какого-либо вещества, а произведение растворимости не зависит от присутствия в растворе дополнительных веществ. Хотя эти две величины взаимосвязаны, что позволяет зная одну величину, вычислить другую.
Зависимость растворимости от температуры и давления
Вода играет важную роль в нашей жизни, она способна растворять большое количество веществ, что имеет большое значение для нас. Поэтому основное внимание уделим именно водным растворам.
Влияние давления на растворимость
Растворимость газов повышается при росте давления газа над растворителем, а растворимость твердых и жидких веществ зависит от давления несущественно.
Уильям Генри впервые пришел к выводу, что
количество газа, которое растворяется при постоянной температуре в заданном объеме жидкости, прямо пропорциональна его давлению.
Данное утверждение известно как закон Генри и выражается оно следующим соотношением:
С = k·P,
где С – растворимость газа в жидкой фазе
Р – давление газа над раствором
k – постоянная Генри
Влияние температуры на растворимость
На следующем рисунке приведены кривые зависимости растворимости некоторых газов в воде от температуры при постоянном давлении газа над раствором (1 атм)
Как видно, растворимость газов уменьшается с ростом температуры, в отличие от большинства ионных соединений, растворимость которых растет с увеличением температуры.
Влияние температуры на растворимость зависит от изменения энтальпии, которое происходит при процессе растворения. При протекании эндотермического процесса происходит увеличение растворимости с ростом температуры.
Это следует из уже известного нам принципа Ле – Шателье: если изменить одно из условий, при котором система находится в состоянии равновесия – концентрацию, давление или температуру, — то равновесие сместится в направлении той реакции, которая противодействует этому изменению.
Представим, что мы имеем дело с раствором, находящимся в равновесии с частично растворившимся веществом. И этот процесс является эндотермическим, т.е. идет с поглощением теплоты из вне, тогда:
Вещество + растворитель + теплота = раствор
Согласно принципу Ле – Шателье, при эндотермическом процессе, равновесие смещается в направлении, способствующее уменьшению поступления теплоты, т.е. вправо. Таким образом, растворимость увеличивается.
Если же процесс экзотермический, то повышение температуры приводит к уменьшению растворимости.
Далее на рисунке показаны зависимости растворимости некоторых ионных соединений от температуры.
Известно, что существуют растворы жидкостей в жидкостях. Некоторые из них могут растворяться друг в друге в неограниченных количествах, как вода и этиловый спирт, а другие — растворяются лишь частично.
Так, если попробовать растворить четыреххлористый углерод в воде, то при этом образуются два слоя: верхний — насыщенный раствор воды в четыреххлористом углероде и нижний — насыщенный раствор четыреххлористого углерода в воде.
При повышении температуры, в основном, взаимная растворимость таких жидкостей увеличивается. Это происходит до тех пор, пока не будет достигнута критическая температура, при которой обе жидкости смешиваются в любых пропорциях. От давления растворимость жидкостей практически не зависит.
При вводе в смесь, состоящую из двух несмешивающихся между собой жидкостей, вещества, которое может растворяться в любой из этих двух жидкостей, его распределение между этими жидкостями будет пропорционально растворимости в каждой из них.
Согласно закону распределения вещество, способное растворяться в двух несмешивающихся растворителях, распределяется между ними так, что отношение его концентраций в этих растворителях при постоянной температуре остается постоянным, независимо от общего количества растворенного вещества:
где С1 и С2 – концентрации вещества в двух жидкостях
Определение и суть
При определённой температуре, зависящей от вида раствора электролита между кристаллами и его содержанием, устанавливается равновесие. Оно является динамическим, так как скорость прямой и обратной реакции совпадают, то есть время растворения и кристаллизации равны. Главным условием для наступления такого процесса является содержание в жидкости малорастворимого электролита.
Протекающая реакция характеризуется двумя константами:
Общей формулой произведения растворимости в химии является выражение: ПР = [Ky]x * [Ax-]y. Таким образом, определяется взаимосвязь между постоянной растворимости и равновесия. То есть это гетерогенное равновесие между кристаллами Кх Ау и раствором.
Любое соединение, образующее раствор, может быть насыщенным или ненасыщенным. Первым называют взаимодействие при определённой температуре, когда можно растворить ещё какую-то часть продукта, а вторым — раствор, в котором скорости реакции и осаждения равны. Существует и третий вид раствора — перенасыщенный. Это состояние реакции, при которой образуется осадок.
Эти три состояния можно описать формулами:
Константа связана и с перераспределением энергии Гиббса. Эта зависимость объединяет температуру, давление и газовую постоянную. Так как свободная энергия — это мощность, равная изменению системы внутри неё, то потенциал Гиббса характеризуется полной энергией, которая используется для химического превращения и позволяет определить возможность прохождения реакции. Находится она по формуле: G = U + PV — TS. Изменение мощности можно описать выражением: ΔG = R * T * LtKa.
Определение влияния константы равновесия и решение уравнений электронного баланса даёт возможность найти равновесные составы уравнений, что важно для описания термодинамических процессов.
Правило активности ионов
В аналитической химии по выпадению осадка часто определяют, какие продукты содержатся в растворе. На изучении осадка построен качественный анализ. В природе не существует веществ абсолютно нерастворимых, поэтому всегда образуются выпавшие частицы или ионы. Для изучения системы осадок-раствор и используют правило произведения растворимости.
Сформулировал этот закон в 1889 году Нернст. Согласно утверждению химика, в высококонцентрированном растворе малорастворимого соединения произведение активностей частиц с их стехиометрическими коэффициентами определяется константой, характерной для растворителя. При этом на показатель также влияет температура.
По факту это правило является следствием второго начала термодинамики применительно к равновесной системе. По сути, осадок представляет двухфазную систему. Правило произведения было установлено эмпирическим путём при изучении слаборастворимых веществ. Его нельзя применять, например, к солям KCl, TaTO3 и другим.
Полный расчёт обычно довольно сложен, так как необходимо определить коэффициенты активности. Поэтому используют упрощённый подход. Расчёт выполняют только для слаборастворимых веществ, у которых активность ионов равна концентрации. Следовательно, она составляет единицу. А также при отсутствии дополнительных кислот или оснований пренебрегают гидролизом.
В качественном анализе большую часть электролитов охватывают следующие типы солей:
Экспериментально установленные значения являются справочными данными и берутся из таблицы произведений растворимости. Зная их величину, вычислить растворимость слаборастворимых продуктов при установленных условиях не составляет труда.
Экспериментальное подтверждение
Для эксперимента нужно поместить в химическую колбу любую труднорастворимую соль, например, AgCl, и перемешать с ней дистиллированную воду. Так как ионы Ag+ и Cl- взаимодействуют с диполями H2O, то через время они начнут отрываться от кристаллической решётки и насыщать раствор.
Сталкиваясь, освободившиеся ионы начнут создавать хлорид серебра и выпадать в виде осадка. Это приводит к тому, что в системе возникают два противоположных друг другу процесса. В итоге наступает динамическое равновесие. То есть за единицу времени в раствор поступает столько частиц серебра и хлора, сколько и выпадает в осадок. После того как отрыв ионов прекратится, раствор станет насыщенным. Таким образом, получится раствор, где будет находиться осадок труднорастворимой соли с находящимся в жидком состоянии соединении этого же вещества.
Процесс образования соединения будет сопровождаться:
Исходя из того, что эта система находится в состоянии равновесия, верным будут следующие выражения: V1 = V2 и K1 = K2. То есть [Ag + ] [Cl — ], где: [ Cl — ] = k 2 / k 1 = cotst, для реакции, протекающей при постоянной температуре. Поэтому можно утверждать, что произведение количества ионов в концентрированном растворе малорастворимого электролита будет постоянной величиной, но только при постоянной температуре: ПР AgCl = [ Ag + ] * [ Cl — ].
Но необходимо учитывать и влияние различных факторов. К ним относят концентрацию раствора, количество осадителя, температуру, присутствие одноимённого иона. Правило произведения важно при растворении осадков в растворе. С его помощью можно заранее узнать выпавшую в осадок часть. Для часто используемых соединений существует таблица, куда внесены экспериментально полученные результаты при температуре 25 0 С.