что такое подавляет агрегацию тромбоцитов
Что такое подавляет агрегацию тромбоцитов
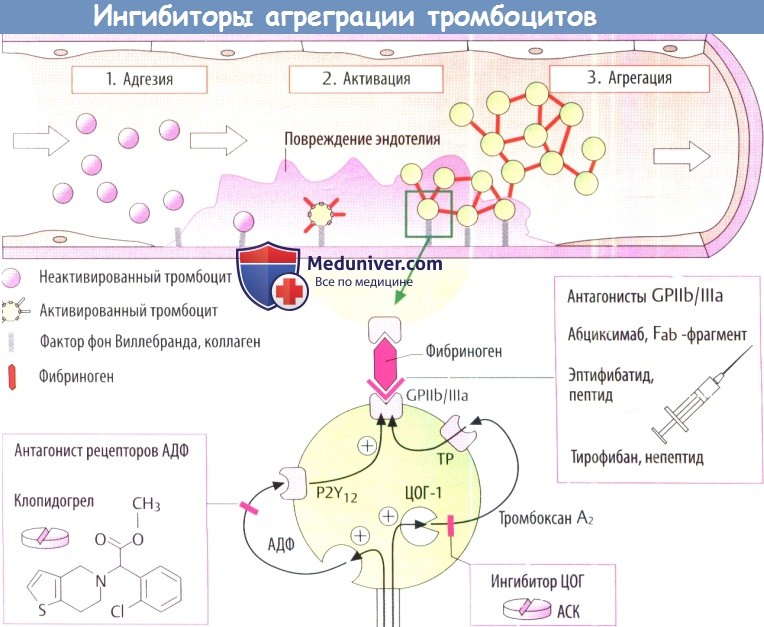
Тромбоциты могут агрегировать при повреждении стенки сосуда или нарушении функции эндотелия (из-за гипертензии, повышенного уровня липопротеидов низкой плотности [ЛПНП] в плазме, нелеченного сахарного диабета, курения). Взаимодействие с фактором фон Виллебранда и коллагеном обеспечивает адгезию тромбоцитов к стенке сосуда и их активацию.
Активация тромбоцитов приводит к изменению их формы и стимулирует выделение веществ, запасенных во внутриклеточных гранулах (аденозиндифосфат [АДФ], серотонин). Кроме того, стимулируется циклооксигеназа (ЦОГ-1), изарахидоновой кислоты образуется тромбоксан А2. Вышедшие АДФ и тромбоксан А2 активируют связанные с G-белками рецепторы (P2Y12 и ТР), что в конечном счете изменяет конформацию гликопротеида GP llb/llla на мембране тромбоцита.
Этот гликопротеид обладает сродством к фибриногену и может вызывать образование поперечных связей между тромбоцитами. Тромб, образующийся над дефектом эндотелия, может затруднять кровоток или вообще закупоривать сосуд (при инфаркте миокарда или инсульте).
Склонность тромбоцитов к агрегированию можно подавлять с помощью различных фармакологических средств.
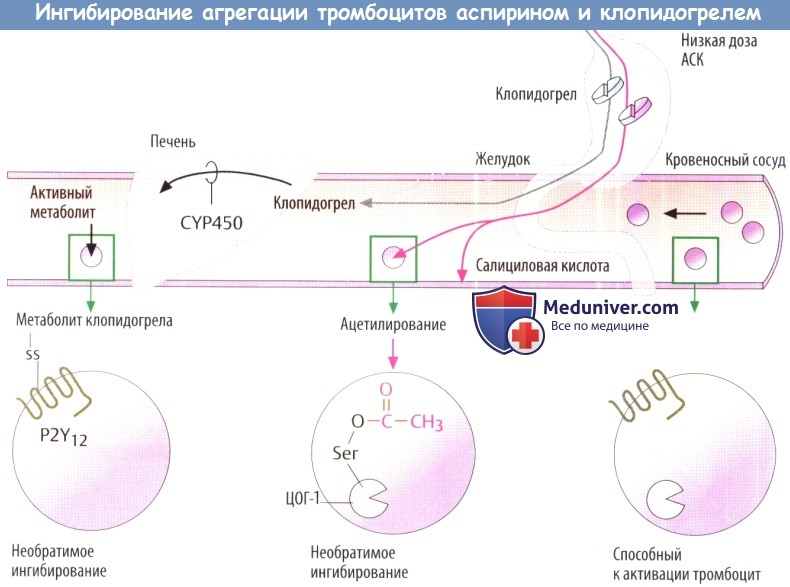
а) Ацетилсалициловая кислота (АСК) предотвращает синтез тромбоксана, опосредованный ЦОГ-1. Низкие суточные дозы (75-100 мг) могут быть недостаточными. Показания к применению включают профилактику повторного инфаркта после перенесенного инфаркта миокарда и предупреждение инсульта. Несмотря на низкую дозировку этого препарата, не исключаются такие неблагоприятные эффекты, как повреждение слизистой оболочки желудка или индуцирование приступов астмы
б) Доступной альтернативой аспирину (АСК) служат антагонисты рецепторов АДФ тиклопидин, клопидогрел и прасугрел, которые также можно принимать внутрь. Антагонисты АДФ, аналогично АСК, вызывают необратимое угнетение функции тромбоцитов. Эти вещества представляют собой неактивные предшественники, превращающиеся в печени с помощью цитохромоксидазы Р450 в активные метаболиты, которые ковалентно связываются с подтипом P2Y-рецепторов АДФ на тромбоцитах.
Следовательно АДФ-опосредованная агрегация тромбоцитов ингибируется на протяжении всего жизненного цикла тромбоцита (7-10 дней). Тиклопидин может вызывать серьезные побочные эффекты, в т. ч. нейтропению и тромбоцитопению. «Правопреемник» тиклопидин, клопидогрел, переносится лучше.
в) Антагонисты интегрина гликопротеида IIb/III. Доступные представители этого класса препаратов пригодны лишь для парентерального введения. Их используют при чрескожной коронарной баллонной ангиопластике или нестабильной стенокардии. Они блокируют белок, сшивающий фибриноген, и тем самым уменьшают фибриноген-опосредованное соединение тромбоцитов независимо от фактора, способствующего преципитации.
Абциксимаб представляет собой гибридный Fa-фрагмент антитела, направленного против GP IIb/III. Тирофибан и эптифибатид действуют как конкурентные антагонисты участка, связывающего фибриноген. Поскольку абциксимаб находится в связанном состоянии c GP IIb/IIIa в течение долгого времен агрегация тромбоцитов снова становится возмож ной лишь спустя несколько дней после инъекции. У эптифтибатида и тифибана это действие длится несколько часов.
Антагонисты GP IIb/IIIa несут риск кровотечения во время лечения, т.к. они ингибируют общий конечный путь активации тромбоцитов.
г) Пресистемное действие ацетипсапициповой кислоты. Аспирин угнетает агрегацию тромбоцитов за счет ацетилирования и блокады тромбоцитарной ЦОГ-1. Специфичность этой реакции достигается следующим образом: необратимое ацетилирование ЦОГ происходит в крови в висцеральной области, т.е. до того, как она дойдет до печени.
Учитывая масивное пресистемное деацетилирование аспирина, она почти не влияет на «постпеченочные» циклооксигеназы ЦОГ-1 угнетаетсяименновтромбоцитах, т.к. нормальные клетки, имеющие ядро, способны заново синтезировать фермент.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Агрегация тромбоцитов — что это такое,расшифровка анализа и методы исследования
Причины понижения и повышения агрегации
Повышение уровня агрегации или гиперагрегация — состояние, при котором кровь медленно течет по сосудам и быстро сворачивается. Провокаторами такого отклонения могут выступать:
Умеренная гиперагрегация тромбоцитов при беременности — норма. Такое отклонение возникает из-за необходимости питать кровью плаценту. Своего пика значение достигает в 3 триместре гестации.
Снижение агрегации тромбоцитов происходит из-за следующих патологий:

Показания к проведению анализа
Агрегация тромбоцитов исследуется при:
Также, это исследование важно в диагностике наследственных геморрагических тромбоцитопатий.
Проведение анализа и его расшифровка
Исследование агрегации тромбоцитов дает возможность обнаружить отклонение от нормы, провести диагностику патологий сердечно-сосудистой или кроветворной систем. Процедура необходима для отслеживания динамики течения некоторых заболеваний и контроля проводимого лечения.
После забора биологического материала в кровь добавляют специальные вещества — индукторы, которые схожи по строению с клетками организма, способствующими тромбообразованию.
В качестве индуктора могут выступать:
В основе методики установления агрегации — прохождение световых волн через плазму крови как до, так и после свертываемости. Учитываются такие свойства световой волны:
Все это происходит в аппарате, который носит название анализатор агрегации тромбоцитов. Оборудование есть в каждой лабораторной службе Хеликс.
Расшифровка анализа проводится гематологом, а показатель зависит от вещества, которое добавили в исследуемую жидкость, и его концентрации.
Агрегация тромбоцитов с адреналином
Агрегация тромбоцитов – норма
Как уже отмечено выше, при установке степени агрегации тромбоцитов может использоваться несколько типов индукторов этого процесса. Непосредственно поэтому показатели нормы агрегации тромбоцитов могут отличаться в зависимости от характера используемого реагента. Имитация склеивания кровяных пластинок производится на стекле с добавлением индуктора. Данные вещества в норме в организме человека запускают реакции свертывания крови. Из используемых только ристомицин (ристоцеин) не имеете биологических аналогов в организме человека. Для каждого индуктора норма своя.
Агрегация тромбоцитов с АДФ
Стоит отметить, что для получения полной картины и с целью точной диагностики анализ для определения агрегации тромбоцитарной может проводиться поочередно с четырьмя индукторами. Зачастую первой осуществляется АДФ индуцированная агрегация тромбоцитов. В норме этот показатель находится в границах 30,8–77,8%. Когда агрегация тромбоцитов не вписывается в названные значения, врачи исключают наличие следующих типов заболеваний:
Агрегация тромбоцитов с адреналином
Исследование агрегации тромбоцитов с использованием в качестве индуктора адреналина является информативным методом диагностики. Этот способ полностью отражает внутренний механизм активации процесса восстановления кровеносного сосуда. За норму принято значение 35,0–92,5%. Превышение показателя говорит о гиперагрегации, уменьшение – о гипоагрегации. Повышенная агрегация тромбоцитов связана с высокой концентрацией тромбоцитов в крови, патологией, стрессом, приемом ряда медикаментозных средств.
Агрегация тромбоцитов с ристомицином
При оценке того, как происходит в организме агрегация тромбоцитов, ристомицин помогает параллельно выявить и синдром Виллебранда. Это заболевание носит наследственный характер. Спонтанная агрегация тромбоцитов, сопровождающая болезнь, характеризуется появлением периодических кровотечений, которые подобны тем, что возникают при гемофилии.
Однако при этой патологии кровотечения отличаются большей продолжительностью, так как у пациента происходит нарушение сразу всех трех звеньев гемостаза. Использовать анализ с ристомицином врачи могут и при оценке эффективности проводимой терапии антиагрегантами, подборе правильной дозировки лекарства. В норме значения должны быть в промежутке 56–167%.
Агрегация тромбоцитов с коллагеном
Зачастую врачи не могут точно установить, какой из этапов свертывания крови нарушен: адгезия или агрегация тромбоцитов – тест с коллагеном помогает это определить. Если при данном типе исследования врачи фиксируют превышение установленных норм, это говорит о сбое процесса адгезии. Тромбоциты не могут нормально зафиксироваться на эндотелии поврежденных кровеносных сосудов, поэтому кровотечение долго не прекращается.
О наличии патологии судят по несоответствию значений параметра установленной норме. Для теста с коллагеном агрегация тромбоцитов должна составлять 46,5–93,2%. Превышение данных значений или снижение параметра указывает на:
Норма тромбоцитов в крови
Чтобы знать, в каком состоянии находится уровень тромбоцитов, нужно иметь представление об их норме.
| Возраст | Показатель, х 10^9/л |
| Новорождённый | 100-420 |
| до 1 года | 160-320 |
| от 1 года до 4 лет | 150-300 |
| от 15 до 18 лет | 180-340 |
| Мужчины после 18 лет | 180-400 |
| Женщины после 18 лет | 150-380 |
Если говорить о норме агрегации, то она составляет 25-75%. В этом случае процесс склеивания тромбоцитов происходит хорошо и никакой опасности для здоровья не представляет.
Агрегация тромбоцитов
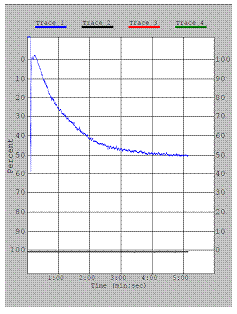
Для оценки функции тромбоцитов в Лаборатории ЦИР проводится анализ на индуцированную агрегацию тромбоцитов. Это анализ высокого качества, выполняется на автоматическом агрегометре. Так как этот анализ резко меняется при приеме препаратов, влияющих на свертывание крови (антиагреганты, например, аспирин, тромбо-асс, антикоагулянты, например, гепарин), желательно сдавать его до начала приема этих лекарств. По каждой агрегатограмме врач-лаборант выдает заключение.
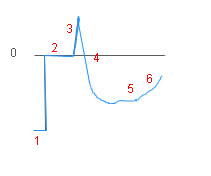
В кривой агрегации оцениваются амплитуда агрегации, форма кривой, наличие одной или двух волн, а также наличие дезагрегации.
Важная информация: сочетание приема пищевых продуктов, фитопрепаратов и пищевых добавок, содержащих компоненты из данного списка, с приемом антиагрегантов (тромбоАСС) и антикоагулянтов (гепарин) является опасной по риску кровотечения комбинацией (категория D по классификации FDA). Риск кровотечения в большинстве случаев превышает потенциальную пользу.
Агрегация с АДФ.
Агрегационный ответ снижен. Дезагрегация практически отсутствует.
Анализ на агрегацию тромбоцитов: диагностика тромбов
В медицинском центре Ейска «Сенситив» есть своя лаборатория для клинической диагностики, в которой проводятся самые современные исследования. Многие из этих исследований стали доступны для ейчан совсем недавно, и анализ на агрегацию тромбоцитов – одно из таких исследований.
Что такое «агрегация тромбоцитов»
Тромбоциты представляют собой бесцветные кровяные клетки, функция которых — защита организма от кровопотерь. Когда ткани организма повреждаются, тромбоциты мгновенно устремляются к месту повреждения и блокируют его, предотвращая чрезмерную кровопотерю. Такая блокировка осуществляется за счет того, что тромбоциты мгновенно склеиваются между собой, образуют блок, который закрывает рану. Это процесс блокировки и называется агрегацией тромбоцитов. Процесс происходит в два этапа:
Когда организм здоров, эта функция носит защитный характер. Но если в организме пошли патологические изменения, образования тромбов способно нарушить питание в жизненно важных органах и тканях.
К чему приводит нарушение агрегации тромбоцитов
Если процесс агрегации нарушен, это может привести к негативным последствиям. Так, если активность бесцветных кровяных клеток повышена, то это может привести к инсульту, инфаркту. А если выработка тромбоцитов понижена, то это может приводить к большой потере крови: человек страдает частыми кровотечениями, которые долго не прекращаются, приводят к истощению и анемии.
Именно для того, чтобы предотвратить эти последствия, проводится анализ агрегации тромбоцитов. Показанием к прохождению анализа являются:
Расшифровка анализа на агрегацию тромбоцитов
В анализе на агрегацию тромбоцитов о хорошем кроветворении говорят показатели 25 – 75%. Это значит, что ткани и органы нормально снабжаются кислородом, и тромбы отсутствуют.
Норма тромбоцитов
| Возраст | Показатель, х 10^9/л |
| Новорождённый | 100–420 |
| Ребёнок до года | 160–320 |
| 1–4 года | 150–300 |
| 15–18 лет | 180–340 |
| Мужчины старше 18 лет | 180–400 |
| Женщины старше 18 лет | 150–380 |
Как сдают анализ на агрегацию тромбоцитов
Анализ крови на агрегацию тромбоцитов требует особой подготовки, так как от этого зависит его результат. Для анализа осуществляется забор крови из вены. Перед этим пациент должен:
Исследование проводится в утренние часы натощак. Перед процедурой разрешается употреблять только чистую негазированную воду.
Если не соблюдать эти правила, результат будет недостоверным из-за веществ, находящихся в крови.
Агрегация тромбоцитов
Тромбообразование играет ключевую роль в развитии различных сердечно-сосудистых осложнений. В патогенезе ишемических болезней органов и систем человеческого организма: ишемической болезни сердца (ИБС) [острый коронарный синдром (ОКС), инфаркт миокарда (ИМ)], ишемического мозгового инсульта, гангрены конечностей и других нарушений кровоснабжения органов и тканей — значительное место занимают воспалительные и атеросклеротические повреждения сосудов с нарушением целостности интимы, замедление кровотока, дисбаланс свертывающей и противосвертывающей системы и нарушение реологических параметров крови.
При повреждении эндотелия сосудов различной этиологии происходит формирование тромба и вследствие этого — критическое сужение просвета сосудов или его полное закрытие (частичная или полная окклюзия). В нарушениях реологических параметров крови агрегационное состояние тромбоцитов и эритроцитов играет ведущую роль [1, 6, 8, 10, 17].
Современное лечение и профилактика сердечно-сосудистых осложнений, в частности ИМ, невозможны без четкого представления механизмов тромбообразования, материальным субстратом которого являются тромбоциты, эритроциты, фибриноген. ИМ — ишемический некроз сердечной мышцы — в 95% случаев развивается в результате формирования тромба в коронарной артерии, что подтверждается данными аутопсии среди умерших в первые 3 ч от начала развития болевого синдрома и результатами коронарографического исследования у больных, поступивших в стационар в первые часы развития миокардиальной катастрофы
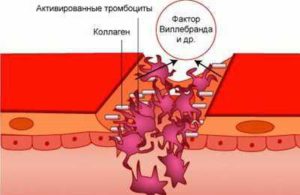
В процессе тромбообразования тромбоцит проходит четыре стадии: активация, высвобождение активных биологических веществ (тромбоксаны, аденозиндифосфат АДФ, серотонин, гликопротеиновые (ГП) рецепторы — IIb/IIIa), агрегация и адгезия. Эти процессы (макро- и микротромбообразование) особенно бурно проявляются при дестабилизации коронарного кровотока — ОКС,, включая ИМ. В основе макро- и микротромбообразования лежат механизмы, стимулирующие агрегационную активность тромбоцитов и эритроцитов — наличие ускоренного, турбулентного тока крови в суженном атеросклеротической бляшкой участке сосуда, что способствует повреждению эндотелия (с развитием эндотелиальной дисфункции) и «обнажению» коллагена, одного из главных факторов агрегации и адгезии тромбоцитов. Тромбоциты вступают в контакт с субэндотелиальным слоем, в частности с главным стимулятором адгезии — коллагеном, образуют отростки с образованием тромбоцитарных конгломератов (агрегация) и приклеиваются (адгезия) на этих участках, создавая белый тромб.
Активация тромбоцитов осуществляется катехоламинами, тромбином, АДФ, серотонином, коллагеном, тромбоксаном А2 — продуктом метаболизма арахидоновой кислоты.
В результате активации тромбоцитов происходит высвобождение из последних биологически активных веществ (АДФ, тромбоксан А2, серотонина) и лабилизация мембраны тромбоцита с образованием ГП-рецепторов IIb/IIIa под действием АДФ и тромбоксана А2.
Агрегация тромбоцитов — образование тромбоцитарных конгломератов в плазме крови — происходит при активации и взаимодействии ГП-рецепторов IIb/IIIa через образования фибриновых мостиков между тромбоцитами.
Адгезия — прилипание тромбоцитарных конгломератов к поврежденной интиме сосудов — контролируется фактором Виллебранда.
Таким образом, активация тромбоцитов — ключевой момент в патогенезе сердечно-сосудистых осложнений, во многом определяющий выраженность нарушений кровоснабжения органов и тканей (сердце, головной мозг, периферические сосуды), поэтому антиагрегационная терапия является патогенетически обоснованной.
В настоящее время выделяют четыре группы антитромбоцитарных препаратов, в основе разделения которых лежат принципы доказательной медицины, учитывающие эффективность и наличие побочных действий.
Первая группа антитромбоцитарных препаратов, применение которых не рекомендуется для практической кардиологии вследствие отсутствия доказательной основы преимуществ перед Аспирином, неэффективности и потенциальной опасности: сульфинпиразон, дипиридамол, простациклин, блокаторы синтетазы тромбоксана А2, антагонисты рецепторов тромбоксана А2, препараты ингибиторов рецепторов IIb/IIIa тромбоцитов для приема внутрь.
Вторая группа, составляющая основу современной антитромбоцитарной терапии, — ингибиторы циклооксигеназы (ЦОГ): ацетилсалициловая кислота (АСК) — Аспирин.
Третья группа — тиенопиридины (клопидогрел — Плавикс, тиклопидин — Тиклин). Четвертая группа — блокаторы ГП-рецепторов IIb/IIIa для внутривенного применения (абциксимаб, эптифибатид, тирофибан, фрамон) [1, 3, 8, 9, 11, 12].
АСК используется в медицинской практике более ста лет. Начиная с 1980-х годов, Аспирин активно применяется в клинической практике при лечении ОКС с целью предупреждения развития ИМ. Проведено несколько значительных исследований (VA, RISC, ISIS-2), которые убедительно продемонстрировали способность Аспирина снизить риск развития острого ИМ и смерти от острой коронарной недостаточности на 41–70%. В 2002 г. Antithrombotic Trialists Collaboration опубликовала данные крупнейшего метаанализа результатов 287 рандомизированных клинических исследований, охвативших 135000 пациентов. Полученные данные свидетельствуют о преимуществах Аспирина у пациентов с высоким риском развития осложнений. В метаанализе убедительно показано, что применение высоких доз Аспирина (500–1500 мг) не имеет преимуществ в терапевтической эффективности по сравнению со средними (160–325 мг) и низкими (75–150 мг) дозами и довольно часто сопровождается побочными действиями со стороны желудочно-кишечного тракта (ЖКТ). Подобные результаты легли в основу постулата: оптимальная доза Аспирина для длительной профилактики сердечно-сосудистых осложнений у пациентов с высоким риском находится в пределах 75–150 мг/сут [1, 4, 8, 11, 13, 17].
Американская диабетологическая ассоциация рекомендует применять АСК в дозе от 81 до 325 мг для вторичной профилактики поражений крупных сосудов у больных диабетом старше 30 лет, сочетающегося с компонентами метаболического синдрома: избыточной массой тела (> 120% от идеальной массы тела, индекс массы тела (ИМТ) > 28 для женщин и > 27,3 для мужчин), атерогенной дислипидемией (триглицериды > 250 мг%, холестерин липопротеидов низкой плотности > 130 мг% и холестерин липопротеидов высокой плотности < 40 мг%), высокое артериальное давление, отягощенный анамнез по ИБС, курение [1, 5, 12].
Кроме того, в метаанализе установлена целесообразность назначения Аспирина больным с фибрилляцией предсердия (в качестве альтернативы варфарину), заболеваниями периферических артерий (стеноз сонных артерий) и терминальной хронической почечной недостаточностью (требующей проведения гемодиализа).
В ряде независимых исследований было установлено, что у больных с ОКС без подъема сегмента ST ЭКГ (ESSENCE, PRISM PLUS) ближайший прогноз зависит от предшествующего приема Аспирина до развития обострения ИБС. Так, в исследовании PRISM PLUS на фоне применения Аспирина при ОКС частота развития ИМ, рефрактерной стенокардии и внезапной смерти к 7-му дню наблюдения составила 12,1% среди больных, не принимавших ранее этот препарат, и 23,5% — среди лиц, принимавших его до развития обострения. Этот факт получил название «аспириновый парадокс», что послужило поводом для D. L. Bhatt и E. J. Topol (2004) отнести Аспирин к «субоптимальным антитромбоцитарным средствам» [12].
Механизм действия АСК представлен на рисунке. Аспирин в первую очередь ингибирует ЦОГ тромбоцитов и эндотелия сосудов, подавляет образование тромбоксана А2 (мощного индуктора агрегации тромбоцитов и вазоконстрикции) — продукта метаболизма арахидоновой кислоты, а в больших дозах — синтез простациклина (дезагрегант и вазодилататор). АСК и другие нестероидные противовоспалительные препараты (индометацин) действуют на уровне метаболизма арахидоновой кислоты, а в больших дозах (Аспирин — от 300 до 500 мг) одновременно блокируют синтез простациклина, что косвенно может поддерживать агрегационное состояние тромбоцитов в результате количественного уменьшения простациклина и его дезагрегационного эффекта.
Существуют и другие механизмы действия АСК, которые отличают ее от других антиагрегантных препаратов и обусловливают ее уникальность. Аспирин оказывает ингибирующее влияние на образование фибрина через подавление образования тромбина (FII ; FIIa) и функционального состояния фибриногена FI (блокирует лизин в молекулах фибриногена). Одновременно АСК способна активировать фибринолиз через высвобождение активаторов плазминогена и «разрыхления» волокон фибрина [3].
В последние годы активно обсуждается проблема резистентности к терапии Аспирином, под которой понимают неспособность препарата у некоторых больных в должной мере подавлять функцию тромбоцитов, снижать синтез тромбоксана А2 и/или удлинять время кровотечения. Распространенность резистентности к терапии Аспирином, по данным различных исследований, составляет от 10 до 45% [2, 7, 17]. Среди возможных причин этого феномена выделяют следующие:
фармакодинамические взаимодействия Аспирина с нестероидными противовоспалительными препаратами;
наличие нетромбоцитарных источников синтеза тромбоксана А2 (эндотелий, моноцитарная/макрофагальная ЦОГ-2);
экспрессия ЦОГ-2 во вновь образующихся тромбоцитах;
гидролиз Аспирина эстеразами слизистой оболочки ЖКТ;
повышенный синтез тромбоксана А2;
гиперлипидемия;
генетические особенности.
Есть основания полагать, что резистентность к терапии Аспирином может быть связана с полиморфизмом гена ЦОГ, затрагивающим активный центр фермента (Ser529), полиморфизмом генов, кодирующих другие ферменты, участвующие в мобилизации и метаболизме арахидоновой кислоты (фосфолипазы, тромбоксансинтетазы) и полиморфизмом генов, кодирующих другие ГП-рецепторы тромбоцитов [7].
Наиболее перспективным c точки зрения эффективности профилактики и лечения тромбозов является использование АСК в сочетании с тиенопиридинами [6, 9, 12, 13, 17, 18].
АСК, дипиридамол, сульфинпиразон обладают рядом побочных эффектов, которые снижают их терапевтический эффект, поэтому в настоящее время группа тиенопиридинов — синергистов Аспирина — представляет интерес для практической медицины. По данным исследования TASS (Ticlopidine Aspirine Stroke Stady), которое было выполнено с целью сравнения профилактической активности тиклопидина (500 мг/сут) и АСК (1300 мг/сут) у больных с ИБС, эффективность тиклопидина была значительно выше при меньшем количестве побочных эффектов: риск развития инсультов и ИМ в группе пациентов, принимавших тиклопидин, был на 24% меньше в первый год наблюдения по сравнению с группой больных, принимавших только Аспирин в указанной дозе [9, 11, 12, 13, 17].
Механизм действия тиенопиридинов опосредуется через блокаду Р2Y12-рецепторов тромбоцитов, что препятствует стимулирующему действию на них АДФ и последующей активации ГП-рецепторов IIb/IIIa.
Экспериментальные исследования механизмов действия тиенопиридинов показали, что препараты высокоэффективны только in vivo. В отличие от АСК, которая ингибирует только вторую фазу агрегации тромбоцитов, индуцированную АДФ, тиклопидин ингибирует обе фазы — агрегацию и адгезию. Тиенопиридины также тормозят активацию тромбоцитов, вызванную коллагеном, адреналином, тромбином и серотонином. При этом (в отличие от АСК) они не затрагивают метаболизм арахидоновой кислоты и, таким образом, не влияют на синтез простациклина эндотелием сосудов [1, 11].
Кроме вышеперечисленного, тиенопиридины повышают пластичность (деформируемость) эритроцитов, способствуя улучшению реологических свойств крови и микроциркуляции, что подтверждено в наших исследованиях: отмечено увеличение электрофоретической подвижности эритроцитов под действием тиклопидина в дозе 400 мг/сут; одновременно препарат понижал вязкость крови путем снижения фибриногена плазмы [9].
В настоящее время накоплен значительный клинический опыт применения тиенопиридинов при различных сердечно-сосудистых патологиях: ОКС, инсульт, облитерирующий атеросклероз сосудов нижних конечностей и диабетическая ангиопатия. В исследовании CAPRIE при сравнении эффективности клопидогрела и Аспирина с целью вторичной профилактики сердечно-сосудистых осложнений показатели частоты ишемических инсультов, ИМ и смерти от внезапной сердечной недостаточности за год в группах пациентов, применявших клопидогрел и Аспирин, продемонстрировал и снижение относительного риска развития указанных осложнений на фоне приема клопидогрела на 8,7%.
Клопидогрел относится к группе тиенопиридинов, обладает наиболее полноценным антитромботическим действием, при нагрузочной дозе 300 мг (600 мг) его действие начинается через 2–4 ч от начала приема препарата и достигает максимума антиагрегантного действия к концу второго-третьего дня лечения. Тиклопедин редко используют в настоящее время в практике лечения ОКС в связи с отсроченным началом антиагрегантного действия, отсутствием выверенной нагрузочной дозы, более частыми, чем у клопидогрела, развитиями осложнений — нейтропении, тромбоцитопении, нарушения функции печени [1, 11, 13].
Наилучшие результаты получены при комбинированном лечении тиенопиридинами в сочетании с Аспирином, что позволило уменьшить терапевтические дозы указанных препаратов, снизить количество побочных эффектов и удешевить лечение.
В исследованиях CATS (Canadian-American Ticlopidin Stady), куда были включены 1053 пациента, перенесших недавно (в последние 4 мес) эпизоды ишемических приступов, было продемонстрировано уменьшение риска развития ИМ, повторного инсульта и смерти от сердечно-сосудистой недостаточности на 30,2% [1, 8, 11, 12].
Сходные результаты представлены французскими учеными Y. C. Aican et al. (1989), аналогичные данные получены в ходе шведского многоцентрового исследования STIM. Французские исследователи наблюдали за 169 пациентами, в исследование STIM было включено 687 пациентов с перемежающейся хромотой. Назначение тиклопидина проводилось по стандартной методике в дозе 250 мг/сут с добавлением 75–100 мг Аспирина в сутки. В обеих группах наблюдения количество сосудистых осложнений снизилось на 38–40% (с одновременным улучшением периферического кровотока).
В исследовании CLARITI-TIMI 28 при добавлении клопидогрела к стандартной терапии Аспирином у 3491 пациента с ОКС с подъемом сегмента ST к 30-му дню лечения документально подтверждено снижение риска смерти от сердечно-сосудистой недостаточности, ИМ, рецидива ишемии (требующего экстренной реваскуляризации) на 20% по сравнению с группой пациентов, применявших плацебо. Аналогичные результаты получены в исследовании COMMIT-CCS-2, включившем 45852 пациента, получавших АСК 162 мг в день и клопидогрел 75 мг в день: риск развития внезапной смерти, повторного ИМ и инсульта снижался на 10% во время пребывания в стационаре [1].
Таким образом, в настоящее время наиболее предпочтительным (по сравнению с монотерапией) с точки зрения эффективности в профилактике эпизодов ишемии, развития ИМ и стоимости лечения больных с ОКС является использование тиенопиридинов (клопидогрел — однократно с нагрузочной дозой 300 мг, затем 75 мг/сут) в сочетании с Аспирином (100 мг/сут) в течение 9–12 мес, так как они являются мощными ингибиторами агрегации и адгезии тромбоцитов и эритроцитов, а следовательно, эффективными антитромботическими средствами, применяющимися в кардиологической практике, с минимальными побочными эффектами.
В острых ситуациях ОКС, при проведении баллонной ангиопластики со стентированием эффективность антиагрегантной терапии возрастает при использовании комбинации АСК с клопидогрелом и/или антагонистами ГП-рецепторов IIb/IIIa. В этих ситуациях используют нагрузочные дозы антитромбоцитарных препаратов (Аспирин — 150–300 мг, клопидогрел — 300–600 мг однократно) с последующим переходом на поддерживающие дозы (Аспирин — 75–150 мг/сут, клопидогрел 75 мг/сут) в течение 12 мес.
Исследование CHARISMA, посвященное изучению эффективности терапии при добавлении клопидогрела в дозе 75 мг/сут к стандартной терапии Аспирином 75–150 мг/сут на протяжении длительного времени (в течение одного года) у 15603 пациентов с хроническими формами сердечно-сосудистых заболеваний, показало результаты, аналогичные по сравнению с группой пациентов, получавших монотерапию АСК (7,3%), — снижение частоты развития ИМ, инсульта, смерти от внезапной сердечной недостаточности до 6,8% при минимальных осложнениях со стороны ЖКТ [1].
Основной клинической проблемой применения Аспирина, помимо риска кровотечений (особенно у пожилых пациентов), являются осложнения со стороны ЖКТ в виде развития диспептических расстройств и эрозивно-язвенного гастрита. Эрозивно-язвенные изменения слизистой ЖКТ на фоне приема АКС в стандартизированных дозах, применяемых в кардиологической практике, — общеизвестный факт [14, 15, 16, 18, 19].
Долгое время единственным и практически 100-процентным решением этой проблемы многие клиницисты считали применение кишечно-растворимых форм АСК: Тромбо АСС, Аспифат, Аспирин-С, Аспирин Упса и др. Однако, согласно результатам последних исследований, отмечено образование эрозий и язв желудка даже при применении Аспирина, покрытого кишечно-растворимой оболочкой (они рубцевались в 90% наблюдений при применении циметидина и антацидов только после отмены этих форм) [18, 19].
Сравнительно малоизвестны и описанные недавно поражения тонкого и толстого кишечника, вызванные Аспирином и другими нестероидными противовоспалительными препаратами: скрытые и явные кровотечения, перфорации, стриктуры, обострения хронических энтероколитов. Частота этих осложнений значительно меньше, чем локализующихся в желудке и начальном отделе двенадцатиперстной кишки. Тем не менее они также оказывают отрицательное влияние на практическую значимость Аспирина в профилактике ишемических приступов.
Поражения тонкого кишечника в виде энтеропатий при приеме АСК встречались чаще, чем в контрольной группе пациентов (не принимавших Аспирин). Наиболее характерными были: диафрагмоподобные стриктуры (синдром обструкции тонкого кишечника) и аспирин-индуцированная энтеропатия (синдром, характеризующийся кишечными кровотечениями, потерей белка и мальабсорбцией).
Патологические изменения толстого кишечника при приеме нестероидных противовоспалительных препаратов бывают двух типов:
в ранее неизмененной толстой кишке (острый колит, одиночные язвы-эрозии в слепой, ободочной, сигмовидной кишках);
в ранее измененном кишечнике (перфорации при дивертикулезе, обострение хронических воспалительных процессов).
Вопросы профилактики повреждения слизистой ЖКТ при назначении АСК до конца не изучены и остаются актуальными в клинической практике. В настоящее время, по данным литературы, очевидно лишь то, что использование кишечно-растворимых форм АСК не решает этой проблемы.
Все вышеперечисленное ставит перед фармакологами и клиницистами задачи создания и внедрения в клиническую практику новых форм лекарственных препаратов, способных защитить ЖКТ от повреждающего воздействия пероральных нестероидных противовоспалительных препаратов.
Аспирин-индуцированные осложнения в слизистой ЖКТ диктуют его отмену и назначение цитопротекторов — антацидов. В ряде клинических и экспериментальных исследований показано, что антациды эффективны в лечении и профилактике эрозий и язв слизистой оболочки желудка при применении нестероидных противовоспалительных препаратов. Было продемонстрировано, что цитопротекторный эффект антацидов реализуется через стимуляцию образования простагландинов в стенке желудка (снижение уровня простагландинов в слизистой желудка — основной механизм эрозивно-язвенного процесса, вызванного применением Аспирина), усиление секреции бикарбонатов и увеличение гликопротеинов в слизистой желудка.
Особый интерес представляет препарат Кардиомагнил, который представляет собой соединение АСК (в наиболее эффективных и безопасных дозах — 75 и 150 мг) с невсасывающимся антацидом — гидроокисью магния [3].
Невсасывающиеся антациды являются одними из наиболее часто применяемых препаратов в гастроэнтерологической практике при лечении заболеваний желудка, в том числе и язвенной болезни. Свой положительный эффект они реализуют через абсорбцию соляной кислоты в желудке. Кроме того, невсасывающиеся антациды обладают и рядом других положительных эффектов: снижают протеолитическую активность желудочного секрета (адсорбируют пепсин, снижают его активность через повышение рН среды), обладают обволакивающим свойством, связывают лизолецитин и желчные кислоты, оказывающие неблагоприятное воздействие на слизистую ЖКТ.
Гидроокись магния, входящая в состав Кардиомагнила, действует быстрее по сравнению с гидроокисью алюминия, что чрезвычайно важно при использовании этого препарата в антиагрегантном лечении. АСК быстро всасывается из ЖКТ: терапевтические концентрации Аспирина в плазме крови достигаются через 15–20 мин от момента приема препарата, при этом специально проведенные исследования показали, что гидроокись магния в составе Кардиомагнила не влияет на скорость всасывания АСК [3, 10].
пожилым людям (после 60 лет);
пациентам с ИБС;
пациентам, страдающим цереброваскулярными заболеваниями;
пациентам, перенесшим инфаркты и инсульты;
людям среднего возраста (35–50 лет), имеющим высокий риск сердечно-сосудистых заболеваний.
Дозы и способы применения Кардиомагнила:
для первичной профилактики: первые 2–3 дня по 150 мг, далее по 75 мг/сут вечером после еды;
для вторичной профилактики и лечения: по 150 мг/сут длительно.
Таким образом, профилактика тромбозов и тромбоэмболий, составляющих ключевой момент в развитии сердечно-сосудистых патологий (ОКС, острый ИМ, ишемические инсульты, тромбоэмболии легочной артерии, поражение почек, периферические ангиопатии), с помощью антиагрегантных препаратов является определяющим направлением в лечении больных в терапевтической и хирургической практике. Тиенопиридины (в частности, клопидогрел (Плавикс)), АСК способствуют активной профилактике тромбоэмболий, а их сочетание позволяет уменьшить количество принимаемого препарата с повышением терапевтической активности и снижением побочных эффектов.
Кардиомагнил — первая применяемая в России комбинация АСК (антиагрегант) и гидроокиси магния (антацидный компонент) — устраняет ульцерогенное и диспептическое действие Аспирина, что позволяет рекомендовать его к применению в широкой практике лечения и профилактики сердечно-сосудистых патологий.
По вопросам литературы обращайтесь в редакцию.
А. М. Шилов, доктор медицинских наук, профессор
С. А. Князева, кандидат медицинских наук
С. А. Мацевич
ММА им. И. М. Сеченова, Москва