что такое натрий хлор в химии
Хлористый натрий
Хлористый натрий
| Хлорид натрия | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | хлорид натрия / Sodium chloride |
| Химическая формула | NaCl |
| Молярная масса | 58.44277 г/моль |
| Физические свойства | |
| Плотность вещества | 2.165 г/см³ |
| Термические свойства | |
| Температура плавления | 800,8 °C |
| Температура кипения | 1465 °C |
| Химические свойства | |
| Растворимость в воде | 35.9 г/100 мл |
| Классификация | |
| номер CAS | [7647-14-5] |
Хлорид натрия известен в быту под названием поваренной соли, основным компонентом которой он является. Хлорид натрия в значительном количестве содержится в морской воде, создавая её солёный вкус. Встречается в природе в виде минерала галита (каменная соль).
Чистый хлорид натрия имеет вид бесцветных кристаллов.
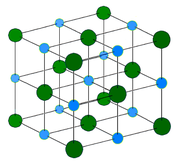
Кристаллическая структура
Хлорид натрия образует кристаллы с кубической симметрией. Более крупные ионы хлора образуют плотную кубическую упаковку, в свободных узлах которой (в вершинах правильного октаэдра) расположены ионы натрия.
Умеренно растворяется в воде, растворимость мало зависит от температуры: коэффициент растворимости NaCl (в г на 100 г воды) равен 35,9 при 21° С и 38,1 при 80° С. Растворимость хлорида натрия существенно снижается в присутствии хлороводорода, гидроксида натрия, солей — хлоридов металлов. Растворяется в жидком аммиаке, вступает в реакции обмена.
| Термодинамические характеристики | |
|---|---|
| ΔfH 0 g | −181,42 кДж/моль |
| ΔfH 0 l | −385,92 кДж/моль |
| ΔfH 0 s | −411,12 кДж/моль |
| ΔfH 0 aq | −407 кДж/моль |
| S 0 g, 1 bar | 229,79 Дж/(моль K) |
| S 0 l, 1 bar | 95,06 Дж/(моль K) |
| S 0 s | 72,11 Дж/(моль•K) |
Диэлектрическая проницаемость NaCl — 6,3
См. также
Полезное
Смотреть что такое «Хлористый натрий» в других словарях:
ХЛОРИСТЫЙ НАТРИЙ — Поваренная соль. Объяснение 25000 иностранных слов, вошедших в употребление в русский язык, с означением их корней. Михельсон А.Д., 1865. ХЛОРИСТЫЙ НАТРИЙ То же, что поваренная соль. Словарь иностранных слов, вошедших в состав русского языка.… … Словарь иностранных слов русского языка
ХЛОРИСТЫЙ НАТРИЙ — (ХН) – кристаллический порошок белого цвета, растворимый в воде; должен храниться в условиях исключающих увлажнение. [Изотов В.С. Химические добавки для модификации бетона: монография / В.С. Изотов, Ю.А. Соколова. М.: Казанский Государственный… … Энциклопедия терминов, определений и пояснений строительных материалов
Хлористый натрий — см. Соль поваренная, Каменная соль и Натрий … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
хлористый натрий — хлорид натрия … Cловарь химических синонимов I
НАТРИЙ — НАТРИЙ. Natrium, химич. элемент, симв. Na, серебристобелый, блестящий, при обыкновенной t° восковой плотности одноатомный металл, делающийся хрупким на холоду и при ярко краснокалильном жаре перегоняющийся; открыт Де.ви (1807) электролизом… … Большая медицинская энциклопедия
хлористый — прилагательное от слова хлор; хлористый этил – жидкость, получаемая из винного спирта и соляной кислоты; ввиду её быстрой испаряемости ею пользуются в медицине для местной анестезии; хлористый кальций – вещество, получаемое при растворении… … Словарь иностранных слов русского языка
ХЛОРИСТЫЙ — ХЛОРИСТЫЙ, хлористая, хлористое (хим.). Находящийся в соединении с хлором, содержащий в себе хлор. Хлористый кальций. Хлористый натрий. Хлористый водород. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
НАТРИЙ — (греч. nitron, лат. natrum). Металл белого цвета, составляющий часть поваренной соли, соды, селитры и др. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. НАТРИЙ белый блестящий мягкий металл, быстро окисляющийся в… … Словарь иностранных слов русского языка
НАТРИЙ — щелочный металл белого цвета, блестящий, быстро тускнеющий на воздухе; при соединении с водой образует едкий натр, энергично выделяя водород. Физические свойства Н.: уд. вес 0,97, темп pa плавления 97,7°. Чистый Н. хранится только в керосине. В… … Технический железнодорожный словарь
Натрий* — (хим.; нем. Natrium, франц. и англ. Sodium). Сведения о соединениях этого металла ведут свое начало от очень старых времен. Еврейское слово neter (греч. νίτρον, лат. nitrum) встречается в Библии как название вещества, которое, по Соломону,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Хлорид натрия
Хлорид натрия или хлористый натрий (NaCl) — натриевая соль соляной кислоты. Известен в быту под названием поваренной соли, основным компонентом которой и является. Хлорид натрия в значительном количестве содержится в морской воде. Встречается в природе в виде минерала галита (каменной соли). Чистый хлорид натрия представляет собой бесцветные кристаллы, но с различными примесями его цвет может принимать голубой, фиолетовый, розовый, жёлтый или серый оттенок.
Содержание
Нахождение в природе и производство
В природе хлорид натрия встречается в виде минерала галита, который образует залежи каменной соли среди осадочных горных пород, прослойки и линзы на берегах солёных озёр и лиманов, соляные корки в солончаках и на стенках кратеров вулканов и в сольфатарах. Огромное количество хлорида натрия растворено в морской воде. Мировой океан содержит 4 × 10 15 тонн NaCl, то есть из каждой тонны морской воды можно получить в среднем 1,3 кг хлорида натрия. Следы NaCl постоянно содержатся в атмосфере в результате испарения брызг морской воды. В облаках на высоте полтора километра 30 % капель, больших 10 мкм по размеру, содержат NaCl. Также он найден в кристаллах снега.
Наиболее вероятно, что первое знакомство человека с солью произошло в лагунах тёплых морей или на соляных озёрах, где на мелководье солёная вода интенсивно испарялась под действием высокой температуры и ветра, а в осадке накапливалась соль. По образному выражению Пифагора, «соль была рождена благородными родителями: солнцем и морем».
Галит
В природе хлорид натрия чаще всего встречается в виде минерала галита. Он имеет гранецентрированную кубическую решётку и содержит 39,34 % Na, 60,66 % Cl. Другими химическими элементами, входящими в состав примесей, являются: Br, N, H, Mn, Cu, Ga, As, I, Ag, Ba, Tl, Pb, K, Ca, S, O. Плотность 2,1—2,2 г/см³, а твёрдость по шкале Мооса — 2. Бесцветный прозрачный минерал со стеклянным блеском. Распространённый минерал соленосных толщ. Образуется при осаждении в замкнутых водоёмах, а также как продукт сгона на стенках кратеров вулканов. Составляет пласты в осадочных породах лагунных и морских фаций, штокоподобные тела в соляных куполах и тому подобных.
Каменная соль
Каменной солью называют осадочную горную породу из группы эвапоритов, состоящую более чем на 90 % из галита. Галит также часто называют каменной солью. Эта осадочная горная порода может быть бесцветной или снежно-белой, но чаще она окрашена примесями глин, талька (серый цвет), оксидами и гидроксидами железа (жёлтый, оранжевый, розовый, красный), битумами (бурая). Каменная соль содержит хлориды и сульфаты натрия, калия, магния и кальция, бромиды, йодиды, бораты, гипс, примеси карбонатно-глинистого материала, доломита, анкериту, магнезита, битумов и так далее.
По условиям формирования месторождений каменную соль подразделяют на следующие виды:
Морская соль
Морская соль является смесью солей (хлориды, карбонаты, сульфаты и т. д.), образующейся при полном испарении морской воды. Среднее содержание солей в морской воде составляет:
| Соединение | Масс. доля, % |
|---|---|
| NaCl | 77,8 |
| MgCl2 | 10,9 |
| MgSO4 | 4,7 |
| KCl | 2,5 |
| K2SO4 | 2,5 |
| CaCO3 | 0,3 |
| Ca(HCO3)2 | 0,3 |
| другие соли | 0,2 |
При испарении морской воды при температуре от +20 до +35 °C в осадке сначала кристаллизуются наименее растворимые соли — карбонаты кальция и магния и сульфат кальция. Затем выпадают более растворимые сульфаты натрия и магния, хлориды натрия, калия и магния, и после них — сульфаты калия и магния. Последовательность кристаллизации солей и состав осадка может несколько варьироваться в зависимости от температуры, скорости испарения и других условий. В промышленности морскую соль получают из морской воды, в основном методом обычного выпаривания. Она отличается от каменной соли значительно большим содержанием других химических солей, минералов и различных микроэлементов, в первую очередь йода, калия, магния и марганца. Соответственно, она отличается от хлорида натрия и по вкусу — горько-солёный привкус ей придают соли магния. Она используется в медицине: при лечении кожных заболеваний, таких как псориаз. Как лечебное вещество в аптечной и обычной торговой сети, распространённым продуктом является соль из Мёртвого моря. В очищенном виде этот вид соли также предлагается в продуктовой торговой сети — как натуральная и богатая йодом пищевая.
Залежи
Залежи каменной соли найдены во всех геологических системах. Важнейшие из них сосредоточены в кембрийских, девонских, пермских и третичных отложениях. Каменная соль составляет мощные пластовые залежи и ядра сводчатых структур (соляных куполов и штоков), образует прослойки, линзы, гнезда и вкрапления в других породах. Среди озёрных месторождений России крупнейшие — Эльтонское, Баскунчак в Прикаспии, Кучукское озеро, Кулундинское озеро, Эбейты и другие озёра в Западной Сибири.
Производство
В древности технология добычи соли заключалась в том, что соляную рапу (раствор) вытаскивали лошадиным приводом из шахт, которые назывались «колодцами» или «окнами», и были достаточно глубокими — 60—90 м. Извлечённый солевой раствор выливали в особый резервуар — творило, откуда она через отверстия стекала в нижний резервуар, и системой жёлобов подавалась в деревянные башни. Там её разливали в большие чаны, на которых соль вываривали.
На Руси поморы вываривали соль на побережье Белого моря и называли её морянка. В 1137 году новгородский князь Святослав определил налог на соляные варницы.
Беломорской солью, называемой «морянкой», торговали по всей Российской империи до начала XX века, пока её не вытеснила более дешёвая поволжская соль.
Современная добыча хлорида натрия механизирована и автоматизирована. Соль массово добывается выпариванием морской воды (тогда её называют морской солью) или рассола с других ресурсов, таких как соляные источники и соляные озера, а также разработкой соляных шахт и добычей каменной соли.
Для добычи хлорида натрия из морской воды необходимы условия жаркого климата с низкой влажностью воздуха, наличие значительных низменных территорий, лежащих ниже уровня моря, или затопляемых приливом, слабая водопроницаемость почвы испарительных бассейнов, малое количество осадков в течение сезона активного испарения, отсутствие влияния пресных речных вод и наличие развитой транспортной инфраструктуры.
Мировое производство соли в 2009 году оценивается в 260 миллионов тонн. Крупнейшими мировыми производителями являются Китай (60,0 млн тонн), США (46,0 млн тонн), Германия (16,5 млн тонн), Индия (15,8 млн тонн) и Канада (14 млн тонн).
Добыча соли в южной части Мертвого моря, Израиль
Хлорид натрия
Характеристики и физические свойства хлорида натрия
Плавится и кипит без разложения. Умеренно растворяется в воде (не гидролизуется), растворимость не зависит от температуры, но сильно снижается в присутствии HCl, NaOH, хлоридов металла.
Рис. 1. Хлорид натрия. Внешний вид.
Основные характеристики хлорида натрия приведены в таблице ниже:
Молярная масса, г/моль
Температура плавления, o С
Температура кипения, o С
Растворимость в воде (25 o С), г/100 мл
Получение хлорида натрия
Хлорид натрия в виде минерала галита образует залежи каменной соли среди пластов горных и осадочных пород, поэтому необходимости его получения в промышленных или лабораторных масштабах нет. Однако, иногда он образуется в качестве побочного продукта, например, в таких реакциях, как:
— взаимодействие натрия с хлором
— реакция нейтрализации между соляной кислотой и гидроксидом натрия
HCl + NaOH = NaCl + H2O.
Химические свойства хлорида натрия
В водном растворе хлорид натрия диссоциирует на ионы:
Хлорид натрия способен вступать в реакции обмена с кислотами (1) и другими солями (2, 3):
В окислительно-восстановительных реакциях хлорид натрия проявляет свойства слабого восстановителя:
При пропускании через насыщенный раствор хлорида натрия смесь газов, состоящую из аммиака и диоксида углерода можно получить гидрокарбонат натрия (выпадает в осадок):
Расплав и раствор хлорида натрия подвергаются электролизу:
Применение хлорида натрия
Хлорид натрия (поваренная соль) служит сырьем для получения хлора, соляной кислоты, едкого натра и карбоната натрия (соды), применяется в красильном деле, в мыловарении и во многих других производствах. Он служит также приправой к пище и применяется в качестве средства, предохраняющего пищевые продукты от порчи.
Примеры решения задач
| Задание | Какой объем хлора надо взять для реакции с 10 г натрия? |
| Решение | Запишем уравнение реакции взаимодействия хлора с натрием: |
Рассчитаем количество вещества натрия, вступившего в реакцию:
n (Na)= 10 / 23 = 0,43 моль.
Согласно уравнению, n (Na) :n(Cl2) = 2 : 1, значит,
n (Cl2) = ½ n (Na) = ½ ×0,43 = 0,215моль.
Тогда, объем хлора, вступившего в реакцию взаимодействия с натрием равен:
V (Cl2) = 0,215 × 22,4 = 4,816л.
| Задание | К 200-м граммам 5%-го раствора хлорида натрия добавили 15 г этой же соли и столько же граммов воды. Чему стала равна массовая доля хлорида натрия в получившемся растворе? |
| Решение | Решение задачи следует начать с записи формулы для вычисления массовой доли растворенного вещества: |
Найдем массу растворенного вещества хлорида натрия в изначальном растворе:
msolute (NaCl) = ω (NaCl) / 100% ×msolution;
msolute (NaCl) = 5 / 100% × 200 = 10 г.
Рассчитаем массу нового раствора:
msolution(new) = 200 + 15 + 15 = 230 г.
Найдем общую массу растворенного хлорида натрия и его массовую долю в новом растворе:
m(NaCl)sum = 10 + 15 = 25г.
ω (NaCl)new= 25 / 230 × 100% = 11%.
Хлорид натрия — важнейший химический реактив
Хлорид натрия составляет основу поваренной соли, самой популярной приправы 
Свойства хлорида натрия
NaCl представляет собой кристаллы с кубической ионной решеткой. Кристаллы без цвета и запаха, с четко выраженным соленым вкусом. Хлористый натрий водорастворим, не гигроскопичен. Растворяется в аммиаке, этиловом и метиловом спирте, муравьиной кислоте, глицерине, этиленгликоле. Не растворяется в ацетоне, соляной кислоте, диэтиловом эфире.
Водный раствор хлорида натрия замерзает при температуре ниже нуля. Благодаря этому свойству химреактив довольно долго использовался в качестве антигололедного средства на дорогах и тротуарах (сейчас этот способ считается экологически вредным и применяется все реже). На этом же свойстве основано применение смеси мелко наколотого льда и поваренной соли в качестве эффективного и простого охладителя, способного понизить температуру смеси на пару десятков градусов.
Хлорид натрия в природе и жизни человека

В природе хлористый натрий встречается в морской воде, соленых озерах, в соляных подземных водах, в ископаемом виде (галит, каменная соль). Галит — это минеральная форма NaCl. Иногда галит называют каменной солью, но это неверно. Каменная соль — это осадочная порода, содержащая 90% галита и примеси железа, гипса, магнезита, талька, битумов, соединений калия, кальция, магния, йода, брома, бора. Каждое месторождение каменной соли имеет свой уникальный состав.
Морская соль, получаемая выпариванием морской воды, содержит больше жизненно важных для человека примесей химических элементов, минералов и солей, чем каменная соль. В ней только 77,8% хлористого натрия. Она имеет горьковатый вкус, используется, преимущественно, в медицине и кулинарии.
Применение NaCl
— Химреактив применяется для производства более полутора тысяч веществ 
— Поваренная соль — готовый продукт, на 97 и более процентов состоящий из NaCl, используется в пищевой промышленности. Чем выше содержание хлорида натрия, тем выше сорт соли. Выпускаются также специализированные сорта с добавками микроэлементов, например, иодированная соль. Пищевая соль применяется как приправа в пищу, в качестве консерванта.
— В промышленной и полупромышленной водоподготовке для регенерации ионообменных смол в натрий-катионитовых фильтрах.
— Растворы хлорида натрия востребованы в медицине для приготовления и разведения лекарственных средств, для восстановления водно-солевого баланса организма, при кровотечениях, в качестве антидота при отравлении нитратом серебра, как антибактериальное средство для обработки ран, для некоторых других целей.
— В зоологии — для добавки в рацион животных.
Магазин «ПраймКемикалсГрупп» предлагает по хорошей цене купить поваренную соль оптом и в розницу. Также у нас широко представлены другие реактивы для лабораторных исследований и промышленности, лабораторная посуда и приборы.
Состав хлорида натрия (NaCl), свойства, применение, токсичность
Хлорид натрия представляет собой кристаллическое белое твердое вещество, которое образуется в результате сочетания натрия, серебристо-белого металла, который бурно реагирует с водой, и элемента хлора, ядовитого, едкого, бледно-зеленого газа..
На верхнем изображении показана часть кристаллов NaCl. Как это возможно, что два элемента столь же опасны, как Na и Cl2, может образовываться пищевая соль? Во-первых, химическое уравнение его образования:
Кроме того, Na + отвечает за генерацию и проведение нервных импульсов в нейрональных аксонах, а также за инициацию сокращения мышц.
NaCl использовался с древних времен для придания аромата пище и сохранения мяса благодаря его способности уничтожать бактерии и предотвращать порчу.
Это также необходимо для производства гидроксида натрия (NaOH) и молекулярного хлора (Cl2) путем взаимодействия NaCl с водой при гидролизе:
В катоде (-) Н накапливается2 (г) и NaOH. Между тем Cl накапливается на аноде (+)2 (G). Гидроксид натрия используется при производстве мыла и хлора при производстве пластика ПВХ.
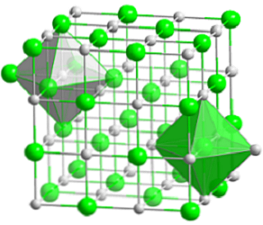
Структура хлорида натрия
Унитарная ячейка
Элементарная ячейка каменной соли является кубической, но какие именно кубы точно представляют ее на изображении выше? Октаэдры дают ответ. Оба покрывают в общей сложности четыре маленьких кубика.
У этих кубиков есть части ионов в их вершинах, краях и гранях. Соблюдая осторожность, ион Na + он расположен в центре и двенадцать из них по краям. Ион на одном ребре может быть разделен на четыре куба. Таким образом, есть 4 иона Na + (12 × 1/4 + 1 = 4).