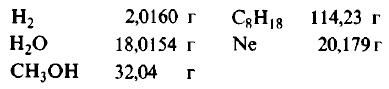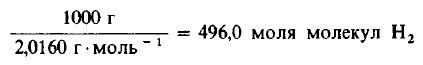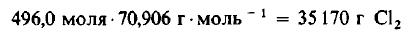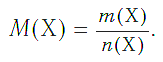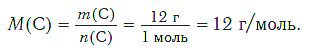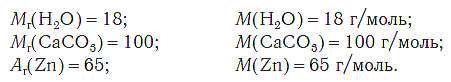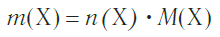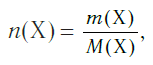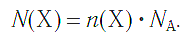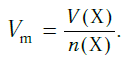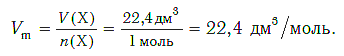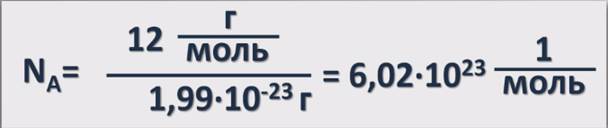что такое моль и молярная масса
Урок 5. Моль и молярная масса
В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.
Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·10 23 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·10 23 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12 C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·10 23 ).
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
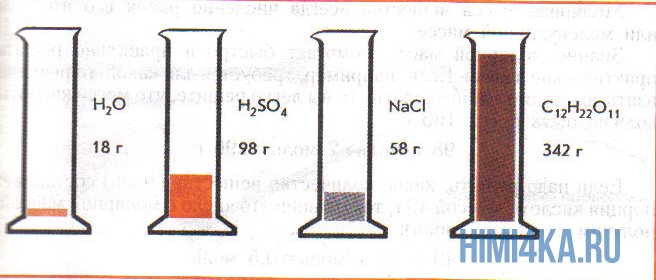
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·10 23 ; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·10 23 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·10 23 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·10 23 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·10 23 молекул/моль, что равно 2,99·10 26 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.
Урок 9. Молярная масса и молярный объем
В уроке 9 «Молярная масса и молярный объем» из курса «Химия для чайников» выясним, что подразумевается под молярной массой и молярным объемом; приведем формулы для их вычисления. Напоминаю, что в прошлом уроке «Химическое количество вещества и моль» мы выяснили, что такое химическое количество вещества; рассмотрели моль в качестве единицы количества вещества, а также познакомились с постоянной Авогадро.
Молярная масса
Вы знаете, что одинаковое химическое количество любых веществ содержит одно и то же число структурных единиц. Но у каждого вещества его структурная единица имеет собственную массу. Поэтому и массы одинаковых химических количеств различных веществ тоже будут различны.
Молярная масса — это масса порции вещества химическим количеством 1 моль.
В Международной системе единиц молярная масса выражается в кг/моль. В химии чаще используется дольная единица — г/моль.
Определим молярную массу углерода. Масса углерода химическим количеством 1 моль равна 0,012 кг, или 12 г. Отсюда:
Молярная масса любого вещества, если она выражена в г/моль, численно равна его относительной молекулярной (формульной) массе.
На рисунке 47 показаны образцы веществ (H2O, CaCO3, Zn), химическое количество которых одно и то же — 1 моль. Как видите, массы разных веществ химическим количеством 1 моль различны.
Молярная масса является важной характеристикой каждого отдельного вещества. Она отражает зависимость между массой и химическим количеством вещества. Зная одну из этих величин, можно определить вторую — массу по химическому количеству:
и, наоборот, химическое количество по массе:
а также число структурных единиц:
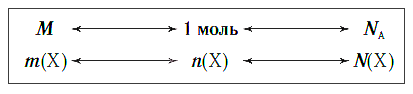
Взаимосвязь между этими тремя характеристиками вещества в любом его агрегатном состоянии можно выразить простой схемой:
Молярный объем
Подобно молярной массе, молярный объем газа равен отношению объема данного газообразного вещества V(Х) к его химическому количеству n(Х) :
Так как объем газа зависит от температуры и давления, то при проведении различных расчетов берутся обычно объемы газов при нормальных условиях (сокращенно — н. у.). За нормальные условия принимаются температура 0 °С и давление 101,325 кПа.
Установлено, что при нормальных условиях отношение объема любой порции газа к химическому количеству газа есть величина постоянная и равная 22,4 дм 3 /моль. Другими словами, молярный объем любого газа при нормальных условиях:
Пример 1. Вычислите химическое количество SiO2, масса которого равна 240 г.
Пример 2. Определите массу серной кислоты H2SO4, химическое количество которой 2,5 моль.
Пример 3. Сколько молекул CO2 и сколько атомов кислорода содержится в углекислом газе массой 110 г?
Пример 4. Какой объем занимает кислород химическим количеством 5 моль при нормальных условиях?
Краткие выводы урока:
Надеюсь урок 9 «Молярная масса и молярный объем» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Данный урок был заключительным в главе «Основные химические понятия».
Молекулярная физика. Моль. Постоянная Авогадро. Количество вещества.
Моль — количество вещества, масса которого, выраженная в граммах, численно равна относительной атомной (молекулярной) массе.
Моль — единица количества вещества в СИ (одна из основных единиц СИ).
В 1 моле содержится столько молекул (атомов или других частиц вещества), сколько атомов содержится в 0,012 кг нуклида углерода 12 С с атомной массой 12.
Из этого определения следует, что в одном моле любого вещества содержится одно и то же число атомов или молекул.
Число это называется постоянной Авогадро и обозначается NA:
Постоянная Авогадро (число Авогадро) — это число атомов (молекул, или других структурных элементов вещества), содержащихся в 1 моле.
Постоянная Авогадро — одна из фундаментальных физических констант. Она входит в некоторые другие постоянные, например, в постоянную Больцмана.
Количество вещества.
Количество вещества — это число частиц вещества (атомов, молекул), выраженное в молях. Учитывая определение моля и числа Авогадро, можно сказать, что количество вещества v равно отношению числа молекул N в данном теле к постоянной Авогадро NA, т.е. к числу молекул в 1 моле вещества:

Что такое моль и молярная масса
Письмо с инструкцией по восстановлению пароля
будет отправлено на вашу почту
В химической практике, имея дело с веществами, а не с отдельными атомами или молекулами, химики редко используют массы, измеряемые в атомных единицах. Масса порции реагирующих веществ или продуктов реакции чаще измеряется в граммах или в более крупных единицах.
Чтобы перейти от молекул к порциям веществ, воспользуемся единицей измерения, которая называется моль.
Химик и физик из Франции Жозеф Луи Гей-Люссак в 1808 году изучал интересную химическую реакцию, в которой в результате взаимодействия двух газов – хлороводорода и аммиака – получалось кристаллическое вещество – хлорид аммония.
Оказалось, что для реакции требуются одинаковые объемы хлороводорода и аммиака. Если одного из этих газов вначале будет больше, то по окончании реакции этот избыток оставался неиспользованным.
Гей-Люссак привел свои наблюдения в статье, но никаких выводов из них не сделал. Важные заключения через три года привел итальянский химик Амедео Авогадро. В 1811 году, в результате экспериментов и расчетов, Авогадро пришел к мысли, что равные объемы газов, находящихся при одинаковых условиях, содержат одно и то же число молекул.
Гипотеза Авогадро долго считалась спорной, поскольку не подтверждалась расчетами, основанными на ошибочном мнении о немолекулярном строении простых газообразных веществ. Однако в 1865 году австрийский физик и химик Иоганн Лошмидт предпринял попытку рассчитать число молекул газа в заданном объеме.
Когда гипотеза Авогадро была признана, ученые получили возможность правильно определять состав молекул химических соединений, рассчитывать атомные и молекулярные массы. Эти знания позволяли легко рассчитывать массовые соотношения веществ в химических реакциях. Пользоваться этими соотношения очень удобно: измеряя массу веществ в граммах, ученые как бы оперировали молекулами.
Количество вещества, численно равное относительной молекулярной массе, но выраженное в граммах, назвали грамм-молекулой или молем.
Слово «моль» придумал в начале XX века немецкий физико-химик, лауреат Нобелевской премии Вильгельм Оствальд. Слово происходит от слова «молекула».
Моль – это количество вещества, содержащее столько структурных единиц (атомов, молекул), сколько содержится атомов в 0,012 кг углерода.
Согласно Международной системе единиц СИ моль является единицей измерения особой физической величины – количества вещества. Под количеством вещества (обозначается греческой буквой ν) понимают число структурных единиц этого вещества (атомов, молекул и др.).
Самое важное заключается в том, что 1 моль любого вещества содержит одно и то же число молекул. Это число называется постоянной или числом Авогадро. Она обозначается символом NA. Постоянная Авогадро рассчитана давно и представляет собой очень большое число.
Если массу 1 моля углерода 12 г/моль разделить на массу 1 атома углерода 1,9910-23 г, то получится число, равное 6,02·1023. Поскольку это число обозначает количество частиц в 1 моле, единицы его пишут как 1/моль, моль-1 или обратный моль.
Чтобы как-то представить это число, скажем лишь, что оно больше, чем число стаканов воды, которое содержится в Мировом океане, а 6,02·1023 зёрен пшеницы имели бы массу порядка 2·1016 тонн.
Для сбора такого урожая потребовалось бы более 2 миллионов лет. Из примеров ясно: применение числа Авогадро для отсчета макротел бессмысленно. Главное его назначение – определение количества частиц (атомов и молекул) микромира и связь единиц микро и макромира.
Зная количество вещества, можно судить о числе частиц в определенной его порции и брать вещества для реакций в необходимых количествах. Таким образом, химики могут определять число атомов и молекул путём взвешивания порций веществ. Приведём примеры таких расчётов. Чтобы вычислить количество вещества, зная число частиц, используем формулу 2 где ν – количество вещества в молях, N – число частиц вещества, NА – постоянная Авогадро.
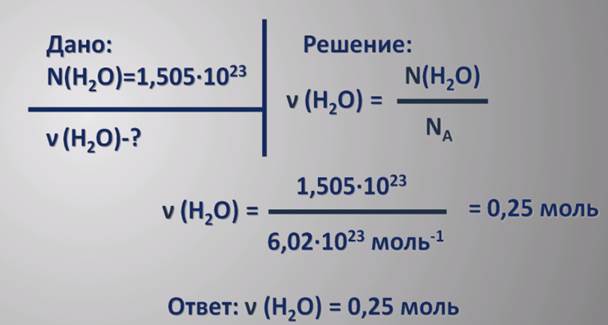
Задача.Какое количество вещества содержит 1,505·1023 молекул воды?
В химии редко используется такая величина как число частиц. Гораздо легче использовать величины, которые легко измерить. Такой величиной является масса вещества. Как же связаны между собой масса и количество вещества? Зная число молекул вещества в одном моле и массу одной молекулы, можно подсчитать массу одного моля вещества. Например, известно, что масса молекулы воды равна
2,992·10-23г. Умножив ее на постоянную Авогадро, 6,02·1023 обратных молей, мы получим
18 г/моль – массу одного моля воды или молярную массу воды.
Молярной массой называется масса вещества, взятого в количестве 1 моль. Измеряется она в г/моль и обозначается латинской буквой М. Чтобы найти молярную массу вещества, нет необходимости проделывать столь сложные расчеты. Достаточно помнить, что молярная масса численно равна относительной молекулярной массе и имеет размерность г/моль.
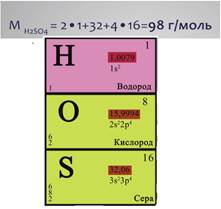
Например, относительная молекулярная масса серной кислоты Н2SО4 равна 2·1+32+4·16=98, следовательно, молярная масса серной кислоты Н2SО4 равна 98 г/моль.
Молярную массу используют для перевода количества вещества в массу и наоборот. Для расчетов используют формулу: количество вещества ν равно отношению массы вещества m к молярной массе этого вещества М.
Решим задачу. Вычислить количество вещества азотной кислоты массой 75,6 г.
Если требуется найти массу, зная количество вещества, формулу преобразуют: масса вещества m равна произведению количества вещества ν на молярную массу этого вещества М.
Количество вещества. Моль. Молярная Масса. Формула
Количество вещества применяться для измерения макроскопических количеств веществ во многих естественных науках таких как, физика, химия, при изучении электролиза, в термодинамика, описывающая состояние идеального газа. Так как молекулы взаимодействуют независимо от их массы в количествах, кратным целым числам, то при описании химических реакций, использовать количества вещества удобнее, чем массу. Для того, чтобы понять, что такое количества вещества в химии, отметим, что у величины есть своя единица измерения.
Определение, единицы измерения, обозначение
Число аналогичных структурных единиц, содержащих в веществе (атомов, электронов, молекул, ионов и других частиц) и есть физическая величина — количество вещества. По международной системе единиц (СИ) измеряется количество вещества в [моль], [кмоль], [ммоль], при использовании в расчетах, обозначается как n (эн).
Применение, значение
В химии при написании химических уравнений, после знакомства законом постоянства массы веществ, становится понятно как использовать величину количества вещества и понятно ее значение. Например, в реакции горения водорода, его требуется 2 к 1 значению кислорода. Зная массу водорода, можно получить количества вещества кислорода, участвующего в реакции горения.
Для вычисления количества вещества на основании его массы пользуются понятием молярная масса, т.е отношение массы вещества к количеству к количеству молей этого вещества:
где m — масса вещества, M — молярная масса вещества.
Молярная масса измерятся в [ г/моль].
Также молярная масса может быть найдена произведением молекулярной массы этого вещества на количество молекул в 1 моле — на число Авогадро.
Количество вещества газообразного определяют на основе его объема:
где где V — объём газа при нормальных условиях, а Vm — молярный объем газа при тех же условиях, равный 22,4 л/моль по закону Авогадро.
Подводя итоги всех расчетов, можно вывести общую формулу для количества вещества:
Вычисления
Чтобы точнее понять, что такое количество вещества, решим простейшие задачи: какое количество вещества содержится в алюминиевой отливке, массой m = 5,4 кг?
При решении это задачи следует помнить, что молярная масса численно равна относительной молекулярной массе, для нахождения которой понадобится таблица Менделеева, округляя значения: μ = 2,7 ⋅ 10-2 кг/моль.
Таким образом, количество вещества находим путем простых вычислений:
n = m/μ = 5,4 кг/ 2,7 ⋅ 10-2 кг/моль = 2⋅ 10-2 моль.
В физике также используется данная величина. Она нужна в молекулярной физике, где проводятся вычисления давления, объема газообразных веществ по уравнению Менделеева-Клапейрона: