что такое интерстициальная жидкость
Что такое интерстициальная жидкость
Примерно 1/6 общего объема тела приходится на межклеточные пространства. Они имеют общее название «интерстиции». Жидкость, заполняющую это пространство, называют интерстициальной (тканевой) жидкостью.
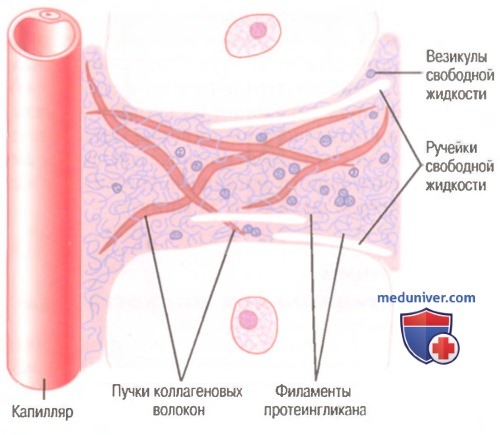
Структура интерстициального пространства показана на рисунке выше. Оно содержит плотные компоненты: (1) пучки коллагеновых волокон; (2) филаменты протеингликана. Пучки коллагеновых волокон имеют большую длину. Они являются особо прочными и обеспечивают значительную часть упругости тканей. Филаменты протеингликана представляют собой очень тонкие свернутые или перекрученные молекулы, состоящие на 98% из гиалуроновой кислоты и на 2% из белка. Эти молекулы настолько тонкие, что никогда не видны в световой микроскоп и с трудом определяются даже при электронной микроскопии. Тем не менее, они формируют плотную мелкоячеистую сеть, похожую на войлок.
а) Гель в интерстициальном пространстве. Жидкость интерстициального пространства образуется путем фильтрации и диффузии из просвета капилляров. Она содержит все компоненты плазмы, кроме белков, поскольку белки в основном не могут выходить из капилляров. Интерстициальная жидкость задерживается главным образом в микроскопических пространствах между молекулами протеингликана. Совокупность этих молекул и жидкости, захваченной ими, имеет свойства геля, и поэтому ее называют тканевым гелем.
Из-за большого количества молекул протеингликана жидкость с трудом протекает через тканевой гель. Вместо этого она диффундирует через гель. Это означает, что жидкость благодаря тепловому движению перемещается из одной точки в другую буквально молекула за молекулой, а не течет общим потоком, в котором участвует сразу большое количество молекул.
Скорость диффузии через гель составляет 95-99% скорости диффузии в свободной жидкости. Поскольку расстояние между капиллярами и клетками тканей очень короткое, диффузия обеспечивает быстрый транспорт не только воды, но также электролитов, низкомолекулярных питательных веществ, метаболитов, углекислого газа и др.
б) Свободная жидкость в интерстиции. Несмотря на то, что почти вся жидкость в интерстиции захвачена тканевым гелем, существуют отдельные маленькие ручейки свободной жидкости и везикулы, содержащие свободную жидкость. Эта жидкость не связана с молекулами протеингликана и поэтому течет свободно. Если в циркулирующую кровь ввести краску, можно видеть, как она протекает в интерстиции маленькими ручейками, чаще всего вдоль коллагеновых волокон или клеточных мембран.
Количество свободной жидкости в тканях обычно невелико — не более 1%. И наоборот, когда в тканях развивается отек, количество везикул и потоков свободной жидкости значительно увеличивается. В этом случае более половины объема жидкости в тканях представляет собой свободно текущую жидкость, не связанную с протеингликанами.
Редактор: Искандер Милевски. Дата публикации: 2.12.2020
Что такое интерстициальная жидкость
или Пневмапсихосоматология человека
Русско-англо-русская энциклопедия, 18-е изд., 2015
22,5 ÷ 27% массы тела и представляет собой водный раствор неорганических солей, питательных веществ и конечных продуктов метаболизма. По составу интерстициальная жидкость почти идетнична плазме крови, отличаясь от нее очень низкой концентрацией белков (
40% концентрации белков плазмы,
1,5 ÷ 6,0 г / дл). Это количество белков обусловливает уровень коллоидного осмотического давления интерстициальной жидкости
8 мм рт ст.
Интерстициальная жидкость играет важнейшую роль промежуточной среды, через которую осуществляется двусторонний обмен веществами (вода, органические и неорганические вещества) между кровью и клетками других тканей. Структурой системы кровообращения, непосредственно участвующей в этом процессе обмена является микрогемациркуляторное русло. В этом процессе участвуют также капилляры системы лимфообращения. Обмен веществами через интерстициальную жидкость осуществляется главным образом путем диффузии и фильтрации.
При косвенной оценке установлено, что нормальное давление интерстициальной жидкости составляет
Схема. Межклеточное пространство.
Модификация: Guyton & Hall. Textbook of Medical Physiology, 12th ed., 2006, 1152 p. См.: Физиология человека: Литература. Иллюстрации.

Около одной шестой части общего объёма тела человека составляет пространство между клетками, или межклеточное (интерстициальное) пространство. Жидкость, находящаяся в этом пространстве называют межклеточной (интерстициальной) жидкостью.
Межклеточное пространство кроме жидкости содержит два главных типа твёрдых структур: пучки коллагеновых волокон и протеогликановые нити. Продольно расположенные пучки коллагеновых волокон обеспечивают эластичность тканей. Тончайшие протеогликановые волокна представляют собой скрученные в форме спиралей или завитков молекулы, содержащие
2% белков. Молекулы настолько тонки, что могут быть неразличимы при рассмотрении с помощью светового микроскопа и обнаруживаются только при электронной микроскопии. Протеогликановые нити в интерстициальных пространствах образуют рыхлую узкопетлистую сеть наподобие войлока.
Жидкость попадает в межклеточное пространство посредством фильтрации и диффузии из кровеносных капилляров. Она содержит почти все те же вещества, что и плазма крови. Исключением являются белки. Их молекулы слишком велики для того, чтобы проходить через поры эндотелия капилляров. Поэтому концентрация белков в интерстициальной жидкости ничтожно мала. Интерстициальная жидкость располагается в мельчайших по объёму пространствах между протеогликановыми волокнами. Получается раствор, взвесь протеогликановых волокон в интерстициальной жидкости, обладающая свойствами геля. Поэтому раствор протеогликановых нитей в интерстициальной жидкости называют тканевым гелем. Поскольку протеогликановые нити образуют рыхлую узкопетлистую сеть, свободное движение растворителя, а также других массивных количеств молекул веществ через ячейки сети ограничено. Вместо этого транспорт отдельных молекул веществ через тканевой гель осуществляется посредством простой диффузии. Диффузия веществ через гель осуществляется почти так же быстро (на 99%), как и диффузия через свободную от протеогликановых нитей интерстициальную жидкость. Большая скорость диффузии и малые расстояния между капиллярами и клетками тканей позволяют проходить через интерстициальные пространства не только молекулам воды, но также и электролитам, питательным веществам с малыми размерами молекул, кислороду, двуокиси углерода и другим конечным продуктам метаболизма клеток, ряду других веществ.
Хотя почти вся жидкость интерстициальных пространств находится в тканевом геле, некоторое количество жидкости находится в мельчайших свободных протоках и свободных пузырьках интерстициального пространства. Потоки свободно протекающей жидкости (свободной от протеогликановых нитей) по интерстициальным пространствам можно наблюдать, если в циркулирующую кровь вводить какой-либо краситель. Краска вместе со свободной жидкостью протекает вдоль поверхностей коллагеновых волокон или по наружным поверхностям клеток. В нормальных тканях количество такой свободно протекающей интерстициальной жидкости очень невелико и составляет менее одного процента. В противоположность этому, при отёках эти мельчайшие ёмкости и протоки значительно увеличиваются. В них может содержаться более 50% интерстициальной жидкости свободной от протеогликановых нитей.
Санкт-Петербург, Россия, 1996-2015
Разрешается некоммерческое цитирование материалов данной энциклопедии при условии
полного указания источника заимствования: имени автора, названия и WEB-адреcа данной энциклопедии
Что такое интерстициальная жидкость
Общая классификация отеков
Отек – нарушение водно-электролитного баланса, характеризующееся усиленным выходом жидкости из сосудистого микроциркуляторного русла в интерстициальное пространство или клеточные элементы различных органов и тканей. Отеки могут быть внутриклеточными и внеклеточными, системными (при сердечной недостаточности, гломерулонефритах, печеночной недостаточности) или местными (в зоне венозной гиперемии различного происхождения, аллергических реакций).
Патогенетической основой как местных, так и генерализованных отеков являются нарушения тех факторов, которые обеспечивают транскапиллярный обмен воды, проанализированных Э. Старлингом (1896). Речь идет о движущих силах транссудации и резорбции. Суть в том, что на уровне капилляров происходит два процесса перемещения жидкости: транссудация (фильтрация) жидкой части крови в интерстициальное пространство и резорбция жидкости из ткани в кровь. В норме эти два процесса должны быть сбалансированы, поскольку содержание жидкости в ткани является величиной относительно постоянной. Отек является результатом нарушения этого баланса с преобладанием транссудации над резорбцией.
Согласно классической теории Э. Старлинга обмен жидкости, с растворенными в ней веществами, определяется нижеприведенными факторами:
1) уровнем гидростатического давления в капиллярах и величиной тканевого сопротивления;
2) коллоидно-осмотическим давлением плазмы крови и тканевой жидкости;
3) проницаемостью сосудистой стенки.
Гидростатическое давление в артериальной части капилляров составляет в среднем 35-40 мм рт. ст., а в венозном – 15-16 мм рт. ст.; сопротивление тканей составляет около 6 мм, внутрисосудистое онкотическое давление – в среднем 22-24 мм рт. ст., а тканевое онкотическое – около 25 мм рт. ст. Следовательно, в артериальном конце капилляров эффективное фильтрационное давление равно примерно 12-15 мм рт. ст., что обеспечивает ультрафильтрацию жидкости. В венозном конце капилляров эффективное онкотическое давление преобладает над гидростатическим, что обеспечивает переход межклеточной жидкости в сосуды под влиянием эффективного внутрисосудистого онкотического давления, равного 6-8 мм рт. ст.
В норме в этих перемещениях устанавливается равновесие, которое в условиях патологии может нарушаться. Повышение давления в артериальной части капилляров встречается редко и может быть связано с общим увеличением объема циркулирующей крови. Повышение же давления в венозной части в условиях патологии бывает достаточно часто (венозная гиперемия, сердечная недостаточность).
Патологическое скопление жидкости в серозных полостях именуется водянкой. Так, выпот жидкости в брюшную полость – это асцит, в плевральную – гидроторакс, в полость околосердечной сумки – гидроперикард, в полость яичка – гидроцеле.
Жидкость невоспалительной природы именуется транссудат, а воспалительной природы – экссудат.
В зависимости от этиологических факторов и пусковых механизмов развития различают следующие виды отеков:
1. Гидродинамические отеки, обусловленные системным или локальным увеличением гидростатического давления и соответственно возрастанием площади фильтрации плазмы крови в сосудах микроциркуляторного русла (системные отеки при сердечной недостаточности или локальные отеки в зоне венозной гиперемии, тромбоза или эмболии венозных сосудов различного генеза).
2. Онкотические отеки формируются при снижении внутрисосудистого содержания белка в случаях развития нефротического синдрома, печеночной недостаточности, кахексии.
3. Осмотические отеки формируются в зоне гиперосмии, возникающей локально при альтерации клеток, синдроме цитолиза или при накоплении промежуточных продуктов распада различных соеденений.
4. Мембранозные отеки. В основе развития мембраногенных отеков лежат дегрануляция тучных клеток с освобождением вазоактивных соединений – гистамина, серотонина, гепарина, а также действие вновь синтезируемых медиаторов: лейкотриенов, простагландинов, свободных радикалов, повышающих проницаемость сосудов.
5. Лимфодинамические отеки имеют место при наследственных или приобретенных формах недостаточности лимфооттока, обусловленных или нарушением структуры сосудов, их тромбоэмболией, или комперссией экссудатом, транссудатом, опухолями, а также при спаечном процессе.
6. Отеки, связанные с нарушением нервной и гуморальной регуляции водно-солевого обмена (в случаях развития сердечной дыхательной, почечной и печеночной недостаточности, а также при ряде эндокринопатий возникает активация ренин-ангиотензиновой и симпато-адреналовой систем).
7. Отеки, связанные с положительным водным балансом (на фоне недостаточности почек, чрезмерного приема осмотически-активных соединений).
8. Аллергические отеки наиболее часто возникают при анафилактических (атопических) реакциях: ангионевротический отек Квинке, сенная лихорадка, атопический дерматит. В результате комплекса патохимических реакций выделяются большие количества гистамина, вызывающего резкое расширение сосудов и повышение проницаемости их стенок, вследствие чего жидкая часть крови начинает интенсивно выходить в ткани. Отек является одним из проявлений патофизиологической стадии аллергической реакции гуморального типа. При анафилактическом шоке возникает, как правило, отек легких в сочетании с отеком кожных покровов, слизистых различных органов и систем. Таким образом, в основе аллергического отека лежит, главным образом, мембранногенный фактор.
9. Кахектические отеки. Кахексия – патологическое состояние, характеризующееся тяжелыми трофическими расстройствами, потерей массы тела, перераспределением внутри- и внесосудистого пула жидкости. Этиологические факторы кахексии включают алиментарный фактор (голодание, вплоть до анорексии), а также расстройства функции эндокринной системы, алкоголизм, онкологические заболевания). Несмотря на различие этиологических факторов вызывающих кахексические отеки, ведущими патогенетическим механизмом развития указанной патологии являются недостаточность синтеза белков, снижение внутрисосудистого онкотического давления. При этом значительно усиливаются процессы ультрафильтрации плазмы крови в микроциркуляторном русле различных органов и тканей. Гипопротеинемические отеки имеют мягкую, тестоватую консистенцию; кожа над ними сухая, истонченная, прозрачная. Отеки симметричны, в основном локализуются в области голени, стопы, лица.
10. Токсические отеки. Ведущим патогенетическим фактором токсических отеков является повышение проницаемости сосудистой стенки на фоне действия бактериальных, токсических, алиментарных патогенных факторов. К токсическим отекам относятся инсектные отеки при укусах насекомых, а также змей. Токсический отек легких возникает на фоне ирритантного воздействия отравляющих веществ (хлора, фосгена, дифосгена и других). Проницаемость сосудистой стенки может повышаться под влиянием токсических соединений бактериальной природы (токсины дифтерийный, сибиреязвенный и др.), при действии экзогенных химических веществ (хлор, фосген и др.), при действии некоторых ядов различных насекомых и пресмыкающихся (комары, пчелы, шершни, осы, змеи и др.). Под влиянием воздействия этих агентов, помимо повышения проницаемости сосудистой стенки, происходит нарушение тканевого обмена и образование продуктов, усиливающих набухание коллоидов и повышающих осмотическую концентрацию тканевой жидкости. Возникающие при этом отеки называются токсическими.
Особенности развития отеков у детей
Ребенок в условиях нормы рождается в состоянии физиологической гипергидратации, которая особенно выражена у недоношенных детей.
Однако в ряде случаев у новорожденного имеет место патологическая гипергидратация, формирующаяся внутриутробно вследствие инфицирования плода, при тяжелых соматических, аллергических и инфекционных болезнях матери. Отеки могут быть следствием гипоксии и асфиксии плода при кровотечениях, травматическом родоразрешении, тромбогеморрагическом синдроме у матери и новорожденных.
В детском возрасте отеки, как и у взрослого человека, могут быть мембраногенными-вазогенными, гемодинамическими, онкотическими, лимфодинамическими или носить сочетанный характер. Достаточно часто у детей развиваются отеки инфекционно-аллергической природы, а в ряде случаев возникает наследственный ангионевротический отек. Нарушения водно-электролитного обмена у детей развиваются довольно быстро в связи с несовершенством механизмов регуляции водно-электролитного баланса.
Принципы терапии отеков
1. Устранение действия патогенетического фактора, патогенетическая терапия.
2. Симптоматическая терапия, включающая следующие мероприятия:
а) ограничение объема потребляемой жидкости, адекватное ее суточной потере;
б) ограничение потребления соли (до 1,0–1,5 г в день), сахара и углеводистой пищи (при сахарном диабете);
в) контроль суточного диуреза (должен соответствовать потребляемой жидкости);
г) назначение мочегонных средств;
д) контроль электролитов в крови (особенно калия).
Стратегия заместительной терапии острой кровопотери. Часть I
Основные принципы коррекции постгеморрагических нарушений гомеостаза.
Заместительной терапии острой кровопотери, возможностях и различных методиках ее коррекции посвящено огромное число работ во всех областях клинической медицины. Само по себе это свидетельствует как о крайней актуальности проблемы, так и об отсутствии единого мнения о путях её решения. То, что совсем недавно принималось за аксиому, на современном этапе развития медицины стало не только ставиться под сомнение, но и порой полностью отвергаться. К примеру, концепция замещения по принципу «капля за каплю» и переливание цельной крови сегодня полностью оставлены. И это притом, что в литературе прошлых лет приводятся десятки и сотни примеров о почти фантастических по своей целебной силе эффектах переливания цельной крови и массивных гемотрансфузий. Эволюция биотехнологий и достижения фарминдустрии сегодня позволяют всё чаще говорить об ограничении трансфузии компонентов крови, порой даже в случаях массивной кровопотери. Однако, возможности использования последних достижений гемотрансфузиологии, к сожалению, ограничены в стационарах неотложной хирургии, хотя именно в них сосредотачивается основная масса пациентов с кровотечениями различной этиологии.
Гипоксия при кровотечении носит как циркуляторный, так и гемический (анемический) характер. Именно двойственность патогенеза нарушений кислородного режима организма при кровотечении обуславливает как тяжелые патофизиологические сдвиги, так и сложность их патогенетической коррекции. Циркуляторная гипоксия, связанная с падением сердечного выброса приводит к снижению величины рО2 в клетках, включению анаэробного пути метаболизма и развитию ацидоза. Особый практический интерес представляет наблюдающаяся с течением времени трансформация нарушений кислородного режима в постгеморрагическом периоде. Так, выходящая на первый план в период продолжающегося кровотечения циркуляторная гипоксия после остановки кровотечения и компенсации макроциркуляции постепенно сменяется на гемическую гипоксию в результате аутогемодилюции, либо вследствие интенсивной инфузионной терапии. В последние годы особое значение уделяется так называемой постинфузионной гемической гипоксии, определена её роль в нарушениях кислородного режима организма и тяжелые патофизиологические последствия. Оптимальным уровнем гемодилюции на фоне введения инфузионных сред большинством автором признается уровень гематокрита не ниже 30%. Именно при этом уровне гемодилюции наблюдается выраженное улучшение реологических свойств крови, и, что самое главное, происходит повышение сердечного выброса без увеличения силы сердечных сокращений и потребности миокарда в кислороде, а лишь за счет улучшения реологических свойств и снижения общего периферического сосудистого сопротивления. Однако, принятая концепция лечения острой кровопотери по принципу «сначала восполняется объем циркулирующей крови, а затем ее качество» порой приводит к выраженной постинфузионной гемодилюции (гематокрит
Эта статья.
. про отделения
Читайте также
Ограничения в связи с профилактикой распространения коронавирусной инфекции COVID-19
Госпитализация (круглосуточно)
8 (499) 394-67-57
Скорая помощь (круглосуточно)
8 (495) 620-84-04
8 (499) 390-80-84
Восстановление легких после коронавируса
Восстанавливаются ли легкие после COVID-19? Да. Но нужно не пропустить сроки реабилитации и серьёзно отнестись к рекомендациям врача.
Новая коронавирусная инфекция, вызванная SARS-CoV-2, недостаточно изучена, однако ясно, что она наносит вред всем органам и тканям человека. Вирус проникает в организм через слизистые оболочки носа, глаз, глотки. Первые симптомы появляются на 2-14 день. Обычно это повышение температуры выше 37.5 градусов Цельсия, насморк, потеря обоняния, сухой кашель, послабление стула, слабость и головная боль. На 6–10 сутки от момента появления первых симптомов могут начать беспокоить одышка, боль в груди, усиление кашля. Это тревожные симптомы, говорящие о поражении легких и требующие проведения дополнительного обследования: компьютерной томографии легких, измерения насыщения крови кислородом (сатурации).
Легкие после COVID-19
Попадая в организм человека через слизистые оболочки дыхательных путей SARS-CoV-2 вызывает мощнейшую воспалительную реакцию. Активируются иммунные клетки, вырабатывается колоссальное количество воспалительных веществ (воспалительных цитокинов). Интенсивность этой реакции скорее всего обусловлена генетически. Именно интенсивностью воспалительной реакции и определяется тяжесть поражения легочной ткани по данным исследований. В легочной ткани поражение при COVID-19 обусловлено как поражением самих альвеол (в которых происходит газообмен и кровь насыщается кислородом из воздуха) нашими собственными иммунными клетками так и поражением легочных сосудов, оплетающих альвеолы. Степень поражения легких можно определить при помощи КТ (компьютерной томографии).
Таблица 1. Поражение лёгких при COVID-19
Процент поражения легочной ткани
Поражена часть лёгкого. Небольшое затруднение дыхания.

