что такое едкий натр и где его взять
Как прочистить канализацию каустической содой?
Каустическая сода, каустик, натр едкий – это альтернативные названия гидроксида натрия, представляющего собой активную щелочь. Выпускается в виде белого мелкокристаллического порошка или готового водного раствора.
Обладает способностью разъедать различные загрязнения, поэтому широко используется в быту. Ей можно почистить металлические и эмалевые поверхности, обезжирить инструменты и даже мыть посуду.
Но наиболее частое применение реагент получил для прочистки канализационных засоров. Он способен быстро разъедать органические вещества на 100 % (волосы, остатки еды, белковые и жировые отложения, закупоривающие трубы) и обладает мощным пробивным действием. Каустическая сода нейтрализует шероховатости во внутренних частях труб, что снижает скорость отложения загрязнений в них.
Реагент используется и для нейтрализации кислотных стоков в трубопроводе, чтобы предотвратить их разрушающее действие на металл. Также им промывают канализацию после «ударной волны», чтобы удалить рыхлую грязь. Едкий натр эффективно разъедает твердые загрязнения и очищает трубы от накопившихся отложений.
Каустик достаточно использовать 1-2 раза в месяц в профилактических целях для отсутствия проблем с эксплуатацией канализации. Он является простым в применении и при этом недорогим средством. Может применяться для чистки всей канализационной системы.
Избавление от засоров с помощью раствора едкого натра
В первую очередь, необходимо рассчитать количество реагента, которое потребуется для чистки канализации. Оно будет зависеть от того, где планируется проводить процедуру: в квартире или в частном доме. В первом случае потребуется 2 кг каустика и 7 л воды (достаточно однократной прочистки). Во втором варианте нужно взять 3 кг каустической соды и 7л воды, процедуру провести дважды.
Если был выбран едкий натр в жидком виде, он уже готов к применению, и никаких дополнительных приготовлений не требуется. Для разведения сухого реагента нужно подготовить прочное пластиковое ведро объемом 10-12 л, пластиковый черпак, а также резиновые перчатки, маску и защитные очки (щелочь разъедает кожные покровы и слизистые оболочки, вызывая серьезные химические ожоги). Помещение, в котором будут проводиться работы, необходимо хорошо проветривать из-за летучести и токсичности каустика.
Очень важным является тот факт, что реагентом можно прочищать только стальной или чугунный трубопровод. Пластиковые трубы, либо другие элементы, выполненные из пластика, могут быть сильно повреждены щелочью.
Для прочищения трубопровода следует насыпать черпаком нужное количество порошка в ведро, налить холодную воду (так как щелочь растворяется в воде с выделением большого количества тепла, низкие температуры жидкости не позволят раствору кипеть и разбрызгиваться) и перемешать до полного растворения реагента. Затем раствор аккуратно заливается в трубу и выдерживается от 3 до 6 часов, после чего нужно включить воду на 10-15 минут для промывки канализации.
Прочищаем засор сухим порошком
Если по каким-то причинам раствор сделать не получается, можно воспользоваться и сухим каустиком. В таком случае реакция будет проходить уже в самих трубах, поэтому такой метод более агрессивный. Но эффект от обоих способов примерно одинаковый.
Чтобы чистить канализацию таким методом, необходимо влить 3 л горячей воды в сливное отверстие, засыпать туда 3 столовых ложки порошка (или 5-6 при сильном засоре), избегая его попадания на сантехнику, кафель и другие поверхности. Затем влить стакан воды и оставить на 3 часа, после чего промыть большим количеством жидкости.
При данном методе также следует использовать средства индивидуальной защиты. Таким образом, каустическая сода при правильном применении поможет быстро избавиться от засоров и наладить работу канализации.
Где купить?
Компания «АКВАХИМ» реализует высококачественную химпродукцию по самым доступным ценам. Для заказа просто нажмите на соответствующую кнопку возле фотографии товара и введите ваши контакты.
Едкий натр
каустическая сода,
едкая щелочь
— 52,2 (20 °C) г/100 мл
Гидроксид натрия лат. Natrii hydroxidum ; другие названия — каустическая сода, каустик, едкий натр, едкая щёлочь. Самая распространенная щёлочь, химическая формула NaOH. В год в мире производится и потребляется более 57 миллионов тонн едкой щёлочи. Гидроксид натрия также используется для мойки пресс-форм автопокрышек, называется Mold Cleaner фирмы «NALCO». Интересна история тривиальных названий как гидроксида натрия, так и других щелочей, название «едкая щёлочь» обусловлено свойством разьедать кожу, бумагу, стекло и вызывать сильные ожоги. До XVII века, щёлочью (фр. alkali) называли также карбонаты натрия и калия. В 1736 французский учёный А. Л. Дюамель дю Монсо впервые различил эти вещества: гидроксид натрия стали называть каустической содой, карбонат натрия — кальцинированной содой (по растению Salsola Soda, из золы которого её добывали), а карбонат калия — поташем. В настоящее время содой принято называть натриевые соли угольной кислоты. В английском и французском языках слово sodium означает натрий, potassium — калий.
Содержание
Физические свойства
ΔH 0 растворения для бесконечно разбавленного водного раствора —44,45 кДж/моль.
Из водных растворов при 12,3 — 61,8 °C кристаллизуется моногидрат (сингония ромбическая), температура плавления 65,1 °C; плотность 1,829 г/см³; ΔH 0 обр −734,96 кДж/моль), в интервале от —28 до —24°С — гептагидрат, от —24 до —17,7°С — пентагидрат, от —17,7 до —5,4°С —тетрагидрат (α-модификация), от —5,4 до 12,3 °C. Растворимость в метаноле 23,6 г/л (t=28 °C), в этаноле 14,7 г/л (t=28 °C). NaOH·3,5Н2О (температура плавления 15,5 °C);
Химические свойства
Гидроксид натрия (едкая щёлочь)— сильное химическое основание (к сильным основаниям относят гидроксиды, молекулы которых полностью диссоциируют в воде), к ним относят гидроксиды щелочных и щёлочно-земельных металлов подгрупп Iа и IIа периодической системы Д. И. Менделеева, KOH (едкий калий), Ba(OH)2 (едкий барит), LiOH, RbOH, CsOH. Щёлочность (основность) определяется валентностью металла, радиусом внешней электронной оболочки и электрохимической активностью: чем больше радиус электронной оболочки (увеличивается с порядковым номером), тем легче металл отдает электроны, и тем выше его электрохимическая активность и тем левее располагается элемент в ряду электрохимической активности металлов, в котором за ноль принята активность водорода.
Гидроксид натрия вступает в реакции:
1.Нейтрализации с различными веществами в любых агрегатных состояниях, от растворов и газов до твердых веществ:
так и с растворами:
(Образующийся анион называется тетрагидроксоцинкат-ионом, а соль, которую можно выделить из раствора — тетрагидроксоцинкатом натрия. В аналогичные реакции гидроксид натрия вступает и c другими амфотерными оксидами.)
(2) H2S + NaOH = NaHS + H2O (кислая соль, при отношении 1:1)
2. Обмена с солями в растворе:
Гидроксид натрия используется для осаждения гидроксидов металлов. К примеру, так получают гелеобразный гидроксид алюминия, действуя гидроксидом натрия на сульфат алюминия в водном растворе. Его и используют, в частности, для очистки воды от мелких взвесей.
например, с фосфором — с образованием гипофосфита натрия:
4. С металлами: Гидроксид натрия вступает в реакцию с алюминием, цинком, титаном. Он не реагирует с железом и медью (металлами, которые имеют низкий электрохимический потенциал). Алюминий легко растворяется в едкой щёлочи с образованием хорошо растворимого комплекса — тетрагидроксиалюмината натрия и водорода:
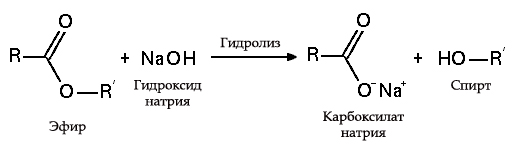
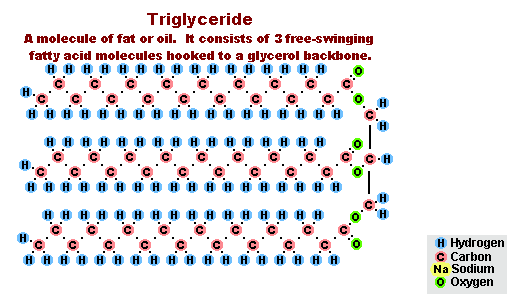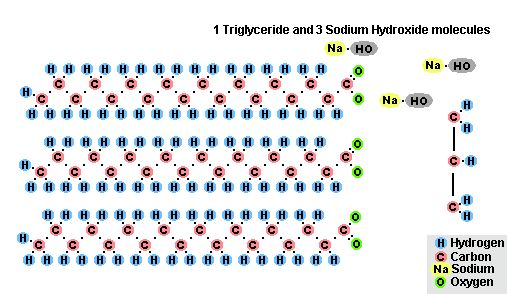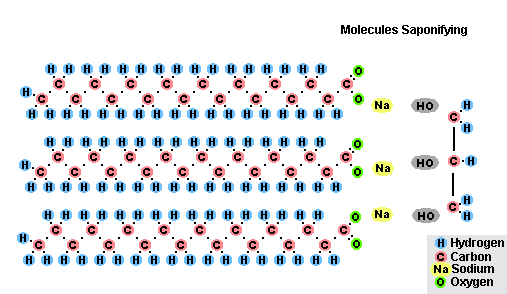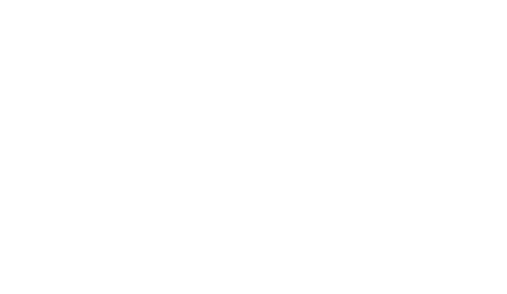
В результате взаимодействия жиров с гидроксидом натрия получают твёрдые мыла (они используются для производства кускового мыла), а с гидроксидом калия либо твёрдые, либо жидкие мыла, в зависимости от состава жира.
6. С многоатомными спиртами — с образованием алкоголятов:
7. Со стеклом: в результате длительного воздействия горячей гидроокиси натрия поверхность стекла становится матовой (выщелачивание силикатов):
Качественное определение ионов натрия возможно несколькими способами
1. По цвету пламени горелки — ионы натрия придают пламени жёлтую окраску:
2. С использованием специфических реакций на ионы натрия:
| Реагент | Фторид аммония | Нитрит цезия-калия-висмута | Ацетат магния | Ацетат цинка | Пикро- | ||
|---|---|---|---|---|---|---|---|
| Цвет осадка | белый | бледно-жёлтый | жёлто-зеленый | желто-зеленый | белый | белый | бледно-жёлтый |
Способы получения
Промышленные способы получения
В промышленном масштабе гидроксид натрия получают электролизом растворов галита (каменная соль NaCl) с одновременным получением водорода и хлора:
Едкие щёлочи, полученные при электролизе с жидким ртутным катодом, значительно чище полученных диафрагменным способом. Для некоторых производств это важно. Так, в производстве искусственных волокон можно применять только каустик, полученный при электролизе с жидким ртутным катодом. В мировой практике используются все три метода получения хлора и каустика, при явной тенденции в сторону увеличения доли мембранного электролиза. В России приблизительно 35 % от всего выпускаемого каустика вырабатывается электролизом с ртутным катодом и 65 % — электролизом с твёрдым катодом (диафрагменный и мембранный методы).
Эффективность процесса производства рассчитывается не только по выходу едкого натра, но и по выходу хлора и водорода, получаемых при электролизе, соотношение хлора и гидроксида натрия на выходе 100/110, реакция протекает в следующих соотношениях:
1,8 NaCl + 0, 5 H2O + 2,8 МДж = 1,00 Cl2 + 1,10 NaOH + 0,03 H2,
Основные показатели различных методов производства даны в таблице:
Технологическая схема электролиза с твёрдым катодом
Диафрагменный метод — Полость электролизёра с твёрдым катодом разделена пористой перегородкой — диафрагмой — на катодное и анодное пространство, где соответственно размещены катод и анод электролизёра. Поэтому такой электролизёр часто называют диафрагменным, а метод получения — диафрагменным электролизом [1]. В анодное пространство диафрагменного электролизёра непрерывно поступает поток насыщенного анолита. В результате электрохимического процесса на аноде за счет разложения галита выделяется хлор, а на катоде за счет разложения воды — водород. Хлор и водород выводятся из электролизёра раздельно, не смешиваясь:
При этом прикатодная зона обогащается гидроксидом натрия. Раствор из прикатодной зоны, называемый электролитическим щёлоком, содержащий неразложившийся анолит и гидроксид натрия, непрерывно выводится из электролизёра. На следующей стадии электролитический щёлок упаривают и доводят содержание в нём NaOH до 42—50 % в соответствии со стандартом. Галит и сульфат натрия при повышении концентрации гидроксида натрия выпадают в осадок. Раствор едкой щёлочи декантируют от осадка и передают в качестве готового продукта на склад или на стадию упаривания для получения твёрдого продукта, с последующим плавлением, чешуированием или грануляцией. Кристаллический галит (обратную соль) возвращают на электролиз, приготавливая из неё так называемый обратный рассол. Из него во избежание накапливания сульфата в растворах перед приготовлением обратного рассола извлекают сульфат. Убыль анолита возмещают добавкой свежего рассола, получаемого подземным выщелачиванием соляных пластов или растворением твёрдого галита. Свежий рассол перед смешиванием его с обратным рассолом очищают от механических взвесей и значительной части ионов кальция и магния. Полученный хлор отделяется от паров воды, компримируется и подаётся либо на производство хлорсодержащих продуктов, либо на сжижение.
Мембранный метод — аналогичен диафрагменному, но анодное и катодное пространства разделены катионообменной мембраной. Мембранный электролиз обеспечивает получение наиболее чистого каустика.
который отводится из электролизёра, а на ртутном катоде образуется слабый раствор натрия в ртути, так называемая амальгама:
Амальгама непрерывно перетекает из электролизёра в разлагатель. В разлагатель также непрерывно подаётся хорошо очищенная от примесей вода. В нем амальгама натрия в результате самопроизвольного электрохимического процесса почти полностью разлагается водой с образованием ртути, раствора каустика и водорода:
Полученный таким образом раствор каустика, являющийся товарным продуктом, не содержит примеси галита, вредной в производстве вискозы. Ртуть почти полностью освобождается от амальгамы натрия и возвращается в электролизер. Водород отводится на очистку. Анолит, выходящий из электролизера, донасыщают свежим галитом, извлекают из него примеси, внесенные с ним, а также вымываемые из анодов и конструкционных материалов, и возвращают на электролиз. Перед донасыщением из анолита извлекают двух- или трёхступенчатым процессом растворённый в нём хлор.
Лабораторные способы получения
В лаборатории гидроксид натрия получают химическими способами, которые имеют больше историческое, чем практическое значение.
В результате реакции образуется раствор гидроксида натрия и осадок карбоната кальция. Карбонат кальция отделяется от раствора, который упаривается до получения расплавленного продукта, содержащего около 92 % NaOH. Расплавленный NaOH разливают в железные барабаны, где он застывает.
Ферритный способ описывается двумя реакциями:
(1) — процесс спекания кальцинированной соды с окисью железа при температуре 1100—1200°С. При этом образуется спек-феррит натрия и выделяется двуокись углерода. Далее спек обрабатывают (выщелачивают) водой по реакции (2); получается раствор гидроксида натрия и осадок Fe2O3, который после отделения его от раствора возвращается в процесс. Раствор содержит около 400 г/л NaOH. Его упаривают до получения продукта, содержащего около 92 % NaOH.
Химические методы получения гидроксида натрия имеют существенные недостатки: расходуется большое количество топлива, получаемый едкий натр загрязнен примесями, обслуживание аппаратов трудоемко. В настоящее время эти методы почти полностью вытеснены электрохимическим способом производства.
Каустическая сода: применение в быту
Эффективность пищевой соды для уборки известна практически всем опытным хозяйкам. Намного меньше известно о ее более сильнодействующем аналоге — каустической соде: ей можно прочищать трубы, очищать сложные загрязнения, использовать для стирки и мытья посуды. Но состав у каустика достаточно агрессивный, поэтому нужно соблюдать правила безопасности при использовании и хранении. Расскажем, как применять каустическую соду в быту, в чем ее плюсы и минусы.
Что такое каустическая сода

По структуре она бывает жидкой или в виде порошка небольших чешуйчатых гранул.
Отличие от других видов
Существуют еще и пищевая и кальцинированная соды. Но между тремя соединениями есть большая разница.
| Характеристика | Пищевая сода | Кальцинированная сода | Каустическая сода |
| Эффективность | Применяется для смывания грязи с овощей и фруктов, чистки посуды, очищения стоков стиральной машины. | Справляется с отложениями ржавчины и известняка, сложными пятнами на хлопковых и льняных тканях, жиром и нагаром. | Используется для растворения жира, волос, остатков пищи, отстирывания пятен мазута с грубой ткани, дезинфекции. |
| Воздействие на кожу | Безопасна | Вызывает аллергию, раздражение, шелушение и сухость. Приводит к обострению хронических дерматологических заболеваний. | В неразбавленном виде оставляет ожоги. |
Где купить
Чаще всего каустик продают в хозяйственных магазинах или в отделах бытовой химии в супермаркетах. Расфасовывают его в пластиковые банки или плотные полиэтиленовые пакеты. Еще купить каустическую соду можно в строительном магазине.
Применение каустической соды в быту
Удаление накипи и нагара с посуды. Сода поможет удалить застарелый налет, копоть и трудновыводимый жир с чугуна или стали. Возьмите: 200 г каустика, 200 г хозяйственного мыла, 150 г канцелярского клея, 10 л воды. Затем приготовьте моющее средство:
С помощью каустической соды можно приготовить чистящую пасту. Небольшое количество щелочи смешайте с чистящим порошком. Разбавьте смесь водой до образования кашицы и нанесите на грязную поверхность. Оставьте на 30 минут, а затем смойте остатки средства. Посуду промойте под проточной водой.
Обратите внимание: таким способом нельзя чистить сковороды с антипригарными покрытиями, оцинкованную посуду и изделия из алюминия, каустик может испортить материал.
Стирка. Раствор каустика подходит для замачивания, ручной и машинной стирок. Особенно хорошо отстирывает кухонные полотенца и вещи из грубых льняных и плотных хлопчатобумажных тканей, например, спецодежду. Для приготовления раствора возьмите пять литров воды и 15 г каустика. В готовом средстве замочите белье на два часа. Затем постирайте обычным порошком.
Каустическую соду в количестве 10–15 граммов можно добавлять к порошку при стирке в машинке. Подходящий температурный режим — 40–60 °С. Состав отстирывает даже застарелые пятна, но не используйте соду для стирки шелковых или шерстяных тканей: она повредит деликатный материал. Такие вещи лучше отдать в химчистку.
Прочистка труб. Каустик эффективно растворяет органический мусор, а также сглаживает внутреннюю поверхность стоков. Есть два основных способа использования соды:
Не стоит использовать каустик для прочистки пластиковой развязки сточных труб. Такое химическое соединение может их сильно повредить. Кроме того не советуют чистить каустической содой эмалированные ванны, раковины и унитазы. Состав мгновенно растворяет загрязнения, но едкий состав разрушает структуру эмали, поэтому она со временем начнет трескаться и откалываться.
Очистка ржавчины. Каустик также хорошо справляется с ржавчиной. Для приготовления очищающего раствора возьмите 1 200 мл воды, 55 г каустика, 50 г аммония, 200 г формалина, а затем:
Дезинфекция. Каустическая сода — универсальный дезинфектант с мощным бактерицидным эффектом. Раствор температурой 70 °С 2–3%-ного едкого натра хорошо справляется со многими инфекциями. Нужно распылить 1 л на 1 кв. м и изолировать помещение на 24 часа. Обработанное помещение оставляют пустым на сутки.
Для домашней дезинфекции подойдет следующий раствор: в пятилитровый таз нужно добавить пару столовых ложек соды и перемешать. Вымыть им пол, затем промыть обычной водой и вытереть.
Меры предосторожности

Требования к условиям хранения
Храните каустик в герметичной упаковке в сухом месте: если в порошок попадет влага, он потеряет свои очистительные свойства. Важно убирать соду подальше от детей и животных, чтобы избежать отравлений и ожогов.
Сода легко воспламеняется, поэтому избегайте попадания прямых солнечных лучей и не храните каустик рядом с плитой и другими электроприборами. Срок годности — один год, потом сода теряет свойства.
Возможные последствия
Контакт с содой приводит к ожогам кожи и слизистых. Если она попала на открытый участок тела, не вытирайте ее полотенцем, иначе вещество еще глубже проникнет в кожу. Лучше тщательно промыть пораженный участок водой, протереть место ожога раствором 5%-ного уксуса или соком лимоном для нейтрализации щелочи, а затем наложить холодную повязку.
Можно ли использовать каустическую соду для мытья рук

Преимущества и недостатки
Плюсы каустической соды:
Выводы
Каустическая сода — это доступное и эффективное средство. Если его правильно использовать, то можно избавиться от засора, отмыть посуду или отстирать въевшиеся пятна на кухонных полотенцах. Но важно соблюдать меры предосторожности, чтобы не повредить материалы и не получить химические ожоги кожи и слизистых.
Что представляет из себя каустическая сода (ликбез)


Каустическая сода, иными словами гидроксид натрия – это самая известная щелочь, которая получается благодаря химическим и электрохимическим методам.
Химически методы можно разделить на:
Электрохимически гидроксид натрия получают электролизом минерала, который состоит из обычной соли NaCl, с параллельным получением водорода и хлора.
Существует две марки едкой щелочи: РД и ТР. Марка РД чаще бесцветная, реже имеет какой-то оттенок жидкость, получена раствором NaCl с выпариванием электролизных щелок. ТР – белая чешуя, осень гигроскопична.
Свойства, инструкция по применению
Каустическая сода — гигроскопический крупный токсичный порошок, быстро расплавляющийся на воздухе. Она принадлежит к сильным основаниям, в жидкой форме летуча.
Гидроксид натрия полностью растворяется в спиртах, но не в ацетоне. Едкий натр не вступает в химическую реакцию с хромоникелевыми и углеродистыми сплавами, искусственными полимерами.
Щелочь разрушает кожу, бумагу и ткани. Вещество взаимодействует с алюминием, цинком, оловом, магнием, и в результате контакта с ними образуется водород, который может стать причиной взрыва.
Внимание! Нельзя допускать контакта едкого натра с аммиаком, так как это чревато возникновением пожара.
Технические характеристики
Характеристики каустической соды (гранулированного каустика) можно условно разделить на химические и физические. Коротко остановимся на каждой группе в отдельности.
Химические характеристики каустической соды
Формула каустика – NaOH. При водном растворе вступает в реакцию с большой силой, с выделением тепла. Также взаимодействует с углекислым газом (в результате получается Na2CO3), с такими металлами, как алюминий, цинк, магний, олово. Разрушает стекло, фарфор, кожу, ткани разных видов. Но не взаимодействует с определёнными типами стали, полиэтиленом, поливинилхлоридом.
Применение в быту

Использование кипятка и соды для очистки труб
В быту едкий натр применяют с целью:
Устранение накипи и нагара с посуды
Едкую щелочь можно применять для устранения загрязнения со стеклянной, чугунной и стальной посуды.
Для этого понадобится:
Применение:
Важно! Таким способом нельзя очищать тефлоновые и алюминиевые изделия.
Изготовление домашнего мыла и моющих средств
Щелочь используют в мыловарении.
Первый рецепт. Ингредиенты:
Приготовление:

Каустик используется еще в одной области — для мыловарения
Второй рецепт. Ингредиенты:
Последовательность действий:
Гидроксид натрия входит в состав стиральных порошков. Его можно добавлять при стирке одновременно с порошком. Каустик сделает воду мягче, что облегчит отстирывание вещей, особенно если они загрязнены жирами и нефтепродуктами.
Количество соды на 1 стирку может варьировать от 3 до 5 ст. л. При добавлении гидроксида натрия температура воды для стирки должна быть минимум +50 градусов.
Устранение засоров

Подготовка раствора для очистки труб
С помощью порошка или раствора едкой щелочи можно прочистить засоры.
К достоинствам каустической соды можно отнести следующие:
Внимание! Химикат не пригоден для удаления отложений в пластиковых трубах, так как он может их разъесть.
Применять соду для промывки труб можно 2 способами:
Обрабатываем растения от паразитов
Едкий натр справляется с гусеницами, серой гнилью и пепелицей, но необходимо помнить, что каустическая сода накапливается в почве, поэтому нельзя ей обрабатывать растения часто.
Для борьбы с болезнями и вредителями на ведро воды берут 5 ст. л. химиката и полученным раствором опрыскивают пораженные культуры.
Широкое применение в быту
Поможет сбросить жир
Каустическая сода прекрасно справится с застарелым жиром, накипью или нагаром, которые появились на кухонной посуде (чайник, сковородка, кастрюля). Для этого нужно соду смешать с любым порошком, добавить немного воды, чтобы было не сильно жидкое, и нанести на загрязнение, на 30 минут. После чего тщательно промыть водой. Запрещено содой чистить изделия из тефлона и алюминия, так как вещество навсегда испортит посуду.
Защитит от паразитов в саду
Интересно то, что каустическую соду применяют в садоводстве и огородничестве. С ее помощью эффективно борются с такими вредителями, как гусеница, мучнистая роса и серая гниль
Перед использованием важно ознакомиться с инструкцией. Для борьбы с вредителями необходимо приготовить содовый раствор
Для этого нужно на ведро воды добавить 5 чайных ложек вещества и хорошенько перемешать. Раствором можно обрабатывать фруктовые деревья, кустарники и овощи.
«Трубочистам» на заметку
Варите мыло пенное
Часто можно встретить на полках магазинов мыло ручной работы, которое стоит достаточно дорого. Мыло можно изготовить собственноручно и для этого понадобится:
Весь процесс изготовления достаточно прост, но требует точности в соблюдении всех пропорций. Соду нужно тщательно растворить в воде. На водяной бане разогреть масло и добавить его в щелочной раствор. Должна получиться вязкая масса. Затем можно добавить любой ароматизатор (несколько капель любого эфирного масла). Полученную смесь нужно аккуратно разложить по формочкам и через 24 часа можно пользоваться качественным мылом собственного производства.
Заменит даже порошок
С помощью едкого натрия можно качественно вымыть полы в помещении. Необходимо сделать раствор, в который нужно добавить 3 столовых ложки соды на 5 л теплой воды. Помыть полы щелочным раствором. После чего поверхность следует вымыть водой и насухо вытереть. Используя такое вещество можно не только избавиться от загрязнений, но и качественно продезинфицировать поверхность в доме.
Как видно, каустическая сода активно применяется в домашних условиях. Разумное применение, такого опасного вещества может сделать много полезного и решить повседневные бытовые вопросы.
Применение в промышленности

Едкий натр широко применяется в промышленности
Химикат широко применяется в промышленности:
Кроме этого, едкий натрий применяют для очищения нефти и воды, производства хлорамина, биодизеля.
Присутствует каустическая сода в составе проявителя фотографий.
Область применения
Говоря о сферах применения гранулированного каустика (каустической соды) эксперты выделяют десять основных направлений:
При этом, есть и другие области, где каустическая сода является востребованным материалом.
Правила безопасности
Химикат вызывает сильные ожоги, поэтому держать его нужно в месте, недоступном для детей и домашних питомцем. Едкий натрий хранится в плотно укупоренной подписанной таре вдали от нагревательных элементов и открытого огня, так как каустик взрывоопасен и легко воспламеняется.
Важно! При работе с химикатом нужно пользоваться перчатками и защищать дыхательные пути и кожные покровы.
В порошке и в виде раствора едкий натр хранится на протяжении 1 года с момента производства.
Что такое каустическая сода?
Каустическая сода-это прежде всего щелочь, способная разъедать органические вещества, при этом она отлично борется с загрязнениями. По сравнению с пищевой и кальцинированной содой, каустическая имеет больший очищающий эффект. Выпускается каустическая сода в виде порошка, в котором можно разглядеть небольшие кристаллы и хлопья, окрашенные в белый цвет. Кроме этого, порошок не имеет какого-либо запаха, а размер крупинок не превышает 1-1.5 мм.
Состав
Каустическая сода состоит из кислорода, молекул натрия и водорода, об этом свидетельствует структурная формула вещества NaOH. Найти каустическую соду в чистом виде не удастся, ее получают из раствора поваренной соли промышленным путем. При этом нормой едкого натра считают показатели не меньше 98.5%. Выпускают каустик как твердым, так и в виде жидкости. Транспортируется в мешках или специальных емкостях.
Принцип действия
Принцип действия у каустической соды в том, что при попадании на жировые отложения, она растворяет жир, а если использовать ее при очистке канализации, то она без труда справится с органическими веществами, которые скапливаются на стенках труб.
Если каустическую соду всыпать в места засора, то она размягчит его, и проблема будет решена в короткий промежуток времени. После отслаивания образовавшегося засора и воздействия вещества, он промывается водой, проталкивая засор дальше по отверстию трубы.
Каустическая сода и кальцинированная сода — это одно и то же?
Каустическая и кальцинированная сода-это два разных вещества, но их объединяет щелочное происхождение и основа. Главным отличием одной соды от другой заключается в химическом составе, а также в эффективности. Известно, что кальцинированная сода обладает несильной эффективностью при борьбе с засорами в канализации, при ее использовании эффекта практически не будет. Каустическая сода, может справиться с данной проблемой в один миг.
Каустик-это щелочь, а кальцинированная сода, практически та же самая пищевая сода, которую многие люди используют для выпечки и в быту.
Что делать при ожоге каустической содой?
При попадании едкого натрия на кожные покровы их нужно промыть под краном, можно обработать пораженный участок 1%-й уксусной кислотой или разбавленной лимонной кислотой. Нельзя протирать место ожога влажной салфеткой.
При попадании каустической соды на слизистые оболочки ее можно смыть водой или нейтрализовать слабым раствором борной кислоты. Если краснота и жжение не пройдут, нужно обратиться к доктору.
Важно! При попадании натрия гидроксида в глаза или при случайном приеме его внутрь следует безотлагательно обратиться в медучреждение, так как химическое средство может стать причиной потери зрения и ожога пищеварительного тракта.