что такое едкая щелочь
Едкие щелочи
Щёлочи — гидроксиды щелочных и щёлочноземельных металлов. К щелочам относят растворимые в воде основания. При диссоциации щелочи образуют ионы OH- и ион металла.
К щелочам относятся гидроксиды металлов подгрупп Iа и IIа периодической системы, например NaOH(едкий натрий), KOH (едкий калий), Ba(OH)2 (едкий барий). Едкие щелочи — тривиальное название гидроксидов лития LiOH, натрия NaOH, калия КОН, рубидия RbOH, и цезия CsOH.
Физические свойства
Химические свойства
Поглощают H2O и CO2 из воздуха. Щёлочи широко применяются в промышленности. Важное химическое свойство щелочей — способность образовывать соли в реакции с кислотами.
Получение
Получают путём электролиза хлоридов щелочных металлов или действием воды на оксиды щелочных металлов.
Полезное
Смотреть что такое «Едкие щелочи» в других словарях:
ЕДКИЕ ЩЕЛОЧИ — ЕДКИЕ ЩЕЛОЧИ, растворимые в воде гидроокиси металлов:. гидроокись калия, едкое кали, КОН; гидроокись натрия, едкий натр, NaOH, применяемый в технике в нечистом виде под названием каустической соды; гидроокись кальция, едкая известь, Са(ОН)2… … Большая медицинская энциклопедия
Едкие щелочи — (хим.) так называются гидраты сильных оснований, характеризующиеся большой прочностью и способностью растворяться в воде, а также высоким тепловым эффектом при нейтрализации сильными кислотами (см. Термохимия) и большой электропроводностью. Они… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ЕДКИЕ ЩЕЛОЧИ — хорошо растворимые в воде гидроксиды щелочных металлов, например, едкий натр NaON, едкое кали КОН; оказывают разъедающее действие на слизистые оболочки и кожу … Металлургический словарь
Щелочи — Щёлочи гидроксиды щелочных и щёлочноземельных металлов. К щелочам относят растворимые в воде основания. При диссоциации щелочи образуют ионы OH и ион металла. К щелочам относятся гидроксиды металлов подгрупп Iа и IIа периодической системы,… … Википедия
Щелочи — [alkalies] растворимые в воде основания. Водные растворы щелочей характеризуется высокой концентрацией гидроксидных ионов ОН. К щелочам относятся оксиды щелочных, щелочноземельных металлов и аммония. Большинство щелочей твердые белые весьма… … Энциклопедический словарь по металлургии
ЩЕЛОЧИ — ЩЕЛОЧИ, растворимые в воде основания (см.), вещества, дающие в водном растворе ион гидроксила. Ион гидроксила и обусловливает. способность Щ.: 1) реагировать с к тами с выделением тепла и образованием солей (реакция нейтрализации); 2) вызывать… … Большая медицинская энциклопедия
Щелочи — (хим.) В настоящее время говорят почти исключительно о едких щелочах (см.), но прежде под Щ. разумели вообще вещества, растворы коих имеют щелочную реакцию и вкус. К числу Щ. относили тогда и карбонаты щелочных металлов (см. Калий). Сода и поташ … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ОТРАВЛЕНИЕ — ОТРАВЛЕНИЕ. Под отравлением разумеют «расстройства функций животн. организма, вызываемые экзогенными или эндогенными, химически или физико химически действующими веществами, к рые в отношении качества, количества или концентрации чужды… … Большая медицинская энциклопедия
Отравления — I Отравления (острые) Отравления заболевания, развивающиеся вследствие экзогенного воздействия на организм человека или животного химических соединений в количествах, вызывающих нарушения физиологических функций и создающих опасность для жизни. В … Медицинская энциклопедия
Гидроксид натрия — распространенная и полезная щелочь
Данный реактив, самая распространенная щелочь, более известен 
Важные особенности гидроксида натрия
Их важно знать, чтобы работа с этим реактивом была безопасной, и чтобы его применение принесло ожидаемые результаты.
Основные сферы применения едкого натра
Техника безопасности в работе с гидроксидом натрия
По ГОСТ 12.1.007-76 каустическая сода относится ко II классу токсичности (высокоопасна). Может вызвать сильный ожог кожи и слизистых, необратимое повреждение зрения при попадании в глаза. Именно поэтому работать с ней нужно в перчатках и защитных очках, использовать специальную одежду с виниловой пропиткой или прорезиненную.
При попадании вещества на слизистую ее как можно скорее нужно промыть большим количеством проточной воды, кожу промыть слабым раствором уксуса.
При большой поверхности ожога, при попадании реактива внутрь или в глаз следует не только приянть эти меры, но и незамедлительно обратиться к врачу.
Вы можете купить щелочь гидроксид натрия в нашем магазине, и мы надеемся, что вы будете соблюдать технику безопасности. Товар продается с доставкой, поэтому вы можете купить щелочь в Москве или другом городе России и вскоре получить его в своем городе.
Едкий натр
каустическая сода,
едкая щелочь
— 52,2 (20 °C) г/100 мл
Гидроксид натрия лат. Natrii hydroxidum ; другие названия — каустическая сода, каустик, едкий натр, едкая щёлочь. Самая распространенная щёлочь, химическая формула NaOH. В год в мире производится и потребляется более 57 миллионов тонн едкой щёлочи. Гидроксид натрия также используется для мойки пресс-форм автопокрышек, называется Mold Cleaner фирмы «NALCO». Интересна история тривиальных названий как гидроксида натрия, так и других щелочей, название «едкая щёлочь» обусловлено свойством разьедать кожу, бумагу, стекло и вызывать сильные ожоги. До XVII века, щёлочью (фр. alkali) называли также карбонаты натрия и калия. В 1736 французский учёный А. Л. Дюамель дю Монсо впервые различил эти вещества: гидроксид натрия стали называть каустической содой, карбонат натрия — кальцинированной содой (по растению Salsola Soda, из золы которого её добывали), а карбонат калия — поташем. В настоящее время содой принято называть натриевые соли угольной кислоты. В английском и французском языках слово sodium означает натрий, potassium — калий.
Содержание
Физические свойства
ΔH 0 растворения для бесконечно разбавленного водного раствора —44,45 кДж/моль.
Из водных растворов при 12,3 — 61,8 °C кристаллизуется моногидрат (сингония ромбическая), температура плавления 65,1 °C; плотность 1,829 г/см³; ΔH 0 обр −734,96 кДж/моль), в интервале от —28 до —24°С — гептагидрат, от —24 до —17,7°С — пентагидрат, от —17,7 до —5,4°С —тетрагидрат (α-модификация), от —5,4 до 12,3 °C. Растворимость в метаноле 23,6 г/л (t=28 °C), в этаноле 14,7 г/л (t=28 °C). NaOH·3,5Н2О (температура плавления 15,5 °C);
Химические свойства
Гидроксид натрия (едкая щёлочь)— сильное химическое основание (к сильным основаниям относят гидроксиды, молекулы которых полностью диссоциируют в воде), к ним относят гидроксиды щелочных и щёлочно-земельных металлов подгрупп Iа и IIа периодической системы Д. И. Менделеева, KOH (едкий калий), Ba(OH)2 (едкий барит), LiOH, RbOH, CsOH. Щёлочность (основность) определяется валентностью металла, радиусом внешней электронной оболочки и электрохимической активностью: чем больше радиус электронной оболочки (увеличивается с порядковым номером), тем легче металл отдает электроны, и тем выше его электрохимическая активность и тем левее располагается элемент в ряду электрохимической активности металлов, в котором за ноль принята активность водорода.
Гидроксид натрия вступает в реакции:
1.Нейтрализации с различными веществами в любых агрегатных состояниях, от растворов и газов до твердых веществ:
так и с растворами:
(Образующийся анион называется тетрагидроксоцинкат-ионом, а соль, которую можно выделить из раствора — тетрагидроксоцинкатом натрия. В аналогичные реакции гидроксид натрия вступает и c другими амфотерными оксидами.)
(2) H2S + NaOH = NaHS + H2O (кислая соль, при отношении 1:1)
2. Обмена с солями в растворе:
Гидроксид натрия используется для осаждения гидроксидов металлов. К примеру, так получают гелеобразный гидроксид алюминия, действуя гидроксидом натрия на сульфат алюминия в водном растворе. Его и используют, в частности, для очистки воды от мелких взвесей.
например, с фосфором — с образованием гипофосфита натрия:
4. С металлами: Гидроксид натрия вступает в реакцию с алюминием, цинком, титаном. Он не реагирует с железом и медью (металлами, которые имеют низкий электрохимический потенциал). Алюминий легко растворяется в едкой щёлочи с образованием хорошо растворимого комплекса — тетрагидроксиалюмината натрия и водорода:
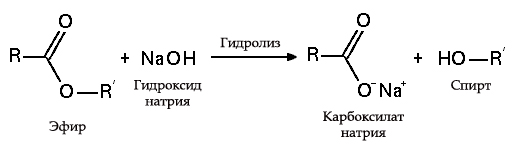
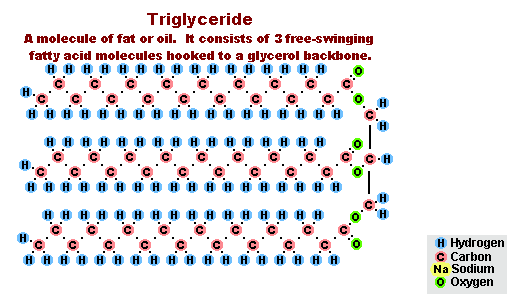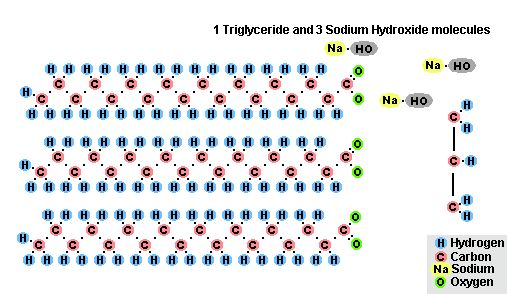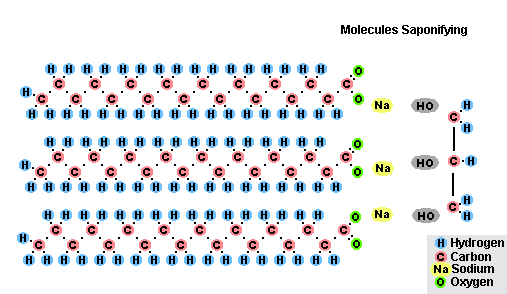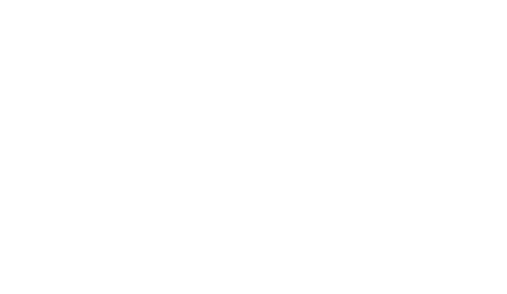
В результате взаимодействия жиров с гидроксидом натрия получают твёрдые мыла (они используются для производства кускового мыла), а с гидроксидом калия либо твёрдые, либо жидкие мыла, в зависимости от состава жира.
6. С многоатомными спиртами — с образованием алкоголятов:
7. Со стеклом: в результате длительного воздействия горячей гидроокиси натрия поверхность стекла становится матовой (выщелачивание силикатов):
Качественное определение ионов натрия возможно несколькими способами
1. По цвету пламени горелки — ионы натрия придают пламени жёлтую окраску:
2. С использованием специфических реакций на ионы натрия:
| Реагент | Фторид аммония | Нитрит цезия-калия-висмута | Ацетат магния | Ацетат цинка | Пикро- | ||
|---|---|---|---|---|---|---|---|
| Цвет осадка | белый | бледно-жёлтый | жёлто-зеленый | желто-зеленый | белый | белый | бледно-жёлтый |
Способы получения
Промышленные способы получения
В промышленном масштабе гидроксид натрия получают электролизом растворов галита (каменная соль NaCl) с одновременным получением водорода и хлора:
Едкие щёлочи, полученные при электролизе с жидким ртутным катодом, значительно чище полученных диафрагменным способом. Для некоторых производств это важно. Так, в производстве искусственных волокон можно применять только каустик, полученный при электролизе с жидким ртутным катодом. В мировой практике используются все три метода получения хлора и каустика, при явной тенденции в сторону увеличения доли мембранного электролиза. В России приблизительно 35 % от всего выпускаемого каустика вырабатывается электролизом с ртутным катодом и 65 % — электролизом с твёрдым катодом (диафрагменный и мембранный методы).
Эффективность процесса производства рассчитывается не только по выходу едкого натра, но и по выходу хлора и водорода, получаемых при электролизе, соотношение хлора и гидроксида натрия на выходе 100/110, реакция протекает в следующих соотношениях:
1,8 NaCl + 0, 5 H2O + 2,8 МДж = 1,00 Cl2 + 1,10 NaOH + 0,03 H2,
Основные показатели различных методов производства даны в таблице:
Технологическая схема электролиза с твёрдым катодом
Диафрагменный метод — Полость электролизёра с твёрдым катодом разделена пористой перегородкой — диафрагмой — на катодное и анодное пространство, где соответственно размещены катод и анод электролизёра. Поэтому такой электролизёр часто называют диафрагменным, а метод получения — диафрагменным электролизом [1]. В анодное пространство диафрагменного электролизёра непрерывно поступает поток насыщенного анолита. В результате электрохимического процесса на аноде за счет разложения галита выделяется хлор, а на катоде за счет разложения воды — водород. Хлор и водород выводятся из электролизёра раздельно, не смешиваясь:
При этом прикатодная зона обогащается гидроксидом натрия. Раствор из прикатодной зоны, называемый электролитическим щёлоком, содержащий неразложившийся анолит и гидроксид натрия, непрерывно выводится из электролизёра. На следующей стадии электролитический щёлок упаривают и доводят содержание в нём NaOH до 42—50 % в соответствии со стандартом. Галит и сульфат натрия при повышении концентрации гидроксида натрия выпадают в осадок. Раствор едкой щёлочи декантируют от осадка и передают в качестве готового продукта на склад или на стадию упаривания для получения твёрдого продукта, с последующим плавлением, чешуированием или грануляцией. Кристаллический галит (обратную соль) возвращают на электролиз, приготавливая из неё так называемый обратный рассол. Из него во избежание накапливания сульфата в растворах перед приготовлением обратного рассола извлекают сульфат. Убыль анолита возмещают добавкой свежего рассола, получаемого подземным выщелачиванием соляных пластов или растворением твёрдого галита. Свежий рассол перед смешиванием его с обратным рассолом очищают от механических взвесей и значительной части ионов кальция и магния. Полученный хлор отделяется от паров воды, компримируется и подаётся либо на производство хлорсодержащих продуктов, либо на сжижение.
Мембранный метод — аналогичен диафрагменному, но анодное и катодное пространства разделены катионообменной мембраной. Мембранный электролиз обеспечивает получение наиболее чистого каустика.
который отводится из электролизёра, а на ртутном катоде образуется слабый раствор натрия в ртути, так называемая амальгама:
Амальгама непрерывно перетекает из электролизёра в разлагатель. В разлагатель также непрерывно подаётся хорошо очищенная от примесей вода. В нем амальгама натрия в результате самопроизвольного электрохимического процесса почти полностью разлагается водой с образованием ртути, раствора каустика и водорода:
Полученный таким образом раствор каустика, являющийся товарным продуктом, не содержит примеси галита, вредной в производстве вискозы. Ртуть почти полностью освобождается от амальгамы натрия и возвращается в электролизер. Водород отводится на очистку. Анолит, выходящий из электролизера, донасыщают свежим галитом, извлекают из него примеси, внесенные с ним, а также вымываемые из анодов и конструкционных материалов, и возвращают на электролиз. Перед донасыщением из анолита извлекают двух- или трёхступенчатым процессом растворённый в нём хлор.
Лабораторные способы получения
В лаборатории гидроксид натрия получают химическими способами, которые имеют больше историческое, чем практическое значение.
В результате реакции образуется раствор гидроксида натрия и осадок карбоната кальция. Карбонат кальция отделяется от раствора, который упаривается до получения расплавленного продукта, содержащего около 92 % NaOH. Расплавленный NaOH разливают в железные барабаны, где он застывает.
Ферритный способ описывается двумя реакциями:
(1) — процесс спекания кальцинированной соды с окисью железа при температуре 1100—1200°С. При этом образуется спек-феррит натрия и выделяется двуокись углерода. Далее спек обрабатывают (выщелачивают) водой по реакции (2); получается раствор гидроксида натрия и осадок Fe2O3, который после отделения его от раствора возвращается в процесс. Раствор содержит около 400 г/л NaOH. Его упаривают до получения продукта, содержащего около 92 % NaOH.
Химические методы получения гидроксида натрия имеют существенные недостатки: расходуется большое количество топлива, получаемый едкий натр загрязнен примесями, обслуживание аппаратов трудоемко. В настоящее время эти методы почти полностью вытеснены электрохимическим способом производства.
Что такое щелочь, в какие реакции вступают самые известные из них
Химия – наука, изучающая различные реакции, протекающие в природе, а также взаимодействия одних соединений с другими. Основными веществами здесь являются кислоты и щелочи, реакции между которыми обычно называются нейтрализацией. Они приводят к образованию растворимой в воде соли.
Что такое щелочь
Гидроксиды щелочных (металлы первой группы главной (А) подгруппы в периодической таблице химических элементов Д. И. Менделеева) и щелочноземельных (металлы второй группы главной (А) подгруппы, включая кальций) металлов, которые бурно взаимодействуют с водой и полностью в ней растворяются, называются щелочами. Так как они способны разрушать органический материал (кожу, древесину, бумагу), их называют едкими. Например, гидроксид калия (KOH) – едкий калий, бария (Ba(OH)2) – едкий барий и так далее.
Физические свойства сильных оснований
Исходя из определения, что такое щелочь, можно добавить, что эти гидроксиды также представляют собой твердые гигроскопичные (способные поглощать из воздуха пары воды) вещества белого цвета. К самым сильным щелочам относятся гидроксиды цезия CsOH и радия Ra(OH)2. Реакции щелочей чаще всего сопровождаются выделением тепла (экзотермические). Также к физическим свойствам таких оснований можно отнести их способность растворяться в некоторых органических соединениях, например, в спиртах: метаноле и этаноле.
Химические свойства
Растворы щелочей способны вступать в различные реакции.
Сильные основания обладают способностью взаимодействовать с кислотными и амфотерными оксидами:
При реагировании с амфотерными металлами (Zn, Al и прочие) также возможно образование как расплава, так и соответствующей комплексной соли. Причем обе реакции сопровождаются выделением газообразного водорода:
Также щелочи способны реагировать с солями, в результате чего образуется другое основание и другая соль. Условием протекания реакции является то, что в результате одно из образовавшихся веществ должно быть не растворимо в воде:
NaOH + CuSO4 = Na2SO4 + Cu(OH)2.
Как уже было упомянуто ранее, щелочи и кислоты вступают в реакцию нейтрализации, образуется соль и вода:
NaOH + HCl = NaCl + H2O.
Щелочи вступают в реакцию с другими основаниями только, если это гидроксиды амфотерных металлов:
NaOH + Al(OH)3 = Na[Al(OH)4].
Некоторые из них могут вступать во взаимодействие со многими органическими веществами: эфирами, амидами, многоатомными спиртами:
2C2H6O2 + 2NaOH = C2H4O2Na2 + 2H2O (продукт реакции – алкоголят натрия).
Как получают сильные основания
Щелочи получают разными способами как в промышленности, так и в лабораториях.
В промышленной индустрии существуют несколько методов получения щелочей: пиролиз, известковый, ферритный, электролиз, который делится на диафрагменный, мембранный и ртутный методы на жидких и твердых катодах.
Это электролиз растворов хлоридов натрия и калия, после чего на аноде и катоде выделяются хлор и водород, и получаются соответствующие гидроксиды:
При пиролизе в 1000 градусов на первом этапе происходит образование оксида натрия:
На втором этапе полученный охлажденный оксид растворяют в воде, в результате чего и получается необходимая щелочь:
В лабораториях также применяется электролиз. Еще щелочи могут получиться путем воздействия на соответствующие металлы водой или взаимодействия солей этих металлов с другими основаниями, в результате чего получается необходимая щелочь и нерастворимый в воде второй продукт реакции – соль.
2Cs + 2H2O = 2CsOH + H2.
В результате действия воды на оксид лития получается щелочь:
Li2O + 2H2O = 2LiOH + H2.
Применение
Опираясь на само определение того, что такое щелочь, можно понять, что они находят широкое применение не только в промышленности, но и в быту:
Меры предосторожности
Становится очевидным, что такие щелочи, как гидроксиды натрия, лития, калия, цезия и прочие, способны сильно повреждать и обжигать кожу и слизистые оболочки глаз даже при попадании туда мельчайших частиц соединения. Чтобы предотвратить это, необходимо носить защитные очки, резиновые перчатки, а также спецодежду, которая обработана специальными веществами, не позволяющими материалу взаимодействовать со щелочами.
Щелочь
Производство широкого спектра потребительских товаров зависит от использования щелочей 
Немного исторических моментов из истории получения щелочи.
Лебланский способ производства доминировал в мировом производстве до конца 19-го века, но после первой мировой войны был полностью вытеснен другим методом конверсии соли, который был усовершенствован в 1860-х годах Эрнестом Солве из Бельгии. В конце XIX века появились электролитические методы производства каустической соды, объемы которых быстро росли.
По методу Солве, аммиачно-содовый процесс производства кальцинированной соды протекал следующим образом: поваренная соль в виде сильного рассола химически обрабатывалась для устранения примесей кальция и магния и затем насыщалась рециркулирующим газом аммиака в башнях. После, аммиачный рассол насыщался газом с использованием газообразного диоксида углерода при умеренном давлении в башне другого типа. Эти два процесса дают бикарбонат аммония и хлорид натрия, двойное разложение которого дает желаемый бикарбонат натрия, а также хлорид аммония. Затем бикарбонат натрия нагревают до разложения его до необходимого карбоната натрия. Аммиак, вовлеченный в процесс, почти полностью восстанавливается путем обработки хлоридом аммония с известью, с получением аммиака и хлорида кальция. Восстановленный аммиак затем повторно используют в описанных выше процессах.
В нескольких местах в мире существуют значительные запасы минеральной формы кальцинированной соды, известной как природная щелочь. На таких месторождениях производят большую часть природной щелочи в мире из обширных месторождений в подземных шахтах.
Природный натрий металлический.
Прочитайте статью Щелочи (источник «Энциклопедический словарь химика»)и получите больше представления о том что такое щелочь, или посмотрите видеоролик об этом химическом реактиве Щелочи.
Использование щелочи в окружающей нас среде
Щелочь снискала широкое применение в нашей жизни. Благодаря щелочи можно в той или иной форме добиться смягчения воды и удалить из нее примеси, такие как марганец, фториды и органические танины. В тяжелых отраслях промышленности используют щелочь в виде извести для поглощения и нейтрализации оксидов серы в выбросах в атмосферу, тем самым уменьшая вероятность выпадения кислотных осадков. Диоксид серы, производимый промышленными предприятиями и выпускаемый в атмосферу, возвращается на землю в виде кислотных дождей или серной кислоты. Такие территории, подвергшихся воздействию кислотных дождей, обрабатываются с помощью авиации препаратами, в состав которых входит щелочь. Это позволяет контролировать и нейтрализовывать критический уровень рН воды и почвы на участках, где произошли такие техногенные выбросы. Внесение щелочи в отходы и сточные воды, поддерживая правильный уровень рН в окислительных процессах при их разложении. Стабилизирует образования осадка в сточных водах и уменьшает запах или образования патогенных бактерий. Обработанный негашеной известью ил из сточных водоемов, соответствует экологическим нормам, что делает его пригодным в дальнейшем в использовании в качестве удобрения на сельскохозяйственных землях.
Промышленное применение щелочи
В промышленных и горных работах применение щелочей в сточных водах помогает нейтрализовать вредные соединения и произвести их очистку. Обработка избыточной щелочью, повышает рН воды до 10,5-11 и может дезинфицировать воду и удалять тяжелые металлы. Щелочи, такие как известь, являются ключевыми в химическом производстве карбида кальция, лимонной кислоты, нефтехимии и магнезии. В бумажной промышленности карбонат кальция является каустифицирующим агентом для отбеливания. Сталелитейная промышленность зависит от извести в качестве компонента для удаления примесей, таких как газообразный монооксид углерода, кремния, марганца и фосфора.
Моющие средства образованные щелочью
Щелочные моющие средства помогают при очистке поверхностей с сильными загрязнениями. Эти экономичные, водорастворимые щелочи с рН от 9 до 12,5 могут нейтрализовать кислоты в различных типах грязи и отложениях.
Щелочь в производстве стекла и керамики
Щелочь является основным сырьем в производстве стекла. Известняк, а также песок, кальцинированная сода, известь и другие химикаты, обжигаются при чрезвычайно высоких температурах и превращаются в расплавленную массу. Стеклодувы и гончары используют щелочи для глазурей и флюсов, которые реагируют с кислотами с образованием силикатов (стекла) при нагревании. Концентрированные щелочи создают более насыщенный цвет в глазури.
Литература о щелочи
«Среди многочисленных веществ, которыми химики с давних времен пользовались в своих лабораториях, почетное место всегда занимали едкие щелочи — едкое кали и едкий натр. Сотни различных химических реакций осуществляются в лабораториях, на заводах и в быту при участии щелочей. С помощью едких кали и натра можно, например, сделать растворимыми большинство нерастворимых веществ, а самые сильные кислоты и удушливые пары можно благодаря щелочам лишить всей их жгучести и ядовитости.
Едкие щелочи — очень своеобразные вещества. На вид это беловатые, довольно твердые камни, ничем как будто не примечательные. Но попробуйте взять едкое кали или натр и зажать его в руке. Вы почувствуете легкое жжение, почти как от прикосновения к крапиве. Долго держать в руке едкие щелочи было бы нестерпимо больно: они могут разъесть кожу и мясо до кости. Вот почему их называют «едкими», в отличие от других, менее «злых» щелочей — всем известных соды и поташа. Из соды и поташа, кстати сказать, почти всегда и по лучались едкие натр и кали.
У едких щелочей сильнейшее влечение к воде. Оставьте кусок совершенно сухого едкого кали или натра на воздухе. Через короткое время на его поверхности неизвестно откуда появится жидкость, потом он весь станет мокрым и рыхлым и под конец расползется бесформенной массой, как кисель. Это из воздуха щелочь притягивает к себе пары воды и образует с влагой густой раствор. Кому впервые приходится погрузить пальцы в раствор едкой щелочи, тот с удивлением заявляет: — Как мыло! И это совершенно правильно. Щелочь — скользкая, как мыло. Больше того: мыло потому и «мыльно» на ощупь, что его изготовляют с помощью щелочей. Раствор едкой щелочи и на вкус напоминает мыло.
Но химик узнаёт едкую щелочь не по вкусу, а по тому, как это вещество ведет себя с краской лакмус и с кислотами. Бумажка, про питанная синей краской лакмус, мгновенно краснеет, когда ее опус кают в кислоту; а если этой покрасневшей бумажкой дотронуться до щелочи, то она тотчас же опять становится синей. Едкая щелочь и кислота не могут мирно существовать рядом ни одной секунды. Они тотчас же вступают в бурную реакцию, шипя и разогреваясь, и уничтожают друг друга до тех пор, пока в растворе не останется ни крупинки щелочи или ни капли кислоты. Только тогда наступает успо коение. Щелочь и кислота «нейтрализовали» друг друга, говорят в таких случаях. От соединения их между собой получается «нейтральная» соль — ни кислая, ни едкая. Так, например, от соединения жгучей соляной кислоты с едким натром получается обыкновеннейшая поваренная соль.»
Отличительные признаки щелочи.
Из выше прочитанного мы уже знаем, что противоположностью щелочи является кислота. Вместо горького вкуса 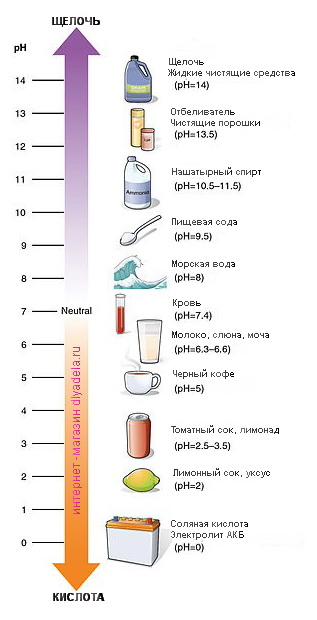
Почему вещество щелочное?
Таким образом, нам уже известно, что рН уровень представляет собой шкалу, значения которой колеблятся от 0-14 и указывают, является ли вещество щелочью или кислотой. Однако мы действительно не знаем, почему. Давайте рассмотрим этот вопрос более детально.
Уровень рH вещества зависит от того, как атомы расположены и объединены в веществе. Чистая вода находится прямо в середине шкалы и имеет pH 7. Это означает, что она содержит равное количество атомов водорода (H +) и гидроксидных атомов (OH-). Когда вещество имеет больше атомов водорода (Н +), это кислота. Когда вещество имеет больше гидроксидных атомов (OH-), оно является щелочным.
Где купить щелочь?
Купить щелочь в Новосибирске со степенью очистки ЧДА (чистая для анализов) в магазине «Для дела» можно на странице заказов: едкий натр NaOH или едкий кали KOH. Для иногородних покупателей товар может быть отправлен Почтой РФ или транспортными компаниями.