что такое блд у ребенка
Бронхолегочная дисплазия
Бронхолегочная дисплазия – это хроническое повреждение легких у недоношенных детей, которое вызывается кислородом и длительной искусственной вентиляцией легких.
Такой диагноз ставится при сохранении у новорожденного потребности в дополнительном кислороде, у детей, которые были рождены раньше срока (на 36-й неделе гестации), и у которых не выявлены другие заболевания, при которых может быть нехватка кислорода, получаемого путем дыхания обычным воздухом (врожденный порок сердца, пневмония).
Среди недоношенных детей это заболевания встречается чаще. Также в группе риска малыши с интерстициальной эмфиземой легких, увеличенным сопротивлением дыхательных путей, высоким пиковым давлением на вдохе, высоким давлением в легочной артерии. Стоит отметить, что среди мальчиков эта болезнь встречается чаще по сравнению с девочками.
Бронхолегочную дисплазию у недоношенных и доношенных детей подозревают, если пациента нельзя снять с ИВЛ, кислородотерапии. У ребенка возникает увеличивающаяся гипоксемия, потребность в кислороде, и возрастает гиперкапния. Под последним состоянием подразумевают как бы отравление организма углекислым газом, это частный случай гипоксии.
Рентгенографические методы позволяют выявить диффузное затемнение, которое возникает по причине скопления экссудата. Позже изображение мультикистозное, имеет схожесть с губкой, в пораженных зонах развиваются рубцы, эмфизема и ателектазы. Также есть вероятность десквамации альвеолярного эпителия, нейтрофилов, макрофагов и медиаторов воспаления, которые обнаруживаются в аспирате из трахеи.
Что провоцирует / Причины Бронхолегочной дисплазии:
Бронхолегочная дисплазия младенцев сначала рассматривалась медиками как негативное влияние кислорода и ИВЛ. Сегодня же этот диагноз считается полиэтиологическим заболеванием.
Факторы развития бронхолегочной дисплазии:
Незрелость легких недоношенного ребенка
Частота и тяжесть бронхолегочной дисплазии коррелирует с массой тела новорожденного и периодом его вынашивания матерью. 73% малышей, которые при рождении весили до 1 кг, обрели диагноз «бронхолегочная дисплазия». Заболеваемость среди детей, родившихся с массой от 1 до 1,5 кг, примерно 40%. Диагносты, учитывая период выношенности ребенка (гестационный возраст), говорят о бронхолегочной дисплазии новорожденных, если малыш родился до 28-й недели.
Токсическое действие кислорода
Кислород имеет значение на ранних стадиях заболевания. Гипероксидное повреждение легких вызывает некротические процессы в эпителии дыхательных путей ребенка, в эндотелии капилляров легких, в трансформации альвеолоцитов 2 типа в 1-й тип. Окислительная атака становится причиной легочной гипертензии и ателектазов, стоит отметить, что нарушается и мукоцилиарный клиренс.
Баротравма легких
При дыхании значительным количеством кислорода у ребенка возникают повреждения эпителия, который является клеточным барьером, в легких развивается протеинсодержащий отек. Возникает необходимость давать ребенку с помощью искусственной вентиляции еще больше кислорода. Это формирует порочный круг, поскольку повреждения легких от этого только усугубляются.
Инфекция
Если в дыхательных путях ребенка поселяются микроорганизмы, у него возрастает риск развития бронхолегочной дисплазии. Некоторые возбудители могут привести к хорионамниониту, слишком ранним родам, поражениям легких, например, гиперреактивности бронхов, воспалению бронхов, инактивации сурфактанта. Вторичная инфекция развивается при попадании в легкие внутрибольничной флоры в процессе интубации трахеи.
Отек легких
Отек легких может быть вызван избыточным объемом инфузионной терапии, наличием открытого артериального протока, нарушениями при выведении жидкости.
Патогенез (что происходит?) во время Бронхолегочной дисплазии:
Патогенез начинается с экспозиции повреждающих стимулов, которые были названы выше (например, перегрузка сосудистого русла объемным кровотоком, ишемия-реперфузия и пр.). Далее эти агенты вызывают локальное повреждение, результатом которого становится разрушения и отмирание клеток. Сигнальная система организма дает ответ, запуская воспалительный процесс, возникает отек ткани легких.
Альвеолит разрешается у части больных, а у других он персистирует, что вызывает бронхолегочную дисплазию недоношенных и доношенных новорожденных. Далее в патогенезе рассматриваемой болезни следует поступление мононуклеарных клеток и пролиферация фибробластов с последующим фиброзом. вместе с выше описанными процессами меняется строение легких – морфология дыхательных путей с воспалением, метаплазией, гипертрофией гладкой мускулатуры. Осуществляется редукция капиллярного кровотока с развитием гипертрофии гладкой мускулатуры артерий, гиперчувствительной к гуморальным стимулам.
Симптомы Бронхолегочной дисплазии:
Типичным симптомом является слишком частое дыхание малыша. Он делает более 60 вдохов/выдохов в минуту, что называется в науке учащенными дыхательными движениями. Мать может заметить одышку, а в легких врачи выслушивают ослабленное или жесткое дыхание легких. Также в легких есть влажные хрипы.
Если при бронхолегочной дисплазии у новорожденного развивается дыхательная недостаточность, то в дыхании принимает участие вспомогательная мускулатура. При вдохе втягиваются внутрь участки между ребрами, бывает втяжение надключичных ямок, раздутие крыльев носа. Также наблюдают посинение кожи в районе носогубного треугольника, потом начинается цианоз ног и рук, а потом и торса.
Диагностика Бронхолегочной дисплазии:
Для диагностики важны данные анамнеза. На бронхолегочную дисплазию у ребенка указывает рождение на сроке до 32 недель, проведение ИВЛ в периоде новорожденности. Также важны клинические данные. У ребенка есть потребность в кислороде (дети до 28 дней жизни).
Врачи проводят осмотр, чтобы зафиксировать одышку и учащенное дыхание. Также применяют обязательно аускультацию легких, выслушивая дыхательные шумы и влажные хрипы. Рентгенограмма показывает замещение легочной ткани соединительной, что является типичным признаком отека и фиброза. В некоторых случаях прибегают к консультации пульмонолога.
Лечение Бронхолегочной дисплазии:
Поддерживающее лечение включает такие компоненты?
Важно вовремя диагностировать и сразу же лечить респираторные инфекции у младенцев до 28 дней. Цель терапии – как можно раньше снять ребенка с искусственной вентиляции легких и кислородной поддержки.
Калорийность рациона рассчитывается по формуле: 120 и более ккал на 1 кг тела ребенка в день. Калорийность должна быть повышена по сравнению с нормой, поскольку на дыхание отводится дополнительная работа, а легкие требуют восстановления и развития. Прием малышом жидкости ограничивают, чтобы не было отека легких и полнокровия. Врачи могут назначить диуретики: хлортиазид по 10-20 мг на 1 кг тела больного в сутки + спиронолактон по 1-3 мг/кг 1 раз в сутки или в 2 приема. Эффективен Фуросемид, который вводят внутривенно по 1-2 мг/кг, внутримышечно по 1-2 мг/кг или внутрь по 1-4 мг/кг через 12-24 часа для новорожденных и через 8 часов для детей боле естаршего возраста. Его можно применять недолго, поскольку длительные курсы вызывают гиперкальциурию и, как следствие, остеопороз, переломы и образование камней в почках. Требуется мониторинг водноэлектролитного баланса на протяжении лечения диуретиками.
Тяжелые формы бронхолегочной дисплазии новорожденных могут вызывать потребность ИВЛ и кислородотерапии на протяжении нескольких недель или месяцев. Давление и фракцию кислорода во вдыхаемом воздухе (FiО2) следует снизить так быстро, как сможет ребенок перенести, однако нельзя позволять ребенку находиться в состоянии гипоксемии. Нужен постоянный контроль оксигенации артериальной крови, для этого применяют пульсоксиметр; поддерживают на уровне больше или равно 88 % сатурации.
Когда ребенка снимают с ИВЛ, есть риск респираторного ацидоза, потому можно лечить его без возврата к прежнему режиму ИВЛ, если рН остается выше 7,25 и у пациента отсутствует тяжелая дыхательная недостаточность. Для снижения госпитализаций по причине РСВ проводят пассивную иммунопрофилактику моноклональными антителами к респираторно-синцитиальному вирусу, паливизумабом. Но эта мера стоит больших денег, ее применяют в основном детям из группы высокого риска.
С ноября по апрель детям вводится противовирусный препарат в дозировке 15 мг на 1 кг тела ребенка через 1 месяц, пока не пройдет 6 месяцев после лечения по поводу острого заболевания. Дети старше 6 месяцев также должны прививаться против гриппа.
Прогноз бронхолегочной дисплазии
Прогноз зависит от тяжести болезни. Вероятность смерти у детей, которые в 36 недель гестации до сих пор находятся на ИВЛ, составляет от 20 до 30% в первые 12 месяцев жизни. Дети с бронхолегочной дисплазией имеют в 3-4 раза более высокую частоту задержки роста и задержки нервнопсихического развития.
У детей с бронхолегочной дисплазией на протяжении 3-4 лет есть повышенный риск заболеть инфекциями нижних дыхательных путей. У них быстро развивается респираторная декомпенсация, если возникает инфекционный процесс в легочной ткани. Ребенок должен быть госпитализирован при выявлении дыхательной недостаточности или клиники респираторной инфекции.
Профилактика Бронхолегочной дисплазии:
Предотвратить данную болезнь можно, если быстро снижать параметры ИВЛ до уровня, который является минимальным переносимым ребенком. Далее нужно снять ребенка с ИВЛ. Важно рано применять эуфиллин как стимулятор дыхания, чтобы избежать для недоношенных интермиттирующей принудительной вентиляции.
Врачи в качестве профилактики могут пренатально назначить глюкокортикоиды. Если у ребенка при рождении очень низкая масса тела, назначают сурфактант. Важна ранняя коррекция открытого боталлова протока и избегание больших объемов жидкости для снижения тяжести и частоты бронхолегочной дисплазии. Если ребенка невозможно снять с искусственной вентиляции легких в нудные сроки, следует исключить нозокомиальную пневмонию и открытый боталлов проток.
К каким докторам следует обращаться если у Вас Бронхолегочная дисплазия:
Бронхолегочная дисплазия у недоношенных детей
Нередко у недоношенных детишек после применения искусственной вентиляции легких (ИВЛ) развивается бронхолегочная дисплзия (БЛД). Возникает она благодаря нескольким факторам: это и собственно незрелость легких недоношенных детей, и интенсивный режим ИВЛ. Заболевание характеризуется полной ремиссией к 3-м годам жизни ребенка.
Почему возникает БЛД?
БЛД может возникать в результате дефицита сурфактанта (пленки, выстилающей альвеолы и препятствующей их спадению), отека легких, длительного применения высоких концентраций кислорода (повреждение свободными разикалами кислорода и т.д.), ИВЛ, воспаления, воздействия бактерий и вирусов и др. В результате действия вышепепречисленных факторов повреждаются практически все структурные компоненты незрелой легочной ткани, что приводит к хроническому нарушению функции легких и замещению здоровой ткани участками фиброза.
Как проявляется БЛД?
При наличии бронхолегочной дисплазии у ребенка отмечается бледность кожи и цианоз, учащается дыхание до 80-100 в мин, дыхание происходит с помощью дополнительной мускулатуры (межреберные мышцы). При выслушивании фонендоскопом: ослабленное дыхание, хрипы, либо жесткое дыхание. Если развивается тяжелая форма БЛД, то повреждаются и другие органы: сердце, почки, печень (ввиду перегрузки малого круга кровообращения).
Как наблюдаться у специалистов после выписки из стационара и на что обращать внимание?
Обязательно наблюдение участкового педиатра, с целью подбора терапии в периоды обострения, своевременного лечения рахита, коррекции анемии. Наблюдение пульмонолога, с целью подбора лечения, либо коррекции терапии БЛД, оценки функции внешнего дыхания.
Также важно следить за питанием малыша. Необходима прибавка в весе, избегание задержки роста. (достигается за счет повышенной каллорийности питания 140-150 ккал/кг/сутки, у матерей кормящих грудным молоком за счет обогащения молока усилителями, либо подбор специальной смеси).
Как часто наблюдаться у специалистов?
В зависимости от тяжести БЛД наблюдение специалистов происходит:
С чем связаны периоды обострения заболевания?
Научная электронная библиотека
Шапошникова Н. Ф., Деларю Н. В., Заячникова Т. Е., Давыдова А. Н.,
6. БРОНХОЛЕГОЧНАЯ ДИСПЛАЗИЯ У НЕДОНОШЕННЫХ НОВОРОЖДЕННЫХ
Бронхолегочная дисплазия – хронический легочный фиброз у новорожденного, развивающийся в процессе интенсивной терапии дыхательных расстройств, с основными проявлениями в виде сохраняющейся зависимости от кислорода к 28-м суткам жизни, дыхательной недостаточности и стойких рентгенологических изменений.
Р 27.1 Бронхолегочная дисплазия, возникшая в перинатальном периоде.
БЛД – заболевание преимущественно недоношенных детей. Частота развития заболевания у недоношенных, находящихся на ИВЛ, составляет 6–33 %; у недоношенных с низкой массой тела – 15–50 %. Заболеваемость братно пропорциональная гестационному сроку. Чаще болеют мальчики. Летельность в течение первых 3-х месяцев жизни составляет 14–36 %, в течение 1-го года жизни – 11 %.
● терапия кислородом более 21 % (FiO2 > 21 %) в возрасте 28 дней и старше (кислородозависимость);
● дыхательная недостаточность, бронхообструктивный синдром в возрасте 28 дней и старше.
● интерстициальный отек, чередующийся с участками повышенной прозрачности легочной ткани, фиброз, лентообразные уплотнения.
1. Клиническая форма болезни: БЛД недоношенных (классическая и новая формы), БЛД доношенных.
Средний гестационный возраст большинства детей, развивающих БЛД, в современных условиях составляет 28 недель; подавляющее большинство случаев (75 %) приходится на детей с массой тела при рождении менее 1000 г. В связи с изменившимися контингентом пациентов и картиной болезни был предложен термин «новая» БЛД – паренхиматозное легочное заболевание, характеризующееся нарушением роста и развития альвеол и сосудов малого круга кровообращения, в результате воздействия различных факторов на незрелое легкое. В отличие от новой формы БЛД, в основе классической формы БЛД лежит фиброз легкого вследствие волюмо- и баротравмы с участками эмфизематозного расширения.
Основные отличия классической и новой форм БЛД
Клиника, принципы терапии и исходы бронхолегочной дисплазии
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
НИИ пульмонологии С.-Пб. ГМУ им. акад. И.П.Павлова, Детская областная клиническая больница, Санкт-Петербург
Б ронхолегочная дисплазия (БЛД) – заболевание легких, развивающееся преимущественно у недоношенных детей в периоде новорожденности, после острого эпизода дыхательных расстройств, требующих искусственной вентиляции легких (ИВЛ). БЛД формируется в результате воздействия многих факторов, среди которых наибольшее значение придается незрелости легких и ИВЛ с жесткими параметрами. Сочетанное действие высокой концентрации кислорода и положительного давления на выдохе, а также баротравма при длительной механической вентиляции играют основную роль в развитии болезни. Диагностическими критериями БЛД в периоде новорожденности являются сохраняющиеся респираторные симптомы, ИВЛ не менее 3 суток, потребность в кислородотерапии не менее 28 дней.
Морфологическое исследование при БЛД выявляет хронический бронхиолит с утолщением стенки и сужением просвета за счет перибронхиолярного склероза, гипертрофию гладкой мускулатуры мелких бронхов и бронхиол, деструкцию межальвеолярных перегородок и эмфизематозную перестройку легочной паренхимы.
В период с 1992 по 2000 г.г. с диагнозом БЛД наблюдались 96 детей в возрасте от 1 месяца до 7 лет. Дети рождались в тяжелом и крайне тяжелом состоянии с признаками дистресс-синдрома новорожденных, что требовало применения ИВЛ длительностью от нескольких дней до нескольких месяцев. В периоде новорожденности отмечались тахипноэ, цианоз, кислородозависимость в течение 28 дней и более, стойкие физикальные изменения в легких (ослабление дыхания, затруднение выдоха, сухие свистящие хрипы, влажные мелкопузырчатые хрипы и крепитация). В раннем периоде у детей на рентгенограммах определялись признаки болезни гиалиновых мембран («воздушная» бронхограмма, ателектазы и дистелектазы на фоне интерстициального отека), симптомы утечки воздуха (интерстициальная эмфизема, пневмомедиастинум, пневмоторакс).
Наблюдение за детьми позволило выявить легкое, тяжелое и среднетяжелое течение болезни. Легкое течение характеризовалось отсутствием тахипноэ в покое и аускультативных изменений в легких, которые обычно появлялись при присоединении вирусной инфекции. Не отмечалось отставания в физическом развитии и признаков легочного сердца. Рентгенологическое исследование грудной клетки выявляло умеренные признаки вздутия. При среднетяжелом течении тахипноэ появлялось при физической нагрузке (плач, беспокойство, кормление), симптомы обструкции были выражены умеренно и нарастали при вирусной инфекции. Инструментальное исследование у части больных обнаруживало признаки легочного сердца. При рентгенографии грудной клетки отмечались вздутие легочной ткани, участки локального пневмосклероза, у отдельных больных – кардиомегалия. Дети с тяжелым течением БЛД имели тахипноэ в покое, усиливающееся при физической нагрузке и вирусной инфекции. Больные значительно отставали в физическом развитии, имелись выраженные аускультативные симптомы обструкции. Эхокардиография выявляла признаки легочного сердца (легочную гипертензию, дилатацию и гипертрофию правого желудочка). При рентгенологическом исследовании наблюдалось значительное вздутие, буллы, множественные участки пневмосклероза, гиповентиляции, перибронхиальные изменения, кардиомегалия, выбухание ствола легочной артерии.
Обычно течение БЛД волнообразное. При наслоении респираторной вирусной инфекции значительно нарастала дыхательная недостаточность, и в ряде случаев требовалась интенсивная терапия или даже реанимационное пособие.
Характер воспаления слизистой дыхательных путей изучали с помощью цитоморфологического исследования бронхиальных смывов. Воспалительные изменения слизистой бронхов характеризовались повышением числа нейтрофилов и лимфоцитов, выявлением пластов дедифференцированного метаплазированного эпителия, что свидетельствовало о длительно сохраняющемся повреждении эпителиального слоя слизистой оболочки бронхов. Выраженность этих изменений коррелировала с тяжестью течения заболевания.
Лечение БЛД включало проведение оксигенотерапии для поддержания сатурации кислорода в пределах 94–96%, назначение стероидных препаратов с целью ликвидации воспалительных изменений в слизистой оболочке дыхательных путей и бронхолитических препаратов, а также витаминов А и Е. В ряде случаев возникала необходимость в применении мочегонных средств. Успех лечения больных зависит также от адекватного энергетического обеспечения, которое достигалось увеличением калорийности пищи в 1,5–2 раза и дотацией белка до 3–3,5 г на 1 кг веса ребенка.
Клинические симптомы бронхиальной обструкции, обусловленные гиперреактивностью и воспалительными изменениями слизистой оболочки, диктуют необходимость назначения стероидных препаратов. При БЛД предпочтение отдавалось ингаляционным стероидам в виде дозированных аэрозолей или жидких форм, которые доставлялись в дыхательные пути при помощи специального спейсера с маской (аэрочамбер или бебихалер) или небулайзера. Начинали с низких доз, которые повышали до минимально эффективной, терапию продолжали до стойкого клинического и рентгенологического улучшения (от 1 месяца до 2,5 лет). Ухудшение состояния требовало удвоения дозы на 2–3 недели. При достижении клинико–лабораторной ремиссии базисную терапию ингаляционными стероидами постепенно отменяли.
Ингаляционные бронходилататоры высокооэффективны при БЛД, что определяется гипертрофией гладкой мускулатуры бронхов, отмечаемой при морфологических исследованиях. Использовались адреномиметики (сальбутамол) и холинолитики (атровент), а также комбинированные формы (беродуал) в виде дозированных ингаляторов через спейсер или жидких форм через небулайзер, в возрастных дозировках сроком от 10 дней до 3 месяцев, обычно совместно с ингаляционными стероидами.
Важным моментом для благоприятного исхода болезни является сотрудничество врача и родителей больного, которые должны знать, что следует делать регулярно, а что – во время ухудшения состояния при наслоении респираторной инфекции. Кроме того, необходимо постоянное мониторирование состояния больного ребенка с целью коррекции лечебных мероприятий (родители должны вести дневник состояния ребенка, отмечать частоту дыхания и частоту сердечных сокращений во сне, а также до и после приема лекарств).
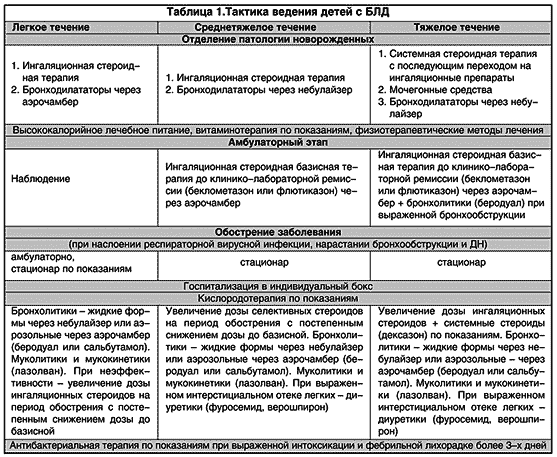
Исходя из того, что наиболее тяжелое состояние у больных с БЛД отмечается на фоне вирусной инфекции, родителям рекомендовалось соблюдение строгого охранительного режима для ребенка; при угрозе инфицирования с профилактической целью назначался интерферон интраназально. Если инфицирования избежать не удавалось, то дозировка базисных препаратов (ингаляционных стероидов) и симптоматических средств изменялась с учетом индивидуальных особенностей ребенка и характера заболевания. При длительном обострении (более 7 дней) с фебрильной температурой более 3 дней, нарастающими катаральными симптомами и дыхательной недостаточностью проводилась антибактериальная терапия коротким курсом (7–10 дней) с учетом выделенной микрофлоры. Тактика ведения больных с БЛД на разных этапах наблюдения и при разной степени тяжести представлена в табл. 1.
Длительное динамическое наблюдение (в течение 2–5 лет) 83 больных БЛД позволило уточнить прогноз этого состояния в раннем детском возрасте. Стратегия этапного наблюдения и противовоспалительная терапия использовались у 76 детей из 83. Дети со среднетяжелой формой болезни (51 ребенок), получавшие противовоспалительную терапию, не нуждались в госпитализации по поводу обострений заболевания (до назначения терапии требовалась госпитализация 2–3 раза в месяц), и к 3 годам у них удалось добиться клинического выздоровления. Однако при этом сохранялись рентгенологические изменения в виде умеренного вздутия и интерстициальной реакции. Дети, имеющие тяжелую форму болезни (25 больных), также получали противовоспалительную терапию, однако клинического выздоровления удалось добиться у 18 больных (73%), 5 детей (23%) умерли в течение первых 1,5 лет жизни, у 1 ребенка (4%) сформировался хронический бронхиолит. Часть больных с БЛД (7 детей из 83) не получали базисную терапию, так как наблюдались в различных лечебных учреждениях с ошибочным диагнозом «рецидивирующая пневмония с обструктивным синдромом». Из них 1 ребенок умер (14%), а у 6 больных (84%) сформировалась тяжелая форма хронического бронхиолита, что послужило основанием для назначения инвалидности.
Что такое блд у ребенка
На современном этапе развития медицинской науки, появились новые ятрогенные заболевания, которые рассматриваются как результат улучшения выхаживания новорожденных, в том числе и бронхолегочная дисплазия (БЛД). Увеличение заболеваемости данной патологией неуклонно растет не только в развитых странах мира, но и в России. Это связано, в первую очередь, с переходом российского здравоохранения на рекомендованные ВОЗ критерии живорождения и мертворождения, которые регламентируют регистрацию новорожденных с массой тела от 500 г и выше, а также с улучшением выживаемости и улучшением выхаживания детей, рожденных с экстремально низкой и очень низкой массой тела.
Как нозологическая единица бронхолегочная дисплазия впервые была выделена доктором W.L.Northway с соавт. в 1967 году. В своей работе он представил обзор данных рентгенологических исследований 32-х недоношенных новорожденных, перенесших синдром дыхательных расстройств и находившихся на искусственной вентиляции легких (ИВЛ) в течение 24 часов и более. Дети имели средний гестационный возраст 32 недели, масса тела при рождении достигала в среднем 2200г. В результате полученных данных Northway сделал заключение о появлении нового хронического заболевания у детей [5]. В России диагноз БЛД впервые был поставлен в Санкт-Петербурге в 1989 г., а в 1995 г. БЛД была внесена в Классификацию клинических форм бронхолегочных заболеваний у детей.
По определению XVIII Национального Конгресса по болезням органов дыхания (2008), бронхолегочная дисплазия (код в МКБ X Р27.0)—это полиэтиологическое хроническое заболевание морфологически незрелых легких, развивающееся у новорожденных, главным образом глубоко недоношенных детей, в результате интенсивной терапии респираторного дистресс-синдрома и (или) пневмонии. Протекает с преимущественным поражением бронхиол и паренхимы легких, развитием эмфиземы, фиброза и (или) нарушением репликации альвеол; проявляется зависимостью от кислорода в возрасте 28 суток жизни и старше, бронхообструктивным синдромом и симптомами дыхательной недостаточности; характеризуется специфичными рентгенографическими изменениями в первые месяцы жизни и регрессом клинических проявлений по мере роста ребенка [4].
Бронхолегочная дисплазия, согласно принятой рабочей классификации клинических форм бронхолегочных заболеваний у детей, по форме подразделяется на классическую и новую ( у недоношенных детей) и БЛД доношенных [3].
Классическая форма БЛД развивается за счёт повреждение незрелых легких кислородом, давлением, объемом при проведении ИВЛ, ведущее к системной воспалительной реакции, поражению дыхательных путей, фиброзу и эмфиземе.
Рентгенологическая картина представляет собой чередование участков ателектазов и эмфиземы с фиброзом по типу «булыжной мостовой».
Бронхообструкция у детей связана с морфологическими изменениями бронхов: уменьшение диаметра бронхов, облитерирующий бронхиолит, персистирующий интерстициальный отек, фиброз, гиперплазия и гипертрофия слизистой мускулатуры бронхов.
Пациенты с такой формой требуют «жестких параметров» ИВЛ и высокую концентрацию кислорода.
Новая форма БЛД – это паренхиматозное лёгочное заболевание, характеризующееся нарушением роста и развития альвеол и сосудов малого круга кровообращения. Новая форма БЛД отличается от классической уменьшенным количеством альвеол при минимальном выраженном фиброзе. Данная форма развивается у детей с гестационным возрастом менее 32 недель, у которых для профилактики и лечения использовались препараты сурфактанта [4].
Бронхолёгочная дисплазия доношенных выделяют у детей с гестационным возрастом более 36 недель, клинические и рентгенологические данные схожи с классической формой БЛД.
По степени тяжести БЛД подразделяют на лёгкую, среднетяжёлую и тяжёлую формы
Таблица 1. Классификация БЛД по степени тяжести
На современном этапе бронхолегочная дисплазия является мультифакториальным заболеванием. К ведущим факторам риска относятся:
a) недоношенность (гестационный возраст менее 32 недель, масса при рождении менее 1500 гр);
b) незрелость лёгочной ткани, дефицит сурфактанта;
c) «жесткие параметры» ИВЛ;
d) тяжёлое течение РДС;
e) генетическая предрасположенность: бронхиальная гиперреактивность, дисплазия соединительной ткани, полиморфизма генов антиоксидантных ферментов (митохондриальная супероксиддисмутаза, микросомальная эпоксигидролаза) и фермента эндотелиальной дисфункции (синтаза оксида азота);
Дальнейший прогноз для детей с бронхолёгочной дисплазией зависит от тяжести поражения легких. Как правило, дети с бронхолёгочной дисплазией склонны к частым респираторным заболеваниям, которые могут осложняться бронхоспазмом, наблюдается гиперреактивность дыхательных путей.
У больных тяжёлой формой бронхолегочной дисплазии развиваются хронические заболевания легких (эмфизема, локальный пневмосклероз). Так же в дальнейшем БЛД может послужить фактором риска развития хронической обструктивной болезни легких (ХОБЛ) у взрослых в молодом возрасте.
Несмотря на значительный прорыв медицинской науки в понимании механизмов развития и диагностики, лечении и профилактике БЛД, остается много научно-практических проблем данного заболевания у детей грудного и раннего возраста. Остаются нерешенными вопросы относительно частоты БЛД в структуре респираторных заболеваний легких у детей раннего возраста, семиотики данной патологии как хронического заболевания легких в данной возрастной категории, а также не определена информативность клинических критериев тяжести БЛД в контексте с анамнестическими критериями тяжести.
Цель: определить факторы риска, охарактеризовать клиническую и рентгенологическую семиотику у детей раннего возраста с бронхолегочной дисплазией.
Материалы и методы: исследование проводилось на базе ОБУЗ «Областная детская клиническая больница» г. Курск. Был проведён анализ 50 историй детей, находившихся на обследовании и лечении в данной клинике, за период с сентября 2016 по ноябрь 2018 года, с диагнозом «Бронхолёгочная дисплазия» в возрасте от 2-х месяцев до 3-х лет. В ходе исследования было выявлено, что мальчики составили 63% всех обследуемых детей, а девочки – 37%. Преобладали пациенты с новой формой бронхолегочной дисплазии – 29 пациентов ( 58%), классическая форма наблюдалась у 21 пациента (42 %).У 25 пациентов (50%) отмечалось легкое течение БЛД, у 16 пациента (32%) было выявлено среднетяжёлое течение БЛД, и у 9 пациентов (18%) тяжёлое течение.
Результаты: в ходе проведенного исследования выявлено, что частота бронхолегочной дисплазии обратно пропорциональна гестационному возрасту и массе тела при рождении. Так, наличие веса при рождении до 850 г. отмечалось у 62% новорожденных, от 850 до 1250 – у 32%, от 1250 г. до 1500 г. – у 4%, от 1500г. и выше – у 2% (табл 2).
Таблица 2. Распределение больных по сроку гестации, полу, возрасту и массе при рождении
28,4
Возраст при обследовании,мес
1,8