что такое бикарбонат фото
БИКАРБОНАТЫ
Смотреть что такое «БИКАРБОНАТЫ» в других словарях:
Бикарбонаты — кислые соли угольной кислоты; современное название Гидрокарбонаты … Большая советская энциклопедия
бикарбонаты — бикарбон аты, ов, ед. ч. н ат, а … Русский орфографический словарь
Гидрокарбонаты — бикарбонаты, двууглекислые соли, кислые соли угольной кислоты (См. Угольная кислота) H2CO3, например NaHCO3 (Гидрокарбонат натрия). Г. получают действием CO2 на карбонаты или гидроокиси в присутствии воды. При нагревании они превращаются… … Большая советская энциклопедия
ГИДРОКАРБОНАТЫ — (бикарбонаты), кислые соли угольной кислоты Н2СО3, напр. питьевая сода NaHCO3 … Естествознание. Энциклопедический словарь
Желудочный сок — Сюда перенаправляется запрос «Желудочная секреция». На эту тему нужна отдельная статья. Желудочный сок сложный по составу пищеварительный сок, вырабатываемый различными клетками слизистой оболочки желудка. Содержание … Википедия
ВОДА — ВОДА. I. Физико химические свойства и состав воды. Водные пространства мирового океана и морей составляют 361 млн. кв. км и занимают 71% всей земной поверхности. В свободном состоянии В. занимает самую поверхностную часть земной коры, т. н.… … Большая медицинская энциклопедия
Кислотно-щелочное равновесие — I Кислотно щелочное равновесие (синоним: кислотно основное равновесие, кислотно щелочной баланс, равновесие кислот и оснований) относительное постоянство концентрации водородных ионов во внутренних средах организма, обеспечивающее полноценность… … Медицинская энциклопедия
АЛКАЛОЗ — АЛКАЛОЗ, alkalosis, повышение щелочности крови и тканей организма. В норме реакция крови слегка щелочная. Концентрация Н ионов ее при 18° равна 0,29.10 7 нормальности и при 37° 0,45.Ю 7, что соответствует 2,ЗЛО 7 и 5,8.Ю 7концентрации… … Большая медицинская энциклопедия
КРОВЬ — КРОВЬ, жидкость, заполняющая артерии, вены и капиляры организма и состоящая из прозрачной бледножелтоват. цвета плаз мы и взвешенных в ней форменных элементов: красных кровяных телец, или эритроцитов, белых, или лейкоцитов, и кровяных бляшек, или … Большая медицинская энциклопедия
Натрия гидрокарбонат (пищевая сода)

Гидрокарбонат натрия — химическое вещество
Натрия гидрокарбонат — лекарственное средство
Терапия гидрокарбонатом натрия беременных и кормящих матерей
В связи с нежелательными побочными эффектами натрия (отек и увеличение веса) некоторые специалисты выступают за использование у беременных альтернативных антацидов, не содержащих гидрокарбонат натрия. Категория риска для плода по FDA при терапии гидрокарбонатом натрия — «C» (исследования на животных выявили отрицательное воздействие лекарства на плод, а надлежащих исследований у беременных женщин не было, однако потенциальная польза, связанная с применением данного лекарства у беременных, может оправдывать его использование, несмотря на имеющийся риск).
В связи с отсутствие данных об экскреции натрия гидрокарбоната в материнское молоко, ограничений для терапии кормящих грудью матерей нет.
Питьевая сода — традиционное, но опасное средство для купирования изжоги
| Bсе наклоненья и залоги Изжеваны до одного. Хватить бы соды от изжоги! Так вот итог твой, мастерство? Б.Л. Пастернак. «Bсе наклоненья и залоги». 1936. |
Натрия гидрокарбонат — традиционное средство для купирования изжоги, всасывающийся антацид. Всасывающимися называют антациды, которые или сами, или продукты их реакции с кислотой желудочного сока растворяются в крови. 
После приема 3 г гидрокарбоната натрия рН желудочного содержимого сохраняется на уровне выше 3 единиц рН лишь в течение 75 минут. Образующаяся при нейтрализации углекислота вызывает отрыжку и вздутие живота. Как редкое осложнение после приема гидрокарбоната натрия, описан разрыв желудка из-за резкого освобождения большого количества газа (А.В. Охлобыстин).
В XIX веке «сода» была одним из самых популярных средств от изжоги, например, её постоянно принимал П.И. Чайковский.
Натрий гидрокарбонат в составе кислотоподавляющих лекарств
Несмотря на отрицательное отношение к гидрокарбонату натрия как средству купирования изжоги, он иногда включается в состав лекарств, предназначенных для снижения кислотности в верхних отделах желудочно-кишечного тракта, в достаточном количестве, чтобы его рассматривать, как еще одно действующее вещество (хотя в инструкции к такому препарату гидрокарбонат натрия может быть перечислен среди вспомогательных, а не активных веществ).

| Основные ингредиенты | Zegerid, капсула | Zegerid, капсула | Zegerid, пакетик* | Zegerid, пакетик* | Zegerid OTC, капсула | Омез Инста, пакетик* |
| Омепразол, мг | 20 | 40 | 20 | 40 | 20 | 20 |
| Натрия гидрокарбонат, мг | 1100 | 1100 | 1680 | 1680 | 1100 | 1680 |
Примечание. *) Пакетик содержит порошок для приготовления суспензии для приема внутрь.

| Основные ингредиенты | Гевискон, 10 мл суспензии | Гевискон, таблетка жевательная | Гевискон форте, 10 мл суспензии | Гевискон Двойное Действие, таблетка жевательная | Гевискон Двойное Действие, 10 мл суспензии |
| Натрия альгинат, мг | 500 | 250 | 1000 | 250 | 500 |
| Натрия гидрокарбонат, мг | 267 | 133,5 | — | 267 | 213 |
Натрия гидрокарбонат в составе других лекарств
Применение гидрокарбоната натрия при исследовании желудка (тест Ноллера)
Тест Ноллера (щелочной тест) выполняется с целью получения информации о количестве соляной кислоты в желудке пациента, об интенсивности кислотообразования, а также, косвенно, о количестве желудочного сока. Тест проводится одновременно с процедурой внутрижелудочной рН-метрии, через 20 минут после стабилизации кислотности в базальных условиях или через 45 минут после введения стимуляторов. При рН равном или выше 4,0 щелочной тест не проводится.
Пациент выпивает 0,5 г гидрокарбоната натрия, растворенного в 30 мл дистиллированной воды. Обычно в теле желудка рН регистрируется ниже 2,5. В результате введения в желудок щелочи показатели рН изменяются до щелочных и в течение определенного времени сохраняются на одном уровне, а затем, через некоторое время, называемое «щелочным временем», возвращаются к исходным. По щелочному времени определяется состояние кислотопродукции желудка пациента (С.И. Рапопорт и др.):
Оценка продукции соляной кислоты в желудке
Бикарбонаты, как естественное средство защиты органов ЖКТ от кислоты
Бикарбонаты вместе со слизью составляют так называемый предэпителиальный уровень защиты слизистой оболочки желудка. Слизь не может защищать эпителий от ионов Н + без постоянно поступающих в нее бикарбонатов, также секретируемых поверхностным эпителием. С помощью бикарбонатов в слизи поддерживается градиент рН: на поверхности, обращенной в просвет желудка, среда кислая, а у эпителиоцитов — нейтральная или слабощелочная. Немедленного смешивания бикарбонатов с кислым секретом в просвете и нейтрализации не происходит: слой слизи образует барьер, благодаря которому и существует градиент рН (Т.Л. Лапина ).
Бикарбонаты также секретируются протоковыми клетами поджелудочной железы и вместе с соком поджелудочной железы поступают в двенадцатиперстную кишку, где участвуют в нейтрализации соляной кислоты (О.А. Саблин и др.).
Гидрокарбонат в минеральных водах
Ионы гидрокарбонатов HCO3 – присутствуют практически во всех природных минеральных водах. Для их определения в воде применяется ГОСТ 23268.3-78 «Воды минеральные питьевые лечебные, лечебно-столовые и природные столовые. Методы определения гидрокарбонат-ионов». Согласно ГОСТ Р 54316-2011. «Воды минеральные природные питьевые. Общие технические условия» содержание гидрокарбонаты указывается на потребительской таре (на этикетках бутылок с минеральной водой).
Что такое бикарбонат фото
Фармакологическое действие
Антацидное средство, регулирует КЩР. Обладает щелочными свойствами, повышает щелочной резерв крови. При приеме внутрь быстро нейтрализует соляную кислоту желудочного сока и оказывает быстрый, но кратковременный антацидный эффект. Раздражает рецепторы слизистой оболочки желудка, усиливает выделение гастрина с вторичной активацией секреции, может вызывать неприятные ощущения в желудке (вследствие его растяжения) и отрыжку.
Обладает отхаркивающим действием за счет уменьшения вязкости мокроты в связи со сдвигом в щелочную сторону реакции бронхиальной слизи.
Всасываясь, приводит к развитию алкалоза. Ощелачивание мочи предупреждает осаждение мочевой кислоты в мочевыводящих путях.
Облегчает симптомы морской и воздушной болезни.
Показания
Метаболический ацидоз (в т.ч. при сахарном диабете, инфекциях, интоксикациях, заболеваниях почек, наркозе, в послеоперационном периоде); в качестве симптоматического средства для купирования изжоги, неприятных ощущений в эпигастрии, связанных с повышенной кислотностью желудочного сока; симптоматическое лечение кашля с вязкой и трудноотделяемой мокротой при различных заболеваниях дыхательных путей; морская и воздушная болезнь.
Для местного применения: воспалительные заболевания полости рта, глаз, верхних дыхательных путей, для разрыхления ушной серы.
Противопоказания
Дозировка
Побочные действия
Лекарственное взаимодействие
При приеме внутрь натрия гидрокарбоната на фоне применения лития карбоната в установленных поддерживающих дозах возможно уменьшение концентрации лития в плазме крови, что обусловлено влиянием ионов натрия.
При одновременном применении с метотрексатом усиливается выведение метотрексата с мочой и уменьшается его токсическое действие на почки вследствие повышения pH мочи под влиянием натрия гидрокарбоната.
При одновременном приеме внутрь уменьшается всасывание тетрациклинов.
Вследствие повышения pH мочи под влиянием натрия гидрокарбоната наблюдается задержка выведения эфедрина из организма и повышается риск развития побочных эффектов (тремор, тревога, нарушения сна, тахикардия).
При в/в капельном введении натрия гидрокарбоната возможно усиление антигипертензивного эффекта резерпина.
Особые указания
Не рекомендуется применять систематически в связи с тем, что при нейтрализации хлористоводородной кислоты желудка натрия гидрокарбонатом происходит выделение углекислоты, которая оказывает возбуждающее действие на рецепторы слизистой оболочки желудка, усиливает выделение гастрина и может вызвать вторичное усиление секреции. Кроме того, при длительном регулярном применении возможно защелачивание мочи и повышение риска образования фосфатных камней.
Интенсивное выведение CO 2 может спровоцировать перфорацию стенок ЖКТ.
У пациентов с сопутствующими заболеваниями сердца или почек избыточное употребление натрия вызывает отеки и сердечную недостаточность.
Бикарбонаты
Смотреть что такое «Бикарбонаты» в других словарях:
БИКАРБОНАТЫ — (двууглекислые соли), однометаллические, кислые соли угольной к ты Н2С03 (напр., NaHC03, двууглекислая сода). Как соли весьма слабой кислоты Б. всеми минеральными и даже большинством органических кислот разлагаются с выделением свободной С02;… … Большая медицинская энциклопедия
бикарбонаты — бикарбон аты, ов, ед. ч. н ат, а … Русский орфографический словарь
Гидрокарбонаты — бикарбонаты, двууглекислые соли, кислые соли угольной кислоты (См. Угольная кислота) H2CO3, например NaHCO3 (Гидрокарбонат натрия). Г. получают действием CO2 на карбонаты или гидроокиси в присутствии воды. При нагревании они превращаются… … Большая советская энциклопедия
ГИДРОКАРБОНАТЫ — (бикарбонаты), кислые соли угольной кислоты Н2СО3, напр. питьевая сода NaHCO3 … Естествознание. Энциклопедический словарь
Желудочный сок — Сюда перенаправляется запрос «Желудочная секреция». На эту тему нужна отдельная статья. Желудочный сок сложный по составу пищеварительный сок, вырабатываемый различными клетками слизистой оболочки желудка. Содержание … Википедия
ВОДА — ВОДА. I. Физико химические свойства и состав воды. Водные пространства мирового океана и морей составляют 361 млн. кв. км и занимают 71% всей земной поверхности. В свободном состоянии В. занимает самую поверхностную часть земной коры, т. н.… … Большая медицинская энциклопедия
Кислотно-щелочное равновесие — I Кислотно щелочное равновесие (синоним: кислотно основное равновесие, кислотно щелочной баланс, равновесие кислот и оснований) относительное постоянство концентрации водородных ионов во внутренних средах организма, обеспечивающее полноценность… … Медицинская энциклопедия
АЛКАЛОЗ — АЛКАЛОЗ, alkalosis, повышение щелочности крови и тканей организма. В норме реакция крови слегка щелочная. Концентрация Н ионов ее при 18° равна 0,29.10 7 нормальности и при 37° 0,45.Ю 7, что соответствует 2,ЗЛО 7 и 5,8.Ю 7концентрации… … Большая медицинская энциклопедия
КРОВЬ — КРОВЬ, жидкость, заполняющая артерии, вены и капиляры организма и состоящая из прозрачной бледножелтоват. цвета плаз мы и взвешенных в ней форменных элементов: красных кровяных телец, или эритроцитов, белых, или лейкоцитов, и кровяных бляшек, или … Большая медицинская энциклопедия
Гидрокарбонат натрия
| Гидрокарбонат натрия | |
|---|---|
 | |
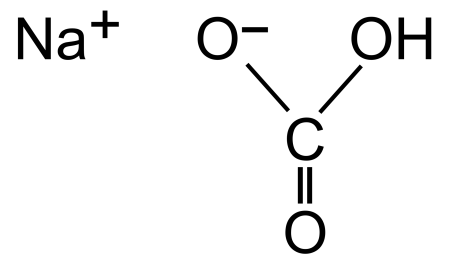 | |
| Систематическое наименование | гидрокарбонат натрия |
| Традиционные названия | пищевая (питьевая) сода, сода двууглекислая, двууглекислый натрий, бикарбонат натрия, кислый углекислый натрий |
| Хим. формула | CHNaO₃ |
| Рац. формула | NaHCO3 |
| Состояние | твёрдое |
| Молярная масса | 84,0066 г/моль |
| Плотность | 2,159 г/см³ |
| Т. разл. | 60—200 °C |
| Растворимость в воде | 9,59 г/100 мл |
| ГОСТ | ГОСТ 2156-76 ГОСТ 4201-79 ГОСТ 32802-2014 |
| Рег. номер CAS | 144-55-8 |
| PubChem | 516892 |
| Рег. номер EINECS | 205-633-8 |
| SMILES | |
| Рег. номер EC | 205-633-8 |
| Кодекс Алиментариус | E500(ii) |
| RTECS | VZ0950000 |
| ChEBI | 32139 |
| ChemSpider | 8609 |
| ЛД50 | 4220 мг/кг |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Гидрокарбонат натрия (лат. Natrii hydrocarbonas ), другие названия: бикарбонат натрия, чайная сада, питьевая или пищевая сода, двууглекислый натрий — неорганическое соединение, натриевая кислая соль угольной кислоты с химической формулой NaHCO3.
В обычном виде — мелкокристаллический порошок белого цвета.
Используется в промышленности, пищевой промышленности, в кулинарии, в медицине как нейтрализатор химических ожогов кожи и слизистых оболочек концентрированными кислотами и для снижения кислотности желудочного сока. Также применяется в буферных растворах.
Содержание
Химические свойства
Гидрокарбонат натрия — кислая натриевая соль угольной кислоты. Проявляет все свойства соли сильного основания и слабой кислоты. В водных растворах имеет слабощелочную реакцию. В широком диапазоне концентраций в водном растворе pH раствора изменяется незначительно, на этом основано применение раствора вещества в качестве буферного раствора.
Реакция с кислотами
Гидрокарбонат натрия реагирует с кислотами с образованием соответствующей кислоте соли, например, хлорида натрия, сульфата натрия и угольной кислоты, которая в процессе реакции распадается на углекислый газ и воду, при этом углекислый газ выделяется из раствора в виде пузырьков:
В быту обычно применяется реакция «гашения соды» уксусной кислотой, с образованием ацетата натрия или гашение лимонной кислотой с образование цитрата натрия, реакция с уксусной кислотой:
Термическое разложение
При температуре выше 60 °C гидрокарбонат натрия начинает распадаться на карбонат натрия, углекислый газ и воду (процесс разложения наиболее эффективен при 200 °C, при более высоких температурах карбонат натрия начинает распадаться на оксид натрия и углекислый газ):
При этом процессе выделения воды в виде водяного пара и углекислого газa масса исходного продукта уменьшается примерно на 37 %.
Получение
В промышленности гидрокарбонат натрия получают аммиачно-хлоридным способом. В концентрированный раствор хлорида натрия, насыщенный аммиаком, под давлением пропускают углекислый газ. В процессе синтеза происходят две реакции:
В холодной воде гидрокарбонат натрия мало растворим, и его отделяют от охлаждённого раствора фильтрованием, а из полученного после фильтрования раствора хлорида аммония снова получают аммиак, возвращаемый в производство вновь:
Применение
Двууглекислый натрий (бикарбонат) применяется в химической, пищевой, лёгкой, медицинской, фармацевтической промышленности, цветной металлургии, в быту. Зарегистрирован в качестве пищевой добавки E500 (ii), входит в состав пищевой добавки E500.
В химической промышленности
Применяется для производства красителей, пенопластов и других органических продуктов, фторорганических соединений, продуктов бытовой химии, наполнителей в огнетушителях, Реагент для отделения диоксида углерода, сероводорода из газовых смесей, например, отходящих газов топливосжигающих установок. В этом процессе углекислый газ поглощается раствором гидрокарбоната натрия при повышенном давлении и пониженной температуре, далее поглощённый углекислый газ выделяется из раствора при подогреве и снижении давления;
В лёгкой промышленности — в производстве резины для подошв обуви и в производстве искусственных кож, кожевенном производстве при дублении и нейтрализации кожи после кислого дубления, текстильной промышленности при отделке шёлковых и хлопчатобумажных тканей;
В пищевой промышленности — в хлебопечении, производстве кондитерских изделий, приготовлении газированных напитков.
В кулинарии
Основное применение пищевой соды в пищевой промышленности и в быту — кулинария, где применяется, преимущественно, в качестве основного или дополнительного разрыхлителя в составе кислого и пресного теста. При добавлении питьевой соды в кислое тесто происходит реакция с молочной кислотой, продуцированной при заквашивании дрожжевыми микроорганизмами, при этой реакции выделяется углекислый газ, вспучивающий тесто.
При добавлении в пресное тесто углекислый газ выделяется при выпечке из-за термического разложения.
При применении соды в чистом виде важно соблюсти правильную дозировку, так как она оставляет в продукте карбонат натрия, дающий определённый привкус. Порядок замешивания для теста: соду — в муку, кислые компоненты (уксус, кефир и пр.) — в жидкость.
В медицине
Традиционно раствор питьевой соды используется для дезинфекции зубов и дёсен при зубных болях и полости рта и горла, при сильном кашле, ангине, фарингите, а также как общепринятое средство от изжоги и болей в желудке.
Применяется при заболеваниях, сопровождающиеся выраженным ацидозом (при диабете, инфекциях и др), для борьбы с ацидозом при хирургических вмешательствах (назначается 3-5 г. внутрь).
Применяется в качестве антиаритмического средства.
Как антацидное средство (как и все другие щелочи) применяется при язвенной болезни желудка, и двенадцатиперстной кишки, при повышенной кислотности желудочного сока.
Имеются так же данные о применении препарата (в виде капельных и внутривенных вливаний) при гипертонической болезни, симптоматической почечной гипертонии, и хронической почечной недостаточности. Эффект связан с увеличением выделения ионов натрия и хлора и возрастанием осмотического диуреза.
В виде свечей применяется против укачивания при морской и воздушной болезнях
Применяется в качестве отхаркивающего средства, т.к. повышая щелочные резервы крови, сдвигает в щелочную сторону реакцию бронхиальной слизи, делая мокроту менее вязкой.
Применяется внутривенно с целью быстрого устранения метаболического ацидоза во время реанимационных мероприятий, заболеваниях почек.
Нужно иметь ввиду, что в результате применения может возникнуть т.н. кислотный рикошет (при реакции содой с соляной кислотой происходит выделение CO2, который оказывает раздражающее действие на стенку желудка, усиливая выделение гастрина).
В альтернативной медицине питьевая сода иногда заявляется как «лекарство» от рака, однако, никакой экспериментально подтверждённой эффективности применения такого «лечения» не существует.
Противопоказания к применению в медицинских целях
Является источником натрия, тем самым увеличивая объём циркулирующей крови, усугубляя отёки и повышая артериальное давление. Применение при сниженной скорости клубочковой фильтрации может привести к метаболическому алкалозу.
Пожаротушение
Гидрокарбонат натрия вместе с карбонатом аммония используется в качестве наполнителя в огнетушителях с сухим наполнением и в стационарных системах сухого пожаротушения. Это применение обусловлено тем, что от воздействия высокой температуры в очаге горения вещество выделяет углекислый газ, атмосфера которого затрудняет доступ кислорода воздуха в очаг горения.
В быту
Применяется как безопасное для здоровья средство для чистки поверхностей столовой и кухонной посуды, поверхностей кухонных столов, иных поверхностей, соприкасающихся с пищей, путем протирки их с помощью влажной тряпки с сухим порошком питьевой соды.
В транспорте
Применяется для нейтрализации следов электролита — серной кислоты на поверхности пластмассовых корпусов свинцовых аккумуляторов насыщенным водным раствором питьевой соды.
Производство
В Российской Федерации двууглекислый натрий выпускается в соответствии с требованиями и техническими условиями, выпускается на предприятиях АО «Башкирская содовая компания» в г. Стерлитамак, Республика Башкортостан, а также на Крымском содовом заводе в г. Красноперекопск, Крымский полуостров.
Хранение
Гидрокарбонат натрия хранят в закрытых упаковках, в сухом месте вдали от источников огня. Гарантийный срок хранения натрия двууглекислого — 12 месяцев со дня изготовления. Срок годности не ограничен.
Безопасность
Вещество нетоксично, пожаро- и взрывобезопасно.





