Цитробактер браакии что это
Цитробактериоз: что нужно знать
Цитробактериоз – это острое инфекционное заболевание пищеварительной системы, возникающее в результате заражения бактериями рода Citrobakter, сопровождающееся выраженной интоксикацией и обезвоживанием.
Citrobakter присутствует в почве, воде и фекалиях человека и животных, поэтому инфекция передается, как правило, фекально-оральным путем. Заражение человека может наступить вследствии употреблении в пищу недостаточно пастеризованного молока, молочных продуктов и сливочного масла, выпущенных недобросовестными производителями, употребление загрязненных кондитерских изделий, а также в результате плохой прожарки мяса и птиц животных.
Дети, в особенности те, у которых ослаблен иммунитет, могут заразиться через грязные руки, игрушки, при контакте с взрослыми, являющимися носителями этих бактерий и прочими контактно-бытовыми способами.
Все бактерии данного вида обладают устойчивостью к дезинфицирующим средствам и по своей структуре схожи с сальмонеллами.
Протекать заболевание может как гастрит, сильное пищевое отравление, энтерит, гастроэнтерит. Его инкубационный период очень короткий – от 2 до 5 часов. Гастрит начинается с появления болей в области эпигастрия, повторяющейся рвоты, периодически усиливающейся тошноты. Температура тела может подниматься до 38,5 градусов. Остальные симптомы отравления могут быть выражены размыто. Длится острое состояние на протяжении 1-2 дней.
Основным лабораторным показателем цитробактериоза является наличие бактерии цитробактер в анализе кала в количестве превышающем допустимую норму. В случае с маленькими детьми анализ кала берут несколько раз и сравнивают количество колоний. Если оно неуклонно растет, то следует как можно быстрее принимать меры.
Бактериологическая лаборатория ФБУЗ «Центра гигиены и эпидемиологии в Тульской области» обладает всеми необходимыми ресурсами для проведения бактериологических исследований на цитробактериоз, что позволяет значительно ускорить диагностику заболевания, поставить адекватный диагноз и своевременно назначить лечение.
В практике бактериологической лаборатории имеется опыт обнаружения цитробактера у детей: при обследовании группы детей школьного возраста при подозрение на инфекционное заболевание у 40% был обнаружен Citrobacter freundii, что было также подтверждено на анализаторе полуавтоматическом бактериологическом Autoscan 4.
Профилактика этой инфекции заключается в соблюдении правил личной гигиены, тщательном мытье и термической обработке продуктов питания, мытье рук перед приемом пищи, соблюдении сроков годности продукта и товарного соседства.
Citrobacter (цитробактер)

Сitrobacter в систематике бактерий
Род цитробактер (Citrobacter) входит в семейство энтеробактерии (Enterobacteriaceae), порядок энтеробактерии (Enterobacteriales), класс гамма-протеобактерии (γ proteobacteria), тип протеобактерии (Proteobacteria), царство бактерии.
Сitrobacter — возбудитель заболеваний человека и животных
Цитробактер является одной из самых частых причин внутрибольничных ангиогенных инфекций и инфекций мочевыводящих путей. Цитробактер способен вызывать вспышки гастроэнтеритов и токсикоинфекций, внутрибольничные инфекции, менингиты, абсцессы мозга, урологические заболевания, гнойные инфекции и сепсис у детей и взрослых людей. В регионах России в последние годы периодически происходят массовые отравления, в том числе в детских учреждениях, вызванные цитробактером, основной причиной которых является нарушение технологии приготовления пищи.
Источником инфекции являются люди и животные. Механизм передачи цитробактера — фекально-оральный. Основной путь передачи — пищевой, через молоко, молочные продукты, масло, кондитерские изделия, мясо птиц и животных. У ослабленных детей раннего возраста возможен контактно-бытовой путь заражения через игрушки, предметы ухода, руки персонала.
Цитобактериоз может протекать по типу пищевого отравления в виде гастрита, энтерита или гастроэнтерита. Инкубационный период цитробактериоза от 2 до 5 часов.
Гастрит начинается остро с тошноты, повторной рвоты, боли в эпигастральной области. Температура тела, чаще всего, в пределах от 37–37,5 до 38–38,5 ° С. Симптомы отравления выражены умеренно. Продолжительность — 1–2 дня.
Гастроэнтерит начинается остро с тошноты, повторной рвоты, болей в животе. Стул частый, жидкий, иногда с примесью слизи, до 10 раз в сутки. Боль в животе в первые дни болезни может быть выраженной, локализуется преимущественно в эпигастральной области, при пальпации определяется болезненность по ходу тонкой кишки. Понос, чаще всего, на несколько часов опережает развитие симптомов отравления. Температура тела повышается до 38° С, сохраняется не более 5 дней. Прогноз благоприятный, продолжительность цитробактериоза — от 4 до 6 дней.
Диагноз на цитробактериоз устанавливается после проведения специальных лабораторных исследований.
Цитробактер способен самостоятельно или в ассоциации с другими микробами вызывать заболевания у домашних и диких животных, рыб и пчёл. В современной России имеются прецеденты, когда циторбактер выявляли в фабрично изготовленном комбикорме. Корма, зараженные цитробактером или с подозрением на цитробактер требуют обязательной проварки при температуре не ниже 100° С не менее часа.
На сайте GastroScan.ru в разделе «Литература» имеется подраздел «Микрофлора, микробиоценоз, дисбиоз (дисбактериоз)», содержащий статьи, затрагивающие проблемы микробиоценоза и дисбиоза отделов ЖКТ человека.
Цитробактер в результатах анализа кала на дисбактериоз
При избыточном росте цитробактера, как следствии дисбактериоза, при медикаментозной терапии применяются различные пробиотки (Бифидумбактерин, Бифиформ, Лактобактерин, Ацилакт, Аципол и др.) и/или адекватные конкретному штамму цитробактера и причине дисбактериоза бактериофаги и антибиотики.
В образцах злокачественных колоректальных новообразований человека концентрация Citrobacter spp. повышена (Marchesi J.R., Dutilh B.E., Hall N. et al. Towards the human colorectal cancer microbiome. PLoS One 2011; 6: e20447).
Антибиотики, активные и неактивные в отношении цитробактера
Антибактериальные средства (из имеющих описание в данном справочнике), активные в отношении цитробактера: ципрофлоксацин, норфлоксацин, офлаксацин. В отношении Citrobacter koseri и Citrobacter freundii активен левофлоксацин.
Цитробактер слабо чувствителен к нифуроксазиду.
Современные подходы к терапии хронического бактериального простатита
Хронический простатит (ХП) принадлежит к числу самых распространенных урологических заболеваний. По данным Н. А. Лопаткина (1998), в России на долю ХП приходится до 35% всех обращений к врачу по поводу
Хронический простатит (ХП) принадлежит к числу самых распространенных урологических заболеваний. По данным Н. А. Лопаткина (1998), в России на долю ХП приходится до 35% всех обращений к врачу по поводу урологических проблем среди мужчин в возрасте от 20 до 50 лет. Для получения данных о частоте встречаемости симптомов простатита с оценкой распространенности дизурии, дискомфорта в промежности и в области полового члена было проведено международное (Англия, Франция, Голландия, Корея) эпидемиологическое исследование Urepik. Анализ, проводившийся на основании шкалы симптомов Nickel и Sorensen (1996), дал возможность выявить признаки простатита у 4800 мужчин в возрасте от 40 до 79 лет. У 35% мужчин за последний год наблюдался как минимум один из симптомов простатита, и для 8% мужчин это представляло, по меньшей мере, неудобство [1].
На долю хронического бактериального простатита (ХБП) приходится 5–15% случаев заболевания [6]. Наиболее распространенными, по мнению большинства исследователей, этиологическими агентами ХБП являются такие грамотрицательные бактерии семейства Enterobacteriaceae, как Escherichia coli, которые обнаруживаются в 65–80% случаев инфекций. Различные виды Serratia, Klebsiella, Enterobacter, Acinetobacter выявляются у 10–15% больных. Большинство исследователей полагают, что на долю таких грамположительных бактерий, как Enterococcus faecalis, приходится от 5 до 10% случаев подтвержденных инфекций простаты [5].
В настоящее время обсуждается роль грамположительных бактерий — коагулазо-негативных стафилококков и стрептококков в развитии ХБП [5, 6, 7]. По нашим данным (Е. Б. Мазо и соавт., 2003, 2004) [1], основанным на результатах микробиологического исследования, которое проводилось в виде четырехстаканного теста Meares–Stamey у 70 больных с ХБП с 2002 г., именно коагулазо-негативные стафилококки играют ведущую роль (66%), если говорить об этиологии ХБП. Между тем на долю грамотрицательных патогенов приходится 19% случаев ХБП, а 15% составляют больные с Enterococcus faecalis. Аналогичными данными располагают М. Ф. Трапезникова и соавторы (2004), суммировавшие результаты идентификации 662 штаммов микроорганизмов у 264 больных ХБП, за которыми велось наблюдение в течение последних 13 лет. При этом выявлена ведущая роль грамположительных кокков в этиологии ХБП: за последние 3 года частота распространения коагулазо-негативных стафилококков составила 87,5% [3]. В то же время удельный вес грамотрицательных палочек — «общепризнанных» возбудителей ХБП — за предыдущие 7 лет неуклонно снижался (с 13,3 до 4,2%). С. Н. Калинина, В. П. Александров, О. Л. Тиктинский (2003) при обследовании 174 больных ХБП также выявили преобладание (82%) грамположительной флоры. Инфекция простаты может быть следствием бактериальной колонизации мочеиспускательного канала. Нормальная флора мочеиспускательного канала у мужчин состоит главным образом из дифтероидов и грамположительных кокков. Сексуальная активность может способствовать колонизации мочеиспускательного канала потенциальными уропатогенами. Blacklock (1974) и Stamey (1980) отметили, что секрет простаты у некоторых мужчин с ХБП содержал те же уропатогены, которые присутствовали в вагинальной флоре их сексуальных партнерш. Бактериальная колонизация может также вызвать персистенцию бактерий в простате. Отличительной чертой этого состояния является персистенция бактерий внутри простаты, несмотря на лечение антибиотиками, что связано с хроническим воспалением и склонностью к обострению инфекции мочевыводящего тракта тем же самым патогеном.
К предрасполагающим факторам развития ХБП относятся: уретропростатический рефлюкс; фимоз; анально-генитальные сношения без предохранения; инфекции мочевых путей; острый эпидидимит; постоянные уретральные катетеры и проведение трансуретральных операций у мужчин с инфицированной мочой без предшествующей антимикробной терапии [1]. У пациентов с ХП может быть выявлено нарушение секреторной функции простаты, характеризующееся изменением состава секрета, т. е. снижением уровней фруктозы, лимонной кислоты, кислой фосфатазы, катионов цинка, магния и кальция; цинксодержащего антибактериального фактора простаты. При этом увеличиваются такие показатели, как рН, отношения изоферментов лактатдегидрогеназы-5 к лактатдегидрогеназе-1, белков воспаления — церулоплазмина и компонента комплемента С3. Эти изменения в секреторной функции простаты также обусловливают неблагоприятное воздействие на антибактериальную природу секрета простаты. Уменьшение действия антибактериального фактора простаты способно снижать врожденную противобактериальную активность секрета, тогда как щелочной показатель рН может препятствовать диффузии в ткань и в секрет простаты основных антимикробных препаратов.
Симптомами ХП являются боли в тазовой области, расстройства мочеиспускания и эякуляции (см. табл. 1).
| Таблица 1 Симптомы хронического простатита | ||
| Локализация боли в тазовой области | Расстройство мочеиспускания | Расстройство эякуляции |
| В промежности В половом члене В яичках В паховой области Над лоном В прямой кишке В крестце | Учащенное мочеиспускание Неполное опорожнение мочевого пузыря Слабая или прерывистая струя мочи Боль или ее усиление во время мочеиспускания | Боли во время или после эякуляции Гемоспермия |
Ведущее место в лабораторной диагностике ХБП принадлежит микробиологическому исследованию — четырехстаканному локализационному тесту, предложенному в 1968 г. Meares и Stamey [8]. Он состоит в получении, после тщательного туалета наружных половых органов (во избежание контаминации поверхностными бактериями), первой (10 мл) и второй (средней) порций мочи для бактериологического исследования, массажа предстательной железы (ПЖ) со взятием секрета для микроскопии и посева, а также третьей порции мочи (после взятия секрета) для посева (рис. 1). Количественные посевы первой и второй порций мочи выявляют бактерии в уретре и мочевом пузыре, в то время как при посевах секрета простаты и порции мочи после взятия секрета (третьей порции мочи) выявляют флору простаты. ХБП характеризуется воспалительной реакцией в секрете (при микроскопии определяется более 10 лейкоцитов в поле зрения при большом увеличении). После инкубации посевов подсчитывают количество колониеобразующих единиц (КОЕ).
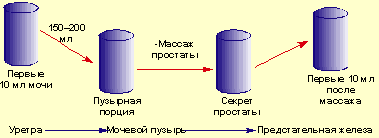 |
| Рисунок 1. Четырехстаканный локализационный тест Meares–Stamey |
Бактериологическое подтверждение ХБП мы проводим на основании, по крайней мере, одного из следующих критериев, предложенных K. G. Naber (2003):
Характерное для ХБП содержание патогенов в образцах примерно следующее:
первая порция мочи 3 КОЕ/мл;
вторая порция мочи 3 КОЕ/мл;
секрет простаты ≥ 10 4 КОЕ/мл;
третья порция мочи ≥ 10 3 КОЕ/мл.
Четкое соблюдение правил микробиологической диагностики и вышеуказанных критериев интерпретации результатов локализационного теста Meares — Stamey на большом количестве наблюдений позволят более точно определить частоту встречаемости истинных патогенов ХБП.
Антимикробная терапия. После идентификации этиологического агента и определения антибиотикорезистентности возникает необходимость назначения больному с ХБП антимикробной терапии. К факторам, оказывающим влияние на выбор антимикробного препарата для лечения ХБП, относятся: чувствительность идентифицированного микроорганизма к антибиотику, его способность в достаточной концентрации проникать через гематопростатический барьер и накапливаться в ткани и секрете простаты, сперме, а также способность препарата преодолевать экстрацеллюлярную полисахаридную оболочку, формируемую микроколониями бактерий, и хорошая переносимость при длительном пероральном приеме. Идеальный антибактериальный препарат для лечения ХБП должен быть жирорастворимым, слабощелочным, с коэффициентом диссоциации, способствующим максимальной концентрации препарата в простате [2]. Антимикробные средства из группы фторхинолонов на сегодняшний день отвечают вышеперечисленным требованиям и являются препаратами выбора для лечения ХБП. Особенностью антибактериального действия фторхинолонов является наличие двух мишеней действия в бактериальной клетке, каковыми являются ферменты (топоизомеразы II типа), ответственные за изменения пространственной конфигурации бактериальной ДНК: ДНК-гираза и топоизомераза IV. ДНК-гираза осуществляет суперспирализацию бактериальной ДНК, а топоизомераза IV — разделение дочерних хромосом в процессе репликации. Ключевым моментом в действии фторхинолонов является образование трехкомпонентного комплекса (бактериальная ДНК–фермент–фторхинолон). Указанный комплекс предотвращает репликацию бактериальной ДНК. Благодаря тому, что топоизомеразы обладают расщепляющей активностью, происходит разрушение молекулы ДНК (С. В. Сидоренко, 2002).
 |
| Рисунок 2. Классификация фторхинолонов (по K.G. Naber,1998) |
В настоящее время в практическое здравоохранение внедрены новые антимикробные препараты из группы фторхинолонов III и IV поколений, которые проявляют активность в отношении как грамотрицательных и грамположительных бактерий, так и атипичных внутриклеточных микроорганизмов, а также обладают способностью воздействовать на бактерии в биологических пленках (см. рис. 2). Антимикробная активность in vitro фторхинолонов III поколения — спарфлоксацина и левофлоксацина, а также фторхинолона IV поколения — моксифлоксацина наглядно представлена в таблице 2.
| Таблица 2 Антимикробная активность in vitro спарфлоксацина, левофлоксацина и моксифлоксацина (МПК90, мкг/мл) [4] | |||
| Микроорганизмы | Спарфлоксацин | Левофлоксацин | Моксифлоксацин |
| Acinetobacter spp. | 0,25 | 16 | 0,5 |
| Citrobacter freundii | 0,25 | 0,5 | 0,5 |
| Enterobacter cloacae | 0,5 | 0,5 | 0,5 |
| Escherichia coli | 0,12 | 0,12 | 0,5 |
| Klebsiella pneumoniae | 0,25 | 0,25 | 0,5 |
| Proteus mirabilis | 0,5 | 0,25 | 0,12 |
| Pseudomonas aeruginosa | 8 | 4 | 16 |
| Staphylococcus epidermidis | 1 | 1 | 2 |
| Staphylococcus saprophyticus | 0,25 | — | 0,5 |
| Enterococcus faecalis | 2 | 16 | 4 |
В 2004 г. мы сравнили чувствительность 25 различных штаммов коагулазо-негативных стафилококков — наиболее распространенных, по нашим данным (Е. Б. Мазо и соавт., 2003, 2004), этиологических агентов ХБП — к левофлоксацину, спарфлоксацину и моксифлоксацину. Бактериологическое исследование проводили классическим методом: выполняли посев мочи и секрета простаты на питательные среды с выделением чистой культуры и идентификацией выделенных штаммов при помощи полуавтоматического микробиологического анализатора Sceptor (Becton Dickinson, USA). Чувствительность выделенных микроорганизмов к левофлоксацину, спарфлоксацину и моксифлоксацину определяли дискодиффузионным методом на среде Мюллера–Хинтона. Результаты оценивали по значениям диаметров зон задержки роста. Всего было изучено 25 штаммов коагулазо-негативных стафилококков (21 — Staphylococcus haemolyticus, 3 — Staphylococcus epidermidis, 1 — Staphylococcus warnerii), выделенных в диагностическом титре из секрета простаты и мочи у больных ХБП при четырехстаканном тесте Meares–Stamey. Проведенный нами анализ чувствительности коагулазо-негативных стафилококков к фторхинолонам III и IV поколений показал наиболее высокую чувствительность этих бактерий к моксифлоксацину — у 24 (96%) штаммов. К левофлоксацину оказались чувствительны 21 (84%), а к спарфлоксацину 20 (80%) штаммов коагулазо-негативных стафилококков. Пять резистентных к спарфлоксацину штаммов были выделены нами у больных после длительной антимикробной терапии этим препаратом. Был выделен также штамм гемолитического стафилококка, резистентный ко всем фторхинолонам III и IV поколений у больного, ранее принимавшего в течение 6 нед моксифлоксацин. Проведенное исследование продемонстрировало высокую чувствительность коагулазо-негативных стафилококков, выделенных от больных ХБП, к фторхинолонам III и IV поколений. Чувствительность исследованных бактерий к моксифлоксацину оказалась наиболее высокой, в то время как к левофлоксацину и спарфлоксацину была практически одинаково ниже. Таким образом, длительная антимикробная терапия моксифлоксацином может привести к селекции устойчивых штаммов и развитию перекрестной резистентности к фторхинолонам III и IV поколений.
На сегодняшний день проведено ограниченное количество клинических исследований применения фторхинолонов в лечении ХБП. Результаты таких исследований, с периодом наблюдения не менее 6 мес, представлены в таблице 3.
Как видно из данных, приведенных в таблице 3, несмотря на существенные различия в количестве больных, принимавших участие в исследованиях, бактериальная эрадикация при различной длительности терапии фторхинолонами, наблюдалась более чем у 60% пациентов. Проведение подобных исследований в будущем, с соблюдением стандартов микробиологической диагностики, позволит выработать единый подход к рациональной антимикробной терапии ХБП.
Согласно актуальным на сегодняшний день рекомендациям Европейской ассоциации урологов по лечению инфекций мочевыводящих путей и инфекций репродуктивной системы у мужчин, принятым в 2001 г., длительность антимикробной терапии ХБП фторхинолонами или триметопримом должна составлять 2 нед (после установления предварительного диагноза). После повторного обследования больного антимикробную терапию рекомендуют продолжать суммарно в течение 4–6 нед только при положительном результате микробиологического исследования секрета простаты, взятого до начала лечения, или в случае, если у больного улучшилось состояние после приема антимикробных препаратов [2].
Антимикробные препараты, используемые для лечения ХБП, а также способы их применения приведены в таблице 4.
| Таблица 4 Способы применения антимикробных препаратов для лечения хронического бактериального простатита | ||
| Группа препаратов | Препараты | Способ применения |
| Фторхинолоны | Ципрофлоксацин (сифлокс, ципролет, цифран) | По 500 мг 2 раза в сутки |
| Офлоксацин (джеофлокс, заноцин, офлоксин 200) | По 400 мг 2 раза в сутки | |
| Ломефлоксацин (ксенаквин, ломфлокс, максаквин) | По 400 мг 1 раз в сутки | |
| Левофлоксацин (таваник) | По 500 мг 1 раз в сутки | |
| Спарфлоксацин (спарфло) | Первый прием 400 мг, затем по 200 мг 1 раз в сутки | |
| Моксифлоксацин (авелокс) | По 400 мг 1 раз в сутки | |
| Триметоприм/ сульфаметоксазол | Ко-тримоксазол (бикотрим, бисептол) | По 960 мг 2 раза в сутки |
Следует отметить, что больные с ХБП должны принимать антибиотик фторхинолонового ряда в течение длительного периода (от 4 до 6 нед) для предотвращения рецидива инфекции нижних мочевых путей. Продолжительная терапия антибиотиками в низких профилактических дозах или супрессивная антимикробная терапия могут применяться в случаях рецидивирующего или невосприимчивого к лечению простатита.
Литература
С. В. Попов
А. К. Чепуров, доктор медицинских наук, профессор
В. И. Карабак, кандидат медицинских наук
РГМУ, Москва
Цитробактер браакии что это
а) Терминология:
1. Синонимы:
• Цитробактерный церебрит
2. Определение:
• Инфекция, вызванная грамотрицательной кишечной бактерией
1. Общие характеристики цитробактерного менингита:
• Лучший диагностический критерий:
о Множественные крупные кистозные поражения белого вещества (БВ)
о Абсцессы «полигональной» формы, полностью замещающие БВ; границы параллельны коре:
— При нарастании масс-эффекта/отека более вероятно инфицированное содержимое абсцесса
— «Округление» краев позволяет предположить увеличение давления/активную инфекцию
• Локализация:
о Склонность к долевому поражению белого вещества больших полушарий
• Размеры:
о Множественные крупные кисты в БВ
• Морфология:
о Абсцессы полигональной формы
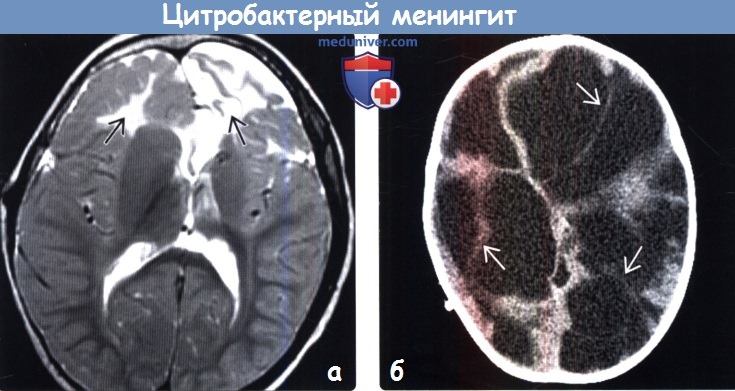
(б) Бесконтрастная КТ, аксиальный срез: у младенца с цитробактерным сепсисом и менингитом определяется прогрессирование последнего. Многоочаговое абсцедирование головного мозга привело к макрокистозной энцефаломаля-ции и формированию множественных полостей, разделенных перегородками.
3. МРТ признаки цитробактерного менингита:
• Т1-ВИ:
о Ранняя фаза (церебрит):
— Фрагментарные мультилобарные гилоинтенсивные зоны
о Поздняя фаза (абсцесс):
— Множественные крупные кисты
— Квадратной формы
— Перегородки
— Уменьшение степени выраженности изменений МР-сигнала на Т1-ВИ
• Т2-ВИ:
о Ранняя фаза (церебрит):
— Фрагментарные мультилобарные зоны гиперинтенсивного сигнала
о Поздняя фаза (абсцесс):
— Множественные полости, часто разделенные перегородками
— Обычно двусторонние абсцессы
— Протяженные гиперинтенсивные зоны в БВ
— Вариабельный отек, масс-эффект
— В конечном итоге полости могут спадаться, вызывая выраженную потерю объема БВ
• FLAIR:
о Повышение интенсивности сигнала от БВ в пределах доли
• Т2* GRE:
о Гилоинтенсивные точечные кальцификаты в перегородках
• Постконтрастные Т1-ВИ:
о Ранняя фаза (церебрит):
— Слабоинтенсивное фрагментарное контрастирование БВ
о Поздняя фаза (абсцесс):
— Фрагментарное контрастирование БВ
— Контрастирование перегородок и стенок абсцесса
— Точечный очаг контрастирования перегородки
• МР-спектроскопия:
о Продукты метаболизма:
— Лактат (1,3 ppm), ацетат (1.9 ppm) и сукцинат (2,4 ppm)
о Конечные продукты протеолиза, высвобождаемые нейтрофилами:
— Валин и лейцин (0,9 ppm)
4. УЗИ признаки цитробактерного менингита:
• В-режим:
о Ранняя фаза (менингит/церебрит):
— Расширение и гиперэхогенность борозд
— Гиперэхогенные зоны в БВ
— Потеря нормальной эхоструктуры БВ
о Поздняя фаза (абсцесс):
— Множественные анэхогенные или гипоэхогенные полости в БВ, разделенные перегородками
• Цветовое допплеровское картирование:
о Слабо выраженный кровоток в пределах перегородок и стенок абсцесса
5. Рекомендации по визуализации:
• Лучший метод визуализации:
о МРТ с контрастированием является лучшим методом оценки локализации и тяжести поражения
• Советы по протоколу исследования:
о МРТ с контрастированием позволяет:
— Обнаружить раннее контрастирование паренхимы при церебрите
— Визуализировать точечные очаги контрастирования перегородок и стенок абсцессов «квадратной» формы
— Обнаружить осложнения инфекционного поражения головного мозга (сосудистого характера, внемозговые скопления гноя)
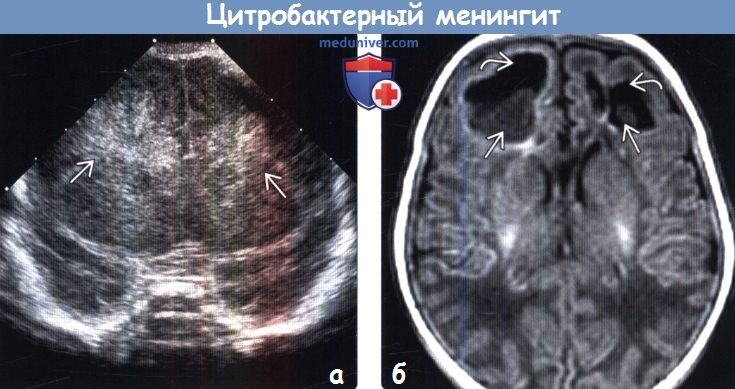
(б) МРТ, Т1-ВИ, аксиальный срез: у новорожденного с перинатальным цитробактерным сепсисом в белом веществе лобных долей определяются абсцессы в виде полостей «квадратной» формы. Эти полостные поражения являются результатом прогрессирования воспалительного процесса в зонах церебрита. Обратите внимание на некротический детрит внутри вышеописанных полостей.
в) Дифференциальная диагностика цитробактерного менингита:
1. Другие бактериальные инфекционные поражения головного мозга:
• Обычно характеризуются большей степенью выраженности перифокального отека и масс-эффекта
• Выполните поиск возможных источников инфекции в придаточных пазухах носа, сосцевидных отростках височных костей или бактериальной эмболии/гематогенное инфицирование
2. Перивентрикулярная лейкомаляция:
• Расположение кист в перивентрикулярном БВ (перитригонально и вокруг передних рогов боковых желудочков)
• Более медленная кистозная трансформация
• Отсутствие ободкового характера контрастного усиления или «точечного» контрастирования перегородок
3. Кистозная энцефаломаляция:
• Поражение коры и глубокого серого вещества
• Кальцификация таламуса и базальных ганглиев
• Замещение кистами БВ
• Пассивное расширение желудочков
4. Разрывы волокон белого вещества при неслучайной черепно-мозговой травме (НЧМТ):
• Поражение БВ лобных долей
• В полостях разрывов может обнаруживаться уровень жидкости
• Ассоциированные внутричерепные проявления НЧМТ:
о Межполушарная/конвекситальная субдуральная гематома, субарахноидальное кровоизлияние
1. Общие характеристики цитробактерного менингита:
• Этиология:
о Нейровирулентные факторы рода Citrobacter:
— Наличие уникального белка наружной мембраны 32-kD
— Устойчивость к фагоцитозу
о Citrobacter попадают в эндотелиальные клетки капилляров путем инвазии/трансцитоза:
— Приводит к геморрагическому некрозу и абсцедированию
о Внутриклеточная репликация Citrobacter происходит в эндотелиальных клетках капилляров:
— Это способствует персистенции инфекции в головном мозге и формированию полостей
• Ассоциированные аномалии:
о Инфицирование: горизонтальное (внутрибольничное) или вертикальное (внутриутробное)
о Колонизация (кожа, культя пуповины) → бактериемия → менингит
о Citrobacter являются факультативными анаэробами:
— Гидролизуют мочевину и ферментируют глюкозу → продукция газа
2. Макроскопические и хирургические особенности:
• Непрозрачность лептоменинкс, гнойный экссудат
• Диффузный эпендимит
3. Микроскопия:
• Отсутствие хорошо сформированной фиброзной капсулы
• Микроорганизмы в стенках гиперемированных сосудов
• Нейтрофилы и некротический клеточный детрит
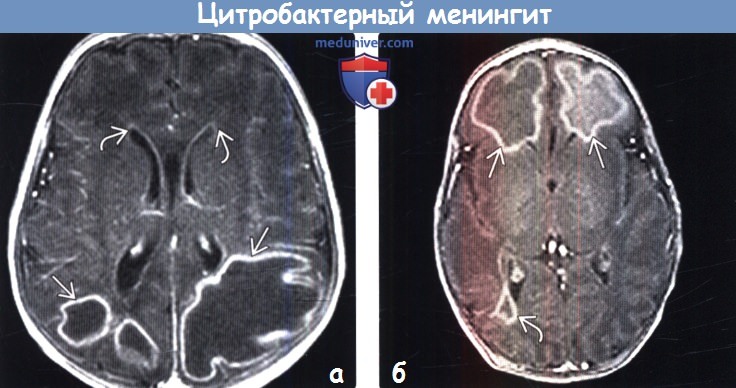
(б) У этого же новорожденного в обеих лобных долях, а также в перитригональной области правого полушария головного мозга определяются абсцессы, характеризующиеся ободковым характером контрастирования. Необходима пролонгированная в/в инфузионная терапия.
д) Клиническая картина:
1. Проявления цитробактерного менингита:
• Наиболее частые признаки/симптомы:
о Новорожденные или недоношенные с сепсисом: выбухание родничка, апноэ, судороги
• Клинический профиль:
о Новорожденный с очень высокой степенью недоношенности:
— Сепсис, возбудимость, плохой аппетит, выбухание родничка
о Повышенный риск заболевания у иммунокомпрометированных пациентов:
— Новорожденные и больные недоношенные относятся к иммунокомпрометированным лицам
2. Демография:
• Возраст:
о Предрасположенность у очень молодых и у очень старых пациентов:
— У новорожденных → сепсис, менингит и абсцессы головного мозга
— У пожилых людей → инфекции мочевыделительной системы, верхних дыхательных путей
о Средний возраст начала сепсиса: 5 дней
о Недоношенные новорожденные наиболее подвержены инфекции
о Цитробактерная инфекция ЦНС у младенцев младше одного месяца встречается редко
• Эпидемиология:
о Цитробактерная инфекция:
— Составляет 5% среди менингитов новорожденных (грамо-трицательных) → 80% абсцессов головного мозга у новорожденных
— Абсцессы могут сформироваться только ближе к завершению курса терапии
о Цитробактерная инфекция ЦНС:
— В большинстве случаев считается спорадической «встречаются вспышки инфекции в ОРИТ новорожденных
3. Течение и прогноз:
• 30% новорожденных и грудных детей с цитробактерной инфекцией ЦНС умирают
• У 80% новорожденных с цитробактерным менингитом развиваются абсцессы головного мозга
• У 50% выживших после цитробактерного менингита/абсцесса имеется значительное повреждение ЦНС
4. Лечение:
• Базисная терапия антибиотиками
• Встречается позднее формирование абсцессов, в этом случае необходима пролонгированная в/в инфузионная терапия
• Дополнительным лечебным мероприятием является хирургическое дренирование абсцессов:
о При увеличении кист на фоне оптимизированной в/в инфузионной терапии
о При плохой реакции на начальную антибиотикотерапию
е) Диагностическая памятка. Советы по интерпретации изображений:
• Минимальная выраженность отека, окружающего абсцессы
• Абсцессы квадратной формы с очаговым контрастированием перегородок
• Не все полости с ободковым характером накопления контрастного вещества являются абсцессами:
о Некоторые из них являются зонами некроза БВ и лейкомаляции
• Инфекционные поражения, вызванное бактериями рода Citrobacter и бактерией Cronobacter sakazakii имеют схожую визуализационную картину
ж) Список литературы:
Редактор: Искандер Милевски. Дата публикации: 10.4.2019
