лучевая или протонная терапия что лучше
Лучевая или протонная терапия что лучше

Заведующая радиологическим отделением
ГУЗ «Областной клинический онкологический диспансер»,
доцент кафедры онкологии и лучевой диагностики
медицинского факультета ИМЭиФК УлГУ,
кандидат медицинских наук,
Ульяновск
Несмотря на то, что ноябрь 2019 года с его важнейшим событием для онкологической общественности нашей страны – XXIII Российским онкологическим конгрессом – остался позади и мы с новыми надеждами смотрим в наступивший 2020, хочется оглянуться для того, чтобы более пристальное внимание уделить одной из тем состоявшейся на конгрессе дискуссионной сессии – протонной терапии. Подобный вопрос: станет ли вскоре вся лучевая терапия протонной? – нередко всплывал на сессиях различных международных конгрессов десять-пятнадцать лет назад, когда мир анализировал первый долговременный опыт применения протонного излучения для лечения больных со злокачественными опухолями различных локализаций. Тогда же в большом количестве начали появляться и доклады, и публикации по результатам проспективных клинических исследований по применению продвинутых технологий фотонного облучения – IMRT, IGRT, VMAT, RapidArc, SBRT и т.д., несколько заслонив собой всегда существовавший интерес к протонной терапии. Все в нашей жизни развивается в соответствии с законами диалектики, и на новом витке нашей реальности мы видим возрождение интереса к данному виду лучевой терапии: тема протонов не раз затрагивается для рассмотрения в различных аспектах, и отнюдь не только на радиотерапевтических конгрессах. К слову, программа грядущего конгресса ESTRO 2020 в Вене содержит несколько сессий, связанных с протонной лучевой терапией. В России в настоящее время функционирует два протонных центра – в Санкт-Петербурге и Димитровграде (Ульяновская область), оба открыты относительно недавно, но в ближайшие годы планируется строительство и запуск еще нескольких центров. Но если радиационные онкологи имеют более-менее четкие представления о протонах, то у представителей других специальностей они весьма размыты, и вопросов о спектре применения протонной терапии, о возможных преимуществах или недостатках этого метода всегда бывает немало. Интерес подогревается и вопросами пациентов, которые нередко спрашивают своих лечащих врачей: стоит ли искать пути попадания на протонную лучевую терапию, зная, что это лечение в большинстве случаев влетит в немалую копеечку? Чем оно предпочтительнее, нежели облучение в родном городе на аппаратах, через которые проходят тысячи других пациентов ежегодно? И главное – является ли этот метод гарантией успеха, некоей радиотерапевтической панацеей? Вряд ли большинство из нас имеет точные ответы на все эти и многие другие вопросы, поэтому в качестве основных лекторов дискуссионной сессии были приглашены специалисты, знающие о протонной терапии не понаслышке: Николай Андреевич Воробьёв, заведующий отделением протонной терапии Медицинского института им. Березина Сергея, Санкт-Петербург, и Тимур Митин из Орегонского университета здоровья и науки, США. В качестве экспертов, призванных участвовать в обсуждении, присутствовали профессор Е.В. Хмелевский, главный радиотерапевт РФ, МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России, Москва, А.В. Филимонов, генеральный директор Онкорадиологического центра ООО «ПЭТ Технолоджи Подольск», Е.А. Маслюкова, заведующая протонным центром ФГБУ ФВЦМР ФМБА России, Димитровград, а также наши коллеги из крупных американских центров, имеющих наибольший опыт работы с протонным излучением, – профессор Alphonse Taghian, Massachusetts General Hospital, и д-р Marsha Reyngold, Memorial Sloan Kettering Cancer Center. Увы, времени на вопросы и обсуждение темы после докладов не осталось, поскольку две предыдущие группы дискутантов далеко вышли за пределы своих временных рамок. Но нам не хотелось бы оставлять столь интригующую тему без логического завершения, поэтому мы разослали экспертам несколько вопросов уже после конгресса. Их ответы, а также содержание лекций «ЗА» и «ПРОТИВ» и стали основой этой публикации.
Николай Воробьев: Станет ли вся лучевая терапия протонной? Аргумент «ЗА»

Противоопухолевый эффект лучевой терапии в большей степени определяется дозой ионизирующего излучения. В то же время безопасность лечения напрямую зависит от того, насколько удалось снизить лучевую нагрузку на здоровые ткани. Несмотря на технический прогресс, в некоторых случаях методика фотонной терапии не позволяет подвести необходимую туморицидную дозу таким образом, чтобы избежать тяжелых лучевых повреждений.
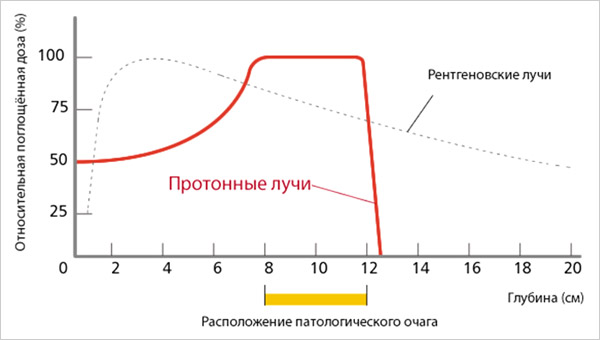
В отличие от других видов излучений, глубинное распределение дозы для протонов имеет зону медленного подъема с увеличением глубины проникновения, называемую «плато», за которым следует дозовый максимум – «пик Брэгга» (рис.1). Амплитуда этого пика в три-четыре раза превышает дозу на поверхности среды. За пиком Брэгга доза очень быстро падает практически до нуля. Протонная терапия является в настоящее время наиболее мощным средством для получения высокой конформности дозных распределений, позволяя значительно уменьшить лучевую нагрузку на нормальные ткани по сравнению с традиционными методами лучевой терапии пучками фотонов и электронов, даже если мишень вплотную прилежит к критическим структурам организма, и безопасно увеличивая ее на опухоли. Более высокая доза приводит, соответственно, к повышению вероятности гибели раковых клеток [1].
Рисунок 1. Распределение дозы излучения в зависимости от глубины проникновения.
Впервые предположение о возможности применения протонов в клинической практике высказал Роберт Ратбун Уилсон – американский физик, работавший в области ядерной физики и ускорителей частиц. В 1946 году Уилсон на страницах журнала «Radiology» высказал предположение о том, что протонный пучок может применяться в клинической практике. Однако, хотя это заявление было сделано в 1946 г., первый клинический Центр протонной терапии был открыт лишь спустя 40 лет – Loma Linda University Medical Center. В клинической практике протонная терапия применяется уже более 30 лет.
Технические системы для доставки дозы в протонной терапии постоянно совершенствуются. Несколько лет назад было представлено второе поколение систем для протонного облучения – система сканирования карандашным пучком (Pencil beam scanning). В результате процесс планирования облучения существенно упростился и сегодня занимает столько же времени, сколько и в случае фотонной терапии, также значительно снизилась стоимость оборудования. Быстрое техническое развитие и снижение стоимости систем для протонной терапии повысило доступность методики, что немедленно отразилось на динамике открытия новых центров протонной терапии.
Основные потенциальные клинические преимущества протонной терапии связаны со значительным снижением лучевой нагрузки на здоровые ткани. Это позволяет снизить частоту и выраженность лучевых реакций, снизить риск инвалидизации после лечения и риск развития радиоиндуцированных опухолей. За счет снижения токсичности появляется возможность более широко применять комбинированное химиолучевое лечение, уменьшить токсичность при проведении повторных курсов лучевой терапии в случае рецидива. В некоторых клинических ситуациях, за счет высокой конформности, протонная терапия позволяет повысить эффективность лечения путем увеличения дозы облучения. Это имеет важное значение в случае так называемых «радиорезистентных» опухолей.
Опухоли центральной нервной системы
Особенности расположения опухолей ЦНС существенно ограничивают возможности фотонной лучевой терапии. Доза, необходимая для достижения стойкого контроля над опухолью, зачастую превышает значения, допустимые для органов риска. В подобной ситуации радиотерапевту приходится принимать сложные клинические решения, делая выбор между подведением высокой дозы, способной обеспечить противоопухолевый эффект, и риском повреждения жизненно важных структур. Даже в том случае, если удастся избежать летальных лучевых повреждений, существует высокий риск развития тяжелых нейрокогнитивных расстройств, которые могут быть временными у взрослых, но у детей часто носят необратимый характер. Исследования по сравнению протонной и фотонной лучевой терапии у пациентов с опухолями ЦНС показывают, что применение пучка протонов позволяет значительно снизить нагрузку на здоровые ткани [2], в частности, при проведении краниоспинального облучения. При использовании фотонов все структуры, находящиеся в проекции спинного мозга вплоть до передней грудной (пищевод, щитовидная железа, сердце) и передней брюшной стенки (кишечник, желудок), подвергаются облучению. При этом существенная лучевая нагрузка приходится на скелет и костный мозг (тела позвонков, ребра, грудина, кости таза). Применение протонной терапии позволяет избежать облучения перечисленных выше здоровых тканей, при этом снизив дозу практически до нуля, не доходя до переднего края тел позвонков. В 2013 году были опубликованы результаты исследования по оценке токсичности при проведении протонного и фотонного краниоспинального облучения у 40 взрослых пациентов, медиана наблюдения составила 57 месяцев. В группе протонного облучения было отмечено многократное снижение частоты таких осложнений, как потеря веса (16% при использовании протонов против 64% при фотонах, p=0,004), тошнота и рвота (26% против 71%), эзофагит (5% против 57%, p
Протонная терапия
Представьте себе медицинский аппарат весом в 196 тонн и размерами с пятиэтажное здание, который воздействует (убивает) раковую опухоль с точностью до долей миллиметра и не повреждает здоровые ткани. При этом побочные эффекты минимальны. Это и будет самым простым описанием протонной терапии.
Показания к назначению
Протонно-лучевая терапия (ПЛТ) показана при диагностировании любых типов злокачественных опухолей, чувствительных к лучевому лечению.
Данный метод может быть выбран в качестве альтернативы облучению на радиотерапевтических рентгеновских установках или линейных акселераторах, а также использоваться для разрушения новообразований, которые невозможно облучать на аппаратах другого типа из-за высокого риска развития побочных эффектов.
В том числе, ПЛТ успешно применяется:
При каких опухолях проводится:
Почему протонная терапия лучше при некоторых опухолях?
Современная лучевая терапия пережила революционные изменения в последние десятилетия и стала эффективной для лечения многих видов рака. В настоящий момент более 60% пациентов со злокачественными опухолями необходимо проведение лучевого лечения. Появилось много хирургически точных видов лучевой терапии, таких как гамма-нож, кибер-нож и различные варианты конформной лучевой терапии. Однако при использовании этих и более традиционных методов есть один недостаток. Излучение состоит из пучка фотонов и электронов, которые повреждают не только опухоль, но и здоровые ткани, расположенные впереди и за опухолью по ходу пучка излучения. Результат? Повреждение здоровых тканей и побочные эффекты. Чтобы снизить их влияние, и избежать непоправимого повреждения здоровых тканей, приходится ограничивать мощность излучения, приложенного к опухоли.
Чем же выгоден метод протонно-лучевой терапии?
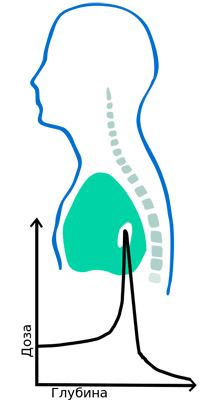
При протонной терапии используется пучок протонов. Особенность протонного излучения в том, что основная энергия лучей высвобождается в определенной точке — участке тканей организма, эта точка называется Bragg peak (кривая Брэгга). Врач радиолог проводит расчет так, чтобы энергия высвобождалась именно в опухоли, повторяя ее очертания, с точностью до единиц миллиметра. Таким образом, разрушается только опухоль, а окружающие ее здоровые ткани практически не подвергаются воздействию.
Где можно пройти протонную терапию сейчас?
В настоящий момент в России открыто несколько центров протонной терапии и ведется ряд проектов по созданию новых. На текущий момент введены в действие только центры:
Также в ближайшие годы будет запущены центры во Владивостоке, Москве, Новосибирске и Дубне. Подробная информация о центрах протонной терапии в России.
В мире же сейчас действует более 50 центров протонной терапии. Ближайшие к России страны, где могут пройти лечение российские граждане: Чехия, Германия, Южная Корея, Греция.
| Страна | Цена | Примечание | Заявка |
|---|---|---|---|
| Германия | 45–75 000 евро | Центры в Мюнхене, Гейдельберге, Берлине. Цена зависит от центра | Послать заявку |
| Чехия | От 35 000 евро | Прага | Послать заявку |
| Южная Корея | От 50 000 долларов | Сеул | Послать заявку |
| Япония | 36 000 евро | Центр работает с 2008 года | |
| Индия | Уточняется | Центр работает с 2015 года |
Особенности метода
Поток ядер атомов водорода (протонов) обладает следующими физическими свойствами:
Расстояние от излучателя до Брегговского пика зависит от плотности тканей, через которые проходит поток, а также от его энергии. При подготовке к сеансу протонно-лучевой терапии специалисты учитывают эти нюансы. Планирование осуществляется с помощью трехмерного моделирования на основе оцифрованных данных, полученных при диагностическом сканировании различными способами.
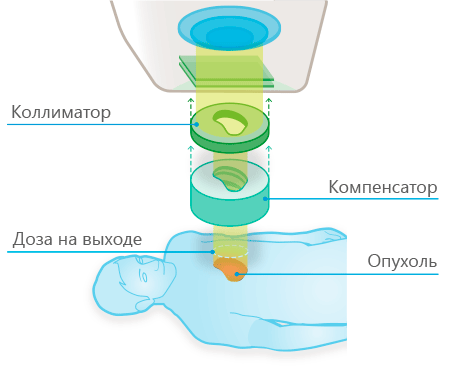
Для дополнительного снижения лучевой нагрузки на здоровые клетки в современных терапевтических установках излучатели монтируются на полой подвижной консоли особого типа (гантри). Использование специального матрацного контура дает возможность единовременного облучения сразу нескольких опухолей с разных направлений.
Как проводится сеанс ПЛТ
Пациента укладывают внутрь полой консоли на специальную матрицу, смоделированную с учетом его индивидуальных анатомических особенностей. Это позволяет обеспечить максимальную неподвижность во время лечения и, при необходимости, предоставляет возможность вести облучение сразу нескольких очагов.
У больных с опухолями головного мозга голова может дополнительно фиксироваться с помощью индивидуальной маски.
После иммобилизации проводится диагностическое КТ- или МРТ-исследование, в процессе которых получают данные о топографии и плотности тканей облучаемой области.
Вслед за этим с помощью специальных компьютерных программ осуществляется планирование с формированием объемной модели очага и воздействующего на него излучения.
Далее проводится сеанс облучения. Длительность процедуры составляет порядка 20-ти минут. В это время консоль медленно вращается вокруг находящегося внутри нее человека, и посылает протоны точно в заданной программой области. После окончания процедуры пациент, как правило, может покинуть центр в тот же день. Нахождения в стационаре не требуется.
Противопоказания и ограничения
В связи с вышеперечисленными особенностями, при облучении протонами круг противопоказаний значительно уже, чем при лечении устаревшими радиотерапевтическими методами.
В то же время, данным способом можно лечить больных с сахарным диабетом, патологиями сердца и сосудов, а также пациентов престарелого возраста, которые обычно плохо переносят традиционную радиотерапию.
Эффективность, переносимость, возможные осложнения
Если облучаемая опухоль не метастазирует, терапевтический эффект ПЛТ максимален и ее результатом может стать полное излечение от рака.
Согласно отзывам пациентов, протонная терапия при онкологии легко переносится: как правило, человек не испытывает никаких неприятных ощущений ни во время сеанса, ни после него. Это дает возможность врачам лечить абсолютное большинство больных амбулаторно.
Вероятность возникновения осложнений, а также их интенсивность и характер зависят от размера и местоположения опухолевого очага. Перед началом лечения пациента информируют о любых возможных рисках.
Протонная терапия в лечении рака: история внедрения метода в мировую онкопрактику
Использовать ядра атомов водорода для ЛТ предложил американский ученый Р. Вильсон в 1946 году.
Первый сеанс протонной терапии для лечения при онкологии был проведен в Швеции одиннадцать лет спустя с помощью ускорителя, плохо приспособленного для терапевтических целей.
Вслед за этим более 40 лет методика отстраивалась и совершенствовалась в Гарвардской циклотронной лаборатории, сотрудничающей с Центральной больницей Массачусетса. Результаты этой работы были использованы при строительстве специализированных центров протонно-лучевой терапии в Калифорнии и Массачусетсе.
В начале 21 века появились современные центры ПЛТ в университете штата Индиана, в онкологическом центре им. Андерсона (штат Техас, город Хьюстон), в университете г. Джексонвилл (штат Флорида), в Оклахоме, Пенсильвании, Иллинойсе.
В настоящее время такие клинические подразделения также имеются в Германии (Мюнхен, Берлин, Эссен, Гейдельберг), Чехии (Прага) и некоторых других европейских и азиатских государствах.
Всего в мире насчитывается порядка 50 действующих установок. При их конструировании, строительстве специализированных помещений и эксплуатации возникает ряд сложностей, устранение которых требует ощутимых финансовых вложений и времени. Следствием этого становится достаточно высокая стоимость лечения, однако результаты протонной терапии по отзывам пациентов и мнению специалистов оправдывают любые затраты.
Отзывы специалистов
Так, например, Стивен Дж. Франк, д.м.н., медицинский директор центра протонной терапии в Хьюстоне, основываясь на результатах собственных наблюдений утверждает, что ограничение действия радиации на нормальные ткани головы и шеи приводит к основательному улучшению качества жизни онкобольных с опухолями верхнечелюстных пазух, хордомами, хондросаркомами, окулярными и периокулярными злокачественными новообразованиями во время и после лечения.
Член-корреспондент РАН, профессор Владимир Егорович Балакин, разработавший отечественный бюджетный терапевтический коллайдер особой конструкции, уверен что «при хорошем медицинском обеспечении (методиках лечения различных видов новообразований) комплекс позволит добиться излечения 80–90 процентов пациентов на всех стадиях заболевания» (для сравнения: эффективность традиционных радиотерапевтических методик не превышает 50%).
Центр протонной терапии в Санкт-Петербурге
Адрес: улица Глухарская, дом 16, корпус 2, Санкт-Петербург, 19114
Консультации по телефону
Центр радиологических консультаций +7 (499) 455-05-53 Москва
Бесплатная консультация от наших ведущих радиотерапевтов
Чтобы понять, возможно ли провести для пациента лечение с помощью протонной терапии, отправьте нашим радиологом заявку с документами. Необходимо отправить выписки (выписной эпикриз) о проведенном лечении и если есть, результаты исследований: МРТ, КТ, ПЭТ КТ, гистология, онкомаркеры и т.п.. Чем полнее будет отправлена информация, тем скорее наши врачи смогут дать ответ об оптимальном методе: радиохиругии или другом методе облучения опухоли. Обычно мы даем ответ в течение 3-х рабочих дней. Если какой-то информации не хватит с вами свяжется наш администратор. Заявку можно отправить:
Консультации по телефону
Центр радиологических консультаций +7 (499) 455-05-53 Москва
Как загрузить файлы
Желательно предварительно упаковать все ваши файлы в один архив ZIP или RAR. Это ускорит загрузку.
Перетащите файлы мышкой из Проводника на Поле загрузки файлов в форме. Либо нажмите на Поле и выберите ваши файлы в появившемся диалоговом окне.
Дождитесь окончания загрузки. Это может занять длительное время, если объем файлов большой или у вас медленное подключение к интернету. Не нажимайте кнопку Отправить до окончания загрузки, иначе мы получим вашу заявку без файлов.
Вы поймете, что файлы загружены, когда на их значках появятся вот такие зеленые галочки:
После этого вы можете отправить заявку.
Передача данных осуществляется по зашифрованному соединению. Ваши документы смогут посмотреть только наши специалисты.
Рак простаты: лучше лечить или удалять ее?
Существует несколько возможностей лечения рака простаты с одинаково хорошими прогнозами. Поэтому решение каждого пациента сводится к вопросу: «На какие побочные эффекты я бы вероятнее всего согласился?» О разных методах лечения предстательной железы и их последствиях журналу Quora рассказывает доктор Гари Ларсон, медицинский директор Центра протонной терапии, Оклахома, США:

Прежде чем продолжить, нужно иметь в виду следующие вещи.
Не все, у кого есть рак простаты, нуждаются в лечении – для многих мужчин будет достаточно активного наблюдения, по крайней мере, в течение короткого периода, а вероятно и всей жизни.
Есть только два метода лечения рака простаты – хирургический и лучевая терапия. Такие вещи как криотерапия, фокусированный ультразвук высокой интенсивности, прогревание микроволновым излучением, лазерная абляция и некоторые другие методы могут быть рекомендованы для рака простаты, повторно появившегося после прохождения основного лечения. Но сами по себе они не могут являться основным лечением.
Андрогенное подавление (гормональная терапия) остановит развитие большинства случаев рака простаты, снизит показатель ПСА практически до нуля и сократит новообразования и метастазы в кости, но его эффект будет только временным – от нескольких месяцев до нескольких лет. Как и методы, указанные выше, это само по себе не радикальное лечение, хотя оно может сочетаться с лучевой терапией для повышения вероятности излечения. Андрогенное подавление имеет набор побочных эффектов, включая усталость, потерю мышечной массы, набор веса, потерю либидо, импотенцию, остеопороз и депрессию.
Урологи любят говорить пациентам: «Если вы пройдете хирургическую операцию, вы всегда сможете после нее получить облучение. Но если вы сначала пролечитесь лучевой терапией, то потом вы не сможете пройти хирургическую операцию». По большей части, это является правдивым утверждением, но данное обобщение упускает некоторые определенные факты.
Во-первых, после лучевой терапии редко возникает необходимость проводить хирургическое вмешательство, так как большинство мужчин, не излечившихся от этой болезни, не имеют рецидивов в простате. Наоборот, при рецидивах после лучевого лечения рака простаты в большинстве случаев обнаруживаются злокачественные опухоли в других органах. Как правило, такие пациенты имели скрытое онкозаболевание помимо простаты, которое нельзя было определить до начала лечения. Скоплениям раковых клеток необходимо разрастись до определенных размеров, чтобы они смогли вызвать повышение показателя ПСА и стали заметными.
Если у пациента после лучевой терапии постоянно отмечается повышенный уровень ПСА, а повторные биопсии железы положительные (между прочим, результаты биопсии являются надежными только спустя два года после лучевой терапии, так как раковые клетки отмирают в течение какого-то времени после лечения), то шансы на рецидив только в железе составляют 50%.
Спасительная в этом случае простатэктомия может быть выполнена после лучевой терапии, хотя это трудная операция из-за интенсивного фиброза вокруг железы и пониженного кровообращения – оба состояния являются результатом перенесенной лучевой терапии. Такие операции лучше всего проводить в крупном урологическом центре, где проводится большое количество подобных вмешательств, вместо того, что доверить эту операцию урологу небольшой клиники. Но даже при высоком мастерстве хирурга существует высокий риск возникновения недержания вследствие простатэктомии, проведенной после лучевой терапии.
Так как риск возникновения рецидива рака только в простате составляет 50 на 50, то и шансы на то, что хирургия приведет к излечению также 50 на 50.
Если первичной была хирургическая операция, то в 20-30% случаев после нее пациент должен пройти лучевую терапию для полного излечения. Послеоперационная лучевая терапия дает 90-процентный шанс ликвидации любого оставшегося рака. Кстати говоря, когда хирурги называют общий процент исцелившихся пациентов, они включают в это число и тех мужчин, которые были вылечены только благодаря послеоперационной лучевой терапии, хотя редко упоминают об этом факте в своих публикациях.
Рак простаты обычно растет медленно. Термин «ранняя стадия» имеет отношение к тому факту, что он все еще локализован в простате или, как минимум, в ближайшей перипростатической ткани. Ранняя стадия также может быть низкого, среднего или высокого риска по шкале Глиссона. Уровень риска определяется врачом после обследования материала биопсии по уровню ПСА и в некоторой степени по количеству положительных образцов биопсии.
Хирургическое лечение и последствия
Импотенция встречается чаще при хирургии по сравнению с лучевой терапией. Хотя хирургические издания часто сообщают о сохранении потенции на уровне выше 50%, они определяют потенцию как «способность получать эрекцию, достаточную для вагинального проникновения». Поэтому если вы можете заниматься сексом в течение 30 секунд, урологи считают вас способным к половому акту.
Я обследовал первых 150 мужчин, которым я проводил брахитерапию в середине 1990-х и просто задал им такой вопрос: «Вы довольны вашей сексуальной жизнью?» Я оставлял им место на опросном листе для подробного ответа. Более 60% ответили, что они довольны их сексуальной функцией. И ни один из тех, кто сказал, что могут только достичь проникновения, не был доволен.
В целом мужчины имеют гораздо лучшую сексуальную функцию и несравненно лучший контроль мочеиспускания (так число случаев недержания практически свелось к нулю – оно почти никогда не встречается при лучевой терапии), если они прошли лечение лучевой терапией, в отличие от хирургии.
Каковы минусы лучевой терапии?
Я коснусь этих моментов, так как они имеют отношение к каждому из различных способов, которыми проводится лучевая терапия.
Для пациентов с низким риском, локализованной болезнью (Глиссон 6 гистология с ПСА менее 10 и менее 4 позитивных образцов биопсии) брахитерапия может использоваться как монотерапия. Пациенты приходят для проведения процедуры разметки, при которой врачи определяют точный контур простаты каждые 5 мм сверху донизу, используя трансректальный ультразвук, а затем в компьютерной программе планирования лечения создают 3-D образ простаты. Рассчитывается оптимальная комбинация радиоактивных зерен, они заранее помещаются в иглы для введения их в железу. В день процедуры пациенту делается общая анестезия и используются от 20 до 40 игл для введения от 60 до 120 зерен в простату при помощи трансректального ультразвукового контроля.
Пациенты могут иметь некоторые неприятные ректальные симптомы в течение нескольких недель. Может появиться ректальная язва в течение года или двух после процедуры лечения, если некоторые зерна оказались близко к ректальной стенке. Такая язва всегда заживает со временем, если только гастроэнтеролог не решит провести ее биопсию, заподозрив рак. В этом случае она может никогда не зажить, и пациенту понадобится колостомия.
При заболевании от среднего до высокого риска, вероятно, придется выбрать внешнюю лучевую терапию как основной метод лечения, а не брахитерапию плюс сокращенный курс лучевой. Обычно курс лучевой терапии состоит курс из 44 процедур за девять недель.
Побочные эффекты внешней лучевой терапии как основного метода лечения рака простаты
Внешняя лучевая терапия может проводиться высокоэнергетическими рентгеновскими лучами, используя технику лучевой терапии с модулированной интенсивностью, или протонной терапией. Я сравню эти два метода. Кстати, Кибер-нож, томотерапия и другие разнообразные линейные ускорители проводят лечение лучевой терапией с модулированной интенсивностью при помощи рентгеновских лучей (фотонов). Между ними в конечном итоге разницы нет, отличаются только машины, которыми проводят лечение. Возможно, вы также слышали термин лучевая терапия с визуальным контролем, который просто означает, что проводится какое-то сканирование пациента на лечебном столе прямо перед проведением лечения. Это может быть КТ, портальное сканирование, стереоскопические рентгеновские лучи и др. Лучевая терапия с визуальным контролем используется со всеми формами лучевой терапии с модулированной интенсивностью, а также с протонной терапией.
Для обоих методов (протоны или фотоны) планирование лечения начинается с КТ сканирования тонкими слоями, которое интегрировано с высоко детализированной МРТ. КТ необходимо для того, чтобы сообщить компьютеру, планирующему лечение, толщину ткани во всех точках, через которые пройдет луч радиации. МРТ дает лучшую анатомическую картинку для определения контура простаты, семенных желез, мочевого пузыря, прямой кишки и т.д.
После нескольких дней, за которые создаются контуры органов, проводится множество опытов с конфигурацией луча, его модуляцией и т.д., вырабатывается оптимальный план лечения. После этого врач проводит проверку соответствия всем условиям для того, чтобы убедиться, что компьютерные расчеты дадут планируемое распределение дозы в ткани. И, наконец, пациент возвращается для первичного «визуального контроля» и первой из 44 процедур.
После нескольких недель лечения может появиться ректальное раздражение, которое выражается в симптомах от слабой диареи до боли, кровотечения и постоянного ощущения в необходимости опорожнить кишечник, хотя в стуле может быть ничего, кроме небольшого количества слизи.
Также после нескольких недель лечения могут появиться раздражающие урологические симптомы, такие как частота походов в туалет, неспособность терпеть позывы, медленное опорожнение мочевого пузыря и необходимость несколько раз вставать ночью. Они могут длиться несколько недель после прохождения лечения.
Риски, которые могут возникнуть в будущем, включают развитие рака, вызванного радиацией. Кроме долгосрочного риска появления вторичного рака, большинство побочных эффектов проходят за срок от нескольких месяцев до года после окончания лучевой терапии.
Протонная терапия
При протонной терапии побочные эффекты выглядят иначе. Усталость минимальная или отсутствует вообще. (Я лечил одного заядлого велосипедиста, который проехал на своем велосипеде более тысячи миль за девять недель, во течение которых проходил терапию).
Ректальные симптомы почти не встречаются, так как только очень маленький объем прямой кишки получает радиацию. Урологические раздражающие симптомы могут появиться на такой же срок, как и при лечении рентгеновскими лучами (фотонами), хотя обычно они менее серьезны.
Множественные эпидемиологические исследования показали, что существует только минимальное повышение риска возникновения рака после облучения протонами по сравнению с рентгеновскими лучами. Вероятно из-за меньшего объема ткани, получающего какую-то дозу радиации. Если у мужчин и появляются немногие побочные эффекты, они обычно проходят за несколько недель после окончания облучения протонами.
Каковы сравнительные данные по побочным эффектам протонной терапии против лучевой терапии с модулируемой интенсивностью?
Мы объединили наши данные с различными онкологическими центрами, обследовали приблизительно 1000 пациентов, которые прошли лечение рака простаты протонной терапией, и сравнили их показатели качества жизни с мужчинами из контрольной группы, которые не проходили лечение (потому что у не было рака простаты).
Все мужчины заполняли опросные листы касательно качества их жизни каждые три месяца с начала лечения до, как минимум, одного года после лечения. Результаты показали, что пациенты, которые прошли лечение протонной терапией, имели такие же показатели качества жизни, как и те, у которых даже не было рака простаты.
Рак простаты обычно растет медленно. Не позволяйте никому подгонять вас при принятии решения, которое будет иметь последствия до конца вашей жизни.