лизис костной ткани что это
ОНА ЖИВАЯ!
Да, обменные процессы в ней идут крайне медленно, а после гибели она, в отличие от мягких тканей, практически не меняет объёма и основных свойств – и это та причина, по которой многие люди, в т. ч. и стоматологи-имплантологи, воспринимают её слишком механистически, как обычный неживой материал для пиления и сверления. Такой отношение приводит к “столярно-слесарному подходу” к имплантации, который можно сформулировать одной фразой: “чем крепче вкрутил – тем лучше держится”. Впрочем, об этом я тоже писал. Про торки, и почему усилия >30 Нсм – это плохо, можно почитать здесь>>.
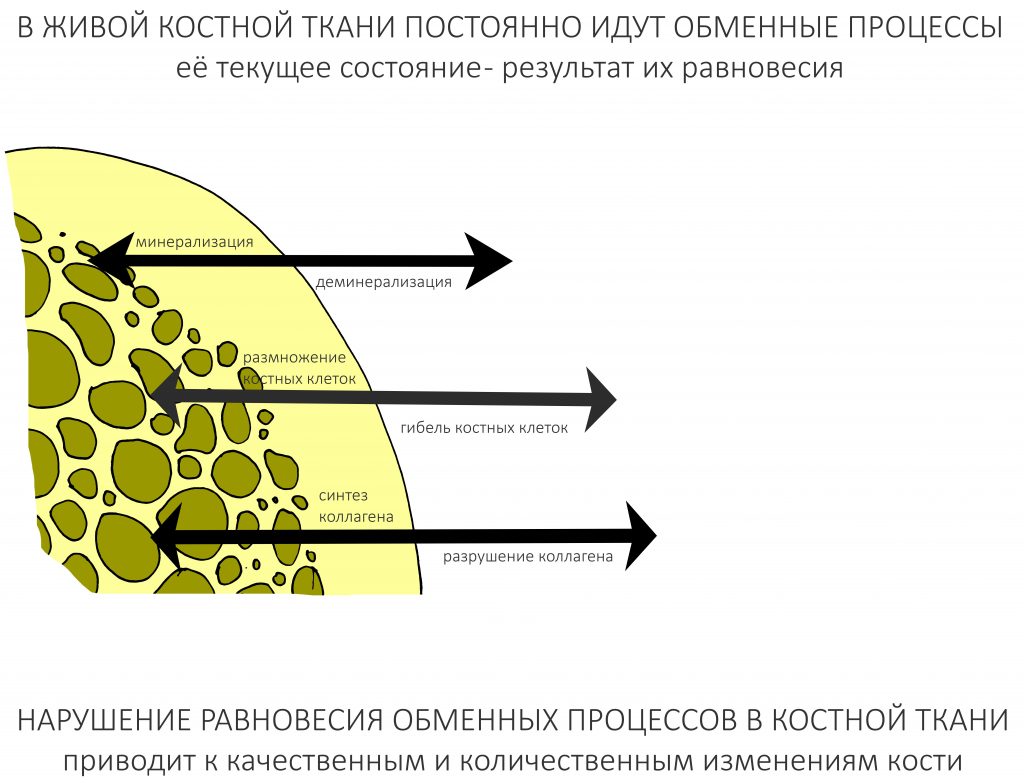
Второе, не менее важное – это то, что текущее состояние костной ткани является результатом биологического равновесия между процессами остеолизиса и остеогенеза. Иными словами, клетки кости делятся и умирают, коллагеновые волокна деградируют и образуются вновь, кальций приходит в костную ткань и уходит из неё – и всё это происходит постоянно и непрерывно.
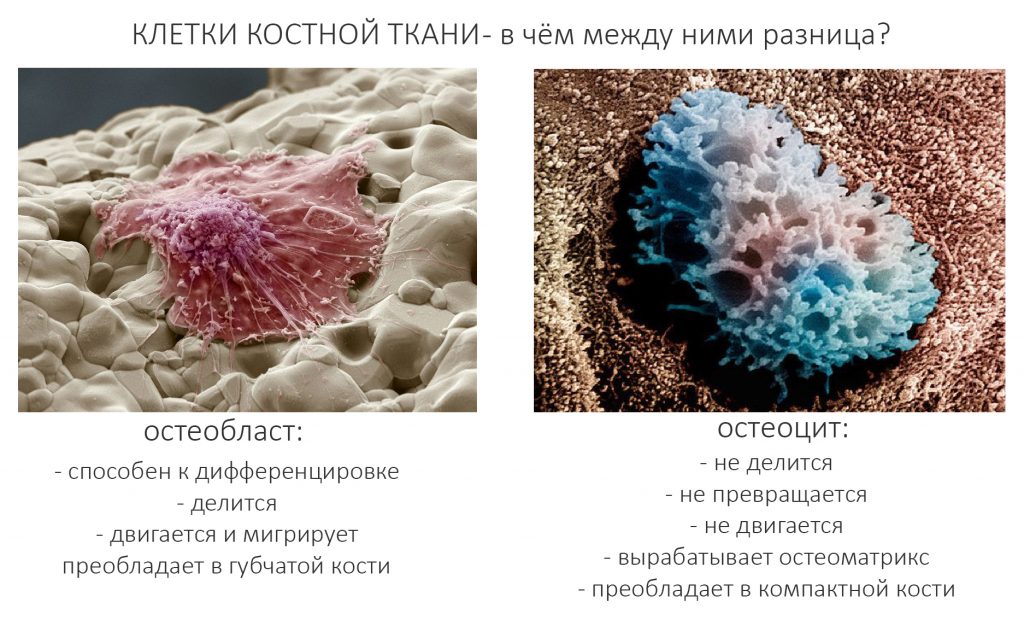
Третья вещь, что вы должны знать о костной ткани – так это то, что основной её компонент как по объёму, так и по массе, межклеточное вещество (остеоматрикс) участвует в регенерации исключительно опосредованно. Поэтому для “наращивания костной ткани” совершенно бесполезно пить кальций – и про это мы тоже уже писали. Как и про то, что источником “костеобразования” являются только живые клетки костной ткани, остеобласты и остеоциты. Между этими клетками есть принципиальная разница:
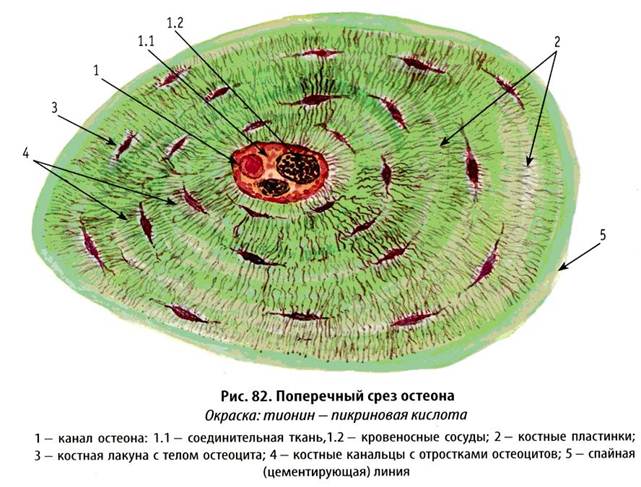
То есть, двигаются и размножаются только остеобласты. Остеоцит – это не способная к делению клетка, основная задача которой – продуцировать остеоматрикс, формируя вокруг себя структурную единицу костной ткани, остеон (картинка честно спижжена из какого-то учебника):
Следовательно, чем “плотнее” костная ткань, чем она тверже и прочнее – тем меньше в ней остеобластов, делящихся клеток, и тем больше в ней остеоцитов, клеток неделящихся. И, чем “плотнее” и “тверже” костная ткань, тем хуже она будет регенерировать, т. е. восстанавливаться после повреждения.
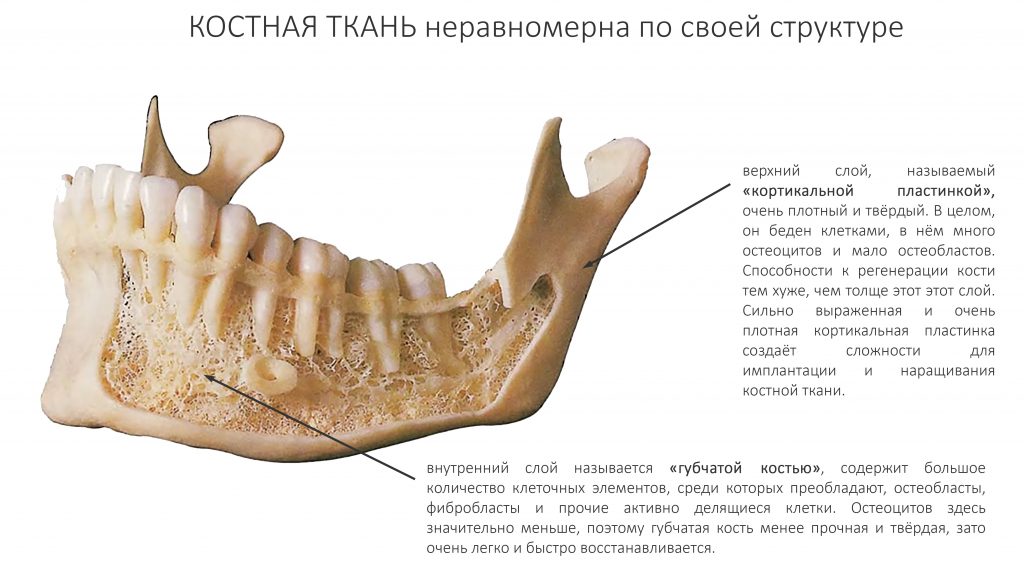
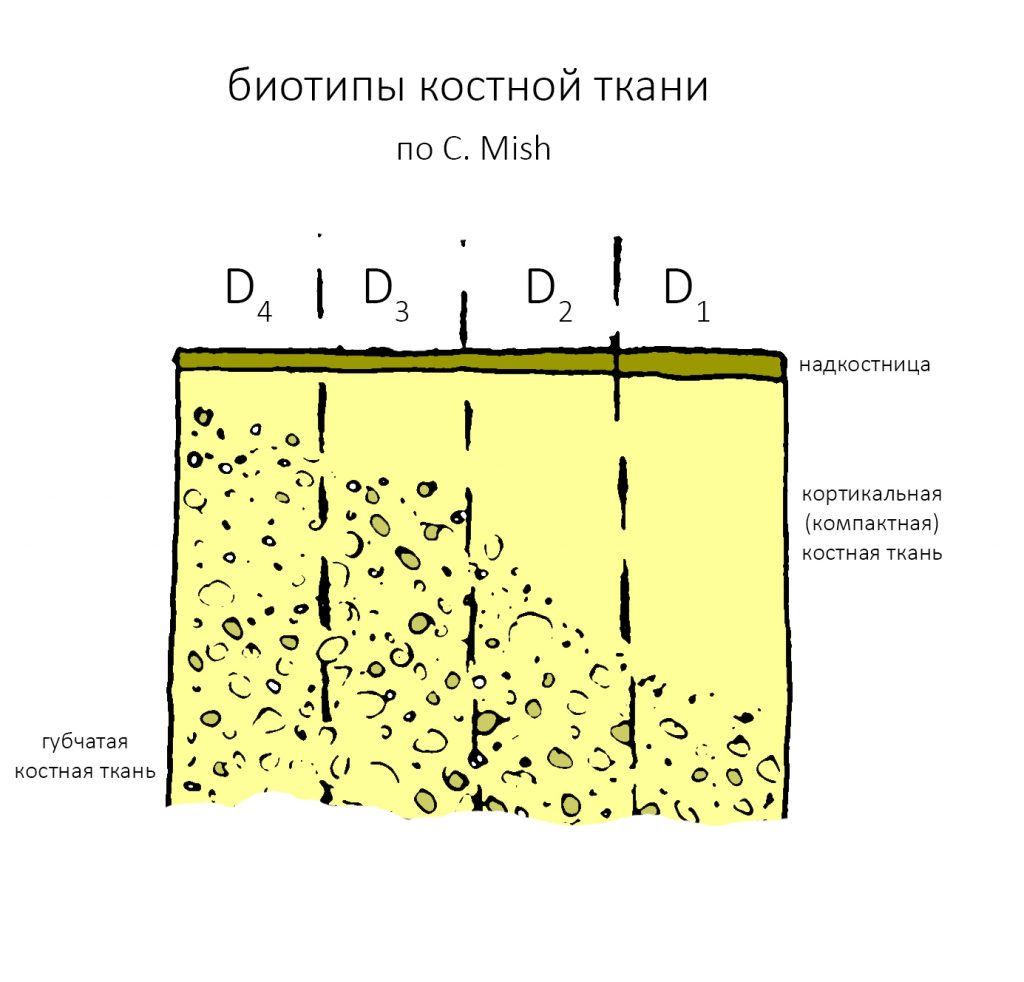
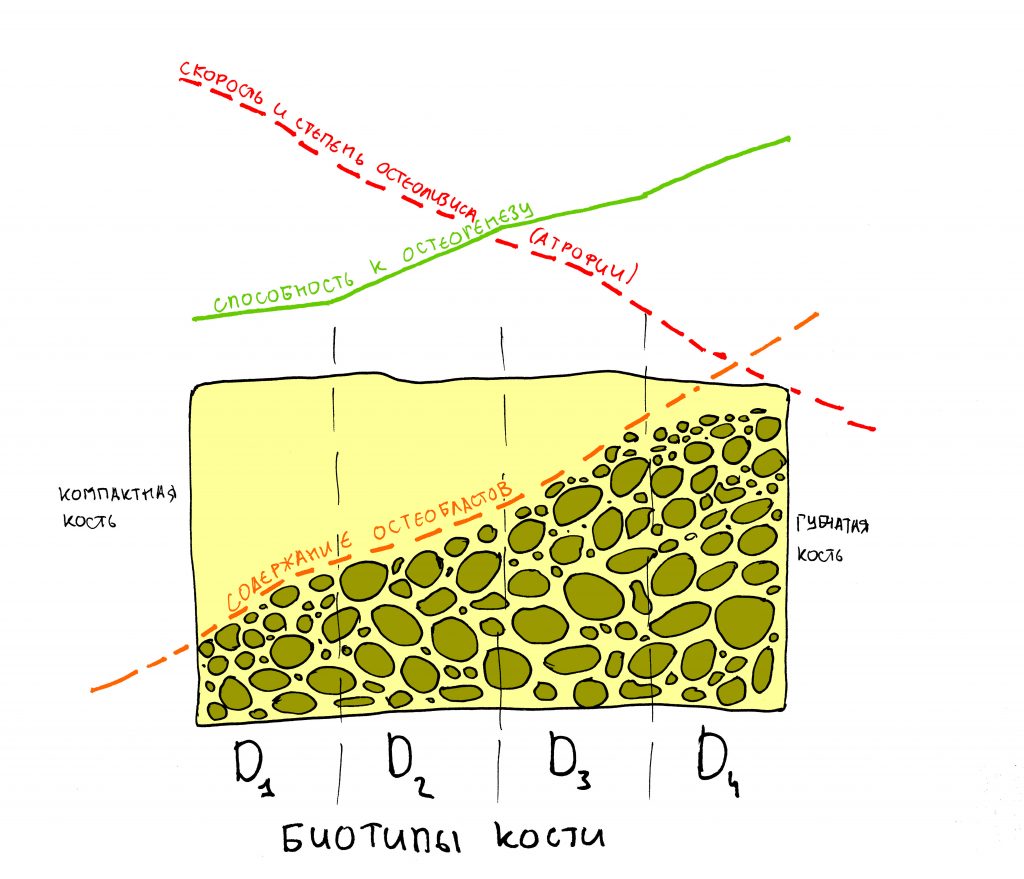
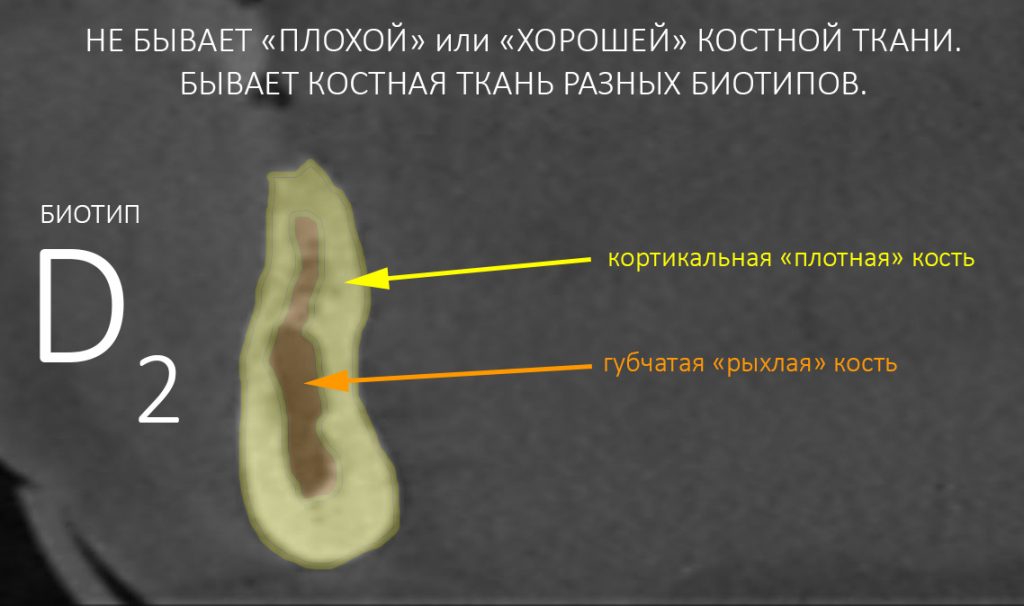
Четвертое – это то, что костная ткань неравномерна по структуре. У неё есть плотный кортикальный слой, называемый “компактной пластинкой” и рыхлая внутренняя часть, называемая “губчатой костью”.
И, в зависимости от соотношения компактной пластинки и губчатой кости, альвеолярную кость принято делить на биотипы. О них мы говорили много-много раз, например здесь>>, здесь>> и тут>>:
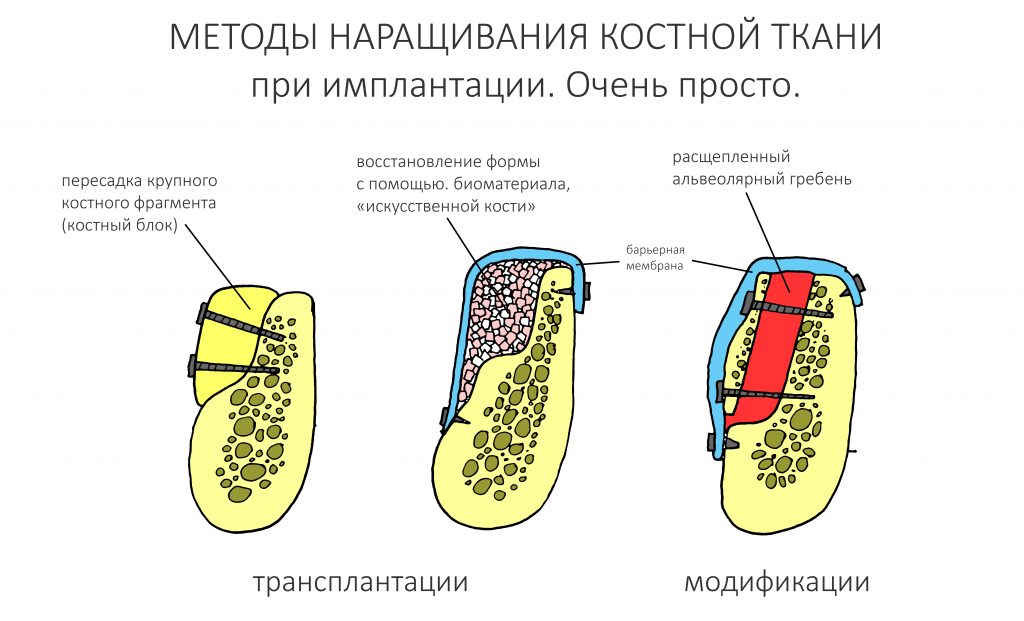
Так вот, друзья, исходя из того, что мы знаем об остеогенезе и клетках костной ткани, регенерация костной ткани разных биотипов будет различаться. Зная это, мы можем адекватно выбирать метод наращивания костной ткани – и всегда добиваться хорошего результата лечения.
И, наконец, пятое, что нужно знать о челюстной костной ткани.
Её убыль – прямое следствие нарушения биологического равновесия, обмена веществ, остеогенеза и остеолизиса и т. д.
Каким образом происходит нарушение?
Любую хирургическую операцию, в том числе удаление зуба, организм воспринимает как травму и реагирует на неё соответствующей реакцией, воспалением.
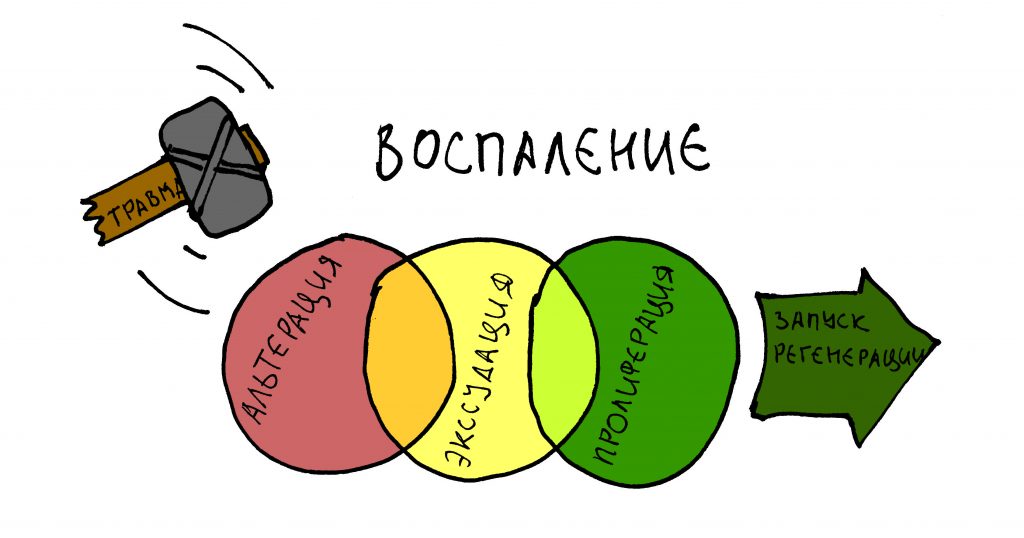
Воспаление – это сложный патофизиологический процесс, состоящий из нескольких плавно перетекающих одна-в-другую стадий:
В ходе воспаления выделяется ряд биологически активных веществ (БАВ) запускающих фагоцитоз, в котором участвуют остеокласты и прочие макрофаги. Они уничтожают всё то, что считают повреждённым (а всё повреждённое маркируется заранее специальными соединениями, антителами).
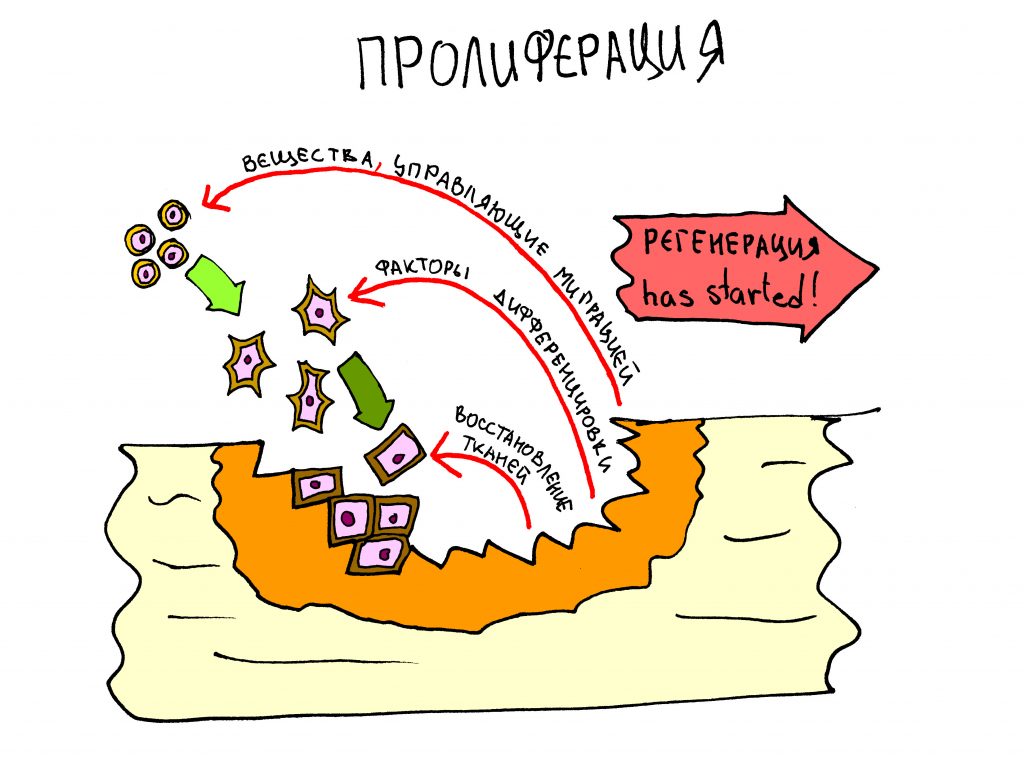
Так, запускается процесс остеолизиса – остеокласты жрут костную ткань, она уменьшается в объёме. И было бы всё очень печально, если бы остеокласты не дохли от своего обжорства – погибая, они выделяют целый ряд медиаторов, т. н. Белков Костного Морфогенеза (БКМ) или, на иностранщине, BMP (Bone Morphogenetic Proteins), которые активируют размножение и дифференцировку фибробластов и остеобластов. Иными словами, запускают остеогенез, рост новой кости:
И вот тут надо сделать пару важных замечаний:
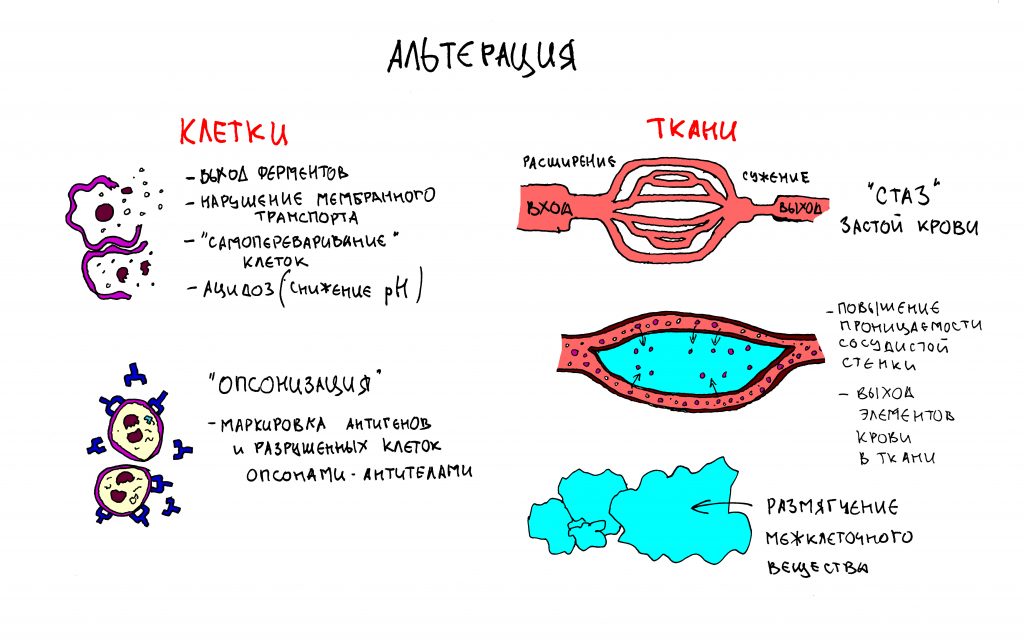
– основные БАВ, запускающие фагоцитоз (белки цитокинового ряда и т. д.) выделяются во время альтеративной стадии воспаления, которая известна своей бурной симптоматикой. Да, друзья, отёк, боль, повышение температуры травмированного участка – всё это происходит в фазу альтерации.
– да, мы все боимся выраженной постоперационной (читай, “воспалительной”) симптоматики и многое делаем для того, чтобы она была как можно мягче. Но интересный факт – слабо выраженная стадия альтерации не даст нужного количества БАВ для запуска остеокластов, а они, в свою очередь – для регенерации костной ткани. Таким образом, между симптоматикой постоперационного воспалительного процесса и последующей регенерацией существует прямая положительная связь: чем более выражена альтеративная стадия воспаления, тем больше выделится управляющих остеогенезом факторов.
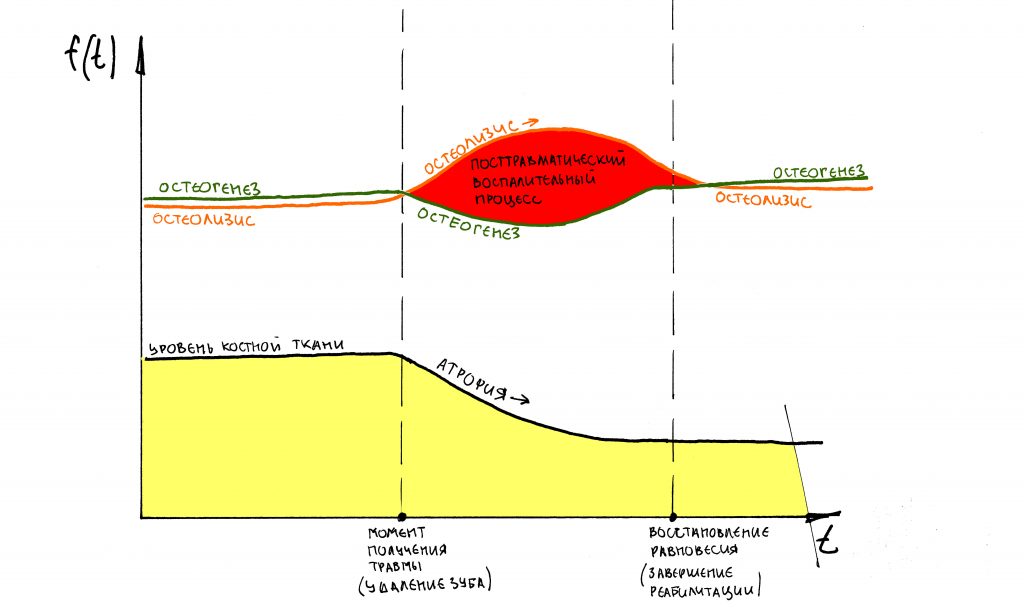
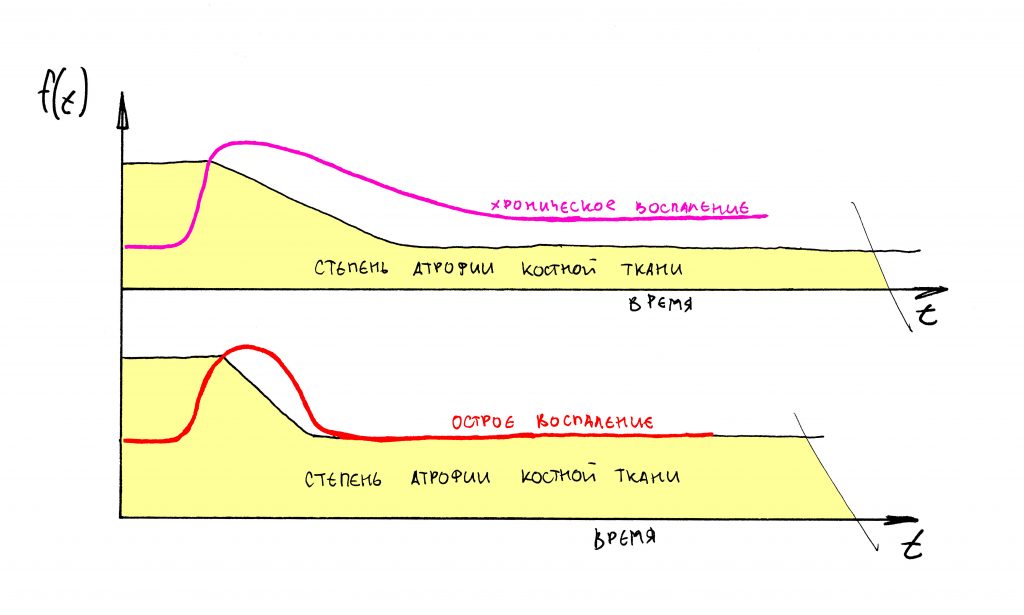
Фактически, посттравматический воспалительный процесс выводит наше уравнение “остеолизис-остеогенез” из состояния равновесия – из-за повышенной активности жрущих кость клеток, остеолизис перевешивает:
К счастью, этот процесс длится недолго. Постепенно, все процессы вновь уравновешиваются, скорость и степень остеолизиса почти сравнивается со степенью и скоростью остеогенеза.
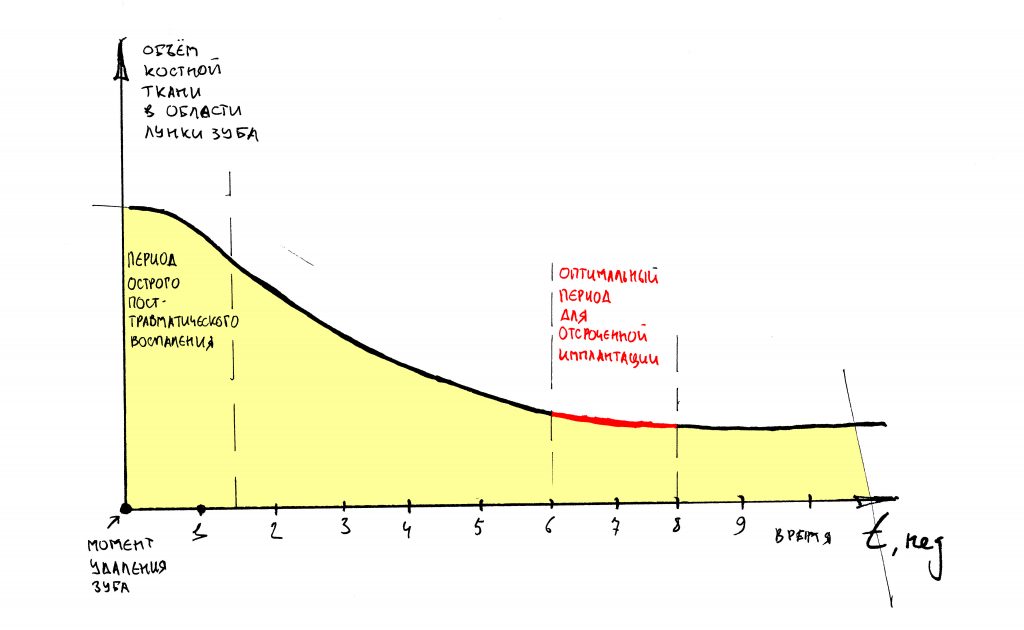
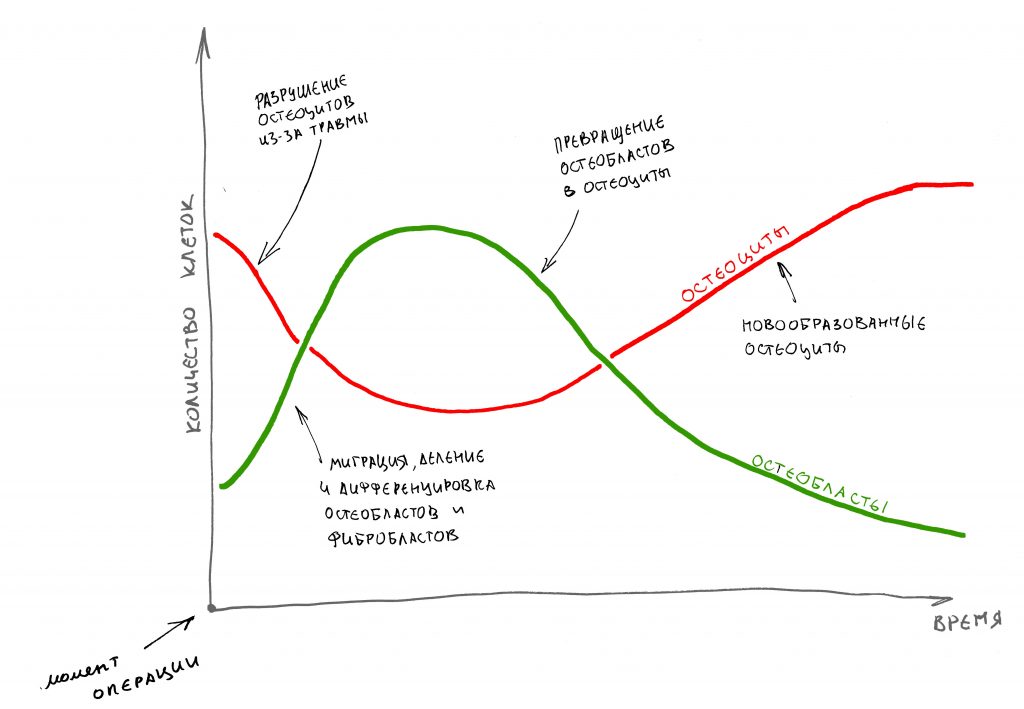
И процесс атрофии замедляется. Если привязать его ко времени и нарисовать график, то получим следующее:
Проще говоря, наибольшая потеря объемов костной ткани происходит в первые 4-8 недель после удаления зуба. Затем, процесс замедляется – и, взяв промежуток времени от 18 до 24 месяцев после удаления, мы с удивлением отметим, что линейные размеры кости практически не меняются:
Но, вернёмся к биотипам костной ткани.
Если существует зависимость между биотипом альвеолярной кости и её регенеративными возможностями (остеогенезом), то, очевидно, есть взаимосвязь между биотипом и скоростью атрофии кости. И вы это неоднократно наблюдали – скажем, если мы видим очень сильно атрофированный альвеолярный гребень, то, как правило, он D1-D2 биотипа, а если форма и объем челюстной кости после потери зубов практически не уменьшаются на протяжение длительного времени, то на 146% D3-D4.
И это легко объяснить, зная, что костная ткань D3-D4 биотипа лучше кровоснабжается, в ней больше остеобластов, а обменные процессы в ней идут интенсивнее. Значительная и требующая остеопластики атрофия такого альвеолярного гребня возникает редко и, как правило, только в случаях очень-очень-очень травматичного удаления зубов, либо на фоне хронического воспалительного процесса, когда остеокласты и прочие макрофаги активны в течение очень-очень-очень большого промежутка времени.
А что на практике?
Знание принципов и закономерностей атрофического процесса, с одной стороны, рвёт шаблон и наше представление об остеопластике, но с другой – предоставляет весьма достоверный прогностический инструмент. С помощью него можно не только предсказать динамику изменения объёмов костной ткани после удаления и имплантации, но и внятно объяснить, в разных клинических условиях работают разные методы наращивания костной ткани.
Что мы знаем о пациенте?
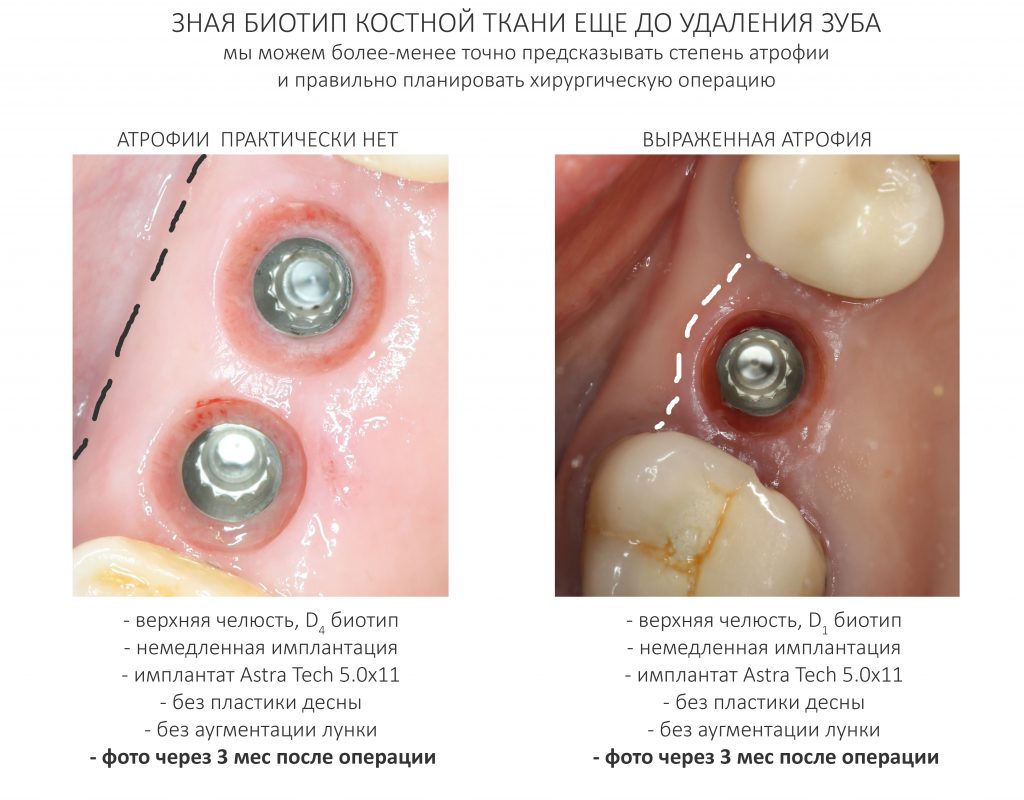
Биотип костной ткани – это то, что мы можем определить по компьютерной томограмме еще до удаления зуба.
Как это использовать?
Зная взаимосвязь между биотипом и атрофией, можно более-менее достоверно определять показания, к примеру, для превентивной консервации лунки, в том числе, при немедленной имплантации.
И, по идее, такой внятный анализ и прогноз атрофии применительно к конкретному клиническому случаю должны заменить устоявшийся в современной имплантологии принцип “Все так делают!” или “Нас так учили!”.
Кроме того, мы можем предсказывать степень атрофии и определять, потребуется ли наращивание костной ткани при отсроченной имплантации даже до того, как зубы удалены.
Заключение
Ключевыми причинами атрофических изменений в костной ткани являются потеря функции (нагрузки) из-за удаления зубов и, как следствие, перестройка микрососудистого русла, нарушение обмена веществ и т. д.
При этом, “движущая сила” атрофии – это макрофагальная (в т. ч. остеокластическая активность), управляемая рядом биологически активных веществ, образующихся, в основном, в ходе воспалительного процесса.
В то же время, остеокласты и прочие макрофаги выделяют вещества, управляющие регенерацией, которые в простонародье называются Белками Костного Морфогенеза (БКМ). Последние активируют размножение и дифференцировку остеобластов и фибробластов – и костная ткань начинает расти.
Уменьшение объёма и линейных размеров костной ткани, в т. ч. после имплантации и остеопластики, будет продолжаться до тех пор, пока процессы остеолизиса и остеогенеза снова не придут в состояние биологического равновесия.
Быстрая потеря регенерата после наращивания кости, периимплантит или резкая убыль костной ткани вокруг имплантатов, может и должна быть рассмотрена как частный случай атрофического процесса, подчиняющегося тем же самым закономерностям, что и вообще. Иными словами, имеет место быть хроническое воспаление со всеми вытекающими.
А еще можно сделать ряд прикладных выводов.
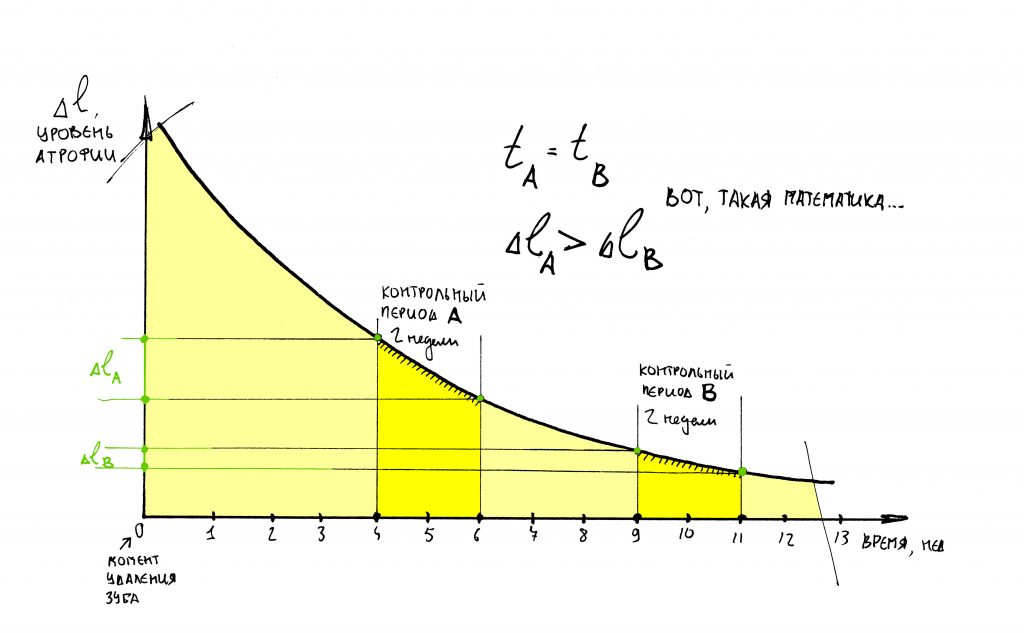
История о том, что “чем больше ждёшь, тем меньше кости останется”, мягко говоря, не совсем правдива. Если пациент пришёл через год после удаления зуба с определённым объёмом костной ткани, то не имеет смысла его торопить и пугать атрофией. Всё, что должно было уменьшиться – уже уменьшилось. Не суетитесь. Спокойно делайте остеопластику и проводите имплантацию.
Немедленная имплантация практически не влияет на скорость и степень атрофии. Именно поэтому в некоторых ситуациях (между прочим, далеко не во всех) при немедленной имплантации нам необходима аугментация лунки с использованием биоматериалов.
Рекомендации о необходимости ждать по полгода с момента удаления зуба до имплантации не имеют под собой оснований. В ожидании более 4-6 месяцев от операции остеопластики до операции имплантации больше вреда, чем пользы. Почему? Читайте здесь>>
Завершая эту, иногда сложную для понимания статью, я хотел бы сделать небольшую ремарку.
Мы живём в мире готовых решений. Нам не надо готовить борщ (есть Яндекс.Еда), не надо чинить, обслуживать и даже заправлять автомобиль (есть Яндекс.Драйв), не нужно помнить Дни Рождения друзей (есть Фейсбук), не нужно уметь ориентироваться (есть Яндекс.Навигатор). Нам не надо читать книжки, чтобы самостоятельно найти ответы на свои вопросы (есть куча пабликов, где можно задать любой вопрос и получить тысячу ответов). Нам не надо знакомиться с девушками/юношами (есть PornHub).
Да, что уж говорить – вы пользуетесь Т9 в переписке, выбирая слова, которые предлагает вам компьютер! И вам совершенно не нужно знать, как это всё работает.
В медицине, в целом, в стоматологии, в частности – это устойчивый тренд. Все мы ждём, что появится какой-то волшебный метод остеопластики, который будет работать всегда и везде, без осложнений и т. д. И нам всё время пытаются внушить, что вот он, этот метод, он существует. Ты просто повтори его так, как это делает лектор или преподаватель – и всё. А если у тебя возникли проблемы – то лишь от того, что ты неправильно его повторил.
Вместо этой статьи я мог бы показать вам какой-нибудь красивый клинический случай с фотографиями “было-стало” и минимумом текста.
Возможно, кто-то из вас восхитился, кого-то стошнило бы от вида расчленёнки – но какую пользу вам принесла бы подобная публикация? Ну знали бы вы, что мы в CLINIC IN умеем делать остеопластические операции с красивым результатом – так все это и так знают!
Нет, друзья, иногда я вынужден рассказывать о малопонятных и скучных, на первый взгляд, вещах, которые, однако, важны для понимания принципов наращивания костной ткани, представления о том, что происходит с вами после хирургической операции и откуда берутся осложнения, необходимы для правильного планирования и прогнозирования стоматологической реабилитации с использованием дентальных имплантатов. Очень надеюсь, что я на верном пути.
Ведь, чем больше вы знаете – тем лучше для всех.
CLINIC IN вам в этом поможет.
Спасибо, что дочитали до конца.
С уважением, Станислав Васильев, имплантолог CLINIC IN.
Болезнь Горхема-Стаута
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «11» января 2019 года
Протокол №51
Болезнь Горхема-Стаута (синонимы: синдром или болезнь Горхема, ангиогенный остеолиз, болезнь исчезающей кости (англ. Gorham’s disease, Gorham – Stout syndrome/disease, GSD, massive osteolysis, vanishing bone disease, phantom bone disease) является редким заболеванием массивного остеолиза, связанного с пролиферацией и расширением лимфатических сосудов. GSD может влиять на любую кость в организме и может быть моностотической или полиотической. Симптомы при представлении зависят от местоположения заболевания; наиболее распространенным симптомом является локализованная боль. Болезнь может быть обнаружена после патологического перелома [1].
Код(ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| D18.1 | Лимфангиома любой локализации |
Дата разработки/пересмотра протокола: 2018 год.
Сокращения, используемые в протоколе:
Пользователи протокола: врачи общей практики, терапевты, онкологи, гематологи, травматологи, ангиохирурги.
Категория пациентов: взрослые, дети.
Шкала уровня доказательности:
Таблица 1. Шкала уровней доказательности
| УД | Характеристика исследований, которые легли в основу рекомендаций |
| А | Высококачественный мета-анализ, систематический обзор рандомизированных клинических исследований (РКИ) или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов |
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы и анамнез:
Заболевание начинается постепенно, с неспецифических симптомов, и диагностика на ранних этапах затруднена.
GSD может возникнуть в любом возрасте, но обычно диагностируется у детей и молодых людей (в среднем 13 лет). GSD может влиять на любую кость в организме, но чаще всего влияет на ребра, за которым следуют череп, ключица и шейный позвоночник. Дополнительные пораженные участки включают челюстно-лицевые кости (главным образом нижнюю челюсть), грудину, плечевую кость, руку, бедренную кость и стопу [1].
GSD может быть моностатическим или полиостатическим, и симптомы варьируются в зависимости от затронутых участков тела [1].
Наиболее распространенным симптомом является локализованная боль [1]. Характерны тупые монотонные скелетно-мышечные боли и слабость.
Также отмечается отек, слабость и функциональное нарушение пораженных конечностей [1].
В области дентоальвеолярной области могут наблюдаться подвижные зубы, неправильный прикус, отклонение нижней челюсти и костная деформация [1].
Пациенты с вовлечением грудной клетки могут проявлять респираторный дистресс (вызванный хилотораксом) [1]. Поражению костей грудной клетки может сопутствовать перикардиальный или плевральный выпот.
Тяжелые неврологические дефекты и паралич, вторичные по отношению к вовлечению позвонков, также наблюдаются. Пациенты с цервикальным позвоночником или основанием болезни черепа могут иметь утечку цереброспинальной жидкости [1].
GSD может быть обнаружен после перелома кости (спонтанная или следующая незначительная травма) [1].
В детском возрасте развивается деформация кости.
Заболевание сопровождается остеолизом и резорбцией кости с фиброзом [4].
Заболевание может как спонтанно регрессировать, так и иметь агрессивное течение с неблагоприятным прогнозом.
Лабораторные признаки: с учетом вариабельности скорости остеолиза наиболее перспективными биомаркерами его активности считаются VGEF-A [22, 23, 27] и интерлейкин-6 [5, 24, 25, 28], уровень которых при GSD может быть повышен. Вместе с тем показатели этих цитокинов могут оставаться и нормальными [26, 27], поэтому продолжаются активные поиски других биомаркеров остеолиза – VEGF-C [27], PDGF-BB [26], sRANKL-растворимый лиганд рецептора активатора ядерного фактора (биохимический маркер резорбции костной ткани) и остеопротегерина [7].
Инструментальные исследования
Магнитно-резонансная томография: показывает полную резорбцию кости и замену инфильтративной мягкой тканью, которая имеет низкую интенсивность сигнала при T1-взвешенном изображении и высокой интенсивности сигнала на T2, с интенсивным усилением контрастного изображения [1].
Рентгенологическими признаками GSD: подтверждение рассасывания кости при отсутствии тенденции к экспансивному или изъязвляющему росту, на ранних стадиях являются небольшие по размеру фокусы затемнения, сливающиеся по мере прогрессирования процесса. Кроме того, поражение трубчатых костей может проявляться концентрическим сужением кости (симптом тающей свечи) [14], а поражение позвонков у детей – наличием остеопении, мультиочагового остеолиза и гетерогенностью костной ткани.
Характерным признаком гиперваскулярности процесса является выявляемый по МРТ гиперинтенсивный сигнал от костного мозга в Т1-режиме [14, 21].
Иммуногистохимические маркеры лимфатических эндотелиальных клеток (LYVE-1, podoplanin / D2-40) выявляют наличие лимфатических сосудов в медуллярных и кортикальных областях костей и в пораженных мягких тканях. Повреждения ребер не должны подвергаться биопсии, так как эта процедура может вызвать рефрактерный хилозный выпот [1].
Гистологические признаки: верифицированный ангиоматоз, отсутствие клеточной атипии, отсутствие или минимальный уровень активности остеобластов, отсутствие дистрофической кальцификации, прогрессирующий характер локального остеолиза, отсутствие поражения внутренних органов.
Диагностический алгоритм
Дифференциальный диагноз
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Генерализованное лимфатическое нарушение | Основным отличительным признаком является прогрессирующий остеолиз, наблюдаемый при болезни Горхема-Стаута | Радиологическое обследование | Отсутствие костных поражений |
| Доминантный вариант акроостеолиза | Остеопороз запястных и плюсневых костей | Наследственный анамнез, отсутствие артрита, при необходимости гистологическое подтверждение | В основном поражение зубов, отсутствие наследственных факторов, пролиферации лимфатических сосудов |
| Мультицентровой карпотарзальный остеолиз с нефропатией или без нее | Деструкция костей запястья и предплюсны, возможно прогрессирование с генерализацией | С раннего детства аритриты Гистология, определение факторароста сосудов эпителия, Генетика-мутация в хромосоме 20q12 | Отсутствие мутации в гене МАFВ, лимфатической пролиферации в костях |
| Липогранулематоз Фарбера | Артрит, без костной деструкции | Генетические на ген АSAH1 (кислой цераминазы) | Отсутствие поражения внутренних органов и соответствующая генетика |
| Синдром Торга-Винчестера и идиопатический фалангеальный акроостеолиз | Остеолиз фаланг и плюстневых костец | Рентген костей, исследование на наличие гена ММР2 | Отсутствует остеолиз и ген |
| Рак (первичный или метастатический) | Диффузный или очаговый остеопороз, патологические переломы, наличие симптома «плюс ткань» | Гистологические, иммуногистохимические исследования | Отсутствие признаков онкологического процесса |
| Эндокринные расстройства (как возможные причины остеолиза) | Диффузный или очаговый остеопороз | Исследования гормонов паращитовидной железы, витамина D, консультация эндокринолога | Отсутствие нарушений в гормональном статусе |
| Аутосомно-рецессивный карпотарзальный остеолиз | Деструкция костей запястья и предплюсны, возможно прогрессирование с генерализацией | С раннего детства аритриты Гистология, определение фактора роста сосудов эпителия, Генетика-мутация в хромосоме 20q12 | Отсутствие суставных поражений, подтверждение генетическим исследованием-мутация в хромосоме 20q12 |
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Альбумин (Albumin) |
| Амброксол (Ambroxol) |
| Ацетилцистеин (Acetylcysteine) |
| Гепарин (Heparin) |
| Дексмедетомидин (Dexmedetomidine) |
| Декстроза (Dextrose) |
| Диазепам (Diazepam) |
| Золедроновая кислота (Zoledronic Acid) |
| Интерферон альфа (Interferon alfa) |
| Калия хлорид (Potassium chloride) |
| Кетопрофен (Ketoprofen) |
| Колистиметат натрия (Colistimethate sodium) |
| Левофлоксацин (Levofloxacin) |
| Меропенем (Meropenem) |
| Метронидазол (Metronidazole) |
| Морфин (Morphine) |
| Налбуфин (Nalbuphine) |
| Натрия ацетат (Sodium acetate) |
| Натрия гидрокарбонат (Sodium hydrocarbonate) |
| Натрия хлорид (Sodium chloride) |
| Омепразол (Omeprazole) |
| Парацетамол (Paracetamol) |
| Пиперациллин (Piperacillin) |
| Плазма свежезамороженная |
| Прегабалин (Pregabalin) |
| Преднизолон (Prednisolone) |
| Пропофол (Propofol) |
| Сиролимус (Sirolimus) |
| Сульбактам (Sulbactam) |
| Сульфаметоксазол (Sulphamethoxazole) |
| Тазобактам (Tazobactam) |
| Талидомид (Thalidomide) |
| Тобрамицин (Tobramycin) |
| Трамадол (Tramadol) |
| Триметоприм (Trimethoprim) |
| Фамотидин (Famotidine) |
| Фентанил (Fentanyl) |
| Цефоперазон (Cefoperazone) |
| Ципрофлоксацин (Ciprofloxacin) |
| Эритроцитарная масса |
| Этамзилат (Etamsylate) |
Группы препаратов согласно АТХ, применяющиеся при лечении
| (A11CC05) Colecalciferol |
| (B03A) Препараты железа |
| (A12AX) Препараты кальция в комбинации с другими препаратами |
| (A12CC) Препараты магния |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Немедикаментозное лечение
Режим: общеохранительный режим, избегать травм.
Диета: №15.
Медикаментозное лечение: проводится лечение сопутствующей патологии в соответствии с клиническими протоколами.
Хирургическое вмешательство: нет.
Дальнейшее ведение:
Диспансерный учет профильного хирурга в зависимости от вида оперативного вмешательства (ортопеда, вертебролога, сосудистого хирурга);
Радиологический контроль не менее 1 раза в 6 месяцев. При наличии хилоторакса рентгенография и КТ грудного сегмента проводят по показаниям (наличия расстройств дыхания, ассимертии грудной клетки).
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе: нет.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Немедикаментозное лечение
Режим: общеохранительный режим, избегать травм.
Диета: № 15.
Медикаментозное лечение
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
Примечание: *Лекарственные средства не зарегистрированы в Республике Казахстан (применение после регистрации на территории РК).
Другие виды лечения:
Лучевая терапия [6].
Хирургическое вмешательство
Виды хирургических вмешательств зависят от их цели:
| Цель | Название операции | Код МКБ-9 |
| Уменьшить или остановить хилоторакс [1] | Плевротомия | 34.59 Другие виды иссесения плевры |
| Плевродез | 34.601 Плевродез | |
| Торакоцентез | 34.04Дренирование плевральной полости | |
| Торакальная проточная эмболизация или лигирование | 39.794 Эндоваскулярная эмболизация сосудов | |
| Дренирование плевральной полости, перевязка и эмболизация грудного лимфатического протока (УД-С) | Торакотомия | 34.02Диагностическая торакотомия |
| Плевротомией | 34.59 Другие виды иссесения плевры | |
| Плевродезом | 34.601 Плевродез | |
| Декортикация легкого (УД-С) | 34.51 Декортикация легкого | |
| Стабилизация, фиксация, коррекция позвоночника | Корригирующие, стабилизирующие фиксирующие операции на позвоночник с применением металлоконструкций (УД-С) | 79.39 Открытая репозиция костных обломков другой уточненной кости с внутренней фиксацией |
| Склерозирование плевральной полости цитостатиками (УД-С) | Введение в плевральную полость циклофосфан по 400мг №7, блеомицин по 30 мг №3-7 | 34.04 Дренирование плевральной полости |
Дальнейшее ведение:
1. Диспансерный учет профильного хирурга в зависимости от вида оперативного вмешательства (ортопеда, вертебролога, сосудистого хирурга);
2. Радиологический контроль не менее 1 раза в 6 месяцев. При наличии хилоторакса рентгенография и КТ грудного сегмента проводят по показаниям (наличия расстройств дыхания, асимметрии грудной клетки).
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
Показания для экстренной госпитализации:
Информация
Источники и литература
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Колеснев Александр Валерьевич – заведующий отделением онкогематологической реанимации «Национального научного центра онкологии и трансплантологии» корпоративного фонда «University Medical Center»;
5) Макалкина Лариса Геннадьевна – кандидат медицинских наук, PhD, заведующая курсом клинической фармакологии и фармации кафедры кардиологии и внутренних болезней АО «Медицинский университет Астана».
Указание на отсутствие конфликта интересов:
Рецензенты:
Сагандыков Ирлан Негметжанович – кандидат медицинских наук, заведующий отделением сосудистой хирургии «Национального научного центра онкологии и трансплантологии» корпоративного фонда «University Medical Center».
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.