литий ионный аккумулятор что это
Литий-ионным аккумуляторам исполнилось 25 лет. Почему за четверть века их активные материалы так мало изменились
В этом году исполнилось 25 лет с момента выхода в продажу первых литий-ионных аккумуляторов, которые изготовила корпорация Sony в 1991 году. За четверть века их ёмкость практически удвоилась с 110 Втч/кг до 200 Втч/кг, но, несмотря на такой колоссальный прогресс и на многочисленные исследования электрохимических механизмов, сегодня химические процессы и материалы внутри литий-ионных аккумуляторов практически те же, что и 25 лет назад. В этой статье будет рассказано, как шло становление и развитие данной технологии, а также с какими трудностями сталкиваются сегодня разработчики новых материалов.
1. Развитие технологии: 1980-2000
Ещё в 70х годах учёными было установлено, что существуют материалы под названием халькогениды (например, MoS2), которые способны вступать в обратимую реакцию с ионами лития, встраивая их в свою слоистую кристаллическую структуру. Тут же был предложен первый прототип литий-ионного аккумулятора, состоящий из халькогенидов на катоде и металлического лития на аноде. Теоретически, во время разрядки, ионы лития, «высвобождаемые» анодом, должны встраиваться в слоистую структуру MoS2, а при зарядке оседать обратно на аноде, возвращаясь в исходное состояние.
Но первые попытки создания таких аккумуляторов были неудачны, так как при зарядке ионы лития никак не хотели обратно превращаться в ровную пластину металлического лития, а оседали на аноде как попало, приводя к росту дендритов (цепочек металлического лития), короткому замыканию, и взрыву аккумуляторов. За этим следовал этап детального изучения реакции интеркаляции (встраивания лития в кристаллы с особой структурой), что позволило заменить металлический литий на углерод: сначала на кокс, а потом и на графит, который используется до сих пор и тоже имеет слоистую структуру, способную встраивать ионы лития.
Литий-ионный аккумулятор с анодом из металлического лития (а) и анодом из слоистого материала (b). Источник: nature.com
Начав использовать углеродные материалы на аноде, учёные поняли, что природа сделала человечеству большой подарок. На графите, при самой первой зарядке, образуется защитный слой из разложившегося электролита, названный SEI (Solid Electrolyte Interface). Точный механизм его формирования и состав еще не до конца изучены, но известно, что без этого уникального пассивирующего слоя электролит продолжал бы разлагаться на аноде, электрод бы разрушался, и аккумулятор приходил бы в негодность. Так появился первый работающий анод на основе углеродных материалов, который был выпущен в продажу в составе литий-ионных аккумуляторов в 90-х годах.
Одновременно с анодом видоизменялся и катод: выяснилось, что слоистой структурой, способной встраивать ионы лития, обладают не только халькогениды, но и некоторые оксиды переходных металлов, например LiMO2 ( M = Ni, Co, Mn), которые не только более стабильны химически, но и позволяют создавать ячейки с более высоким напряжением. И именно LiCoO2 был использован в катоде первого коммерческого прототипа аккумуляторов.
2. Новые реакции и мода на наноматериалы: 2000-2010
В 2000х в науке начался бум наноматериалов. Естественно, прогресс в нанотехнологиях не обошёл стороной и литий-ионные аккумуляторы. И именно благодаря им учёные сделали совершенно, казалось бы, непригодный для данной технологии материал, LiFePO4, одним из лидер ов по использованию в катодах электромобильных аккумуляторов.
А дело всё в том, что обычные, объёмные частицы железофосфата очень плохо проводят ионы, да и электронная проводимость у них очень низкая. Но засчёт наноструктурирования литию не надо продвигаться на большие расстояния чтобы встроиться в нанокристалл, поэтому интеркаляция проходит гораздо быстрее, а покрытие нанокристаллов тонкой углеродной плёнкой улучшает их проводимость. В результате в продажу вышел не только менее опасный материал, который не выделяет кислород при высокой температуре (как оксиды), но и материал имеющий способность работать на более высоких токах. Именно поэтому такой катодный материал предпочитают производители автомобилей, несмотря на чуть меньшую ёмкость чем у LiCoO2.
В то же время учёные искали новые материалы, взаимодействующие с литием. И, как выяснилось, интеркаляция, или встраивание лития в кристалл- не единственный вариант реакции на электродах в литий-ионных аккумуляторах. Так, например, некоторые элементы, а именно Si, Sn, Sb, и т.д., формируют «сплав» с литием, если использовать их в аноде. Ёмкость такого электрода в 10 раз превышает ёмкость графита, но есть одно «но»: такой электрод во время формирования сплава сильно увеличивается в объёме, что приводит к его быстрому растрескиванию и приходу в негодность. И для того, чтобы уменьшить механическое напряжение электрода при таком увеличении объёма, элемент (например, кремний) предлагают использовать в виде наночастиц, заключённых в углеродную матрицу, которая «амортизирует» изменения объёма.
Но изменения объёма- не единственная проблема материалов, образующих сплавы, и препятствующая их широкому применению. Как было сказано выше, на графите образуется «подарок природы»- SEI. А на материалах, образующих сплав, электролит разлагается непрерывно и повышает сопротивление электрода. Но тем не менее, периодически мы видим в новостях, что в некоторых аккумуляторах используется «кремниевый анод». Да, кремний в нём действительно используется, но в очень маленьких количествах и смешанный с графитом, чтобы «побочные эффекты» не слишком были заметны. Естественно, когда количество кремния в аноде составляет всего несколько процентов, а остальное- графит, значительного увеличения ёмкости не получится.
И если тема анодов, образующих сплавы, сейчас развивается, то некоторые исследования, начатые в прошлом десятилетии, очень быстро заходили в тупик. Это касается, например, так называемых реакций конверсии. В этой реакции некоторые соединения металлов (оксиды, нитриды, сульфиды и т.д.) взаимодействуют с литием, превращаясь в металл, смешанный с соединениями лития:
И, как можно себе представить, с материалом во время такой реакции происходят такие изменения, которые даже кремнию не снились. Например, оксид кобальта превращается в наночастицы металлического кобальта, заключённые в матрицу из оксидов лития:
Источник: J. Phys. Chem C 117, 14518 (2013)
Естественно, такая реакция плохо обратима, к тому же между зарядкой и разрядкой большая разница напряжений, что делает такие материалы бесполезными в применении.
Интересно заметить, что когда эта реакция была открыта, в научных журналах стали публиковаться сотни статей на эту тему. Но тут хочестся процитировать профессора Тараскона из Коллеж де Франс, который сказал, что «реакции конверсии были настоящим полем экспериментов для исследования материалов с наноархитектурой, что давало учёным возможность делать красивые картинки с помощью просвечивающего электронного микроскопа и публиковаться в известных журналах, несмотря на абсолютную практическую бесполезность этих материалов».
В общем, если подвести итог, то, несмотря на то, что в последнее десятилетие были синтезированы сотни новых материалов для электродов, в аккумуляторах до сих под используются практически те же материалы, что и 25 лет назад. Почему же так получилось?
3. Настоящее время: главные трудности в разработке новых аккумуляторов.
Как можно заметить, в вышеописанном экскурсе в историю литий-ионных аккумуляторов ни слова не было сказано об ещё одном, важнейшем элементе: электролите. И на это есть причина: электролит за 25 лет практически не изменился и работающих альтернатив предложено не было. Сегодня, как и в 90-е годы, в виде электролита используются соли лития (в основном LiPF6) в органическом растворе карбонатов (этилен карбонат (EC) + диметил карбонат (DMC)). А ведь именно из-за электролита прогресс в увеличении ёмкости аккумуляторов в последние годы замедлился.
Приведу конкретный пример: на сегодняшний день существуют материалы для электродов, которые могли бы значительно увеличить ёмкости литий-ионных аккумуляторов. К ним относится, например, LiNi0.5Mn1.5О4, который позволил бы сделать аккумулятор с напряжением ячейки в 5 Вольт. Но увы, в таких диапазонах напряжения электролит на основе карбонатов становится нестабильным. Или ещё один пример: как было сказано выше, сегодня, чтобы использовать значительные количества кремния (или других металлов, образующих сплавы с литием) в аноде, надо решить одну из главных проблем: образование пассивирующего слоя (SEI), который бы препятствовал непрерывному разложению электролита и разрушению электрода, а для этого надо разработать принципиально новый состав электролита. Но почему же так сложно найти альтернативу существующему составу, ведь солей лития полно, да и органических растворителей достаточно?!
А трудность заключаетя в том, что электролит должен одновременно обладать следующими характеристиками:
Естественно, создать электролит, обладающий сразу всеми данными характеристиками очень сложно, но учёные не теряют надежды. Во-первых, ведутся активные поиски новых растворителей, которые бы работали в более широком диапазоне напряжений, чем карбонаты, что позволило бы использовать новые материалы и увеличить энергоёмкость аккумуляторов. В разработке находятся несколько видов органических растворителей: эстеры, сульфоны, сульфоксиды и т.д. Но увы, увеличивая устойчивость электролитов к окислению, уменьшается их устойчивость к восстановлению, и в результате напряжение ячейки никак не меняется. К тому же, не все растворители формируют на аноде защитный пассивирующий слой. Именно поэтому зачастую в электролит подмешивают специальные добавки, например, винилен карбонат, которые искусственно способствуют формированию этого слоя.
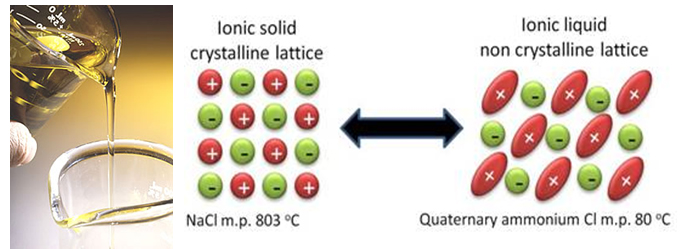
Параллельно с улучшением уже существующих технологий, учёные работают и над принципиально новыми решениями. И решения эти можно свести к попытке избавиться от жидкого растворителя на основе карбонатов. К таким технологиям относятся, к примеру, ионные жидкости. Ионные жидкости-это, по сути, расплавленные соли, у которых очень низкая температура плавления, и некоторые из них даже при комнатной температуре остаются жидкими. А всё из-за того, что у этих солей особенная, стерически затрудненная структура, которая усложнят кристаллизацию.
Казалось бы, отличная идея- полностью исключить растворитель, который легко воспламеняется и вступает в паразитические реакции с литием. Но на деле, исключение растворителя создаёт на данный момент больше проблем, чем решает. Во-первых, в обычных электролитах часть растворителя «приносит себя в жертву» для построения защитного слоя на поверхности электродов. А компоненты ионных жидкостей с этой задачей пока не справляются (анионы, кстати, тоже могут вступать в паразитические реакции с электродами, как и растворители). Во-вторых, очень сложно подобрать ионную жидкость с правильным анионом, так как они влияют не только на температуру плавления соли, но и на электрохимическую стабильность. И увы, самые стабильные анионы формируют соли, которые плавятся при высоких температурах, и, соответственно, наоборот.
Ещё один способ избавиться от растворителя на основе карбонатов- использование твёрдых полимеров (например, полиэфиров), проводящих литий, которые, во-первых, минимизировали бы риск утечки электролита наружу, а также препятствовали бы росту дендритов при использовании металлического лития на аноде. Но главная сложность, стоящая перед создателями полимерных электролитов- их очень низкая ионная проводимость, так как ионам лития сложно передвигаться в такой вязкой среде. Это, конечно, сильно ограничивает мощность аккумуляторов. А понижения вязкости влечёт за собой прорастание дендритов.
Также исследователи изучают твёрдые неорганические вещества, проводящие литий с помощью дефектов в кристалле, и пытаются применить их в виде электролитов для литий-ионных аккумуляторов. Такая система на первый взгляд идеальна: химическая и электрохимическая стабильность, устойчивость с повышению температуры и механическая прочность. Но у этих материалов, опять же, очень низкая ионная проводимость, и использовать их целесеобразно только в виде тонких плёнок. К тому же, работают такие материалы лучше всего при высокой температуре. И последнее, с твёрдым электролитом очень сложно создать механический контакт между электолитом и электродами (в этой области жидким электролитам нет равных).
С момента выхода в продажу литий-ионных аккумуляторов, попытки увеличить их ёмкость не прекращаются. Но в последние годы увеличение ёмкости замедлилось, несмотря на сотни новых предложенных материалов для электродов. А дело всё в том, что большинство этих новых материалов «лежат на полке» и ждут, пока не появится новый, подходящий им электролит. А разработка новых электролитов- на мой взгляд гораздо более сложная задача, чем разработка новых электродов, так как нужно учитывать не только электрохимические свойства самого электролита, но и все его взаимодействия с электродами. В общем, читая новости типа «разработан новый супер-электрод. » надо проверять, как такой электрод взаимодействует с электролитом, и есть ли для такого электрода подходящий электролит в принципе.
Electrochem. Soc. Interface Fall 2016 volume 25, issue 3, 79-83
Chem. Rev., 2014, 114 (23), pp 11503–11618
Все, что вы хотели знать о Li-Ion аккумуляторах, но боялись спросить (часть 1).
Сейчас на рынке представлено огромное разнообразие Li-Ion аккумуляторов различных марок, как с защитой, так и без. Взрывной рост их популярности пришелся на 2008-2010гг., когда на рынке появились большое количество мощных светодиодных фонарей в зарубежных интернет-магазинах.
Но, стоит признать, что, до сих пор, для большинства пользователей, этот тип элементов питания является достаточно новым и незнакомым. Чтобы не запутаться во всем этом многообразии мы хотим вам дать несколько советов, чтобы помочь определиться, какой именно литиевый аккумулятор вам необходим (защищенный-незащищенный) и как не купить откровенно некачественный товар.
Что нужно знать при использовании Li-Ion аккумуляторов.
В силу технологии Li-Ion аккумуляторы имеют ряд ограничений, которые необходимо соблюдать в процессе эксплуатации.
Это:
• максимальное напряжение (напряжение перезаряда) не должно превышать 4,25-4,35В
• минимальное напряжение (напряжение переразряда) не должно быть ниже 2,2-2,5В
• ток разряда не должен превышать 2ух-кратное значение емкости (2С): т.е. для аккумулятора с емкостью 2200мАч максимальный ток разряда не должен быть выше 4400мА, а обладателя емкости в 3100мАч можно смело разряжать током до 6200мА. Есть особые типы высокомощных Li-Ion аккумуляторов, которые предназначены для работы с большими разрядными токами, превышающими величину их емкости в 5-10 раз.
• ток заряда не должен быть выше половины значения емкости аккумулятора (0,5С).
По аналогии с током разряда для аккумулятора с емкостью 2200мАч максимальный ток заряда не должен быть выше 1100мА, а аккумулятор с емкостью 3100мАч можно зарядить током в 1550мА.
• Li-Ion аккумулятор НЕ ЗАРЯЖАЕТСЯ при минусовой температуре, но достаточно спокойно относится к работе на морозе с небольшой потерей емкости. Т.е. зарядили аккумулятор дома, пошли, — поработали на улице, потом, опять, принесли заряжать аккумулятор домой. Это утверждение вы можете проверить в действии на вашем смартфоне или фотоаппарате/видеокамере, — там стоит такой же литиевый аккумулятор, только в другом типоразмере.
• Незащищенные аккумуляторы нельзя паять. Если вы хотите собрать из отдельных аккумуляторов большую батарею,
то следует учитывать, что Li-Ion аккумуляторы очень не любят перегрева, а при попытке припаять провод к контакту аккумулятора вы, скорее всего, его перегреете.
Поэтому собирают аккумуляторные батареи с помощью контактной сварки и специальной ленты.
Опять же, для обслуживания такой батареи вам понадобится контроллер,
который будет следить за процессами заряда-разряда аккумуляторов.
Но, перейдем от теории к практике и попробуем дать ответы на самые распространенные вопросы, которые возникают у покупателей при выборе Li-Ion аккумулятора.
1. Защищенный или нет.
Как мы уже говорили, Li-Ion аккумуляторы должны работать в диапазоне напряжений 4,2-2,5В. Для того, чтобы в процессе работы напряжение на АКБ не выходило за пределы этого диапазона на минусовой контакт незащищенного Li-Ion АКБ (их еще называют «ячейка») ставят небольшую электронную плату защиты (зачастую, она именуется просто «защита»).
Именно эта плата обеспечивает работу ячейки в допустимом диапазоне напряжений, предохраняет от перегрузки по току и от короткого замыкания.
Плата защиты приваривается стальной лентой к контактам аккумулятора
и весь этот «бутерброд», упаковывается в термо-пленку с обозначение бренда и емкости (как реальной так и совершенно бредовой, в некоторых случаях).
Из-за платы защищенные аккумуляторы на пару миллиметров длиннее своих незащищенных сородичей и на 0,5 мм толще.
А, так как, качественная Li-Ion ячейка имеет длину 65мм, то защищенный Li-Ion АКБ вырастает в длине до 68-70мм. Такие аккумуляторы могут обозначаться типоразмером 18700 (где первые две цифры это диаметр в мм., а вторые две- длина). Это надо учитывать при выборе аккумулятора, — сможет ли такой аккумулятор влезть, к примеру, в ваш фонарь или зарядное устройство.
PS. На некоторых зарядных устройствах для Li-Ion аккумуляторах производители заранее указывают, что их продукт может заряжать аккумуляторы типоразмера вплоть до 18700.
Защищенные аккумуляторы можно применять в любых устройствах, которые расчитаны на работу с Li-Ion источниками питания и не имеют встроенного контроллера заряда-разряда. В настоящее время основными потребителями защищенных АКБ являются светодиодные фонари, так как именно такие аккумуляторы способны обеспечить питанием мощные светодиоды в течении продолжительного времени.
Так же, защищенные аккумуляторы находят все большее распространение в разнообразной маломощной бытовой электронике, которая работает от одного-двух АКБ.
При необходимости собрать более серьезный источник питания прибегают к изготовлению аккумуляторных батарей. Тут уже в ход идут только незащищенные аккумуляторы.
Такие батареи стоят в большинстве современных ноутбуках, в электроинструменте, фото-видео технике, электровелосипедах и т.д. Управляет такими батареями специальный контроллер, который следит за напряжением на каждом отдельном аккумуляторе в батарее и необходимости в индивидуальных платах защиты нет.
Подитог: если у вас светодиодный фонарь, с вероятностью 99% вам необходим защищенный аккумулятор. Если вы хотите отремонтировать батарею в ноутбуке или в шуруповерте или просто вам нужна БАТАРЕЯ из LI-Ion аккумуляторов, то вам необходимы именно незащищенные АКБ.
Часть 2
За последний десяток лет литий-ионные аккумуляторы из дорогостоящей экзотики перешли в разряд самых распространенных источников автономного питания. Неудивительно, что они стали популярными и в руках самодельщиков, в том числе и начинающих. Иногда от технических решений в их творениях волосы становятся дыбом – ведь особенностью аккумуляторов данного типа является их повышенная опасность, в первую очередь – пожарная. Мой рассказ о том, как правильно «готовить» эту «рыбу фугу», чтобы никто не сгорел и не взорвался.
Предыдущая статья на «взрывную» тему здесь.
Принцип работы литий-ионнного аккумулятора.
Знаете, почему нельзя заряжать обычные батарейки? Казалось бы, при протекании тока в зарядном направлении, на электродах будут идти процессы «в обратном порядке»: на отрицательном электроде будет осаждаться цинк, а на положительном – активная масса, бывшая когда-то двуокисью марганца и отдавшая свой кислород, будет снова окисляться, вновь превращаясь в свежую MnO2. Но все портит то, что одновременно с этими процессами разлагается и вода в электролите. Выделяющиеся газы раздувают корпус батарейки и выдавливают электролит наружу с печальными последствиями для аппаратуры.
В этом направлении работали и за рубежом, и кое-чего даже добились, применяя механически более прочные керамические сепараторы, особые методы заряда, специальные добавки в электролит. Но все равно опасность дендритообразования сохранялась – слишком опасным был такой аккумулятор для его практического применения, если превышал размеры и емкость крохотной часовой батарейки-таблетки.
Прорыв принесли два открытия. Первое – это обнаружение способности некоторых сложных оксидов и сульфидов, содержащих литий, отдавать и поглощать обратно ионы лития на катоде. Второе – способность соединений слоистой структуры (графит, дисульфид молибдена) обратимо поглощать в межслоевое пространство значительные количества лития (вплоть до соединения состава LiC6), захватывая его атомы немедленно после разрядки ионов Li + на аноде и предотвращая его выделение в металлической форме, а значит, предотвращая образование дендритов. За эти открытия и изобретение литий-ионного аккумулятора в прошлом году была присуждена Нобелевская премия. Ее лауреаты – М.С. Уиттингем, первооткрыватель явления интеркаляции лития в дисульфиды титана и молибдена, впервые предложивший использовать это явление в аккумуляторах, Дж. Гуденаф, исследовавший обратимость поглощения и выделения ионов лития кобальтитом лития на катоде, и собственно, изобретатель литий-ионного аккумулятора Акира Ёсино.
Принцип работы литий-ионного аккумулятора Акиры Ёсино, изобретенного им в 1991 году, состоит в следующем. Однозарядные катионы лития – это практически единственный ион, переносящий ток в органическом неводном электролите. Противоионом является громоздкая и малоподвижная молекулярная «конструкция», обладающая отрицательным зарядом.
Ион Li+ при зарядке аккумулятора разряжается на поверхности графитового анода, превращаясь в нейтральный атом лития. Этот атом немедленно вступает поглощается графитом, проникая между слоями его кристаллической решетки. Образуется графитид лития – так называемый интеркалят или соединение внедрения. По своим химическим свойствам это сильный и активный восстановитель.
Одновременно с этим, кобальтит лития на катоде поставляет в раствор ионы лития, а сам при этом, теряя литий, все больше по составу приближается к двуокиси кобальта, в результате чего становясь сильным и активным окислителем.
Разность электрохимических потенциалов между этими окислителем и восстановителем равна ЭДС литий-ионного аккумулятора.
При разряде происходят обратные процессы. Литий, покидая межслоевое пространство на аноде, отдает во внешнюю цепь электрон и приобретает заряд, становясь катионом, а графитид лития – просто графитом. На катоде эти катионы возвращается в вакансии кристаллической решетки кобальтита лития, который теряет свои окислительные свойства, принимая электрон во внешнюю цепь.
Из-за отсутствия побочных процессов данная электрохимическая система обладает весьма высокой степенью обратимости и по этой причине характеризуется прекрасным КПД.
Литий-полимерные аккумуляторы не являются, как многие думают, каким-то отдельным видом аккумуляторов. В них вместо жидкого электролита используется гелеобразный на полимерной основе, а все электрохимические процессы в них ничем не отличаются. Отсутствие (вернее, минимальное количество) жидкого электролита позволяет придавать им практически любую форму и вместо прочного металлического корпуса помещать их в корпуса из полимерной пленки в виде запаянного пакетика, что помимо прочего повышает плотность хранения энергии.
Существуют также разновидности литий-ионных аккумуляторов с различными электрохимическими системами, такие, как литий-железофосфатные и литий-титанатные. Принцип действия у них тот же самый, но иные материалы катодной массы и, соответственно, другие напряжения. Удельная емкость этих аккумуляторов ниже, чем у классической кобальтовой литий-ионной системы, но они превосходят их по сроку службы, способности отдавать ток при низких температурах и, по утверждению производителей – по безопасности.
Собственно, безопасность – едва ли не основная «беда» литий-ионных аккумуляторов.
Скрытая угроза
Увы, «укротив» литий, Акира Ёсино не сделал этого огненного льва безобидным мышонком. Да и как можно ожидать полной безопасности от устройства, в котором, повторюсь, сильный и активный окислитель соседствует с столь же сильным и активным восстановителем и разделяют их лишь несколько десятков микрон пористой полимерной пленки-сепаратора? Стоит этой пленке где-нибудь прохудиться, допустив короткое замыкание, лавинообразный процесс саморазогрева и саморазрушения уже не остановить. Содержимое аккумулятора превращается во взрывчатую смесь горючего и окислителя. И эту смесь уже подожгли.
То, что литий-ионные аккумуляторы обычно не взрываются, обусловлено множеством предосторожностей, которые соблюдаются при их эксплуатации. Соблюдаются не силами пользователя – за этим следят автоматические электронные устройства. Там, где применяется литий-ионный аккумулятор, нет места простейшим зарядным устройствам из мира «свинца» и «никель-кадмия». Зарядное устройство обязано быть «умным». Процесс заряда литий-ионного аккумулятора многостадийный, требует строгого выдерживания параметров и должен быть вовремя завершен, и перекладывать ответственность за это на пользователя категорически недопустимо, так как его забывчивость в таком случае может привести к пожару или взрыву.
Дело в том, что отсутствие побочных процессов в литий-ионном аккумуляторе не абсолютно. Для того, чтобы их не было, нужно не выйти за определенную «безопасную» территорию. Так, при напряжении выше 4,2..4,5 В или при слишком большом токе заряда графит уже не успевает «впитать» литий, и он образует металлическую фазу. То же происходит, если графит теряет активную поверхность, что происходит, например, из-за переразряда. Как только на поверхности появляется металл, он начинает образовывать дендриты и… можно вызывать пожарных. Наконец, перенапряжение может вызвать электролиз компонентов электролита (в том числе и неконтролируемых примесей) и выделение газов, давление которых может нарушить герметичность аккумулятора, что также чревато пожаром – соединение внедрения лития в графит самовоспламеняется на воздухе.
Опасна и перегрузка при разряде. Перегрев разрядным током может вызвать вскипание или термическое разложение электролита, выделение кислорода из катодной активной массы, повреждение сепаратора. Результат тот же: КЗ и пожар. К тому же эффекту приведет и механическое повреждение аккумулятора.
Является «правилом хорошего тона» не полагаться на надежность зарядного устройства. В абсолютном большинстве промышленно выпускающихся устройств (за исключением «маргинальных» случаев вроде электронных сигарет и авиамоделей), содержащих литий-ионные аккумуляторы, независимо от контроллера, на который возложены функции заряда, имеется еще один контроллер, выполняющий функции защиты. В простейшем своем варианте (например, на микросхеме DW01A, являющейся основой плат защиты почти всех китайских аккумуляторов), он отключает аккумулятор при перезаряде (превышении допустимого напряжения), переразряде, слишком большом зарядном и разрядном токе, перегреве. В более сложных случаях к этим базовым функциям добавляется балансировка батареи (если она состоит из нескольких элементов, соединенных последовательно), контроль за ее «здоровьем», подсчет ампер-часов при заряде и разряде (что позволяет определить оставшийся процент заряда гораздо точнее, чем при простом измерении напряжения) и другие функции. Данный контроллер – его называют Battery management system (BMS) или просто «платой защиты», как правило, является неотделимой частью аккумуляторной батареи, находясь с ней в одном корпусе и будучи наглухо припаянным к его выводам.
Есть еще третья ступень защиты. Это механическое устройство, разрывающее цепь при повышении давления или температуры внутри «банки» аккумулятора. К сожалению, оно – не панацея, так как во многих случаях нагрев и газовыделение начинаются уже после того, как возгорание батареи уже нельзя остановить.
Видео и фотографии взрывов и возгораний литий-ионных аккумуляторов в сети можно найти много. Надеюсь, они убедят вас, что все более чем серьезно.
Заряжаем и разряжаем правильно
А теперь разберемся с тем, как правильно заряжать эти опасные литий-ионные аккумуляторы, чтобы они не были так опасны.
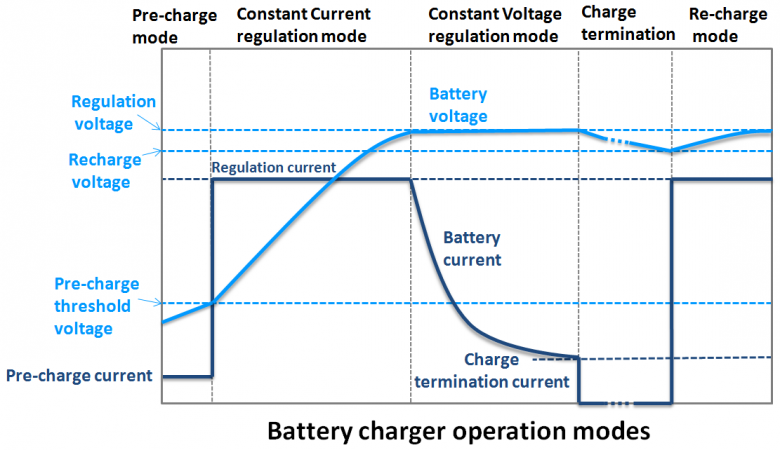
Общепринятым, рекомендуемым всеми производителями литий-ионных аккумуляторов, является алгоритм CC-CV. Это означает, что начинается заряд стабилизированным током, а при достижении определенного напряжения далее оно стабилизируется на этом уровне. Этот метод близок к методу заряда свинцовых аккумуляторов, отличаясь от него лишь режимом.
Для большинства стандартных литий-ионных аккумуляторов напряжение перехода от стадии CC к стадии CV при комнатной температуре – 4,20 В. Некоторые старые аккумуляторы с анодом на основе каменноугольного кокса следует заряжать лишь до 4,10 В, тогда как в последнее время все чаще встречаются «высоковольтные» аккумуляторы, которые допускают заряд до 4,35 и даже 4,45 В. Небольшое превышение этого напряжения вызывает резкое сокращение срока службы, а более значительное превышение приводит к возгораниям и взрывам. Требуемая точность установки порогового напряжения для стандартных аккумуляторов составляет ±50 мВ, а у «высоковольтных» тем выше, чем выше напряжение, вплоть до ±5 мВ при пороговом напряжении 4,45 В. Разумеется, пониженное напряжение приводит лишь к снижению доступной емкости, а вот повышение напряжения недопустимо ни при каких случаях.
Стандартным током заряда считается 0,5С и большинство аккумуляторов без ущерба позволяют заряжать их током до 1С, а некоторые допускают и более высокие токи при условии недопущения перегрева. С здесь – ток в амперах, численно равный емкости в ампер-часах. Но таким током нельзя заряжать глубоко разряженные аккумуляторы, напряжение на клеммах которых снизилось ниже 2,9-3,0 В. В этом случае необходима стадия предварительной зарядки (precharge) – аккумулятор заряжается током 0,05-0,1С, пока напряжение не достигнет трех вольт. А вот слишком глубоко разряженные аккумуляторы заряжать нельзя вообще. Зарядное устройство должно не допускать зарядки аккумулятора, если напряжение на его клеммах снизилось ниже 2,5 В. При таком глубоком разряде аккумулятор обычно сильно теряет в емкости, но это еще полбеды: его заряд сопряжен с опасностью металлизации лития и возгорания. Кстати, «высоковольтные» аккумуляторы более чувствительны к глубокому разряду, и не следует допускать их разряда ниже 2,75 В.
На стадии CV ток снижается по экспоненте. На этой стадии аккумулятор не должен оставаться до бесконечности. Заряд должен быть автоматически прекращен после снижения тока до 0,05-0,1С.
Как крайний случай, можно заряжать литий-ионные аккумуляторы током 0,1С до достижения 4,10..4,15 В с последующей отсечкой. Но, по некоторым данным, предположительно, такой режим плохо сказывается на токоотдаче и сроке службы аккумуляторов.
Балансировка
Процесс заряда осложняется, если мы имеем дело с батареей из последовательно соединенных элементов. Дело в том, что двух одинаковых аккумуляторов не бывает. Если емкость одного из них будет чуть больше, а другого – чуть меньше, напряжение на последнем будет расти быстрее, чем на первом. В таком случае, если мы будем заряжать батарею до 8,40 В, этот аккумулятор окажется в итоге немного перезаряженным. Со временем эти небольшие перезаряды приведут к более быстрому износу, а значит, напряжение на этом аккумуляторе будет завышаться с каждым разом все сильнее. Возникает «снежный ком» нарастающей разбалансировки батареи, который может закончиться взрывом.
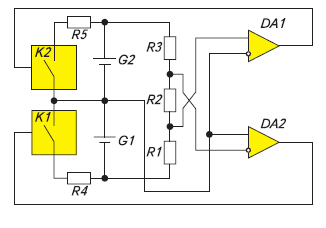
Чтобы этого не допустить, необходимо контролировать напряжение не только всей батареи, но и каждого элемента в отдельности, не допуская превышения напряжений каждого из них. Обычно применяются те или иные схемы балансировки, шунтирующие «опережающие» элементы во время заряда, когда те достигают максимального напряжения. Это так называемые пассивные схемы балансировки. Очевидно, при их работе часть энергии рассеивается в виде тепла, что существенно снижает КПД зарядки и ухудшает тепловые условия внутри аккумуляторной сборки. Более эффективными и лучше использующими емкость являются методы активной балансировки, обеспечивающие перекачку энергии с клемм уже зарядившейся «банки» к еще недозаряженным.
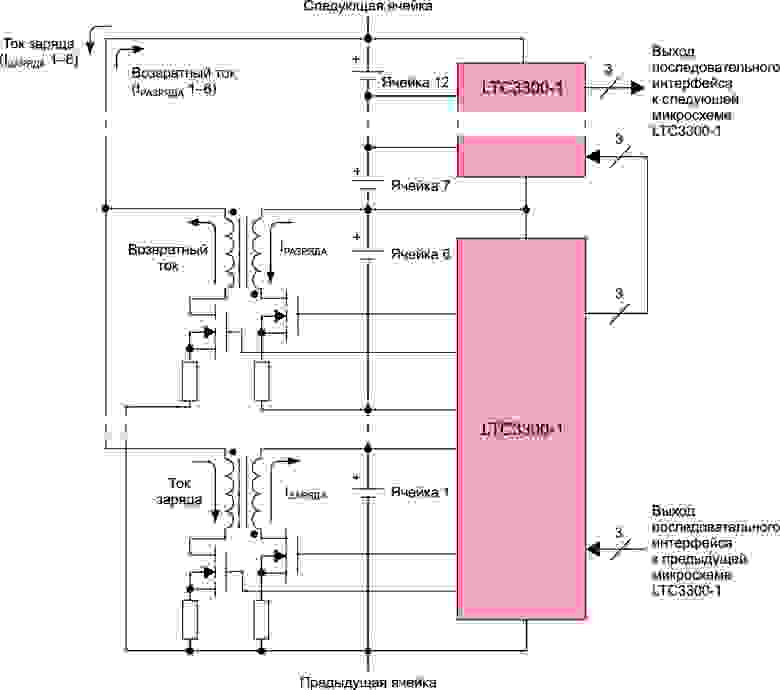
В настоящее время распространение получили интеллектуальные системы балансировки, лучше использующие емкость аккумуляторов за счет компромиссного распределения зарядного тока, которое определяется реальными емкостями каждого из элементов, измеренными в предыдущих циклах.
Как обращаться, хранить, куда девать остатки
Исходя из вышесказанного, обращаться с литий-ионными аккумуляторами следует с осторожностью. Опасность возгорания и взрыва возникает при неправильном заряде, коротком замыкании и механических повреждениях. Последнее особенно актуально для литий-полимерных аккумуляторов, лишенных прочного защитного корпуса. Случайно или намеренно проколов или разорвав пленку, защищающую аккумулятор, вы можете уже через 10-15 секунд получить у себя в руках ослепительный красный огонь. Это же может случиться при изгибе и сдавливании аккумулятора, а в особенности, если каким-либо инструментом проткнуть его насквозь. Такое случается при попытках извлечь аккумулятор, приклеенный на двусторонний скотч, из мобильного телефона для его замены на новый. Риск снижается при извлечении разряженного аккумулятора, поэтому это следует сделать перед началом работы. По этой же причине, а также по причине того, что при замыкании он может выдать десятки, если не сотни ампер тока, хранить такие аккумуляторы следует надежно и аккуратно упакованными, а не в куче радиохлама.
Вообще перед хранением эти аккумуляторы следует довести до уровня заряда 30-50%. Хранить их следует при комнатной температуре. А то некоторые «специалисты» утверждают, что их нужно держать в холодильнике. Не нужно. А вот старые, убитые и особенно вздувшиеся аккумуляторы хранить ни в коем случае нельзя, от них нужно избавиться как можно скорее, так как они непредсказуемы и могут в любой момент стать причиной пожара.