лимфоцитарная инфильтрация и фиброз шейки матки что это
Клинико-морфологические параллели при доброкачественных заболеваниях шейки матки
| Среди гинекологических заболеваний доминирующее положение занимают доброкачественные, в том числе и предраковые, заболевания шейки матки. Многочисленные исследования, раскрывающие вопросы этиологии и патогенеза заболеваний шейки матки, до настоящего времени не позволили окончательно решить эти проблемы. Неоднозначны взгляды на вопросы лечения и профилактики этой патологии. |
В литературе имеются указания на высокое содержание в подэпителиальных тканях лимфоцитов, в том числе киллеров [2, 3], роль которых при доброкачественных процессах шейки матки окончательно не выяснена.
Если этиологический фактор эпителиальной дисплазии в литературе получил достаточно широкое освещение, то в отношении псевдоэрозии шейки матки такой ясности нет. Отсутствие четкой кольпоскопической картины предраковых процессов шейки матки затрудняет их клиническую диагностику, выбор места биопсии и своевременное лечение [1, 4, 8, 10].
Целью работы явилась сравнительная оценка клинических проявлений и патоморфологических изменений при доброкачественных заболеваниях шейки матки, выявление этиологических и патогенетических механизмов в развитии фоновых и предраковых заболеваний шейки матки.
Всем больным были выполнены расширенная кольпоскопия и прицельная биопсия шейки матки. Всего было взято 116 биоптатов. Патоморфологическое исследование проводилось в серийных срезах с окраской препаратов гематоксилином и эозином, по Папаниколау, Паппенгейму, гистохимическими методами. Препараты исследовали под увеличением до 1200 раз. Проведен сравнительный анализ результатов клинических и патоморфологических исследований. В последующем всем больным было проведено криохирургическое лечение выявленных патологических изменений шейки матки.
Результаты и их обсуждение
Таким образом, проведенное кольпоскопическое исследование показало, что в процессе заживления псевдоэрозии шейки матки формируется патологическая зона, характеризующаяся выраженным полиморфизмом.
После выполненной в прошлом диатермокоагуляции и лазеровапоризации псевдоэрозии у 21 женщины железистые структуры под многослойным плоским эпителием были обнаружены вновь, что свидетельствует о неэффективности проведенного лечения. У 1 женщины после криодеструкции шейки матки железистые структуры отсутствовали.
Следует отметить, что из 31 женщины с выявленной патологией верхнего отдела полового аппарата у 15 диагностировано вирусное поражение шейки матки, у 27 лимфоцитарная инфильтрация в строме.
Поскольку выявление вирусных телец в эпителиальных клетках при патоморфологическом исследовании биопсированных тканей представляет большие трудности, следует предположить, что они в исследованном материале обнаружены не во всех случаях. Тем не менее сопутствующая вирусной инвазии лимфоцитарная инфильтрация стромы, легко выявляемая при исследовании, может служить индикатором вирусного поражения.
Таким образом, кольпоскопическую картину эндоцервикоза в стадии завершенной эпидермизации не следует интерпретировать как выздоровление.
При кольпоскопической картине, характеризовавшейся усилением сосудистого рисунка и наличием атипических сосудов в зоне перекрытия, морфологически ЦИН диагностирована у 8 из 15 больных, причем во всех случаях усиление сосудистого рисунка и атипические сосуды сопутствовали картине вирусного цервицита.
Таким образом, полученные результаты свидетельствуют о том, что для ЦИН характерны кольпоскопические картины основы лейкоплакии, полей, открытых протоков желез с эпидермизацией в зоне перекрытия, лейкоплакии. Наличие кистовидно расширенных желез в зоне перекрытия не характерно для ЦИН, тем не менее, у 1 (2,38%) больной из 42 она была выявлена в стенке такой железы.
У большинства больных ЦИН находилась в краях псевдоэрозии в зонах стыка различных типов эпителия.
1. Клиническая картина доброкачественных заболеваний шейки матки, определяемая кольпоскопическим методом, не всегда отражает истинный характер патологического процесса. Невозможна клиническая диагностика предраковых заболеваний (цервикальная интраэпителиальная неоплазия). Вероятность ЦИН наиболее высока при кольпоскопической картине основы лейкоплакии, лейкоплакии, полей, открытых протоков желез с их эпидермизацией.
2. Любые изменения шейки матки, выявленные при расширенной кольпоскопии, требуют биопсии с патоморфологическим уточнением диагноза.
3. Кольпоскопическая картина эндоцервикоза в стадии завершенной эпидермизации патоморфологически представляет собой сложный патологический процесс, включая ЦИН, и не может считаться состоянием выздоровления.
4. Подтверждены данные литературы о том, что этиологическим фактором ЦИН и лейкоплакии является вирусное поражение тканей шейки матки. Индикатором его может служить лимфоцитарная инфильтрация стромы, диагностируемая при патоморфологическом исследовании.
5. Можно предположить, что одним из этиологических факторов псевдоэрозии шейки матки (эндоцервикоза) может быть вирусная инвазия, приводящая к дегенерации многослойного плоского эпителия шейки матки, замещению его цилиндрическим эпителием цервикального типа с пролиферативными процессами в нем и образованием железистых структур.
Хронический эндометрит: от совершенствования диагностического подхода к оптимизации лечения
Хронический эндометрит (ХЭ)— клинико-морфологический синдром, при котором в результате персистирующего повреждения эндометрия инфекционным агентом возникают множественные вторичные морфофункциональные изменения, нарушающие циклическую трансформ
Хронический эндометрит (ХЭ)— клинико-морфологический синдром, при котором в результате персистирующего повреждения эндометрия инфекционным агентом возникают множественные вторичные морфофункциональные изменения, нарушающие циклическую трансформацию и рецепторный статус слизистой оболочки тела матки.
С позиций общей патологии течение инфекции с тенденцией к хронизации можно было бы отнести к «синтаксическим» вариантам, при которых биосистема «…предпочитает существовать с патогеном, активное отторжение которого сопряжено с большими трудностями, энергетически не выгодно или вообще нереально в силу специфики пускового фактора». Наиболее устоявшейся на сегодняшний день является точка зрения о возникновении ХЭ в результате дисбаланса между гормональной и иммунной системами организма, с одной стороны, и патогенами— представителями микробиоценоза, с другой.
В современных условиях ХЭ характеризуется рядом особенностей: изменением этиологической структуры с увеличением значимости вирусной и условно-патогенной флоры, ростом резистентности флоры к фармакотерапии, трансформацией клинической симптоматики в сторону стертых форм и атипичного течения, длительными сроками терапии и ее высокой стоимостью. В 95% случаев эндометрит является экзогенным (первичным), вызванным штаммами микроорганизмов, передающихся половым путем, а также возникающим после внутриматочных лечебных и диагностических манипуляций. Лишь в 5% случаев эндометрит является вторичным и развивается при попадании инфекции из экстрагенитальных очагов гематогенным, лимфогенным или нисходящим путем. «Интегральными» возможно назвать клинические классификации ХЭ (C. Buckley, H. Fox (2002) и T.C.Michels (1995)). Согласно им выделяют специфический (обусловленный бактериальной флорой, вирусами, грибами, хламидиями, микоплазмами) и неспецифический варианты ХЭ, при котором специфическая флора из эндометрия не выделяется.
Поддержание стерильности эндометрия за счет циклического отторжения функционального слоя во время менструации на протяжении нескольких десятилетий заставляло исследователей сомневаться в существовании хронической формы эндометрита. В дальнейшем было доказано вовлечение в хронический воспалительный процесс не только функционального, но и не отторгающегося базального слоя эндометрия.
Изучение микробного пейзажа эндометрия имеет сравнительно недолгую историю. Факт персистирования микоплазмы в эндометрии упоминается впервые в работе Koren Z. (1978). В эндометрии обнаружена персистенция более 20 видов микроорганизмов условно-патогенной группы. Всего выделено 129 штаммов, в том числе облигатные анаэробы— 64% (бактероиды, эубактерии, пептострептококки, клостридии), микроаэрофилы— 31,8% (генитальные микоплазмы и дифтероиды), факультативные анаэробы— 12%. Только у 14% женщин выделены монокультуры, у остальных обнаружены ассоциации 2–6 видов микроорганизмов. Вполне возможно, что антиген персистирующей инфекции «запускает» иммунный ответ с реакцией гиперчувствительности замедленного типа. Из числа обследованных нами пациенток с предшествующими неудачами экстракорпорального оплодотворения (ЭКО) и морфологически подтвержденным ХЭ у 76% при микробиологическом исследовании содержимого полости матки был выявлен возбудитель инфекционного процесса (Enterococcus fecalis— 20%, Staphylococcus epidermidis— 28%, Staphylococcus spp. — 16%, Ureaplasma urealyticum— 24%, вирус простого герпеса (ВПГ)— 12%, цитомегаловирус (ЦМВ)— 8%, в большинстве случаев наблюдались ассоциации микроорганизмов), у 24% пациенток проведенное исследование не позволило выявить возбудителя.
Защитные механизмы при внутриматочной инфекции делят на специфические и неспецифические. Среди неспецифических антимикробных механизмов, действующих на клеточном уровне, следует отметить фагоцитоз с помощью макрофагов и полиморфноядерных лейкоцитов. Неспецифические гуморальные факторы включают белок плазмы трансферрин, связывающий железо, необходимое для роста многих бактерий; опсонины, усиливающие фагоцитарную активность клеток; лизоцим цервикальной слизи, бетализин, выделяющийся тромбоцитами в очаге воспаления. К специфическим факторам защиты относят: Т-лимфоциты, иммуноглобулины. Однако, несмотря на достаточно четкие представления о секреторной иммунной системе слизистых оболочек пищеварительного тракта и дыхательных путей, сведения об иммунной системе эндометрия и ее значении для женских половых путей остаются немногочисленными.
Широко освещен в литературе вопрос факторов риска развития ХЭ. По нашим данным, наиболее значимыми (р
Е. Б. Рудакова, доктор медицинских наук, профессор А. А. Лузин, О. Н. Богданова, С. И. Мозговой, кандидат медицинских наук, доцент, О. А. Лобода, М. А. Пилипенко, О. М. Бурова ОмГМА, ОмОКБ, ОмЦРМ, Омск.
Лимфоцитарная инфильтрация и фиброз шейки матки что это
Комплексное иммуногистохимическое исследование экспрессии специфических иммунологических маркеров хронического эндометрита (натуральных киллеров CD56 и CD16, B-клеток (CD20), плазматических клеток (CD138) и активированных лимфоцитов (HLA-DR), позволяющее провести более точную диагностику и спрогнозировать течение процесса, оценить эффективность проводимой терапии и провести ее коррекцию.
Иммуногистохимическое исследование биоптата эндометрия.
Синонимы английские
Immunohistochemical analysis of endometrial biopsies.
Какой биоматериал можно использовать для исследования?
Образец ткани (в парафиновом блоке).
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Иммуногистохимия – это метод исследования тканей и клеток, основанный на обнаружении специфических антигенов с помощью присоединения к ним антител, меченных флюорохромом или ферментом. Антигены – молекулы белков или углеводов, имеющие уникальную трёхмерную структуру, способные индуцировать образование антител. Антитела – это иммуноглобулины, распознающие антигены и присоединяющиеся к ним во время реакции «антиген-антитело». Антигены и антитела – это молекулы, неразличимые при исследовании методом световой и электронной микроскопии. Для обнаружения специфических антигенов к образцу ткани или клеток добавляют реагент, содержащий меченные флюорохромом или ферментом антитела, в результате чего образуется иммунный комплекс «антиген-антитело». Комплексы формируют специфическое окрашивание тканей и клеток, обеспечивая детекцию патологических изменений на молекулярном уровне. Иммуногистохимическое исследование позволяет верифицировать онкологические заболевания, метастатические поражения, определить их гистологический подтип, экспрессию биомаркеров, определяющих прогноз заболевания и схему лечения.
Эндометрий – это слизистая оболочка, выстилающая полость матки изнутри, необходимая для имплантации оплодотворенной яйцеклетки и развития плаценты во время беременности. Он подвергается динамическим структурным и функциональным изменениям во время менструального цикла под действием женских половых гормонов. Для исследования эндометрия в фазе пролиферации материал для исследования забирается с 5 до 14 день менструального цикла. Пролиферативная фаза прекращается в момент овуляции, когда зрелая яйцеклетка выходит из фолликула яичника в маточную трубу. Под действием гормона желтого тела яичника – прогестерона приостанавливается рост желез эндометрия и стромы, начинается секреторная фаза, характеризующаяся образованием вакуолей секретом в клетках желез (15-18 день). Позже секрет выделяется в просвет желез, формируется гипертрофия стромальных клеток, появляются видимые спиральные артериолы. Морфологические изменения сопровождаются небольшой нейтрофильной и лимфоцитарной инфильтрацией.
Ряд патологических состояний нарушает нормальное циклическое функционирование эндометрия у женщин репродуктивного возраста. Наиболее распространенными причинами считаются хронический эндометрит, полипы эндометрия, ановуляция и миома матки.
Хронический эндометрит – это воспалительное заболевание эндометрия, чаще поражающее женщин репродуктивного возраста, но встречающееся и в постменопаузе. Факторами риска являются воспалительные заболевания органов малого таза, внутриматочные контрацептивы (спирали), хирургические манипуляции в полости матки (выскабливание), недавняя беременность. Возбудителями заболевания чаще всего являются Chlamydia trachomatis, Neisseria gonorrhoeae, Streptococcus agalactiae, Mycoplasma hominis и различные вирусы. Наиболее распространенный симптом – маточные кровотечения, не связанные с менструацией. Кроме того, хронический эндометрит может быть причиной бесплодия и самопроизвольного прерывания беременности.
Золотым стандартом диагностики хронического эндометрита является гистологическое исследование биоптата эндометрия. Главным маркером является инфильтрация стромы эндометрия плазматические клетками (CD138). Также часто обнаруживаются и другие воспалительные элементы: нейтрофилы (обычно в поверхностном эпителии и железах), субэпителиальные лимфоцитарные инфильтраты, гистиоциты с гемосидерином и редкие эозинофилы.
Поскольку эпизодические плазматические клетки обнаруживаются и в поздней секреторной фазе, и в строме полипов эндометрия, их присутствие не всегда означает инфекционную этиологию. В очень редких случаях обнаружение плазматических клеток в биоптате эндометрия может свидетельствовать о лимфопролиферативном заболевании.
Для дифференциальной диагностики используется метод иммуногистохимии, позволяющий определить маркеры хронического эндометрита на молекулярном уровне и идентифицировать воспалительные клетки (плазматические клетки CD138), натуральные киллеры CD56 и CD16, B-клетки (CD20) и активированные лимфоциты (HLA-DR).
При верификации диагноза назначается специфическая антибактериальная терапия. По результатам исследования можно оценить эффективность проводимой терапии, определить показания к ее коррекции.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Исследование назначается при наличии клинико-анамнестических данных и по результатам предварительно проведенного гистологического исследования.
Структуры эндометрия, соответствующие фазе пролиферации, наблюдаемые в физиологических условиях в первую половину 2-фазного менструального цикла могут отражать гормональные нарушения, если их обнаруживают во второй половине цикла (это может указывать на ановуляторный, однофазный цикл или на ненормальную, удлиненную фазу пролиферации с запоздавшей овуляцией при двухфазном цикле), при железистой гиперплазии эндометрия в различных участках гиперплазированной слизистой оболочки матки и при дисфункциональных маточных кровотечениях у женщин в любом возрасте.
Обнаружение специфических маркеров (натуральных киллеров CD56 и CD16, B-клеток CD20), плазматических клеток (CD138) и активированных лимфоцитов (HLA-DR) в биоптате эндометрия в пролиферативную фазу свидетельствует о хроническом эндометрите.
Кто назначает исследование?
1) Techniques of immunohistochemistry: principles, pitfalls, and standardization. Richard W. Cartun, Clive R. Taylor and David J. Dabbs. Diagnostic Immunohistochemistry, Chapter 1, 1-46.
2) Benign Endometrium. David W Kindelberger and Marisa R Nucci. Gynecologic Pathology: A Volume in the Series: Foundations in Diagnostic Pathology, Chapter 6, 197-232.
3) The Female Genital Tract. Lora Hedrick Ellenson and Edyta C. Pirog. Robbins and Cotran Pathologic Basis of Disease, Chapter 22, 991-1042.
4) Immunohistochemical analysis of CD56-positive natural killer cells in the human endometrium. Maja Weber, Bettina Toth, Isabel Santillan, Christin Bär, Ekkehard Schleußner and Udo R. Markert. Journal of Reproductive Immunology, 2016-06-01, Volume 115, Pages 79-80.
5) Genital Tract Infections: Vulva, Vagina, Cervix, Toxic Shock Syndrome, Endometritis, and Salpingitis. Carolyn Gardella, Linda O. Eckert and Gretchen M. Lentz Comprehensive Gynecology, 23, 524-565.
Онкологические аспекты гиперпластических процессов эндометрия
Гиперплазия — это увеличение количества клеток без увеличения их размеров. Гиперпластические процессы могут предшествовать развитию онкологического заболевания. Гиперплазия эндометрия — одна из форм патологических пролиферативных изменений эндометрия, с преимущественной пролиферацией железистого компонента по сравнению со стромальным компонентом [1].
Существует гистологическая классификация гиперпластических процессов эндометрия, предложенная ВОЗ (2014) [2]:
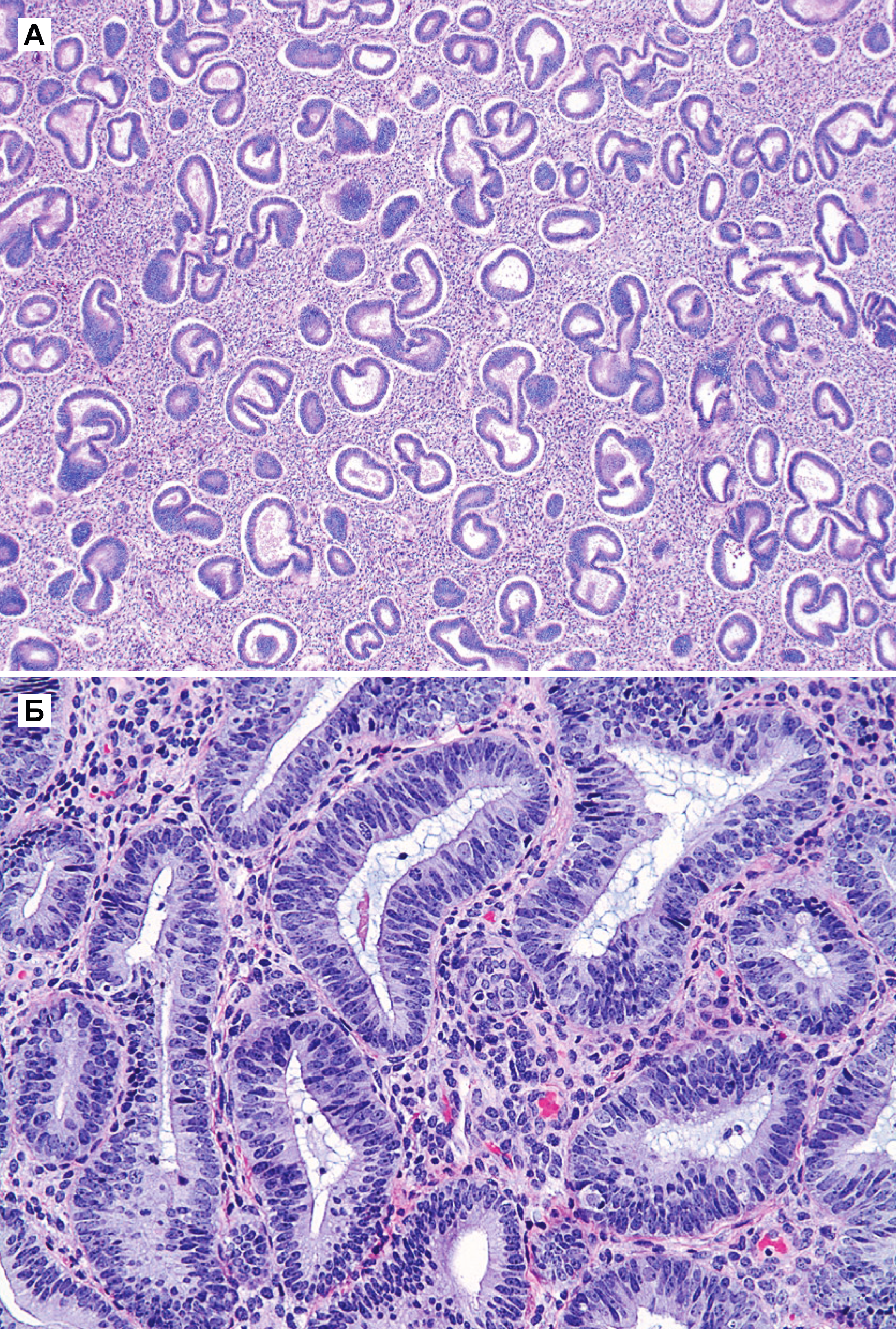
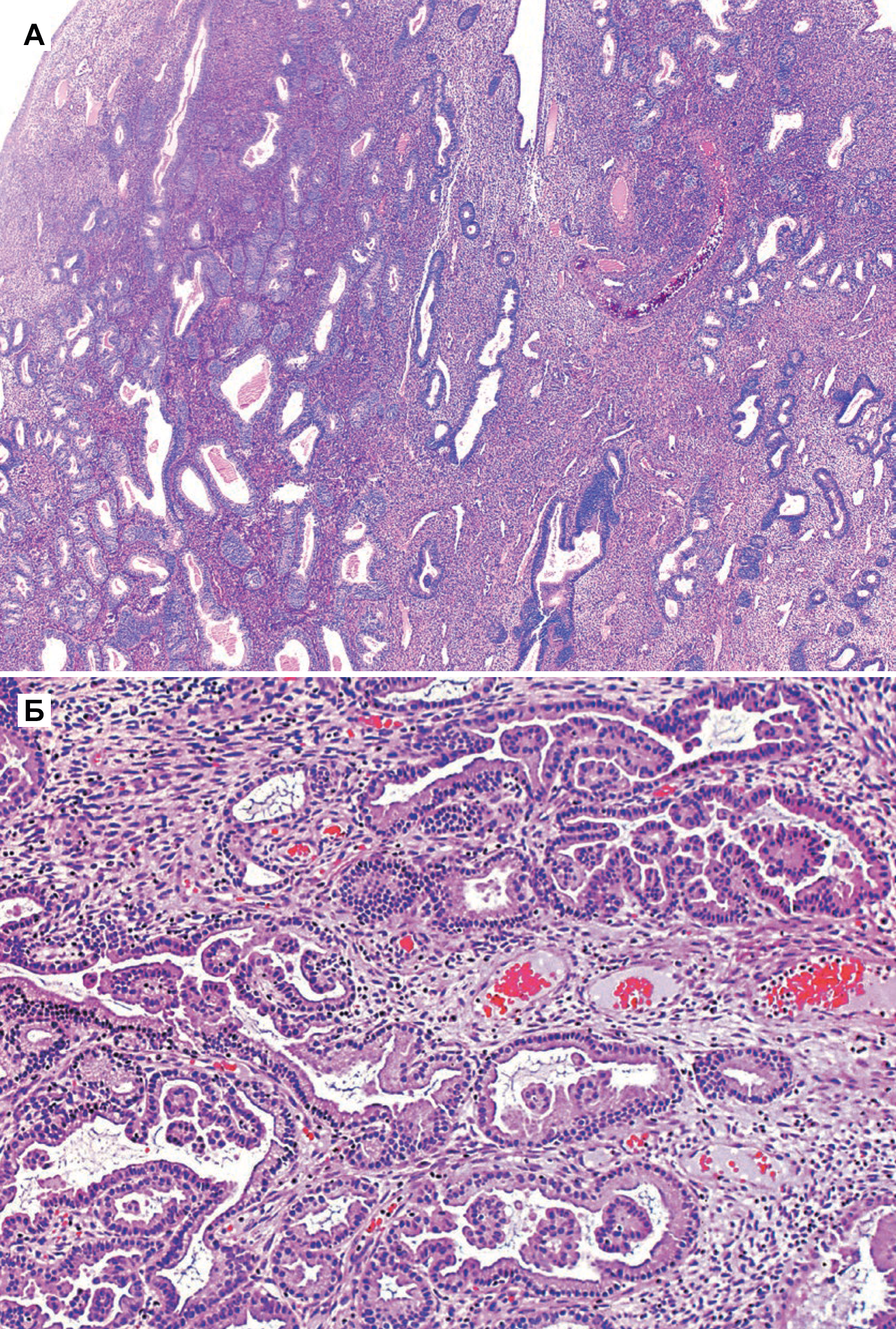
Гиперплазия эндометрия без атипии — это пролиферация с изменением строения желез и клеток, но без клеточной атипии. Изменения в строении обычно видны при малом увеличении, но важной особенностью, которая определяет прогноз и возможность малигнизации — это клеточная атипия. Все типы гиперплазии характеризуются увеличением отношения железы к строме, неравномерностью формы железы и изменением размера железы (рис. 1 а и б). При гиперплазии без атипии железистый эпителий напоминает пролиферирующий эндометрий (рис. 1 б). Клетки столбчатые с амфофильной цитоплазмой и имеют псевдостратифицированные ядра, ориентированы к базальной мембране и имеют овальную форму с гладкими контурами, равномерно распределенный хроматин и небольшие незаметные ядрышки. Митотическая активность может быть переменной и может быть меньше, чем в пролиферирующем эндометрии. Частота митоза не влияет на диагноз [5].
Как правило, гиперплазия диффузная, но может быть очаговой из-за локальных различий в содержании рецепторов эстрогена и прогестерона в эндометрии. При простой гиперплазии присутствует строма в значительном объеме. Строение стромы напоминает нормальное, характерное для пролиферативной фазы, строма состоит из маленьких овальных клеток со скудной цитоплазмой. Как и в железах, в строме отмечена митотическая активность. Когда гиперплазия является полипоидной, строма может содержать артерии с толстой стенкой, подобные тем, которые наблюдаются в полипах. По мере прогрессирования гиперплазии железы располагаются более тесно. Обычно железы плотно прилегают друг к другу, хотя всегда присутствует небольшое количество стромы между ними [5].
К предраковым заболеваниям эндометрия относятся [2]:
Эндометрий — мишень половых гормонов, так как эта ткань имеет специфические рецепторы. Клетки эндометрия обновляются ежемесячно под влиянием гормональной регуляции. Нарушение гормонального статуса женщины может изменять рост и дифференцировку клеток. Поэтому могут возникнуть гиперпластические процессы [2].
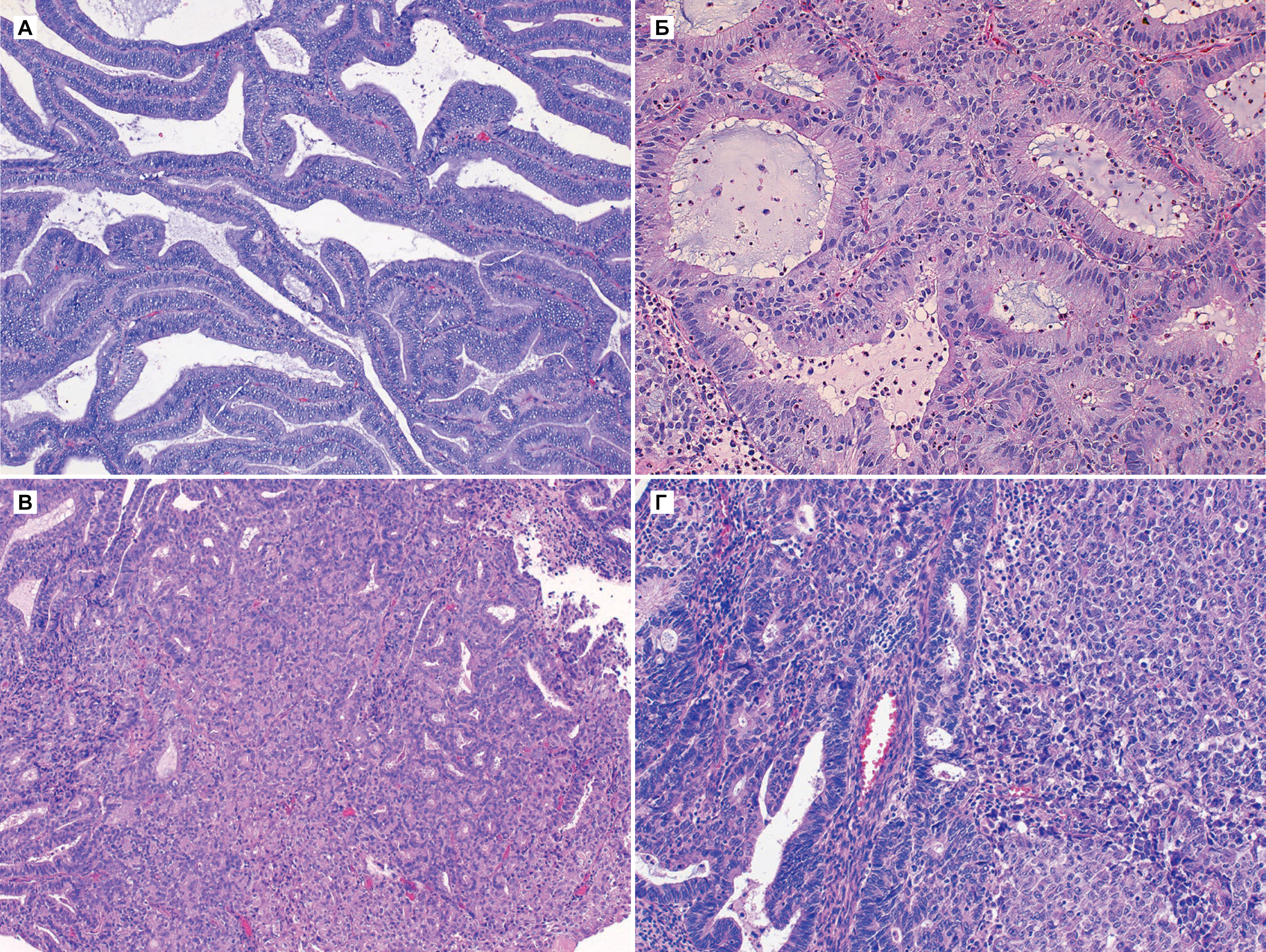
Атипичная гиперплазия отличается наличием ядерной атипии и сложным строением с тесно расположенными железами. Железы обычно неправильной формы и размера. Каждая железа имеет базальную мембрану, окруженную тонким слоем стромы, отделяющей его от соседних желез. Однако в некоторых случаях железы расположены далеко друг от друга. Встречаются как железы без клеточной атипии, так и атипичные [5].
Специфические особенности при атипичной гиперплазии включают: стратификацию, увеличение размера ядер с измененным хроматином и ядрышками. В ядрах отмечена истинная стратификация (2–4 слоя), и потеря ориентирования к базальной мембране [5].
На фоне гиперпластических процессов в эндометрии, возникающих при длительной пролиферации желез эндометрия без перехода их в секреторную фазу, может развиваться рак тела матки (РТМ) — это злокачественная опухоль, происходящая из слизистой оболочки тела матки (эндометрия). Чаще всего РТМ носит спорадический характер, и в 5 % случаев РТМ ассоциирован с наследственными синдромами, например, с синдромом Линча. Среди факторов риска: гиперэстрогения, ранние менархе, отсутствие родов в анамнезе, поздняя менопауза, возраст старше 55 лет, применение тамоксифена [3].
Эпидемиология РТМ
РТМ — самая частая злокачественная опухоль женских половых органов в развитых странах и вторая по частоте после рака шейки матки злокачественная опухоль женских половых органов в мире. В США в 2015 г. зарегистрировано более 54800 новых случаев заболевания РТМ, и более 10150 смертей от этого заболевания. В России ежегодно регистрируется более 21 тысячи больных РТМ. В структуре заболеваемости женского населения в России в 2016 г. РТМ занимал 3-е ранговое место (7,7 %). Средний возраст заболевших РТМ в России составляет 62,6 года [3,4].
Патогенез
Развитие РТМ обусловлено гиперэстрогенией, основной причиной которой является нарушение овуляции. Клиническое изучение метаболических нарушений у больных раком тела матки и морфологические особенности рака эндометрия позволили обосновать концепцию о двух основных патогенетических вариантах заболевания [2].
I тип (более частый). Опухоль развивается в более молодом возрасте, в отличие от пациенток II патогенетического варианта, на фоне длительной гиперэстрогении и гиперплазии эндометрия. У больных РТМ I патогенетического типа часто наблюдаются ожирение, сахарный диабет и гипертоническая болезнь, возможны эстрогенсекретирующие опухоли яичников или синдром склерокистозных яичников. Опухоли I патогенетического варианта, как правило, высокодифференцированные, имеют более благоприятный прогноз [2].
II тип. Опухоли эндометрия обычно низкодифференцированные, имеют менее благоприятный прогноз. Опухоли II патогенетического типа возникают в более старшем возрасте, в отсутствие гиперэстрогении, на фоне атрофии эндометрия. Примерно у 80% больных РТМ диагностируют эндометриоидную аденокарциному [2].
Выделяют три степени дифференцировки аденокарциномы эндометрия [2]:
G1 — высоко дифференцированная;
G2 — умеренно дифференцированная;
G3 — низко дифференцированная или недифференцированная.
Клиника
Ранний симптом прогрессирования рака эндометрия — появление жидких водянистых белей, нередко с примесью крови, и зуда наружных половых органов. Кровянистые выделения из половых путей бывают в виде мажущих серозно-кровянистых выделений, которые становятся порой обильными. Кровотечение, как правило, контактное или появляется после физической нагрузки [2].
Возможны боли внизу живота, которые на ранних стадиях рака носят схваткообразный характер. Это связано с сокращениями эндометрия и опорожнением матки от скопившейся в ней крови или гноевидной жидкости (гематометра, пиометра), отток которой в результате обтурации внутреннего зева затруднен. После таких схваткообразных болей появляются обильные выделения из матки — гной и кровь. При поздних стадиях боли постоянные, особенно интенсивные по ночам, связаны со сдавлением раковым инфильтратом нервных сплетений в малом тазу. При переходе процесса на мочевой пузырь и прямую кишку появляются симптомы нарушения функционирования этих органов [2].
Хирургическое вмешательство рекомендуется как наиболее эффективный метод лечения РТМ независимо от стадии как самостоятельно, так и в комбинации с другими методами [6].
Список литературы: