кровь на ферритин что это такое у беременных
Кровь на ферритин что это такое у беременных
Депонированное железо, металлопротеид, индикатор запасов железа.
Мкг/л (микрограмм на литр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Ферритин – белок, в форме которого в основном запасается железо в организме.
Оно всасывается из пищи и затем переносится трансферрином – специальным белком, который образуется в печени. Железо необходимо для образования эритроцитов и является важнейшей частью гемоглобина – белка, заполняющего эритроциты и позволяющего им переносить кислород от легких к органам и тканям. Кроме того, оно входит в состав мышечного белка миоглобина и некоторых ферментов.
В норме в организме содержится 4-5 граммов железа. Около 70 % от этого количества составляет как раз железо, «встроенное» в гемоглобин эритроцитов. Оставшееся главным образом запасается в тканях в составе белковых комплексов – ферритина и гемосидерина, – которые в основном содержатся в печени, а также в костном мозге, селезенке и мышцах. Хотя в крови ферритин присутствует в небольших количествах, его концентрация отражает запасы железа в организме.
Когда железа начинает не хватать, например в случае уменьшения приема его с пищей или частых кровотечений, организм начинает использовать резерв из тканей. Количество ферритина при этом, соответственно, уменьшается. Длительная нехватка поступающего железа может привести к анемии. Уровень ферритина же бывает сниженным задолго до появления симптомов железодефицита и позволяет вовремя диагностировать анемию.
С другой стороны, если железа поступает слишком много, это может приводить к его чрезмерному накоплению и, как следствие, к поражению печени, сердца и поджелудочной железы.
Стоит отметить, что использование разных анализов, отражающих обмен железа в организме, дает более полную и достоверную информацию о недостатке или переизбытке этого микроэлемента, чем только тест на ферритин.
Для чего используется исследование?
Когда назначается исследование?
На ранних стадиях дефицит железа может протекать бессимптомно. Если человек в остальном здоров, то признаки заболевания иногда появляются только при снижении гемоглобина ниже 100 г/л. О развитии анемии свидетельствуют следующие жалобы: хроническая слабость/утомляемость, головокружение, головные боли.
При тяжелой анемии пациент может страдать от одышки, боли в грудной клетке, сильных головных болей, слабости в ногах. У детей появляются трудности с обучением.
Помимо основных, есть еще несколько признаков, характерных для дефицита железа: желание употреблять в пищу необычные продукты (мел, глину), жжение кончика языка, заеды – трещины в углах рта.
Для чего сдавать кровь на ферритин
Ферритин – это белок, растворимый в воде. Он играет важную роль в нормальной жизнедеятельности человеческого организма. В составе этого белка в тканях организма запасается железо. Основная часть ферритина содержится в печени и костном мозге, но он присутствует также в других тканях и биологических жидкостях организма.
Общие сведения
Железо жизненно необходимо организму. Оно входит в состав гемоглобина, ряда ферментов, мышечного белка, необходимо для образования эритроцитов. В составе белковых комплексов в организме запасается около 30% от общего количества железа. Этот резерв начинает расходоваться, если организм испытывает дефицит железа по различным причинам (например, его недостаточно поступает с продуктами питания). Количество ферритина в крови снижается значительно раньше, чем появляются жалобы на здоровье и можно заподозрить наличие анемии. Переизбыток железа чреват его чрезмерным накоплением, что приводит к поражению внутренних органов.
Показания к исследованию
Уровень ферритина определяется в процессе исследования крови из вены. Сдать данный тест врач может порекомендовать в следующих случаях:
Подготовка к сдаче крови
Кровь из вены для проведения этого теста сдают натощак (пищу нельзя употреблять в течение 8-ми часов). В этот период допускается только чистая вода, чай, кофе и газированные напитки необходимо исключить. В течение получаса перед сдачей крови нужно избегать значительных физических нагрузок, отказаться от курения. Прием препаратов, в состав которых входит железо, приостанавливают за три дня до проведения теста (перед прекращением их приема необходимо проконсультироваться с врачом).
Рекомендации по подготовке могут предоставляться лечащим врачом или сотрудниками лаборатории.
Общие рекомендации:
В день взятия крови можно пить только обычную воду (газированные напитки, в том числе, и не содержащие сахар, необходимо исключить).
Интерпретация результатов
Анализ крови на ферритин используется для диагностики анемии, появившейся на фоне инфекционных заболеваний, развития злокачественного новообразования или воспалительного процесса. Также его назначают при необходимости дифференциальной диагностики железодефицитной анемии. Референсные значения отличаются в зависимости от пола. Для женщин они составляют 10-150 нг/мг, а для мужчин 20-350 нг/мг.
Если в организме развивается острое воспаление, концентрация ферритина значительно увеличивается. Небольшое снижение его количества у беременных женщин укладывается в пределы нормы и не указывает на наличие патологии. Для железодефицитной анемии характерен недостаток ферритина.
Повышение показателей возможно в следующих случаях:
Данный тест не предназначен для самодиагностики, интерпретацию его результатов должен выполнять только врач. Самолечение может нанести здоровью непоправимый вред, поэтому рисковать не стоит, необходимо обращаться к врачу. При интерпретации результатов учитываются данные других исследований, индивидуальные особенности организма и ряд других факторов. Если отклонения от нормы выявляются на ранних стадиях, во многих случаях для их нормализации достаточно приема курса витаминно-минерального комплекса, но назначать такой препарат должен врач. Для максимально достоверной оценки обмена железа, как правило, проводится комплекс лабораторных исследований, а не один анализ.
Железодефицитные состояния и железодефицитная анемия у женщин детородного возраста
Рассмотрены эпидемиология железодефицита, особенности обмена железа, этиология и патогенез дефицита железа у беременных, подходы к диагностике железодефицитной анемии и железодефицита, методы профилактики и лечения железодефицитных состояний у женщин дето
Epidemiology of iron-deficiency, characteristics of iron exchange were considered, as well as aetiology and pathogenesis of iron-deficiency in the pregnant, approaches to iron-deficiency anemia and iron-deficiency diagnostics, methods of prevention and treatment of iron-deficiency states in women of child-baring age.
Железо является одним из важнейших элементов в организме человека и входит в состав многих субстратов и ферментов, отвечающих за транспорт кислорода к клеткам, функционирование дыхательной цепи митохондрий, окислительно-восстановительные клеточные реакции, антиоксидантную защиту, функционирование нервной и иммунной систем и др.
В организме взрослого человека в среднем содержится около 3–4 г железа (Fe) (около 40 мг Fe/кг массы тела у женщин и около 50 мг Fe/кг массы тела у мужчин). Большая часть железа (60%, или более 2 г) содержится в гемоглобине (Hb), около 9% железа — в миоглобине, около 1% — в составе гемовых и негемовых ферментов. 25–30% железа находится в депо, будучи связано в основном с белком ферритином, а также с гемосидерином [1, 2] (табл. 1).
Исключительная роль железа и его значительное количество в организме определяют высокую суточную потребность в железе, которая зависит от возраста и пола.
Наиболее высокая потребность в железе наблюдается у детей первых лет жизни (около 1 мг в сутки), что связано с высокими темпами роста и развития; в период пубертата, особенно у девочек в связи с началом менструаций (около 2 мг/сут); у женщин детородного возраста, имеющих ежемесячные менструальные потери железа (около 2,5 мг/сут), у беременных женщин, особенно в III триместре беременности (до 6 мг/сут), что связано с ростом и формированием плода и увеличением количества эритроцитов у матери, у кормящих женщин (около 3 мг/сут) [3]. Наиболее низкая потребность в железе характерна для взрослых мужчин — около 1 мг/сут, что сопоставимо с потребностью ребенка первого года жизни [4, 5]. Чем выше суточная потребность в железе, тем более вероятно развитие дефицита железа (ЖД) и его наиболее тяжелой стадии — железодефицитной анемии (ЖДА).
Большое значение в обеспечении организма железом имеет характер питания. Во многих продуктах растительного происхождения и грибах содержатся большие количества железа, однако представлено оно в виде солей, обладающих низкой биодоступностью, из-за чего всасывается в кишечнике лишь незначительный его процент (1–7%). В продуктах животного происхождения железо представлено в виде гема, что обеспечивает его высокую всасывательную способность (биодоступность 25–30%) [5]. Поэтому для обеспечения организма железом необходимо потребление мяса, печени и других продуктов животного происхождения. Учитывая, что многие женщины детородного возраста увлекаются разнообразными «диетами» с низким содержанием животных продуктов, риск развития ЖД у них возрастает.
Эпидемиология железодефицита
Недостаток железа определяется как дефицит общего количества железа, обусловленный несоответствием между возросшими потребностями организма в железе и его поступлением или его потерями, приводящими к отрицательному балансу [2]. По оценкам Всемирной Организации Здравоохранения (2002 г.) ЖД различной степени выраженности страдают около 4 миллиардов человек, что составляет более 60% населения Земли. Из них на долю ЖДА приходится почти 2 миллиарда, что делает ЖДА самым распространенным заболеванием в мире и самой частой среди анемий (90%) [6].
Наиболее высокие показатели ЖД характерны для указанных групп риска. Так, ЖД регистрируется более чем у 51% женщин детородного возраста, что связано с ежемесячными кровопотерями и беременностями.
Без поступления железа извне у большинства женщин во время беременности возникает ЖД [7]. В исследовании S. Kagamimori и соавт., проведенном в 1998 г., было показано, что у 78% японских школьниц уже через 3 года после начала менструаций выявляется ЖД различной степени выраженности [8].
Распространенность ЖД зависит от социально-экономического развития общества. В развитых странах встречаемость ЖД в несколько раз ниже, чем в развивающихся. ЖД, включая ЖДА, наблюдается почти у 60% беременных женщин в развивающихся странах, тогда как в развитых странах этот показатель не превышает 14–15%. Среди женщин детородного возраста эти показатели составляют около 50% и 11% соответственно [9, 10].
ЖД у беременной может развиваться на любом сроке, однако наиболее часто он регистрируется в III триместре беременности, поскольку потребность в железе в этот период наиболее высокая. Более того, по мнению некоторых авторов, ЖД различной степени выраженности к концу беременности наблюдается почти у всех беременных женщин. Риск ЖД возрастает при многократных беременностях и при коротких промежутках между ними.
Представление о распространенности ЖД и ЖДА в РФ затруднено из-за низкой выявляемости, особенно латентного ЖД. По данным Минздрава РФ, приблизительно в 45% случаев завершенной беременности отмечается ЖДА, а по данным ряда независимых исследований, эта цифра близка к 60% [11–13].
Особенности обмена железа, этиология и патогенез дефицита железа у беременных
ЖД всегда является вторичным. Принципиально можно выделить две группы состояний, приводящих к ЖД. Первая группа включает физиологические и патологические состояния, связанные с повышенной потребностью в железе. К ним относятся периоды усиленного роста у детей, беременность, кормление грудью, острые и хронические кровопотери и т. д. Вторая группа причин — это состояния, связанные с недостаточным поступлением железа в организм: бедная «гемовым» железом диета, голодание, нарушение кишечного всасывания и т. п.
Женщины детородного возраста относятся к группе риска по развитию ЖД, поскольку имеют более высокие потребности в железе. Многие из них имеют хронический латентный дефицит железа, который, как правило, долго остается недиагностированным, так как отсутствуют выраженные клинические симптомы, а организм хорошо к нему адаптирован.
Еще одной важной проблемой ЖД у молодых женщин являются особенности питания: увлечение «диетами», исключение или значительное ограничение в рационе основных железосодержащих продуктов, избыточное потребление продуктов, тормозящих всасывание железа (шоколад, чай, кофе, злаковые и другие).
Поэтому к моменту наступления беременности до 50–60% женщин не имеют достаточных запасов железа не только для обеспечения развития плода, но даже для собственных возросших потребностей. Но даже при достаточных запасах депо железа у беременной истощается приблизительно к началу II триместра беременности [2, 11–13].
Во время беременности железо интенсивно расходуется на развитие и рост плода (до 500 мг железа), увеличение массы эритроцитов беременной (до 700 мг железа), формирование маточно-плацентарного комплекса (до 150 мг железа). С учетом индивидуальных ежедневных потерь всего для нормально протекающей беременности требуется 1000–1500 мг железа [2, 11, 12].
В I триместре источником железа для беременной является преимущественно депо. Всасывание железа в кишечнике в этот период меняется мало, компенсируя лишь ежедневные потребности женщины, и в начале II триместра депо железа истощается. Дальнейшее обеспечение все возрастающих потребностей в железе может покрываться только всасыванием в кишечнике. Интенсивность всасывания железа у беременной начиная со II триместра постепенно увеличивается, иногда достигая десятикратного превышения показателей у небеременной женщины. Таким образом, диета беременной должна содержать большое количество легкодоступного железа с учетом новых высоких способностей по его всасыванию [2].
Роды резко снижают потребности женщины в железе. Однако сами роды, с учетом кровопотерь, могут привести к потере 100–200 мг железа. Наступающая вслед за этим лактация также требует около 0,3 мг железа в сутки, что увеличивает ежедневную потребность в железе кормящей матери до 1,3–1,5 мг в сутки. Возобновляющиеся через некоторое время менструации приведут к росту ежедневных потребностей до 2,5–3,0 мг [2].
Учитывая вышеизложенное, можно утверждать, что практически все женщины в период беременности и кормления грудью испытывают дефицит железа различной степени выраженности.
Диагностика ЖДА и ЖД
Диагностика железодефицитной анемии обычно не вызывает затруднений. Однако выявление дефицита железа до стадии ЖДА, как правило, осуществляется плохо.
Принципиально могут быть выделены две стадии недостатка железа [14]. Латентный дефицит железа характеризуется снижением железа в депо (снижается уровень ферритина); затем присоединяется дефицит транспортного железа (снижается процент насыщения трансферрина железом, возрастает железосвязывающая способность сыворотки крови). Депо полностью истощается, а эритропоэз приобретает характер «железодефицитного» (увеличивается количество гипохромных эритроцитов и концентрация протопорфирина в эритроцитах). На всех этих этапах показатели периферической крови остаются нормальными, что значительно усложняет диагностику железодефицита. Лишь на финальных стадиях развивается ЖДА (клинически выраженный дефицит железа). Таким образом, выявленные случаи ЖДА представляют собой только «верхушку айсберга» от количества случаев дефицита железа.
Диагностика ЖД и ЖДА должна основываться, прежде всего, на лабораторных показателях. Наиболее информативными показателями для выявления ЖДА и ЖД являются уровень гемоглобина, количество эритроцитов и показатель гематокрита капиллярной крови, уровень сывороточного ферритина, процент (коэффициент) насыщения трансферрина железом, процент гипохромных эритроцитов. Менее достоверными показателями являются уровень сывороточного железа и общая железосвязывающая способность выворотки [1].
Гемоглобин, эритроциты, гематокрит
Уровень гемоглобина в периферической крови является основным показателем для выявления анемии и оценки ее степени тяжести. Нижней границей уровня гемоглобина у женщин детородного возраста считается 120 г/л, для беременных женщин в I и III триместре беременности — 110 г/л, во II триместре — 105 г/л. Таким образом, значение гемоглобина ниже 120 г/л для небеременной женщины и ниже 105 г/л для беременной указывает на наличие анемии [15].
В зависимости от степени снижения гемоглобина анемию у беременных подразделяют на три степени тяжести [16]:
Клинически значимым критерием оценки послеродовой анемии считают уровень гемоглобина ниже масса тела (кг) × 2,21 + 1000.
Полученное значение будет соответствовать величине, необходимой для коррекции ЖДА и восстановления запасов железа в организме на 1000 мг. Длительность курса вариабельна, зависит от степени тяжести состояния и может составлять от 4–5 недель до 6 месяцев приема препаратов железа, при этом необходимо учитывать как эффективность терапии, так и возникновение побочных эффектов и осложнений проводимой терапии. В среднем пациентки при легкой степени ЖДА должны получать 150–200 мг железа в сутки, а при среднетяжелой и тяжелой 300–400 мг/сут. Суточную дозу разделяют на 2–4 приема.
На данный момент препараты железа разделяют на две основные группы: неионные и ионные соединения (табл. 3).
В терапии ЖДА и ЖД предпочтение в большей степени отдается соединениям трехвалентного железа с гидроксид-полимальтозным комплексом (ГПК), к которым относятся такие препараты, как Мальтофер, Мальтофер фол и др. Препараты данного соединения обладают рядом преимуществ: повторяют свойства ферритина, физиологически связывающего железо, риск воздействия свободных радикалов очень низок, поскольку железо всасывается в трехвалентном состоянии. Благодаря большому размеру молекул, их пассивная диффузия через мембрану слизистой происходит в 40 раз медленнее по сравнению со скоростью диффузии молекулы гексагидрата железа, Fe (III) из ГПК всасывается в активном абсорбционном процессе, только железосвязывающие белки, присутствующие в гастроинтестинальной жидкости и на поверхности эпителия, могут захватывать Fe (III) из ГПК с помощью конкурентного лигандного обмена. Данные особенности фармакокинетики обеспечивают следующие преимущества: высокую терапевтическую эффективность, высокую безопасность, хорошую переносимость (табл. 4).
Особенно эффективно может быть назначение препаратов железа в сочетании с его саплиментами, в первую очередь фолиевой кислотой и витамином В12, что позволяет быстрее нормализовать уровень гемоглобина и показатели обмена железа [22]. Р. Geisser и соавт. показали, что применение препарата Мальтофер фол, содержащего ГПК трехвалентного железа и фолиевую кислоту, у беременных позволяет быстро нормализовать не только ферропоказатели и уровень гемоглобина, но и содержание фолиевой кислоты [23]. Схожие данные обнародовал Beruti E., показавший высокую эффективность назначения ГПК железа в сочетании с фолиевой кислотой в III триместре беременности [24].
Парентеральное введение препаратов железа показано только пациенткам с расстройствами всасывания, непереносимостью энтеральных препаратов, больным с хроническими кровотечениями, при которых потребность в железе не может быть удовлетворена энтеральным путем. Основная опасность парентеральной терапии — развитие анафилактической реакции, особенно такой реакции подвержены пациентки, страдающие коллагенозами. В связи с этим для парентерального введения должны использоваться препараты с высокой степенью доказанной безопасности. К таким препаратам может быть отнесен гидроксид-сахарозный комплекс трехвалентного железа (Венофер).
Эффективностью терапии препаратами железа служат следующие критерии: ретикулоцитарная реакция (начало реакции ожидается на 3–4 день от начала терапии, пик на 10–12 день), подъем уровня Hb обычно достигается на 3–4 неделе, исчезновение клинических проявлений ЖДА через 1–2 месяца, преодоление тканевой сидеропении через 3–6 месяцев от начала лечения (контроль по ферритину). Терапия препаратами железа продолжается до тех пор, пока концентрация ферритина не превысит 50 нг/мл.
Таким образом, несмотря на то, что ЖД и ЖДА являются серьезной проблемой здоровья женщин детородного возраста, особенно беременных и кормящих, своевременная диагностика и правильно назначенное лечение позволяют эффективно и быстро ликвидировать данные нарушения, избежав их нежелательных последствий.
Литература
А. В. Малкоч*, кандидат медицинских наук
Л. А. Анастасевич**, кандидат медицинских наук
Н. Н. Филатова*, кандидат медицинских наук
* ГБОУ ДПО РМАПО, ** ГБОУ ВПО РНИМУ им. Н. И. Пирогова, Москва
Железодефицит у беременных
Железодефицитная анемия — одно из тех редких осложнений беременности, которое можно легко предотвратить на этапе планирования. Даже здоровые беременные подвержены риску развития анемии в связи с физиологической гемодилюцией и расходованием запасов железа для роста плода и материнского эритропоэза [1]. Учитывая тот факт, что развивающийся плод очень требователен к концентрации кислорода и железа в поступающей к нему крови, плацента способна увеличивать количество рецепторов к железу и хранить его в резидентных ретикулоэндотелиальных клетках [1,3]. Следует различать дефицит железа и железодефицитную анемию (ЖДА). Распределение железа в организме идет преимущественно в пользу гемового железа, следовательно, развитие анемии на фоне железодефицита — это сигнал о выраженном недостатке микроэлемента в депо [3]. В связи с этим выделяют три стадии дефицита: предлатентный — снижение резервного железа без уменьшения расходования его на эритропоэз, латентный — истощение депо и дефицит транспортного железа, без признаков анемии и манифестный или ЖДА [8].
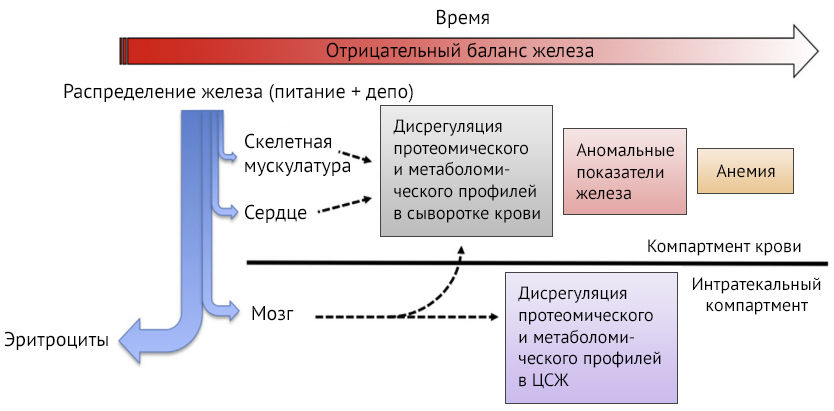
Рисунок 1 | Изменения в организме на различных стадиях железодефицита. Синей стрелкой указано распределение поступающего в организм железа — в первую очередь на эритропоэз, затем на синтез миоглобина и ферментные системы. Красной стрелкой указано прогрессирование дефицита с течением времени [3].
Потребность в железе на разных сроках беременности варьирует. В первом триместре суточная потребность снижается по сравнению с небеременным состоянием преимущественно за счет отсутствия менструальной кровопотери, а также за счет снижения эритропоэза. Во втором триместре объем циркулирующей крови увеличивается на 45 %, объем плазмы — на 50 %, а масса эритроцитов — на 35 %, следовательно, потребность в железе растет. В третьем триместре максимально возрастает потребность плода в железе, а кровопотеря в процессе родов уносит с собой около 150 мг железа [4].
Таблица 1 | Среднее увеличение потребности в железе в период беременности и в послеродовом периоде для женщин с массой тела до беременности от 55 до 60 кг [4,9]
Факторы риска развития железодефицита и железодефицитной анемии у женщин детородного возраста [4,8]:
Проявления дефицита крайне неспецифичны и могут списываться женщиной на саму беременность: быстрая утомляемость, слабость, раздражительность, нарушение концентрации внимания, бледность кожи и слизистых, головная боль, головокружение, тахикардия, одышка, усталость в ногах. Некоторые женщины отмечают пристрастие к специфическим продуктам: сырому мясу, сырым крупам, мелу, почве [1,8,10].
Существуют определенные опасности, связанные с дефицитом железа: повышение риска послеродовой депрессии, послеродового кровотечения (предположительно из-за снижения сократительной способности матки в условиях дефицита кислорода в тканях), некоторые исследования также говорят о риске развития послеродового сепсиса [1,10]. Женщин с анемией чаще подвергают гемотрансфузиям и родоразрешают путем кесарева сечения [2]. Преимущественно в странах с низким уровнем доходов показатели гемоглобина Железодефицит у плода и новорожденного
Железо в организме плода делится на гемовое железо, негемовое железо и депо, находящееся преимущественно в печени. В эритроцитах содержится 55 мг/кг железа в виде гемоглобина, нормальная концентрация которого у доношенных детей составляет 133–184 г/л. В депо хранится около 12 мг/кг железа в виде ферритина, нормальная концентрация которого в пуповинной крови доношенного ребенка составляет 170 мг/л. Наименьшее количество железа (около 8 мг/кг) участвует в метаболических процессах и переносе кислорода в мышцах. Дефицит негемового железа трудно отследить из-за отсутствия специфических биомаркеров, лабораторно он обнаруживается только в совокупности с дефицитом железа в депо и, как следствие, сниженным ферритином. Концентрация ферритина
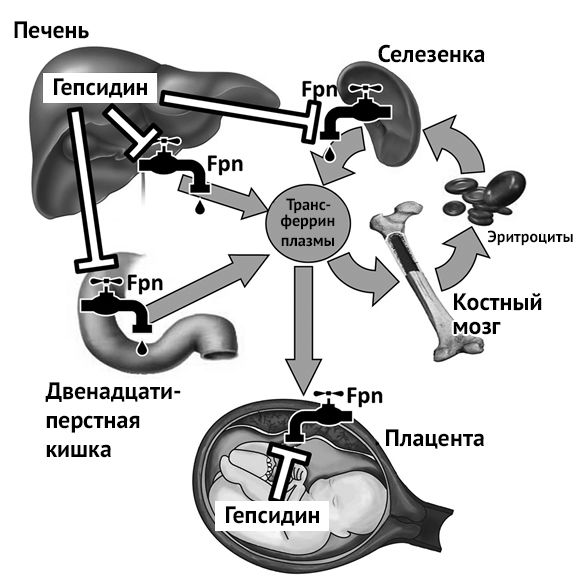
Рисунок 2 | Регуляция гомеостаза железа в организме беременной женщины. Fpn — ферропортин, Fe-Tf — трансферрин
В отношении влияния на развитие плода и исходы для новорожденного все не так однозначно: считается, что анемия матери связана с более высоким риском перинатальной и неонатальной смертности, низкой массой тела при рождении, преждевременными родами, однако метаанализ рандомизированных клинических исследований по влиянию добавок железа на перинатальные исходы показал лишь умеренное влияние на массу тела при рождении и неопределенное влияние на частоту преждевременных родов [1,2]. В то же время, некоторые исследования сообщают о 30% увеличении риска развития задержки роста плода на каждые 10 г/л сниженного гемоглобина до 20 недель беременности, а снижение гемоглобина
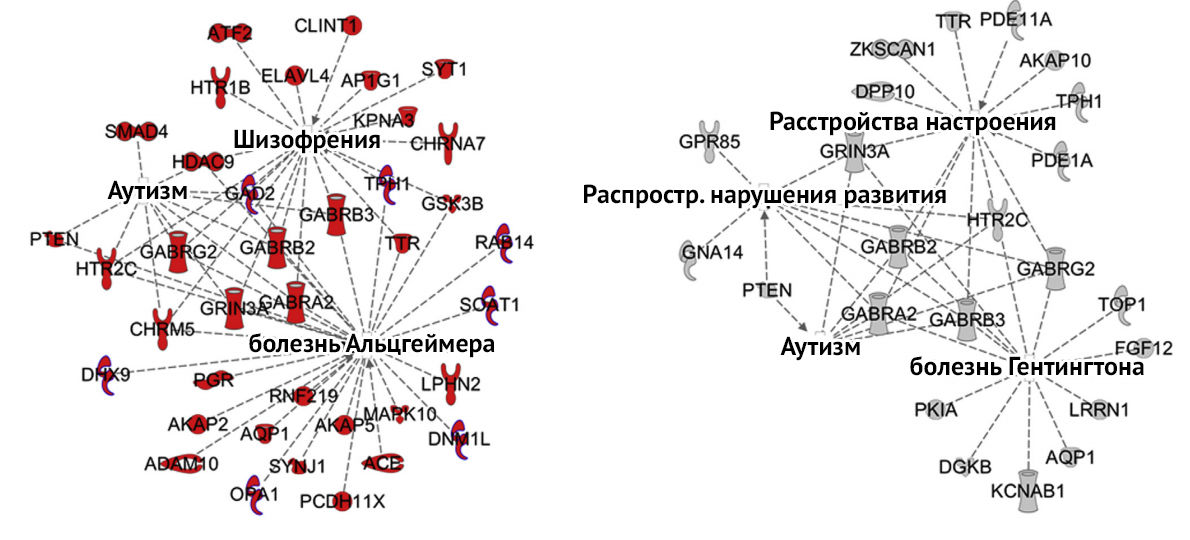
Рисунок 3 | Изменения экспрессии генов при железодефиците. Слева – непосредственное влияние дефицита на экспрессию, справа – эпигенетические нарушения. [3]
Диагностика дефицита железа
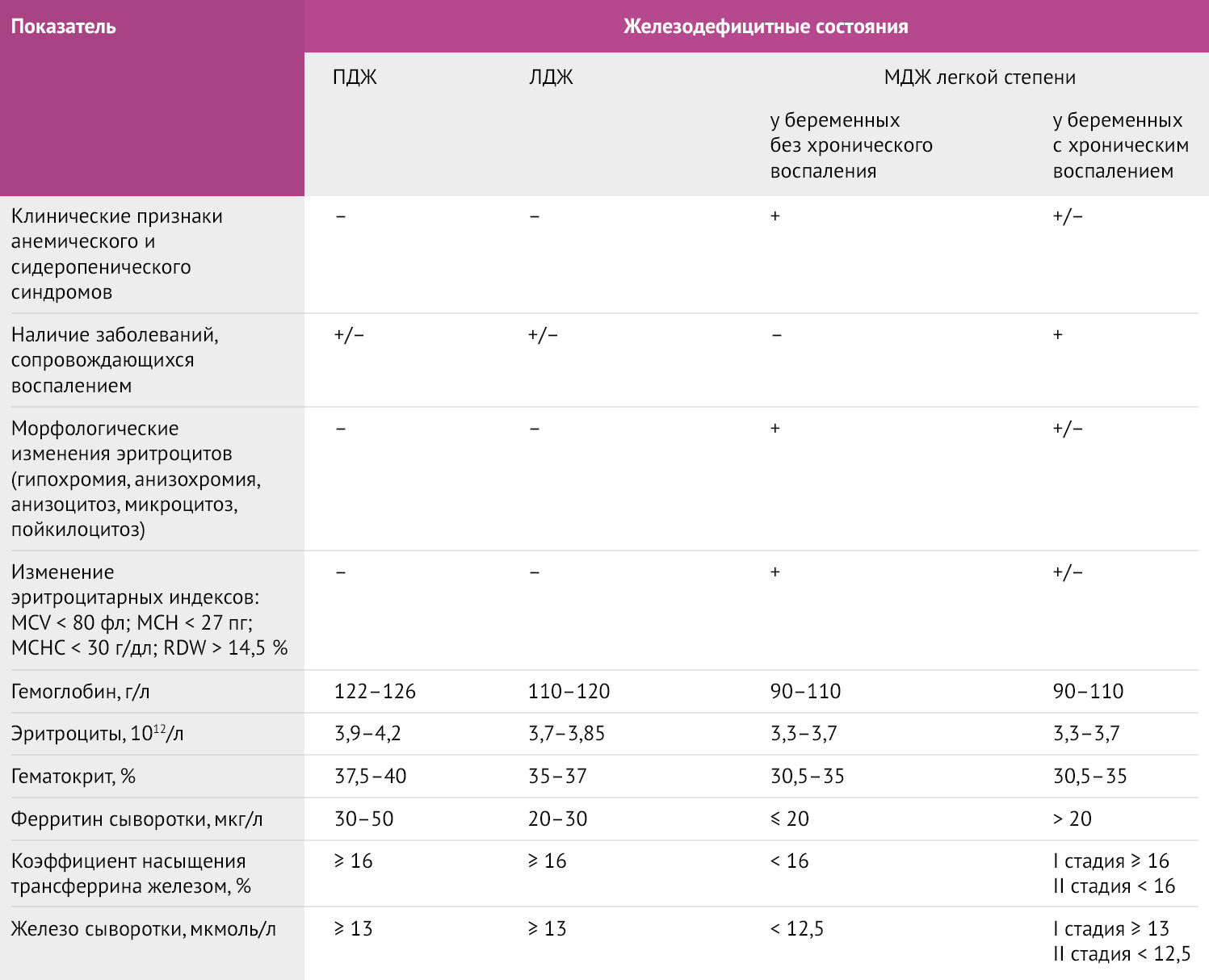
Как правило, железодефицит наряду с другими анемиями диагностируется во время рутинного исследования уровня гемоглобина в рамках общего анализа крови. Диагностика анемии у беременных имеет некоторые особенности в связи с вариабельностью показателей гемоглобина в зависимости от триместра. Для первого триместра пороговым значением является Hb Таблица 2 | Диагностические критерии железодефицитной анемии у беременных. ПДЖ – предлатентный дефицит железа, ЛДЖ – латентный дефицит железа, МДЖ – манифестный дефицит железа. [7,8]
Наиболее широко у беременных используется ферритин – маркер депонирования железа в печени матери и плаценте. Именно ферритин поддерживает стабильный уровень железа, выводя из депо необходимое для синтеза гема количество. Диагностически значимым является снижение уровня сывороточного ферритина Источники:
.gif)
.gif)