кровь на белок для чего при коронавирусе
С-реактивный белок при коронавирусе: показатели, что показывает? Белок повышен в крови при ковиде?
Анализ крови на С-реактивный белок – СРБ – остается актуальным и в наши дни, поскольку по его результатам можно судить о наличии и активности воспалительных процессов. Диагностировать коронавирусную инфекцию или любую другую болезнь таким образом нельзя, однако значение СРБ дает возможность своевременно принять меры по предотвращению осложнений.
СРБ при Covid-19
Уровень С-реактивного белка при коронавирусе – это один из ключевых лабораторных показателей, которые требуют медицинского контроля при среднетяжелой и тяжелой форме инфекции. Его обязательно определяют также у пациентов, находящихся в критическом состоянии.
Именно С-реактивный белок (С — наша буква Ц) является основным маркером поражения легких, растущим по мере увеличения тяжести инфекционного процесса и масштабности воспалительных изменений.
Уровень СРБ обязательно определяют при затрудненном дыхании, когда число вдохов ≥ 22/мин, и сатурации
Сатурация измеряется специальным прибором – пульсоксиметром.
Норма
Нормальное значение С-реактивного белка не превышает 5 мг/л. Это универсальная величина, не зависящая от возраста, пола. У новорожденных детей она не должна подниматься больше 0.15 мг/л.
Если СРБ повышен, значит, в организме развивается воспаление, об интенсивности которого свидетельствует степень данного повышения.
Благодаря многолетним клиническим исследованиям и внедрению высокотехнологичных методик ученые вывели еще один параметр – так называемого «базового значения СРБ». Его уровень позволяет оценить, насколько высок риск поражения сердечно-сосудистой системы у человека.
Заметим, что указанный риск можно определить даже при отсутствии воспалительной реакции. Норма базового значения СРБ ≤ 1 мг/л.
Для максимально точных результатов рекомендуется сдавать анализ на С-реактивный белок в одной и той же лаборатории, так как в разных клиниках могут использоваться различные методики:
Нефелометрия, основанная на интенсивности светового потока, рассеиваемого взвешенными частицами вещества.
Если повторные анализы сделать другими методами, то интерпретация результатов может быть неточной.
Кому показан анализ
Тест на С-реактивный белок в обязательном порядке делается при поступлении больного в стационар и диагностировании Covid-19 как минимум средней тяжести. Далее анализ повторяют по мере необходимости.
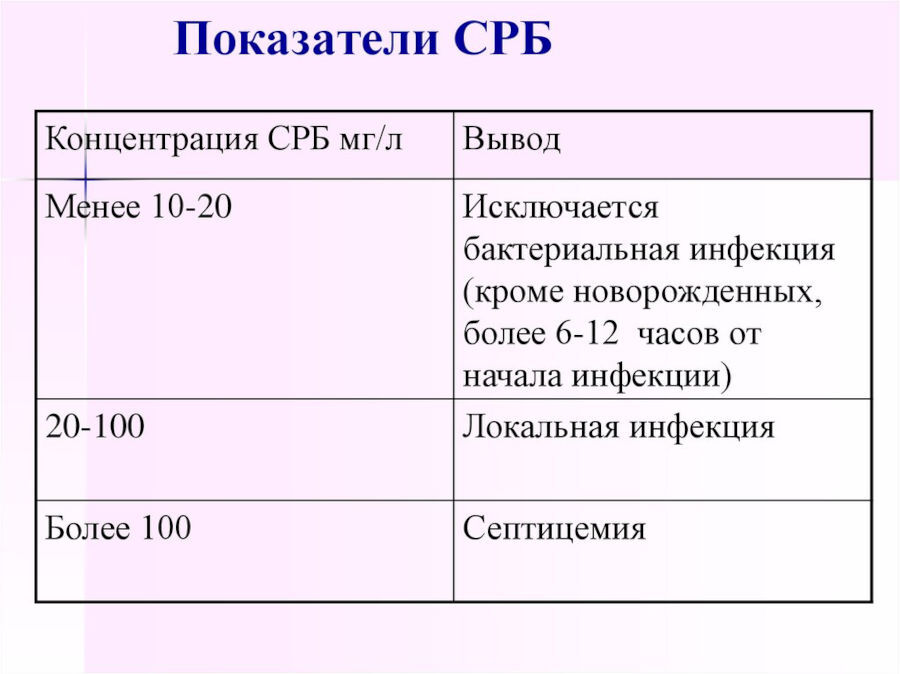
Результаты интерпретируются в соответствии со следующими значениями:
Если на фоне приема антибиотиков существенного снижения уровня СРБ не наблюдается, то крайне высок риск летального исхода.
Выработка С-реактивного белка начинает расти в первые 5 часов после заражения и достигает своего пика ко 2-3 дню болезни.
Более детальная расшифровка результатов анализа выглядит так (мг/л):
СРБ и СОЭ
Помимо С-реактивного белка, воспалительный процесс показывает также СОЭ – скорость оседания эритроцитов. Оба этих параметра увеличиваются на ранних стадиях заболеваний, но между ними есть существенная разница.
Во-первых, СРБ появляется и исчезает быстрее, чем меняется СОЭ. Поэтому на начальных этапах диагностики он более информативен.
Во-вторых, при адекватном лечении СРБ уменьшается уже примерно через неделю, тогда как СОЭ падает не раньше чем через 2-3 недели.
В-третьих, на показатель СОЭ оказывает влияние время суток, состав плазмы крови, уровень эритроцитов, пол (у женщин СОЭ почти всегда выше). Параметр СРБ не зависит от указанных факторов.
Следовательно, анализ на С-реактивный белок является более точным методом оценки интенсивности воспалительного процесса, нежели СОЭ. Поэтому его проводят для установления диагноза, выявления острых и хронических воспалений, а также их активности. Кроме того, результаты данного анализа позволяют оценить эффективность проводимой терапии.
При СРБ >60 мг/л или его увеличении втрое на 7-14 день заболевания обязательно назначаются ингибиторы интерлейкинов – Тоцилизумаб, Сарилумаб, Канакинумаб. В тяжелых случаях, если компьютерная томограмма показала 2-3 степень поражения легких, используются следующие препараты:
Для назначения перечисленных в списке средств нужно соблюдение 2-3 пунктов из перечня ниже:
Содержание в крови С-реактивного белка уменьшается у каждого пациента с разной скоростью. Пограничными показателями, свидетельствующими о начале выздоровления, считаются следующие:
При таких параметрах больного можно выписывать из больницы и переводить на амбулаторное лечение.
Особенности С-реактивного белка в пожилом возрасте
Уровень СРБ у пожилых людей может повышаться из-за возрастных изменений и на фоне сопутствующих болезней. Одна из причин – деменция, при которой С-реактивного белка становится очень много.
Старческое слабоумие наиболее часто развивается при генерализованном – общем – воспалении, связанном с атеросклерозом сосудов, высокой концентрацией триглицеридов (жиров) и липопротеинов низкой плотности.
Кроме того, при нарушении биологических процессов, обусловленных сменой дня и ночи (циркадных ритмов), и недостатке ночного сна в крови повышается содержание веществ, вызывающих воспаление. Растет при этом и уровень С-реактивного белка.
Повышение СРБ характерно для гипертонии на фоне сужения сосудов из-за холестериновых отложений, а также ожирения. Инсульт нередко является осложнением атеросклероза, который сопровождается воспалением сосудистой стенки, поэтому сразу после приступа происходит резкий выброс С-реактивного белка в кровь.
Одной из причин повышения СРБ может быть пародонтоз – воспаление десен. Причем чем выше его уровень, тем тяжелее степень пародонтоза.
Увеличенные концентрации СРБ сопровождают воспалительные патологии кишечника, связанные с нерациональным питанием и нездоровым образом жизни, а также болезнь Крона и язвенный колит.
Роль СРБ в организме и возможные причины повышения
С-реактивный белок – это связующее звено между антигенами и иммунными клетками. При попадании в организм чужеродных агентов – вирусов, бактерий, фрагментов поврежденных клеток – в печени стартует выработка СРБ. В его задачу входит распознавание вражеского «профиля» и активация иммунного ответа.
Такой механизм действует при ряде патологий, среди которых:
Виновник воспаления найден: S-белок коронавируса
Ученые специалисты по молекулярной биологии исследовали механизм воспалительного процесса при попадании Sars-CoV-2 в организм и выявили особую роль белка S. Именно сильное повреждение тканей (в основном легочной) является одним из наиболее грозных осложнений коронавирусной инфекции, способной привести к смерти.
В ходе исследования было установлено, что основная часть коронавирусного S-белка, либо вся его молекула могут вызвать внутритканевые повреждения, напрямую провоцируя воспаление.
Такой вывод сделала группа ученых под руководством П. Уорка из университета Ньюкасла. В нее вошли эксперты из Китая и Австралии. Результаты проведенного эксперимента были напечатаны в электронной библиотеке bioRxiv.
Оказалось, что S-белок Sars-CoV-2 обладает свойством изменять работу клеток и заставлять их синтезировать в большом объеме сигнальные молекулы, создающие условия для воспалительных процессов.
Ранее в медицинском сообществе эти воспалительные реакции считали следствием сверхактивной работы иммунной системы, чрезмерно реагирующей на коронавирус. Но открытие Уорка и его группы показало, что виновником избыточного иммунного ответа является коронавирусный белок S.
Полученные сведения ученые планируют использовать в лечении Covid-19 и протестировать ряд препаратов от онкологии. Возможно, они сумеют нейтрализовать S-белковые вирусные молекулы.
Коронавирусный S-белок как основа для вакцин
Обнадеживающие результаты получила еще одна совместная группа ученых из университета Техаса и Национального института аллергических и инфекционных болезней США под руководством Д. Маклиллана. В статье научного журнала Science в деталях описано трехмерное строение S-белка, который является ключевым элементом «Короны» Covid-19.
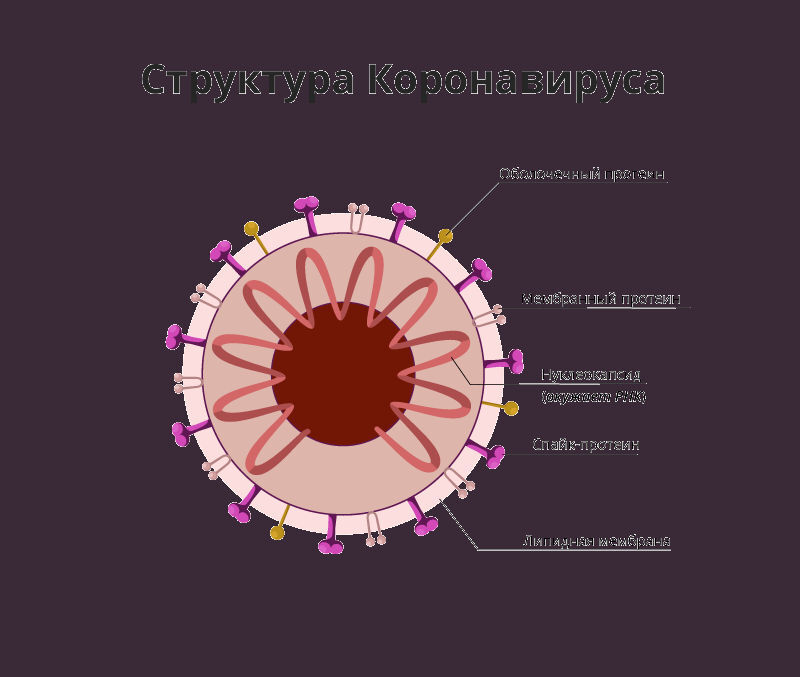
S-белки располагаются на поверхности вирионов – вирусных частиц. Они отходят от нее подобно лучам или иглам, благодаря чему называются Spike («шип», англ.). Именно эти белки подвергаются атакам антител, синтезируемых организмом-донором.
А самому коронавирусу S-белки нужны для заражения клеток. Их внешняя поверхность почти не отличается от знакомых клеткам молекул, что позволяет вредному микробу беспрепятственно соединяться с соответствующими рецепторами на мембранах и проникать внутрь. Именно таков механизм взаимодействия коронавирусных белков с ангиотензинпревращающим белком АПФ 2.
Применив крио-ЭМ – криогенную электронную микроскопию – ученые увидели трехмерную форму поверхности S-белка с разрешением до 3.5 А и установили, что белок меняет пространственное расположение атомов внутри молекулы: приготовившись к инфицированию, она имеет одну форму, а после связывания с клеткой-мишенью – другую.
Маклиллан и его коллеги изучали свойства первой молекулы, до ее преобразования, и установили, что соединяющийся с ферментом АПФ 2 участок белка обладает повышенной аффинностью, то есть может легко и прочно связываться с клетками, следовательно, быстро распространяться в организме.
Знания о точной структуре и свойствах S-белка позволяют увидеть новые возможности для создания эффективных вакцин и антител. Не исключено, что вакцину удастся получить даже непосредственно на основе коронавирусного S-белка, просто модифицировав его. И тогда грозная инфекция наконец сама станет мишенью.
Советы по получению максимально точных результатов и вопросы
Перед сдачей анализа необходимо предупредить врача о принимаемых препаратах, так как повышать уровень СРБ могут оральные контрацептивы и эстрогенсодержащие средства. Стероиды и салицилаты, напротив, снижают его.
Выработка СРБ может увеличиваться при курении и ожирении, после травм и недавних оперативных вмешательств. Поэтому за 3-4 часа до взятия биоматериала нежелательно курить.
Как определяют эффективность лечения по уровню С-реактивного белка?
СРБ «живет» примерно 6 часов, и при улучшении состояния пациента его концентрация быстро падает. По анализам крови эту тенденцию легко отслеживать.
Как быстро появляется С-реактивный белок в крови после заражения?
Его содержание в крови увеличивается сразу после инфицирования – в первые 6-12 часов, максимум – на 2-й день. При воспалениях он может вырасти в десятки и даже сотни раз, благодаря чему тест на СРБ весьма информативен.
Кроме того, данный параметр позволяет определить вирусную и бактериальную природу воспалительного процесса по цифровому показателю степени концентрации. На фоне адекватной терапии он быстро уменьшается уже на 2-й день.
«Внутрисосудистое свертывание крови при COVID-19 определяет весь ход болезни»
 Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
Сегодня известно, что при COVID-19, в первую очередь, страдает свертывающая система крови. Вот почему у всех умерших от осложнений новой коронавирусной инфекции находят большое количество тромбов. Как это объяснить? Почему это заметили не сразу? Каким образом и почему это происходит? Можно ли предотвратить развитие такого осложнения? Об этом – наш разговор с А.Д. Макацария, академиком РАН, одним из крупнейших в мире специалистов по изучению нарушений свертываемости крови, создателем Школы клинической гемостазиологии, заведующим кафедрой Сеченовского университета. Александр Давидович и его ученики активно сотрудничают с университетом Сорбонны, Венским, Римским, Миланским и Тель-Авивским университетами, Технион в Хайфе. Под его руководителем защищено 150 кандидатских и докторских диссертаций. Автор более 1200 научных трудов, в том числе 40 монографий.
– Александр Давидович, в последнее время во всем мире появляется всё больше сообщений о том, что при COVID-19 страдает свертывающая система крови. Так ли это, и если да, то чем вы объясняете этот феномен?
– Безусловно, это так. Более того, хочу сказать, что практически нет такой инфекции (вирусной или, тем более, бактериальной), которая бы не влияла на свертывание крови. Доказательство тому – учение о сепсисе и септическом шоке как универсальной модели ДВС-синдрома – синдрома диссеминированного внутрисосудистого свертывания крови. Степень тяжести тромботических нарушений зависит от особенностей возбудителя и организма-хозяина (иммунная система, система гемостаза, наличие сопутствующих заболеваний и т.д.).
– Но ведь не у всех пациентов развивается сепсис и септический шок?
– Конечно, не у всех. Поэтому очень актуальным и далеко не изученным в настоящее время является механизм патогенеза осложнений, вызванных коронавирусной инфекцией. Во многом это обусловлено особенностями вируса, а также особенностями организма человека, начиная от количества и качества рецепторов, представленных у человека и их способностью связываться с этим вирусом. Безусловно, на исходы заболевания огромное влияние оказывает коморбидность, то есть наличие сопутствующих хронических заболеваний у пациента.
– Почему, по вашему мнению, эта особенность течения болезни проявилась не сразу?
— Я считаю, что все это проявилось сразу, но не было адекватно оценено врачами изначально: еще не было такого количества вскрытий и широкого тестирования на гемостазиологические маркеры. Надо сказать, мы занимаемся изучением этой проблемы довольно давно, практически с самого начала эпидемии. Еще в самом начале апреля мы опубликовали работу, основанную на первых наблюдениях наших китайских коллег. Работа называлась «COVID-19 и синдром диссеминированного внутрисосудистого свертывания крови». Она имела чрезвычайно широкий резонанс, поскольку уже тогда врачи начали понимать роль свертывающей системы крови в инфекционном процессе.
– Каков механизм тромбообразования при covid-19 и отличается ли он от этого процесса при других патологиях?
– Это очень непростой вопрос. На сегодняшний день однозначно можно утверждать – при этом вирусе с самого начала имеет место активация гемостаза, внутрисосудистое свертывание крови и тромбообразование в сосудах мелкого калибра жизненно важных органов. При этом повреждаются не только легкие, а блокада микроциркуляции и ее необратимый характер определяют исход заболевания. Позднее начало антикоагулянтной терапии является неблагоприятным фактором. Причем этот процесс внутрисосудистого свертывания в капиллярах легкого играет важную роль в развитии острого респираторного дистресс-синдрома (ОРДС), о котором все говорят. Но далеко не все с самого начала уловили связь между внутрисосудистым свертыванием крови и ОРДС.
В западной литературе даже появился термин «легочная интраваскулярная коагуляция». Практически во всех случаях имеет место активация системного воспалительного ответа. Это общебиологическая реакция, которая особенно проявляется в ответ на инфекцию, вирусные возбудители. Международные организации признали, что коронавирусная инфекция – это сепсис.
Таким образом, цитокиновый и тромботический шторм усугубляют состояние больного и определяют степень тяжести. Но есть и особенности. Возможно, при COVID-19 в первую очередь повреждается фибринолиз – часть системы гемостаза, которая обеспечивает процесс разрушения уже сформированных кровяных сгустков, тем самым, выполняя защитную функцию предотвращения закупорки кровеносных сосудов фибриновыми сгустками. Отсюда синдром фибринирования при меньшей частоте геморрагических осложнений. И отсюда же открывается перспектива применения тромболитиков, о чем сейчас так много говорят и пишут. А впервые предложили такую схему наши американские коллеги.
– А ведь есть немало людей с нарушениями свертываемости крови. Сейчас, во время эпидемии, для них настали трудные времена.
– Это так. В нашей популяции есть люди не только с явными, но и со скрытыми нарушениями гемостаза, предрасполагающими к тромбозам – генетические тромбофилии, антифосфолипидный синдром и ряд других заболеваний, сопровождающихся избыточной активацией системы гемостаза; а также люди с высокой готовностью к супервоспалительному ответу (врожденные факторы и ряд ревматологических и иммунных заболеваний). Им сейчас важно контролировать своё состояние, а врачам не забывать об этом.
Вообще надо сказать, что открытие NET расширило горизонты в понимании биологии нейтрофилов и роли этих клеток в организме. Использование организмом хозяина хроматина в сочетании с внутриклеточными белками в качестве естественного противомикробного агента имеет древнюю историю и меняет наше представление о хроматине как только о носителе генетической информации. Благодаря избыточному и неконтролируемому формированию NET, нейтрофилы могут способствовать развитию патологического венозного и артериального тромбоза, или «иммунотромбоза», а также играют важную роль в процессах атеротромбоза и атеросклероза. Высвобождение NET является, как выяснилось, одной из причин тромбообразования при таких состояниях, как сепсис и рак. Наличие NET при этих заболеваниях и состояниях дает возможность использовать их или отдельные компоненты в качестве потенциальных биомаркеров. NET и их компоненты могут быть привлекательны в качестве терапевтических мишеней. Дальнейшие исследования нейтрофилов и NET необходимы для разработки новых подходов к диагностике и лечению воспалительных и тромботических состояний.
– Размышляя о высокой летальности у пациентов, которым пришлось применить ИВЛ, вы констатируете, что мы, возможно, пошли не тем путем. А какой путь может оказаться более верным?
– Да, я имел в виду, что при оценке вентиляционно-перфузионных нарушений при COVID-19 превалируют перфузионные нарушения, нарушения микроциркуляции, а это значит, что главная терапевтическая мишень – восстановление нормальной перфузии тканей, то есть противотромботическая терапия, а возможно, даже и фибринолитическая. Механическая вентиляция не может решить вопрос перфузионных нарушений.
– Видите ли вы, что в связи с эпидемией стали более частыми проблемы тромбообразования в акушерско-гинекологической практике?
– Случилось так, что во многом и благодаря нашим стараниям (лекциям и публикациям), большинство акушеров сегодня осведомлены о том, что беременность – это состояние так называемой физиологической гиперкоагуляции, и этим пациенткам нередко назначаются антикоагулянты во время беременности. Тем не менее, требуются дальнейшие исследования для вынесения суждения о частоте тромбозов у беременных с COVID-19.
Вообще надо сказать, что большинство осложнений беременности либо обусловлены, либо сочетаются с высоким тромбогенным потенциалом. Генетические факторы свертывания крови, особенно антифосфолипидный синдром, являются факторами риска огромного количества осложнений беременности – это и внутриутробные гибели плода, и неудачи ЭКО, и задержка внутриутробного развития плода, и преждевременная отслойка плаценты, что приводит к тяжелым тромбогеморрагическим осложнениям, это, наконец, тромбозы и тромбоэмболии. Поэтому, конечно, можно ожидать, что в условиях COVID-19 эти осложнения могут представлять собой еще большую опасность. Ведь вирус может быть фактором, активирующим факторы свертываемости крови. Конечно, тут нужны обобщающие исследования, но уже сейчас наши отдельные наблюдения говорят о том, что риск таких осложнений возрастает.
– Являются ли, на ваш взгляд, одним из проявлений этой проблемы случаи тяжелого течения covid-19 в педиатрии (состояния, похожие на синдром Кавасаки)?
– Глава ВОЗ Тедрос Аданом Гебрейесус призвал врачей всех стран обратить особое внимание на сообщения о том, что у некоторых детей, заразившихся коронавирусом, проявляются симптомы, схожие с еще одним заболеванием — синдромом Кавасаки (мультисистемным воспалительным синдромом). Действительно, в сообщениях из Европы и Северной Америки говорилось, что некоторое число детей поступало в отделения интенсивной терапии с мультисистемным воспалительным состоянием, с некоторыми симптомами, похожими на синдром Кавасаки и синдром токсического шока.
Синдром Кавасаки был впервые описан в 1967 году японским педиатром по имени Томисаку Кавасаки. Он обычно поражает детей до пяти лет. При этом синдроме у пациента начинается воспаление кровеносных сосудов (васкулит) и лихорадка. Болезнь Кавасаки имеет четко выраженный набор симптомов, включая постоянно высокую температуру, покраснение глаз и области вокруг рта, сыпь на теле и покраснение и отек ног и рук.
13 мая нынешнего года в авторитетном медицинском издании The Lancet было опубликовано исследование итальянских врачей, которые сообщили, что в провинции Бергамо, одной из наиболее пострадавших от эпидемии коронавируса, была зафиксирована вспышка синдрома Кавасаки или схожего с ним синдрома.
Важно, что в большинстве случаев дети также имели положительный результат теста на антитела к КОВИД-19, предполагая, что синдром последовал за вирусной инфекцией.
Болезнь Кавасаки имеет тенденцию проявляться в группах генетически похожих детей и может выглядеть немного по-разному в зависимости от генетики, лежащей в основе группы. Это говорит о том, что различные триггеры могут вызывать воспалительную реакцию у детей с определенной генетической предрасположенностью.
Вполне возможно, что атипичная пневмония SARS-COV-2, вызванная вирусом COVID-19, является одним из таких триггеров. Это важный вопрос, требующий пристального изучения.
– Александр Давидович, как вы думаете, почему у всех COVID-19 проявляется по-разному?
– Тут очень важна проблема факторов риска. Всё дело в том, что, помимо видимых болезней типа сахарного диабета или гипертонии, существуют болезни невидимые, о которых мы зачастую даже не подозреваем. В последние годы большое распространение получило учение о генетической тромбофилии. Во всем мире это примерно до 20 процентов людей, которые являются носителями той или иной формы генетической тромбофилии. С этим можно жить сто лет, но если возникает инфекция, травма, делается операция – больной может погибнуть от тромбоэмболии, даже если операция выполнена на высочайшем техническом уровне. Причиной тому – скрытая генетическая тромбофилия – мутация, которая делает её носителя подверженным высокому риску тромбообразования.
Высокая контагиозность вируса и большое количество заболевших поневоле «позволяет» вирусу выявить людей с изначальной явной или скрытой предрасположенностью к тромбозам. Это пациенты не только с генетической тромбофилией или антифосфолипидным синдромом, но и с сахарным диабетом, ожирением, ревматическими болезнями и другими патологическими состояниями, ассоциированными с повышенным свертыванием и/или воспалением.
– Какие методы профилактики и лечения covid-19 вы считаете перспективными?
– Помимо уже названных, это противовирусная терапия, терапия специфическими иммуноглобулинами, противотромботическая терапия и лечение, направленное на снижение воспаления (так называемые антицитокиновые препараты). Многое нам предстоит ещё понять об этом новом для нас заболевании, но постепенно мы движемся в сторону лучшего объяснения многих его механизмов. Вы знаете, я всегда много работал, но, пожалуй, никогда ещё я не был так занят исследовательской и практической работой, как сейчас. Уверен, что она даст свои важные результаты.
Беседу вела Наталия Лескова.
Кровь на белок для чего при коронавирусе
Общий и биохимический анализы крови пациентов с СОVID-19 относятся к неспецифическим методам диагностики, но при этом играют большую роль в оценке тяжести заболевания, позволяют прогнозировать его развитие и исход, корректировать схемы лечения. Данная тема подробно обсуждалась в ходе одной из онлайн-сессий в рамках республиканского научно-практического вебинара «Актуальные вопросы биобезопасности и лабораторной диагностики COVID-19».

Людмила Анисько отметила, что изменения лабораторных показателей крови зависят от стадии инфекции. Этих стадий три:
Лимфоцитопения
Людмила Анисько:
Снижение уровня лимфоцитов, главных клеток иммунной системы, — один из основных признаков при COVID-19. Лимфоцитопения встречается у 80 % пациентов.
В ряде ретроспективных исследований показана прямая связь между выраженностью лимфоцитопении и вероятностью развития острого респираторного дистресс-синдрома.
Факторами, способствующими снижению уровня лимфоцитов при COVID-19, являются: лизис (непосредственное влияние вируса SARS-CoV-2 на лимфоциты); апоптоз (этому способствует повышенный уровень интерлейкина); снижение лимфопоэза в костном мозге (при гиперактивации иммунной системы и продукции противовоспалительных цитокинов).
Соотношение нейтрофилы/лимфоциты
Основная составляющая популяции лейкоцитов, участвующая в уничтожении патогенных микроорганизмов, — нейтрофилы, которые продуцируют сосудистый эндотелиальный фактор роста, противовоспалительные цитокины (ИЛ-1, ФНО, у-IFN).
Людмила Анисько:
В ряде исследований было показано, что повышенный показатель соотношения нейтрофилы/лимфоциты может рассматриваться как прогрессирование COVID-19. Соотношение более 3,13 расценивается как неблагоприятный признак с высоким риском летального исхода.
Тромбоцитопения
Снижение уровня тромбоцитов связано, во-первых, с прямой инфекцией гематопоэтических клеток костного мозга SARS-CoV-2, что приводит к угнетению кроветворения. Во-вторых, с увеличением их потребления, поскольку повреждение легочной ткани сопровождается активацией, агрегацией и удержанием тромбоцитов в местах повреждения, образованием тромбов.
Людмила Анисько:
В большинстве исследований за пороговое значение количества тромбоцитов принималось 150×109/л, — сообщила Людмила Анисько. — Так, по результатам крупного китайского исследования количество тромбоцитов менее 150×109/л наблюдалось в 31,6 % случаев, при этом у тяжелых пациентов — в 57,7 % случаев. Тромбоцитопения статистически значимо ассоциирована с увеличением риска тяжелого течения COVID-19 более чем в 5 раз. Динамика снижения уровня тромбоцитов ассоциирована с летальным исходом.
Повышение активности клеточных ферментов крови
Причинами повышения активности клеточных ферментов являются нарушение проницаемости мембраны клеток (при воспалительных процессах); нарушение целостности клеток (при некрозе); повышенная пролиферация клеток с ускорением клеточного цикла и др.
Аспартатаминотрансфераза (АСТ)
Обратимо катализирует трансаминирование, в частности, межмолекулярный перенос аминогруппы с 1-аспарагиновой кислоты на альфа-кетоглутаровую кислоту. Содержится во всех органах и тканях, больше всего в сердечной мышце.
Аланинаминотрансфераза (АЛТ)
Обратимо катализирует трансаминирование, в частности, межмолекулярный перенос аминогруппы с аланина на альфа-кетоглутаровую кислоту. Содержится во всех органах и тканях, больше всего в клетках печени.
Людмила Анисько:
Ретроспективное когортное исследование в США (n=130) выявило повышение уровня трансаминаз в 56 % случаев у пациентов с COVID-19. Повышенные уровни АСТ и АЛТ были связаны с тяжелым течением и худшим прогнозом, риск летального исхода у таких пациентов повышался в 2,9 раза.
Креатинфосфокиназа (КФК)
Катализирует обратимую реакцию креатинина с участием АТФ, в результате чего образуются креатинфосфат и АДФ. Повышается при травмах, операциях, инфаркте миокарда, миопатиях, мышечных дистрофиях, отравлениях, сопровождающихся комой, инфекционных болезнях.
Людмила Анисько:
Большинство исследователей отмечают повышенные уровни КФК почти у всех госпитализированных пациентов с COVID-19. Одна из причин повышения КФК — развитие воспалительной реакции в мышечной ткани. Метаанализ клинических проявлений (1995 пациентов) показал проявление миалгий в 35,8 % случаев.
Также сообщается о развитии миокардита у пациентов с COVID-19. При аутопсии умерших пациентов описаны некроз миоцитов и инфильтраты мононуклеарных клеток в миокарде. Кроме того, высказываются предположения о том, что вирус может дестабилизировать имеющиеся атеросклеротические бляшки и обусловить развитие острых коронарных синдромов.
Лактатдегидрогеназа (ЛДГ)
Катализирует обратимое восстановление пирувата до лактата. Повышается при остром повреждении сердца, эритроцитов, почек, скелетных мышц, печени, легких, кожи (в норме в перечисленных органах и тканях уровень ЛДГ более чем в 500 раз выше, чем в сыворотке крови).
Изменение уровней электролитов — Na, K, Ca
Людмила Анисько:
У большинства пациентов, находящихся на стационарном лечении, отмечается снижение уровня натрия, калия, кальция в крови. Так, в пяти исследованиях с общей выборкой 1 415 пациентов (17,8 % с тяжелой формой COVID-19) выявлено значительное снижение натрия (ДИ 1,33–0,5 ммоль/л), калия (ДИ 0,18–0,07 ммоль/л), кальция (ДИ 0,25–0,20 ммоль/л).
У 20 % пациентов с тяжелой инфекцией COVID-19 отмечается гипокалиемия. Ее вероятные причины: увеличение экскреции калия почками, потери калия с диареей и рвотными массами, повышенное потоотделение при лихорадке, ведущее к потере электролитов, в т. ч. калия.
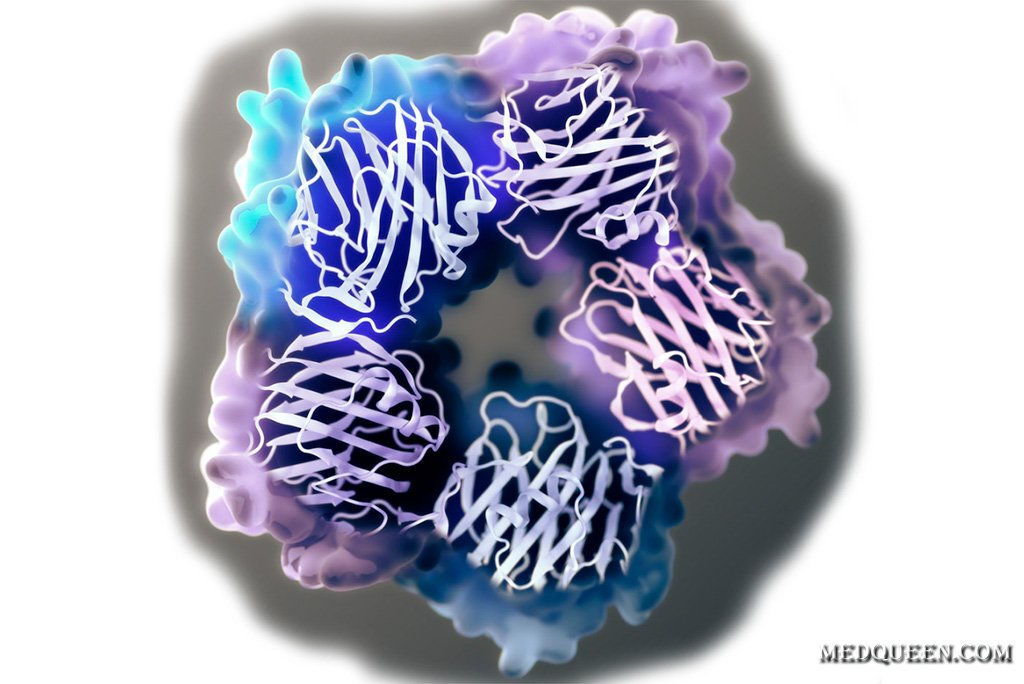
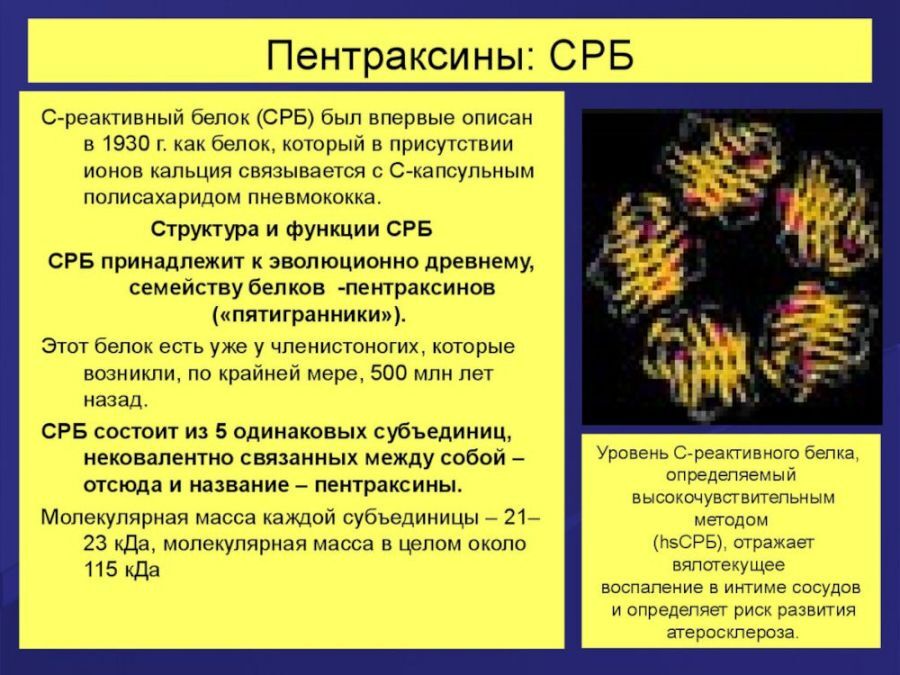
Белки острой фазы
Самый распространенный белок острой фазы, определение которого используется в клиниках, это С-реактивный белок. Его основные функции — ограничение поврежденных тканей, нейтрализация воспалительного агента, запуск механизмов репарации для восстановления повреждений. При остром воспалении концентрация С-реактивного белка в течение 12 часов повышается в десятки и сотни раз.
Людмила Анисько:
У 60 % пациентов с COVID-19 С-реактивный белок повышен с первых дней заболевания! Для того чтобы как можно раньше диагностировать присоединение вторичной бактериальной инфекции в условиях стационара, необходимо использовать определение прокальцитонина (ПКТ). Повышенный уровень ПКТ — предиктор неблагоприятного исхода заболевания, он говорит о том, что к коронавирусной инфекции присоединилась бактериальная флора и пациенту требуется назначение антибактериальных препаратов.
Дополнительно уровень С-реактивного белка может использоваться как косвенный маркер активности интерлейкина-6.
Интерлейкин-6 (ИЛ-6)
ИЛ-6 является маркером цитокинового шторма, его избыточное образование ведет к повреждению тканей, усилению проницаемости сосудов, снижению сократимости миокарда и др. Определение ИЛ-6 применяется при оценке прогноза тяжести синдрома высвобождения цитокинов, а также при мониторинге эффективности терапии блокаторами рецепторов ИЛ-6.
Людмила Анисько:
Повышенный уровень ИЛ-6 наблюдается более чем в 50 % случаев при COVID-19. Исследования показали, что по мере прогрессирования тяжести заболевания уровни противовоспалительных цитокинов в сыворотке также увеличиваются и имеют корреляцию с летальностью.
Согласно метаанализу, средний сывороточный уровень ИЛ-6 у пациентов с тяжелым течением в 2,9 раза выше по сравнению с нетяжелым течением заболевания. Пороговые значения сывороточного ИЛ-6 для выявления пациентов с риском тяжелого течения инфекции — 55 нг/мл, риском летального исхода — 80 нг/мл.
Ферритин
Цитозольный белок (способен связывать до 4 500 атомов железа), состоящий из легкой L и тяжелой H субъединиц, соотношение которых варьируется и может изменяться при воспалительных и инфекционных заболеваниях. Уровень ферритина в плазме обычно отражает общие запасы железа в организме, при этом 1 нг ферритина на 1 мл указывает примерно на 10 мг общих запасов железа.
Людмила Анисько:
Ферритин является ключевым медиатором иммунной дисрегуляции при тяжелом прогрессирующем течении COVID-19. Метаанализ 6 320 пациентов показал повышение уровня ферритина у тяжелых пациентов. Ретроспективное многоцентровое исследование выявило повышенные уровни ферритина — в среднем 1297,6 нг/мл — у умерших пациентов против 614,0 нг/мл у выживших.
D-димеры
Продукты распада фибринового сгустка, образуются в результате расщепления плазмином стабильного фибрина. По их уровню можно оценить процессы тромбообразования и фибринолиза. Референтное значение до 500 нг/мл. Повышенный уровень D-димера наблюдается при тромбозах, тромбоэмболиях, массивных поражениях тканей, обширных гематомах, обширных хирургических вмешательствах, сепсисе, ИБС, сердечной недостаточности, онкологических и тяжелых инфекционных заболеваниях, осложнениях в послеродовом периоде, тяжелых заболеваниях печени.
Людмила Анисько:
У пациентов с COVID-19 часто повышен уровень D-димера, высокая концентрация которого является предиктором летального исхода. Эксперты Международного общества специалистов по тромбозу и гемостазу (ISTH) полагают, что повышение уровня D-димера в 3–4 раза у пациента с COVID-19 является самостоятельным показанием для госпитализации.
 Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии