контуры m psoas что это значит
Контуры m psoas что это значит
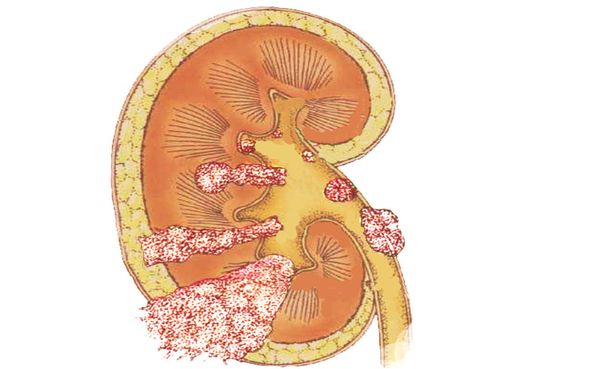
Обязательным этапом обследования больных пожилого и старческого возраста острым панкреатитом следует считать обзорную рентгенографию брюшной полости и грудной клетки, которые позволяют обнаружить косвенные признаки заболевания. Отмечается также пневматоз поперечноободочной и тонкой кишки, уровень жидкости в проекции ДПК, симптом «дежурной» петли. На фоне дилятированных петель кишечника выявляется контур m. psoas, что считается характерным признаком панкреонекроза.
Начиная с этапа приемного отделения стационара, а также в процессе лечения целесообразно проведение ультразвукового исследования (УЗИ) благодаря доступности, возможности повторений неограниченное число раз, высокой точности методики.
УЗИ уже в приемном отделении стационара помогает проведению дифференциального диагноза, особенно при отсутствии параллелизма между клиническими проявления заболевания и находками, что особенно актуально у больных пожилого и старческого возраста. Исследование может быть затруднено из-за пареза кишечника и при ожирении больных IV ст.
При УЗИ оцениваются размеры поджелудочной железы, контуры, структура паренхимы, состояние протока и сальниковой сумки.
Ввиду частого развития панкреонекроза на фоне патологии билиарного тракта уже при первичном исследовании необходимо осмотреть внепеченочное желчное дерево.
Оценивая состояние паренхимы поджелудочной железы у лиц пожилого и старческого возраста, следует помнить, что даже при отсутствии клинических проявлений заболевания ткань всегда имеет повышенную эхогенность при нормальных размерах.
При отечной форме острого панкреатита отмечается увеличение поджелудочной железы, контуры ровные, четкие. Эхоструктура паренхимы однородная, низкой эхогенности. Плотность паренхимы становится ниже плотности печени. Контуры прилежащих к железе сосудов четкие.
При повторном обострении процесса в поджелудочной железе выявляются кальцинаты. Почти у каждого пятого больного при отечной форме заболевания лоцируется вирсун-гов проток в виде линейной эхонегативной структуры, расположенной в середине паренхимы. Диаметр протока от 2 до 4 мм.
Жидкость при отечной форме острого панкреатита в сальниковой сумке скапливается редко. При данной форме заболевания почти в 10% случаев выявляется незначительное количество жидкости в брюшной полости.
В желудке и двенадцатиперстной кишки отмечается небольшое количество содержимого, даже если исследование проводится натощак.
При панкреонекрозе ультразвуковая картина, по сравнению с отечной формой панкреатита, более пестрая. В зависимости от объема поражения железы увеличиваются различные ее отделы, контуры становятся нечеткими. Паренхима крайне неоднородная.
При жировом панкреонекрозе преобладают зоны повышенной эхогенности с зонами разряжения, при геморрагическом — преимущественно определяются эхонегативные зоны, соответствующие некротически расплавленным тканям.
Практически у каждого второго больного с панкреонекрозом расширен вирсунгов проток. У каждого третьего пациента в фазе токсемии выявляется узкая полоска жидкости в различных отделах сальниковой сумки.
Многообразны и косвенные признаки панкреонекроза. У 90,8% больных обнаруживается жидкость в брюшной полости. УЗИ позволяет диагностировать даже ее незначительное количество в отлогих местах, а также признаки гастростаза и паралитической кишечной непроходимости.
Динамические ультразвуковые исследования помогают оценивать состояние ПЖ и забрюшинной клетчатки, органов гепатопанкреатодуоденальной зоны. При неэффективности лечения обнаруживаются дегенеративные изменения, жидкостные структуры сальниковой сумки и забрюшинной клетчатки.
Прежде всего деформируются контуры поджелудочной железы в соответствии с локализацией инфильтративного процесса. При тотальном панкреонекрозе орган не контурируется вообще в 95% случаев.
Из сосудистых структур определяется лишь аорта. При этом всегда пальпируется плотное образование в эпигастральной области. Оценивать структуру инфильтрата следует с дифференцировки полых органов (антрального отдела желудка, двенадцатиперстной и поперечноободочной кишки).
Компрессия выходного отдела желудка и двенадцатиперстной кишки приводит к дуодено- и гастростазу, которые выявляются с помощью УЗИ еще до появления клинических признаков.
При жировом некрозе за стенкой желудка определяются плотные структуры, чередующиеся с мелкими эхопозитивными включениями.
У 20—30% больных панкреонекрозом обнаруживаются скопления жидкости в сальниковой сумке — псевдокисты — даже при улучшении состояния и нормализации лабораторных показателей.
В панкреатологии хорошо известно, что эффективность различных вариантов лечения зависит от степени сформированности стенки кисты (особенно при проведении пункционных вмешательств).
Усиление сигнала за гнойником определяется в 70% случаев. Это объясняется тем, что лишь однородное содержимое полости хорошо проводит ультразвуковые волны. Вязкий гной служит существенным препятствием на пути ультразвуковых волн диагностической частоты.
Таким образом, широкие возможности контактного УЗИ позволяют считать эту методику обязательным этапом обследования больных с осложненным и неосложненным панкреонекрозом.
В последнее время для оценки состояния паренхимы поджелудочной железы и периампулярной зоны применяется сочетание ультразвукового сканирования и эндоскопии. Подобная методика дает возможность с большей достоверностью оценивать характер поражения ПЖ, объемных образований, прилежащих к задней стенке желудка.
Плотность поджелудочной железы в норме у пожилых и стариков превышает 40 ед. по шкале Хаунсфилда. После внутривенного контрастирования она повышается до 80 ед.
Компьютерная томография позволяет установить форму острого панкреатита, распространенность процесса как в железе, так и в забрюшинной клетчатке.
К прямым признакам острого панкреатита относится увеличение поджелудочной железы, нечеткость ее контура, негомогенность паренхимы и снижение денситометрической плотности.
При компьютерной томографии обнаруживаются полости в парапанкреатической клетчатке, содержащие гной и газ. Выявляются резидуальные абсцессы и прогнозируется течение гнойных осложнений.
Компьютерная томография практически безошибочно диагностирует псевдокисты. При внутривенном введении контрастного вещества кистозные образования (как и абсцессы) сохраняют первичную плотность. Положительное качество метода — возможность с высокой точностью оценить степень сформированности стенки кистозного образования.
Таким образом, компьютерная томография эффективна в распознавании различных форм острого панкреатита.
Обязательный этап обследования больных острым панкреатитом — гастродуоденоскопия. Гастроскопия помогает выявить лишь косвенные признаки заболевания (оттеснение стенок желудка и ДПК, инфильтрацию их стенок и стенозирование).
Вместе с этим значимость ее велика при оценке состояния слизистой указанных органов, обнаружении признаков воспаления, диагностике ее изъязвлений и язвенных дефектов, особенно при имеющихся признаках желудочно-кишечного кровотечения. Эти изменения встречаются как при отеке железы, так и при панкреонекрозе.
При гнойных осложнениях панкреонекроза гастроскопия может выявить высокие внутренние гнойные свищи при спонтанном вскрытии очагов в просвет желудка и ДПК. Катетеризация свищевого хода с последующим контрастированием полости (фистулография) помогает в оценке топографии полости, выявляет сообщение с протоковой системой поджелудочной железы.
Особое значение имеет дуоденоскопия с осмотром БДС и периампулярной области при вторичном панкреатите. При этом обнаруживаются признаки папиллита, ущемленного конкремента БДС, околососочковые дивертикулы (одиночные, множественные, с признаками дивертикулита), расширение продольной складки ДПК, полипы БДС. Подобные находки позволяют установить возможную причину панкреатита и провести этиотропное лечение.
Дуоденоскопия — обязательное исследование при остром панкреатите, амилаземии.
Несмотря на широкое использование в повседневной работе высокоинформативных методов диагностики, не потеряла своей значимости при остром панкреатите у больных пожилого и старческого возраста диагностическая лапароскопия.
В настоящее время при панкреонекрозе лапароскопия расценивается больше как лечебная методика. Проведение ее затруднено после повторных операций на органах брюшной полости, у больных с большими вентральными грыжами.
Исследование, требующее пневмоперитонеума, с особой осторожностью должно выполняться у пациентов, находящихся в крайне тяжелом состоянии, с нарушениями дыхательной и сердечной деятельности.
В настоящее время накопление опыта лапароскопии позволило сделать вывод о возможности получения прямых и косвенных доказательств различных форм аутолиза поджелудочной железы — как отека, так и панкреонекроза.
При отечной форме прямых признаков заболевания нет.
При сдавлении терминального отдела холедоха поджелудочной железой диагностируется увеличенный, напряженный желчный пузырь без признаков воспаления его стенки.
Ошибки в диагностике панкреонекроза составляют около 4%. В неясных случаях целесообразна динамическая лапароскопия, которая осуществляется через специальную гильзу или по ходу дренажа, установленного при первичном исследовании.
В настоящее время большинство хирургов единодушны во мнении о целесообразности применения уточненной диагностики в поздних стадиях заболевания.
Необходимость идентификации гнойного процесса при инфицированном панкреонекрозе заставило прибегать к тонкоигольным пункциям клетчаточных пространств с помощю игл Chiba под визуальным контролем, осуществляемым с помощью УЗИ и компьютерной томографии.
Своевременное выявление инфицированных очагов дает возможность аргументированно применять инвазивное лечение.
При проведении подобных манипуляций необходимо избегать повреждения сосудистых структур, что достигается визуальным контролем.
Получение жидкости помогает идентифицировать ее характер и выявить микрофлору. Это особенно важно при динамическом наблюдении за парапанкреатическим инфильтратом.
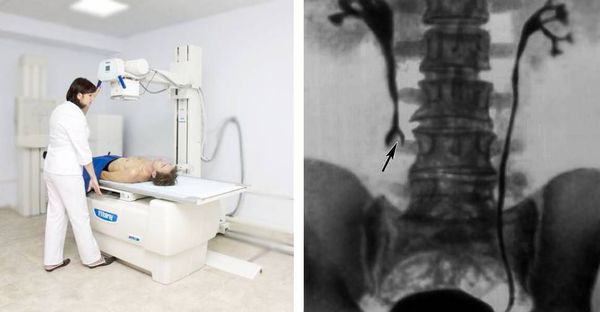
При дообследовании больных острым панкреатитом пожилого и старческого возраста значимо использование различных рентгеноконтрастных методов. Рентгенография желудка и ДПК помогает диагностировать нарушение эвакуации, явления гастроптоза, разворот подковы ДПК, сдавление ее горизонтальной ветви, увеличение ретрогастрального пространства при полипозиционном исследовании.
При имеющихся свищах, после дренирования полостей, сформированных на фоне панкреонекроза, необходимо проведение фистулографии водорастворимыми контрастными веществами. Это дает возможность четко определить характер свищевых ходов, выявить сообщение их с желудком, толстой, тонкой кишкой и т.п., а также локализацию и размеры полости, наличие затеков.
Таким образом, обследование больных острым панкреатитом — комплексный процесс, что подчеркивает необходимость госпитализации пациентов в специализированные стационары, где к этому есть все условия.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое стриктура мочеточника? Причины возникновения, диагностику и методы лечения разберем в статье доктора Мутин М. Ю., уролога со стажем в 6 лет.
Определение болезни. Причины заболевания
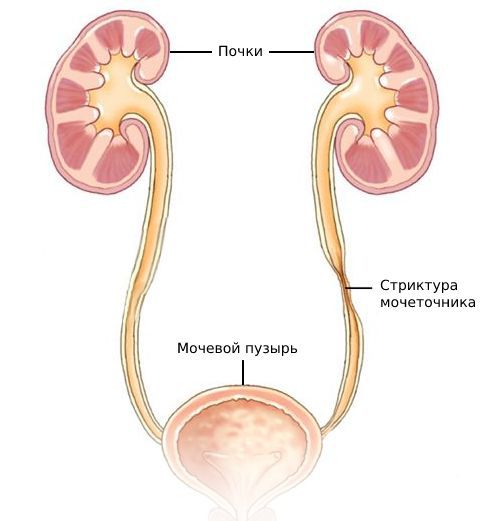
Стриктура (стеноз) мочеточника — это сужение его просвета, нарушающее нормальный отток мочи. Стриктуры могут возникать в любом участке мочеточника и в различной степени влиять на работу почки.
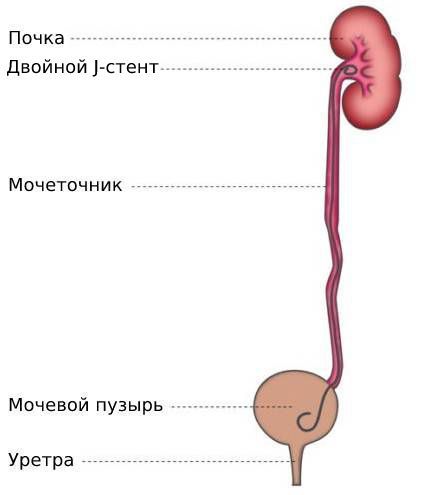
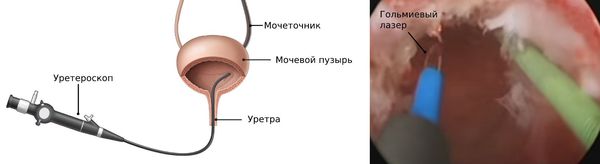
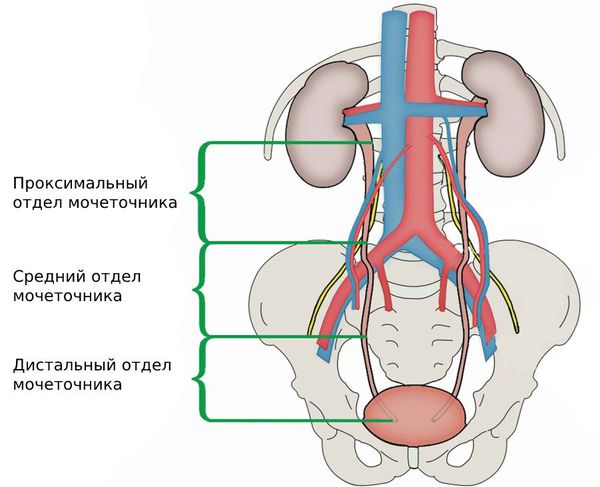
Мочеточник — это мышечная трубка, по которой моча из почки попадает в мочевой пузырь. Его длина около 25 см, верхняя половина находится в области живота, а нижняя — в области таза.
Причины стриктуры мочеточника
К основным причинам образования стриктуры мочеточника относятся:
Своевременная диагностика и лечение стриктуры мочеточника позволяют сохранить функцию почек и исключить злокачественные новообразования. Например, за доброкачественную стриктуру мочеточника может быть принята переходно-клеточная карцинома.
Кроме того, опухоли, такие как рак шейки матки, предстательной железы, яичников, груди и толстой кишки, могут проявляться как стриктура мочеточника.
Любое инструментальное воздействие на мочеточник в перспективе может привести к развитию его стриктуры. Повреждения мочеточника при операциях на органах брюшной полости и малого таза встречаются с частотой 0,1–0,2 %. Из всех интраоперационных повреждений мочеточника:
Мочеточники нередко повреждаются и при кесаревом сечении, как правило, при извлечении плода.
Другая причина образования стриктуры мочеточника — его непреднамеренное повреждение при операциях на других органах. Чаще это операции выполняются по поводу опухолей яичников, матки и толстой кишки.
Прочие причины доброкачественных стриктур мочеточника:
Пациентов со стриктурами мочеточника неизвестного происхождения следует обследовать с помощью компьютерной томографии. Это поможет исключить внутреннее злокачественное новообразование мочеточника или поражение, вызывающее внешнюю компрессию.
Симптомы стриктуры мочеточника
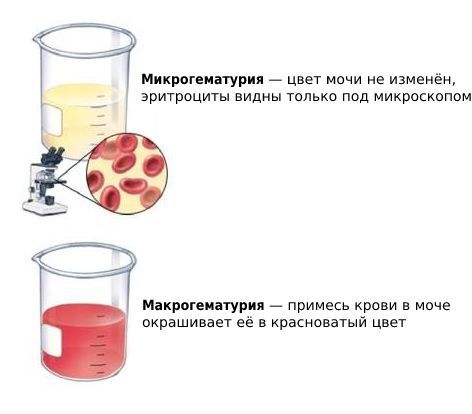
Большинство пациентов испытывают постоянную тупую боль в поясничной области, у других выявляется кровь в моче (гематурия) и признаки инфекции мочевыводящих путей. Также возможна комбинация этих симптомов.
Симптомы инфекции верхних мочевых путей:
У пациентов с единственной почкой, сопутствующей хронической болезнью почек или двусторонним поражением могут возникать симптомы почечной недостаточности.
Почечную недостаточность можно заподозрить при сочетании следующих симптомов:
Патогенез стриктуры мочеточника
Просвет мочеточника может сужаться при его случайной перевязке, развитии рубцовой ткани в стенке или при сдавлении извне, например крупной опухолью или рубцовым процессом в забрюшинном пространстве.
Классификация и стадии развития стриктуры мочеточника
Стриктуры мочеточника классифицируют по протяжённости, локализации и причине возникновения.
Классификация стриктур мочеточника
Злокачественные стриктуры:
Доброкачественные стриктуры:
Осложнения стриктуры мочеточника
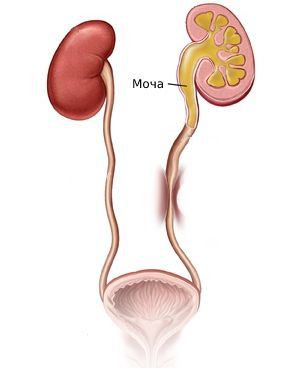
Сужение просвета мочеточника блокирует верхние мочевые пути с поражённой стороны и нарушает отток мочи. Затруднение пассажа мочи ведёт к прогрессивному ухудшению функции почки, вплоть до полной её потери.
Диагностика стриктуры мочеточника
Методы визуализации мочевыводящих путей:
В сложных случаях может потребоваться тест Уитакера для исследования давления-потока и постановки окончательного диагноза.
В настоящее время наиболее информативным диагностическим неинвазивным методом является мультиспиральная компьютерная томография с контрастированием (МСКТ).
Метод позволяет оценить:
Завершающим диагностическим, а в большинстве случаев и успешным лечебным шагом, является рентгенэндроурологическое вмешательство. При невозможности отведения мочи из почек без создания наружных свищей показана реконструктивная операция.
Показаниями к вмешательству являются:
Лечение стриктуры мочеточника
Эндоскопическое лечение
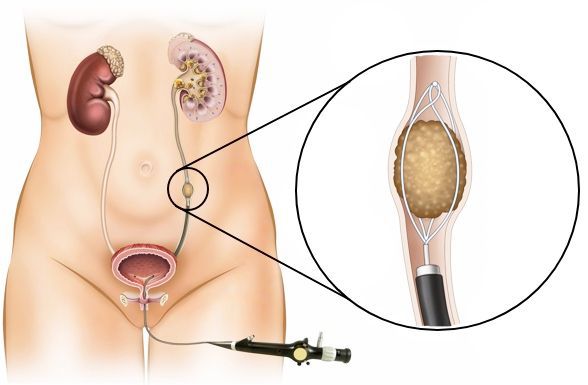
К эндоскопическим вмешательствам относятся:
Установка мочеточникового стента эффективна при лечении большинства стриктур мочеточника, в частности их внутренних разновидностей. При плохом прогнозе пациенту предлагается установить хронический стент с периодической его заменой. Хронический стент следует применять с осторожностью, особенно при лечении обструкции мочеточника при внешнем сдавлении, — в подобных случаях дренаж часто недолговечен.
Антеградная и ретроградная баллонная дилатация мочеточника. Вмешательство показано при функционально значимой обструкции. К противопоказаниям относятся инфекция в стадии обострения или стриктура длиной более 2 см — в таких ситуациях процедура редко бывает успешной. Более того, при стриктурах, превышающих 2 см, любая эндоскопическая техника может потерпеть неудачу.
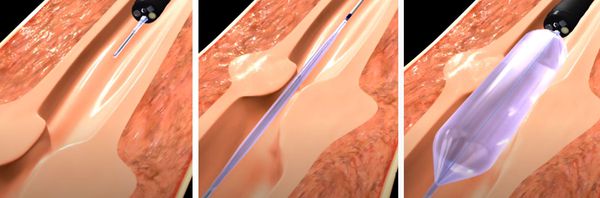
Операция заключается во введении в мочеточник специального баллона под контролем эндоскопа и рентген-аппарата. Баллонный катетер размещается поперёк области стриктуры. Правильно расположить его помогают рентгенконтрастные маркеры на концах балона.
Затем баллон надувается. Через 10 минут тампонады его сдувают и извлекают. После процедуры устанавливают внутренний стент-катетер, который оставляют на 2—4 недели. Контрольные исследования обычно проводятся через один месяц после извлечения стента, а затем с интервалами от 6 до 12 месяцев.
Эндоуретеротомия. Внутрипросветный разрез мочеточника — продолжение баллонной дилатации для малоинвазивного лечения стриктур. Процедура проводится с использованием уретероскопического или рентгеноскопического контроля. Сам разрез выполняют с помощью холодного ножа, режущего электрода или гольмиевого лазера.
Перед хирургическим вмешательством тщательно оценивают характер, местоположение и длину стриктуры мочеточника. Предоперационная оценка обычно включает внутривенную урографию (или антеградную пиелографию) и ретроградную пиелографию при наличии показаний. Пиелография — это прямое введение контрастного вещества в просвет верхних мочевых путей. Препарат можно ввести ретроградно, то есть через катетер, установленный в мочеточник, или антеградно — через иглу или нефростомическую трубку.
Другие исследования, такие как γ-сцинтаграфия для оценки функции почек и уретероскопия для исключения карциномы, назначаются строго индивидуальны.
Основные преимущества эндоуретеротомии:
Эффективность эндоуретеротомии и баллонной дилатации мочеточников в лечении постлучевых стриктур мочеточника, к сожалению, крайне мала. Это обусловлено нарушением регенерации облученной ткани мочеточника. Одна из основных трудностей в лечении пациентов с постлучевыми поражениями мочеточников — это риск рецидивирования болезни, обусловленный долго незаживающими поражениями тканей.
Уретероуретеростомия
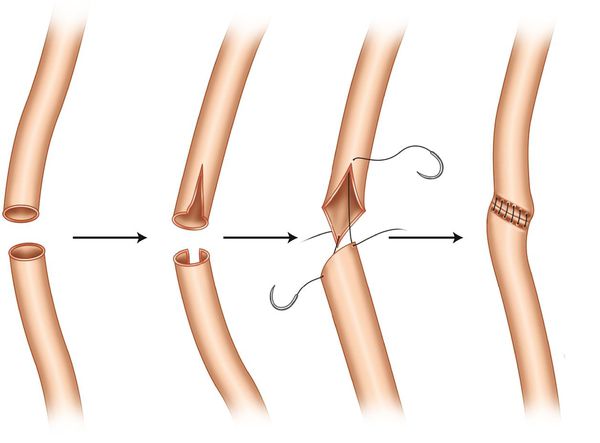
При коротком дефекте, затрагивающем верхний или средний отдел мочеточника, либо после недавней травмы рекомендована уретероуретеростомия — операция по искусственному соединению мочеточников.
Прямая уретеронеоцистостомия. Уретеронеоцистостомия без применения методов Psoas hitch или лоскута Боари проводится у взрослых при травме или обструкции, затрагивающей дистальные 3-4 см мочеточника.
После хирургического разреза мочеточник рассекается на уровне обструкции. Прямая уретеронеоцистостомия выполняется только в том случае, если возможно соединить участки мочеточника без натяжения (наложить анастомоз).
При лечении дистальной стриктуры мочеточника уретеронеоцистостомия обычно выполняется через брюшную полость. В послеоперационном периоде, как и при открытой хирургии, применяется стентирование мочеточника.
Клинические исходы лапароскопического лечения дистальных стриктур мочеточника благоприятны и сопоставимы с результатами при открытых хирургических операциях. Лапароскопия проводится через проколы на поверхности тела. Лапароскоп передаёт изображение внутренних органов на монитор, где хирург с увеличением видит всё необходимое для операции.
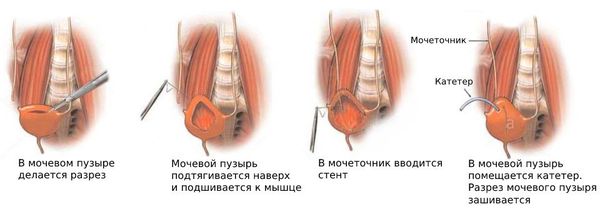
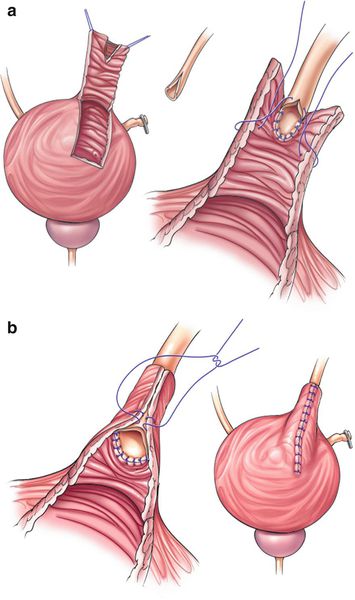
Psoas hitch
Мочеточник выводится в просвет мочевого пузыря, после чего проводится анастомоз без натяжения с подслизистым туннелем или без него. Для дренирования обычно используется двойной J-стент.
Осложнения возникают редко, но возможно формирование мочевого свища, непроходимости мочеточника, уросепсиса, повреждения кишечника и подвздошной вены. Результаты применения лапароскопического доступа на сегодняшний день удоволетворительны и эквивалентны открытой хирургии.
Лоскут Боари
Метод состоит в выкраивании из стенки мочевого пузыря П-образного лоскута, которым замещают часть мочеточника с нарушенной проходимостью.
Замещение мочеточника отключённым сегментом подвздошной кишки
Метод противопоказан при исходной почечной недостаточности с уровнем креатинина сыворотки более 2 мг/дл, дисфункции мочевого пузыря, обструкции выходного отверстия, воспалительном заболевании кишечника и лучевом цистите.
Аутотрансплантация
Прогноз. Профилактика
Злокачественные стриктуры — осложнение распространённого опухолевого процесса, поэтому прогноз напрямую зависит от течения основного заболевания.
Несмотря на внедрение малоинвазивных технологий в различных хирургических специальностях, проблема травмы мочеточников до сих пор остаётся актуальной, особенно после акушерско-гинекологических операций. Это объясняется близостью внутренних половых органов и мочевых путей и их обильным кровоснабжением.