что такое зона мантии
Мантийноклеточная лимфома: причины, симптомы, стадии, диагностика, лечение, прогноз
Мантийноклеточная лимфома (МКЛ) — злокачественная опухоль из В-лимфоцитов, клеток иммунной системы. Относится к так называемым неходжкинским лимфомам, когда злокачественная опухоль возникает не только в лимфоузлах, но и миндалинах, селезенке и других органах нашей иммунной системы.
МКЛ составляет 6-10% от всех диагностированных неходжкинских лимфом. Данный вид рака характеризуется высокой агрессивностью. Встречается чаще всего у мужчин старше 60 лет. МКЛ может поражать отдельные лимфатические узлы, селезенку, органы (костный мозг, оболочки головного мозга, желудочно-кишечный тракт), или быть генерализованной, распространяясь по всему организму с током крови.
Главной причиной развития мантийноклеточной лимфомы считают генные мутации, приводящие к повышенной экспрессии (активности) ядерного белка циклина D1, участвующего в регуляции клеточного деления. Повышение синтеза этого белка приводит к ускорению деления клеток и способствует развитию опухоли.
Симптомы лимфом из клеток мантии
Клиническая картина МКЛ не отличается от таковой при других типах лимфомы и будет зависеть от локализации и стадии процесса. На начальных этапах опухоль может протекать бессимптомно, или же могут проявляться общие симптомы:
• Необъяснимое повышение температуры тела в вечернее или ночное время.
• Снижение массы тела без видимых на то причин.
• Слабость и быстрая утомляемость.
• Усиленная потливость в ночное время.
• Кожный зуд.
Если опухоль локализуется в селезенке, наблюдается её увеличение и как следствие тяжесть в левом подреберье. О вовлечении в опухолевый процесс лимфатических узлов свидетельствует их безболезненное увеличение. Опухоль, развивающаяся в слизистой оболочке желудка или кишечника, может выглядеть как полип на начальных этапах и протекать бессимптомно. При прогрессировании опухоли появляются симптомы диспепсии, боли в животе и даже кишечная непроходимость (тошнота, рвота, задержка стула, вздутие и схваткообразные боли в животе). При поражении миндалин наблюдается увеличение их размеров, заложенность носа, нарушение глотания и дыхания. При локализации опухоли в ЦНС развиваются расстройства слуха и зрения, головные боли, парезы и параличи. По мере прогрессирования опухоли, проявления будут усиливаться, и клиническая картина будет формироваться из симптомов, характерных для пораженного органа.
Стадии мантийноклеточной лимфомы
Стадия 1 — опухолевое поражение одной группы лимфоузлов.
1Е — опухолевое поражение одного экстранодального (вне лимфатических узлов) органа.
Стадия 2 — вовлечение в опухолевый процесс двух групп лимфоузлов по одну сторону диафрагмы.
2Е — вовлечение одного экстранодального органа и одной группы лимфоузлов по одну сторону диафрагмы.
Стадия 3 — опухолевое поражение лимфоузлов по обе стороны диафрагмы, сочетающееся с:
3Е — поражением экстранодального органа;
3S — опухолевым поражением селезенки;
3E+S — поражением экстранодального органа и селезенки.
Стадия 4 — многофокусное поражение одного или нескольких экстранодальных органов с или без вовлечения лимфатических узлов.
Диагностика мантийноклеточной лимфомы
1) Сбор анамнеза. Уточняются наличие у близких родственников опухолевых процессов, наличие у пациента хронических заболеваний, ранее перенесенных инфекций.
2) Физикальное обследование. Обращают на себя внимание бледность кожных покровов, увеличение в размерах селезенки и лимфоузлов при пальпации.
3) Лабораторная и инструментальная диагностика.
• Общий анализ крови с подсчетом лейкоцитарной формулы (в том числе определение количества ретикулоцитов и тромбоцитов).
• Биохимический анализ крови (общий белок, альбумин, мочевина, креатинин, мочевая кислота, электролиты, АЛТ, АСТ, щелочная фосфатаза, ЛДГ, глюкоза).
• Общий анализ мочи.
• Коагулограмма (фибриноген, АЧТВ, протромбиновый индекс, Д-димеры).
• Иммунохимическое исследование мочи и крови с измерением концентрации b2-микроглобулина.
• Биопсия с патогистологическим и иммуногистохимическим исследованиями опухолевой ткани.
• Трепанобиопсия костного мозга с подсчетом миелограммы.
• Цитогенетическое исследование или FISH-исследование опухолевой ткани или костного мозга.
• Люмбальная пункция с цитологическим исследованием ликвора по показаниям.
• ПЦР и ИФА для диагностики инфекций.
• УЗИ органов брюшной полости.
• КТ органов шеи, грудной клетки, брюшной полости и полости малого таза.
• КТ и МРТ костей лицевого скелета и головного мозга по показаниям.
• Позитронно-эмиссионная томография (позволяет выявить распространенность опухолевого процесса).
• ФГДС и колоноскопия с обязательным проведением биопсии, даже при неимении визуальных признаков поражения.
• ЭКГ и ЭХоКГ.
Лечение мантийноклеточной лимфомы
Лечение МКЛ подбирается в каждом случае индивидуально, зависит от стадии лимфомы, ее морфологического строения, возраста и общего состояние пациента.
У пациентов с 1-2 стадией опухоли преимущественно используется комбинация химиотерапии и лучевой терапии, что дает возможность достичь ремиссии в 95% случаев.
Пациентам с 3-4 стадией до 65 лет при отсутствии противопоказаний проводится 6-8 курсов интенсивной полихимиотерапии в сочетании с препаратами из группы моноклональных антител (таргетных препаратов) и последующей аутотрансплантацией гемопоэтических стволовых клеток (аутоТГСК — трансплантация пациенту собственных гемопоэтических стволовых клеток). В течение года после проведения аутоТГСК каждые три месяца проводятся контрольные исследования, в том числе трепанобиопсия. В последующие пять лет исследования проводятся каждые 6 месяцев. В случае рецидива назначается курс таргетных препаратов или полихимиотерапия.
Пациенты с 3-4 стадией в возрасте старше 65 лет получают 6-8 курсов полихимиотерапии с последующей поддерживающей терапией таргетными препаратами. Поддерживающая терапия назначается каждые 2 месяца в течении двух лет.
Прогноз мантийноклеточной лимфомы
МКЛ является агрессивным видом рака. До недавнего времени медиана выживаемости составляла 3 года. Однако современные схемы высокодозной химиотерапии и аутоТГСК у молодых пациентов, появление большого числа эффективных альтернативных схем химиотерапии для последовательного применения при рецидивах МКЛ или при резистентности к лечению, появление новых таргетных препаратов для лечения МКЛ и развитие стратегий поддерживающей терапии привели к улучшению показателей выживаемости. В последние годы медиана выживаемости больных со впервые диагностированной МКЛ увеличилась с 3 до 6 лет.
Следует отметить, что в 15% случаев болезнь протекает благоприятно и прогноз продолжительности жизни составляет 10 лет и более.
Лимфома мантийной зоны
Содержание Скрыть
Лимфома из клеток мантийной зоны представляет собой первичную форму онкологического процесса одной из разновидностей рака лимфатической системы. Диагностируется заболевание в 6 процентах случаев от всех неходжкинских лимфом. Часто выявляется у пожилых людей, в большей степени у мужской половины населения.
Течение болезни может быть медленным или стремительным. Заболевание не поддается излечению, есть только варианты, как достичь стойкой ремиссии.
Что такое
Мантийноклеточная лимфома представляет собой патологический процесс, который характеризуется мутированием хромосом. Болезнь протекает бессимптомно, первые признаки появляются уже на поздних стадиях. При таком состоянии поражению подвергаются не только лимфоузлы, но также и другие внутренние органы.
Заболевание в каждом случае характеризуется индивидуальным течением. Если у одних больных оно развивается медленными темпами, то у других может отличаться более агрессивным ростом.
Классификация
Выделяют несколько форм данного онкологического процесса.
Нодальная
В патологической процесс могут вовлекаться различные группы узлов лимфатической системы. Иногда поражается селезенка.
Первично-экстронодальная
Для этого типа характерно изолированное поражение глаз, желудка. Также может отмечаться локализация в области слюнных желез и слизистой тонкого кишечника.
Селезеночная
Опухолевые клетки располагаются на слизистой носовых пазух, носа или глотки.
Генерализованная
Ее формирование происходит в результате распространения злокачественных клеток по человеческому организму. При этом опухоль затрагивает разные группы лимфоузлов, костный мозг, селезенку, слизистую органов ЖКТ. Также клетки могут выявляться в периферической крови.
Согласно классификации Ann-Abor, онкологическое заболевание проходит 4 стадии в своем развитии.
Первая
Болезнь имеет локализованный характер. Как правило, в процесс вовлекается только 1 группа узлов. В периферической крови атипичных клеточных структур не обнаруживается.
Вторая
Заболевание поражает соседние области лимфатических узлов, которые локализуются только с одной стороны диафрагмы. Другими словами, наличие патогенных клеток можно установить только в области брюшинного пространства или грудной клетки.
Третья
Поражаются все области. Другими словами, злокачественные клетки могут проникать в смежные области, которые располагаются ниже или выше диафрагмы.
Четвертая
Злокачественная опухоль выходит за пределы лимфосистемы. Метастазирование распространяется на сердце, желудочно-кишечный тракт, печень и другие жизненно важные органы.
Причины
Точные предрасполагающие факторы, которые могут способствовать развитию лимфомы, так установить не удалось. Согласно наблюдениям, было выявлено, что у большинства пациентов в организме присутствовали злокачественные клетки с изменениями на уровне генетики. Другими словами, при делении отмечается измененная структура в 11 и 14 парах хромосом.
На фоне такого генетического дефекта выработка циклина Д1 начинает увеличиваться. Именно этот элемент осуществляет контроль за ростом и делением клеток. При таком состоянии В-лимфоциты начинают бесконтрольно увеличиваться.
Также не было выявлено причин, которые могли бы объяснить такую клеточную транслокацию. Однако удалось выяснить, что риск развития лимфомы мантийной зоны значительно возрастает при воздействии на организм некоторых химических веществ, а также радиоактивного излучения.
Симптомы
Течение онкологического процесса, как правило, сопровождается следующей клинической картиной:
Стоит также отметить, что в большей степени проблемам подвергается желудочно-кишечный тракт, о чем свидетельствует формирование полипов, изъязвлений, эрозий. Кроме того, слизистая начинает уплотняться. Часто наблюдается формирование лимфатических фолликулов.
Диагностика
При первом посещении пациента специалист, прежде всего, должен собрать всю необходимую информацию относительно анамнеза его жизни и имеющихся жалоб. После этого проводится физический осмотр, при котором врач уже может распознать, что лимфоузлы имеют увеличенные размеры.
Мы делаем медицинскую информацию понятной, доступной и актуальной.
Лимфома из клеток мантийной зоны: причины возникновения, симптомы и методы лечения
Лимфома из клеток мантийной зоны (синоним – мантийноклеточная лимфома) – редкий подвид неходжкинской лимфомы, который развивается у 2-3 из каждых 100 000 человек. Чаще всего страдают от патологии пациенты пожилого возраста – средний возраст – 65 лет. Мужчины заболевают ежегодно примерно в 4 раза чаще, чем женщины. В международной классификации болезней (МКБ-10) лимфома из клеток мантийной зоны обозначается кодом C83.1.
В чем суть заболевания?
Для мантийноклеточной лимфомы характерно поражение лимфоузлов, селезенки, печени и костного мозга
Большинство клеток организма живут только в течение ограниченного времени и должны постоянно меняться – делиться. Клеточное деление приводит к образованию двух идентичных дочерних клеток из одной. Процесс похож на копирование – дублируется вся информация клетки. Из-за ошибок естественный цикл может выйти из равновесия. Поскольку клетка продолжает делиться, она распространяет «ошибочную» информацию.
Деление и специализация В-лимфоцитов происходят в так называемых зародышевых центрах, которые также именуют лимфоидными фолликулами. Это сферические B-клеточные скопления, которые встречаются в местах с большим количеством патогенов – особенно в лимфатических узлах, селезенке и миндалинах. При мантийноклеточной лимфоме наблюдается увеличение количества «дефектных» В-лимфоцитов. Злокачественные клетки напоминают В-лимфоциты, которые обычно находятся в пограничной области – мантийной зоне.
Причины
Точная причина развития лимфомы из различных клеток мантийной зоны до конца не изучена. У многих пациентов имеются опухолевые клетки с характерным изменением генетической информации – в ходе деления возникают изменения на 11 и 14 парах хромосом. В результате генетического дефекта увеличивается синтез циклина D1, который контролирует деление и рост клеток. Это приводит к неконтролируемому увеличению количества В-лимфоцитов.
Факторы, которые вызывают эту транслокацию, также неизвестны, но некоторые химические вещества и радиация могут увеличить риск развития генетических мутаций.
Симптомы
При заболевании лимфомы ощущается сильная слабость и вялость во всем организме
Накопление злокачественных клеток приводит к увеличению лимфатических узлов и селезенки. В большинстве случае лимфоузлы и селезенка не реагируют на давление или прикосновение болью, поэтому патология зачастую выявляется только на поздних стадиях.
Клетки лимфомы также оседают в костном мозге: они препятствуют нормальному образованию клеток крови и, таким образом, вызывают симптомы, которые могут возникать и при других, более безвредных заболеваниях и инфекциях. Многие пациенты с лимфомой ощущают сильную слабость и снижение производительности труда.
Причиной этой слабости является отсутствие эритроцитов, которые отвечают в организме за перенос кислорода. Образование лейкоцитов, особенно нейтрофильных гранулоцитов и «здоровых» В-лимфоцитов, также ограничено при вовлечении костного мозга. Снижение концентрации лейкоцитов приводит к повышенной восприимчивости к инфекциям. Уменьшенное количество тромбоцитов – клеток, которые участвуют в заживлении ран, – может косвенно увеличивать кровоточивость десен, провоцировать кровотечение из носа. Если клетки мантийноклеточной лимфомы накапливаются в желудочно-кишечном тракте (25-60%) или в центральной нервной системе (4-20%), могут возникать симптомы, связанные с этими органами – нарушения пищеварения и неврологические расстройства.
Диагностика
С помощью анализа иммунофенотипирования можно узнать, в какой стадии развития находятся злокачественные клетки лимфомы
В начале каждого диагностического обследования обычно собирается анамнез. При физическом осмотре врач может выявить увеличенные лимфатические узлы. Изменение органов брюшной полости – увеличение селезенки или печени – врач часто может распознать и без технических вспомогательных средств. Чтобы выяснить, действительно ли пациент страдает от лимфомы из клеток зоны мантии, необходимо провести обследование крови, а затем осмотреть увеличенный лимфоузел.
Если клетки лимфомы оседают в костном мозге, они мешают нормальному образованию крови, это приводит к отклонениям в картине крови. С помощью общего анализа можно выявить количество красных и белых кровяных телец, а также тромбоцитов. Поскольку лимфома не выявляется в анализах крови на ранней стадии, могут потребоваться дополнительные обследования.
Если возникает подозрение на лимфому, проводится гистологическое исследование лимфатической ткани, которое помогает точно поставить диагноз. Ткань для исследования берут из увеличенных лимфоузлов. Хирургическая процедура обычно не занимает много времени и часто выполняется в амбулаторных условиях под местной анестезией.
Существуют также варианты лимфом из клеток мантийной зоны, которые очень похожи на другие типы злокачественных новообразований: хроническую лимфоцитарную лейкемию или диффузную В-крупноклеточную лимфому. Поэтому всегда необходимо проводить дополнительные анализы. С помощью так называемой флуоресцентной гибридизации можно выявить генетические мутации, типичные для мантийноклеточной лимфомы.
Другое исследование относится к скорости роста опухолевых клеток: ее определяют с помощью теста на антитела и выражают в процентах. Чем выше этот процент, тем быстрее делятся раковые клетки. Патологоанатом также исследует поверхностные структуры опухолевых клеток, что называется иммунофенотипированием. Также с помощью иммунофенотипирования можно узнать, в какой стадии развития находятся злокачественные клетки.
Классификация
Уровень стадии заболевания зависит от того, в какой степени лимфома распространилась в организме и от каких симптомов страдает пациент. Для этой цели используется относительно простая схема, которая установлена на международном уровне для оценки стадии заболевания – классификация Анн-Арбор. В классификации учитывают не только лимфатические узлы, но и органы вне них.
Дополнительные обозначения в зависимости от наличия или отсутствия симптомов:
Лечение
Примерно у 10-15% пациентов мантийноклеточная лимфома протекает бессимптомно. В этих случаях начало терапии часто задерживается на некоторое время. Тем не менее, в течение этого времени болезнь должна регулярно контролироваться, так как некоторые изначально вялотекущие лимфомы могут превращаться в агрессивные формы.
Терапия не начинается до тех пор, пока не появляются значимые симптомы: увеличение размера лимфоузлов или появления новых патологий. Некоторые лабораторные значения могут указывать на прогрессирование заболевания (например, значение лактатдегидрогеназы, количество лейкоцитов).
Радиотерапия
Облучение эффективно только в краткосрочной перспективе, если заболевание находится на 3-4 стадии
Если мантийноклеточная лимфома выявляется на I и II стадии и сопровождается незначительным увеличением лимфоузлов, она может быть подавлена лучевой терапией. Опухолевые клетки обычно более чувствительны к радиации, чем окружающие здоровые клетки организма. Как и при химиотерапии, лучевая терапия подразделяется на несколько этапов. Большую часть времени облучают определенные области тела, в которых присутствует наибольшее количество злокачественных клеток.
Химиотерапия
Основой большинства подходов к лечению лимфомы являются химиотерапевтические препараты, которые используются в разных комбинациях или дозировках. Химиотерапия – это лекарственная терапия, которая непосредственно повреждает опухолевые клетки. Поскольку раковые клетки размножаются быстро и неконтролируемо, они особенно восприимчивы к цитостатическим препаратам.
Химиотерапия влияет на все тело и разрушает не только видимые большие опухоли, но и иногда здоровые клетки организма. Цитостатические препараты можно вводить в комбинации с другими средствами. Обычно пациенту вводят лекарства через капельницу, но на фармацевтическом рынке также продаются цитостатические таблетки. Поскольку только одна часть опухолевых клеток может быть повреждена с помощью сеанса химиотерапии, обычно она назначается в несколько циклов с интервалом в несколько дней или недель.
Иммунохимиотерапия
В сочетании с химиотерапией, при лимфоме часто назначаются антитела
Если в дополнение к цитостатическим средствам вводят антитела, это называют иммунохимиотерапией. Моноклональные антитела не разрушают напрямую быстрорастущие клетки, но помогают иммунитету распознавать их поверхностные структуры. В зависимости от того, какое антитело используется, оно оказывает прямое вредное воздействие на опухолевые клетки. Антитела часто назначаются в сочетании с химиотерапией. Однако их также можно вводить отдельно в качестве поддерживающей терапии.
Поддерживающая терапия
Если возможно подавить лимфому иммунохимиотерапией, следует использовать поддерживающую терапию Ритуксимабом. Цель поддерживающей терапии – сохранить успех лечения на длительное время. Поскольку Ритуксимаб еще не одобрен для поддерживающей терапии при мантийноклеточной лимфоме, необходимо согласовать применение с лечащим врачом.
Прогноз
Примерно у 9 из 10 пациентов мантийноклеточная лимфома поражает органы вне лимфатической системы. Большинство мантийноклеточных лимфом диагностируются на III-IV стадии по классификации Анн-Арбор. Поскольку это очень агрессивная неходжкинская лимфома, лечение обычно начинается сразу после выявления заболевания. На I и II стадии болезнь может быть вылечена лучевой терапией, в то время как на III и IV стадии ее можно только подавить.
Лимфомы клеток мантийной зоны. Новые возможности диагностики и лечения (эпидемиологическое исследование)
Полный текст:
Аннотация
Введение. Лимфома клеток мантийной зоны — редко встречающийся вариант В-клеточной неходжкинской лимфомы. По статистике из 100 000 человек заболевает 2–3, что составляет примерно 6 % от общего количества больных неходжкинскими лимфомами. Известно, что различные молекулярно-генетические характеристики пациентов с лимфомой мантийной зоны могут обеспечить персонифицированный подход при определении прогноза болезни и тактики лечения.
Материалы и методы. Проведен ретроспективный анализ 45 пациентов с лимфомой зоны мантии, наблюдавшихся в ГАУЗ РКОД Минздрава в период с 2015 г. по настоящее время. При анализе учитывались данные клинико-лабораторного обследования, позитронно-эмиссионная томография, цитологическое, гистологическое и иммуногистохимическое исследования биоптата опухоли и костного мозга. Проанализированы эпидемиологические данные, клинические характеристики пациентов, терапевтические подходы, непосредственные и отдаленные результаты лечения.
Результаты и обсуждение. Установлено, что наиболее часто в патологический процесс вовлекается костный мозг (44 %) и селезенка (41 %). Распределение MIPI: высокий у 14 (30 %), средний у 20 (45 %), низкий у 11 (25 %). Ki67 в 4 случаях менее 30 %, в остальных более 30 %. Пациентам c 2015 по 2017 г. в первой линии проводилась химиотерапия в режиме R-CHOP с последующей поддержкой ритуксимабом. Средняя БПВ составила 20 месяцев, 8 (17 %) пациентов в статусе длительной ремиссии (с 2015 г.). С 2017 г. в первой линии терапии начали применяться режимы R-BAC (схема с высокодозным цитарабином для кандидатов на ТСК) и R-B (для пожилых и коморбидных). С 2018 г. 8 пациентам проведена аутоТСК (в 1-м позднем рецидиве) как этап консолидации лечения. На данный момент обследование на del17p и мутацию TP53 проведено 13 пациентам в федеральных центрах.
Заключение. Продемонстрирована необходимость и варианты терапии в зависимости от результатов молекулярно-генетического анализа лимфомы клеток мантийной зоны.
Ключевые слова
Для цитирования:
Канкумашева Э.И., Валиахметова Ч.Х. Лимфомы клеток мантийной зоны. Новые возможности диагностики и лечения (эпидемиологическое исследование). Креативная хирургия и онкология. 2019;9(4):261-265. https://doi.org/10.24060/2076-3093-2019-9-4-261-265
For citation:
Kankumasheva E.I., Valiakhmetova C.K. Mantle Zone Cell Lymphomas. New Opportunities for Diagnosis and Treatment (Epidemiological Research). Creative surgery and oncology. 2019;9(4):261-265. (In Russ.) https://doi.org/10.24060/2076-3093-2019-9-4-261-265
Введение
Лимфома клеток мантийной зоны (ЛКМЗ) — это редко встречающийся вариант В-клеточной неходжкинской лимфомы. По статистике из 100 000 человек заболевает 2-3, что составляет примерно 6 % от общего количества больных неходжкинскими лимфомами. Среди впервые выявленных случаев соотношение между мужчинами и женщинами составляет 4:1, а медиана возраста — 65 лет. В Западной Европе, Скандинавии и США частота ЛКМЗ варьирует от 0,5 до 0,7 на 100 000 населения, у людей старше 65 лет заболеваемость возрастает до 3,9 на 100 000 [1,2]. Таким образом, различные молекулярно-генетические характеристики у пациентов с лимфомой мантийной зоны могут обеспечить персонифицированный подход при определении прогноза болезни и тактики лечения. В этой связи основной целью данного исследования является анализ эпидемиологической ситуации в Республике Башкортостан, диагностических и терапевтических подходов у пациентов с лимфомой зоны мантии в период от 2015 г. по настоящее время с оценкой возможностей внедрения новых методов диагностики и лечения ЛКЗМ.
Материалы и методы
В ретроспективный анализ были включены 45 пациентов с лимфомой зоны мантии, наблюдавшихся в ГАУЗ РКОД Минздрава в период с 2015 г. по настоящее время. При анализе учитывались данные клинико-лабораторного обследования (100 % обследованных), позитрон- но-эмиссионная томография (100 % обследованных), цитологическое, гистологическое и иммуногистохимическое исследования биоптата опухоли и костного мозга (100 %). Проанализированы эпидемиологические данные: распределение по полу, возрасту и местности проживания. Проанализированы клинические характеристики пациентов: зоны поражения, распространенность, лабораторные показатели, имму- ногистохимические особенности. Проанализированы терапевтические подходы (режимы химиотерапии, использованные в дебюте заболевания и в рецидивах), непосредственные и отдаленные результаты лечения.
Результаты и обсуждение
В основном ЛКМЗ является агрессивно протекающей лимфомой, при которой поражаются лимфатические узлы, кольцо Вальдейера, селезенка, костный мозг, печень, желудочно-кишечный тракт, орбита и другие экс- транодальные органы. Лишь в 10 % случаев ЛКМЗ обладает индолентным течением.
Из года в год лимфома клеток мантийной зоны привлекает к себе пристальное внимание, что связано с особенностью патогенеза и, как следствие, диагностики и лечения.
С целью диагностики и адекватного стадирования ЛКМЗ используются практически все методы инструментального исследования. Наряду с ПЭТ/КТ крайне важны методы эндоскопического исследования: фиброларингоскопия, фибробронхоскопия, фиброгастродуоденоскопия, фиброколоносокпия, т.к. при ЛКМЗ поражаются любые органы и системы. Морфологическая верификация возможна благодаря иммуногистохимическому и молекулярно-генетическому методам. Современные исследования показали, что ЛКМЗ характеризуется гиперэкспрессией ядерного белка циклин D1 и хромосомной транслокацией t(11;14)(q13;q32). Имеет 6 морфологических вариантов: моноцитоидоподобный, с плазмоцитарной дифференцировкой, пролимфоцитоидный, классический, мелкоклеточный, бластоидный (плеоморфный).
Таким образом, основным моментом в патогенезе ЛКМЗ считается транслокация t(11; 14)(q13; q32). Оптимальным способом определения t( 11; 14)(q13; q32) является флуоресцентная гибридизация in situ (FISH): частота выявления транслокации этим методом при ЛКМЗ достигает 99 %. В результате мутаций гена CCND1, находящегося в 13-м локусе длинного плеча 11-й хромосомы, происходит гиперэкспрессия белка-регулятора клеточного цикла циклина D1. Установление факта избыточной экспрессии циклина D1 является одним из основных молекулярных и иммунологических маркеров ЛКМЗ [3, 5-7].
Нейрональный фактор транскрипции SOX11 напрямую регулирует несколько онкогенных путей, включая пролиферацию, контроль клеточного цикла и апоптоз, дифференцировку В-клеток, ангиогенез, и микроокружение опухоли. В зависимости от экспрессии SOX11 выделяют 2 варианта ЛКМЗ: SOX11 позитивный, характеризующийся агрессивным течением и неблагоприятным прогнозом, и SOX11 негативный, для которого характерна стабильность генома, индолентное течение и более благоприятный исход [4, 8-10]. Пролиферативный индекс Ki-67 может быть сопряжен со степенью клинической агрессивности ЛКМЗ, т. е. низкий пролиферативный индекс обычно соответствует более благоприятному клиническому течению, в то время как высокий пролиферативный индекс сопряжен с меньшей продолжительностью выживания после установления диагноза [1].
ЛКМЗ характеризуется нестабильностью кариотипа и значительным количеством вторичных хромосомных аберраций. В последнее время описано большое количество случаев ЛКМЗ, сопровождающихся наличием однородительских дисомий, способствующих инактивации генов-супрессоров опухоли. Например, одна из наиболее часто обнаруживаемых однородительских дисомий включает участок короткого плеча 17-й хромосомы и способствует инактивации гена TP53, кодирующий белок 53, транскрипционного фактора, регулятора клеточного цикла. Р53 выполняет функцию супрессора, соответственно ген TP53 является антионкогеном. Известно, что пациенты с данной мутацией относятся к группе с крайне неблагоприятным прогнозом с медианой общая выживаемость (ОВ) не более 1,5 года даже после проведения высокодозной химиотерапии [3, 5, 7, 11-13].
В связи с такими молекулярно-генетическими особенностями современные подходы к лечению ЛКМЗ меняются. И описанные выше факторы необходимо учитывать при выборе терапии. Так, если в предыдущие десятилетия стандартом лечения считался режим R-СНОР, то основными тенденциями в терапии ЛКМЗ за последнее десятилетие являются: интенсификация индукционной терапии высокими дозами цитарабина для пациентов моложе 60 лет; проведение аутоТГСК в качестве консолидации первой ремиссии у пациентов моложе 60-65 лет; применение комбинаций средних доз цитарабина с бендамустином, платиносодержащими препаратами, бортезомибом; а также добавление бортезомиба к CHOP-подобным режимам для пациентов старше 60-65 лет; а пациентам, у которых выявлена делеция короткого плеча хромосомы 17 или мутации TP53, применение ингибиторов тирозинкиназы Брутона — ибрутиниба [6, 12-16].
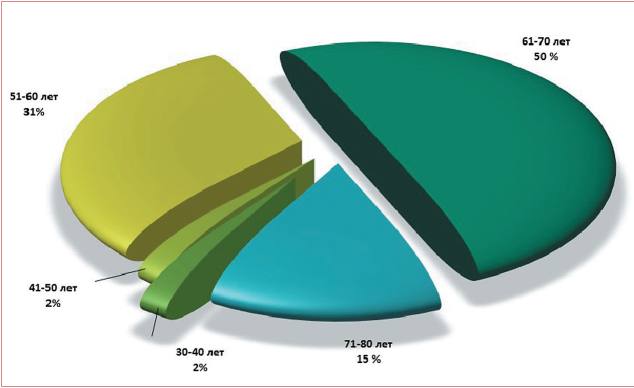
По результатам нашего анализа установлено, что пациенты с лимфомой зоны мантии в Республике Башкортостан составляют около 7 % от общего числа пациентов с неходжкинскими лимфомами, что практически сопоставимо с данными по России и с мировыми данными, где на долю лимфомы зоны мантии приходится 6-7 % от общего числа всех неходжкинских лимфом [1]. Увеличения заболеваемости в зависимости от пола не выявлено, т. е. количество женщин и мужчин в исследуемой группе было одинаково, что, в свою очередь, отличается от данных мировой статистики, где описывают, что болеют преимущественно мужчины и отношение М:Ж — (2-4):1. Медиана возраста пациентов с ЛКМЗ в исследуемой группе составила 64 года, что сопоставимо с данными литературы (рис. 1) [1]. Около 40 % пациентов на момент постановки диагноза имели распространенные стадии, что объясняется агрессивным течением ЛКМЗ.
Рисунок 1. Распределение ЛКМЗ по возрасту в Республике Башкортостан
Figure 1. MCL patients by age, Republic of Bashkortostan
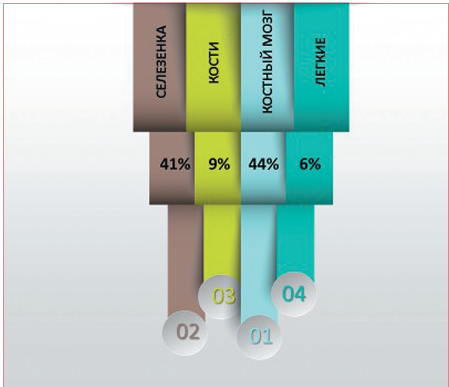
Среди проанализированных случаев жители городской местности составили большую часть (65 % против 35 %). При изучении частоты вовлечения в патологический процесс органов и систем установлено: поражение костного мозга — у 20 (44 %), селезенки — у 18 (41 %), костей — у 4 (9 %), легких — у 3 пациентов (6 %) (рис. 2). Распределение MIPI: высокий у 14 (30 %), средний у 20 (45 %), низкий у 11 (25 %). Ki67 в 4 случаях менее 30 %, в остальных более 30 %.
Рисунок 2. Частота поражения органов и систем при ЛКМЗ в РБ
Figure 2. Incidence of lesions in organs and systems in patients with MCL in RB
Ретроспективный анализ показал, что пациентам с 2015 по 2017 г. в большинстве случаев в первой линии проводилась химиотерапия в режиме R-CHOP с последующей поддержкой ритуксимабом до 2 лет. Средняя беспрогрессивная выживаемость (БПВ) составила 20 месяцев, 8 (17 %) пациентов в статусе длительной ремиссии (с 2015 г.). С 2017 г. в первой линии терапии ЛКЗМ начали применяться режимы R-BAC (схема с высокодозным цитарабином для кандидатов на ТСК) и R-B (для пожилых и коморбидных). С 2018 г. 8 пациентам проведена аутоТСК (в 1-м позднем рецидиве) как этап консолидации лечения. На данный момент обследование на del17p и мутацию TP53 проведено 13 пациентам с ЛКМЗ в федеральных центрах. С ноября 2019 года, впервые в Республике Башкортостан, 2 пациентам с ЛКМЗ начали терапию ингибиторами тирозинкиназы Брутона — ибрутинибом.
Заключение
За последние годы во всем мире значительно поменялись подходы к терапии пациентов с лимфомой зоны мантии. Наряду с гистологическим и иммуногистохи- мическим исследованиями опухолевых тканей в практику все больше внедряется метод молекулярно-генетического исследования, что дает больше возможностей в выборе тактики лечения пациентов.
Информация о конфликте интересов. Конфликт интересов отсутствует.
Информация о спонсорстве. Данная работа не финансировалась.
Список литературы
1. Поддубная И.В., Савченко В.Г. (ред.) Российские клинические рекомендации по диагностике и лечению лимфопролиферативных заболеваний. М.; 2018.
2. Поддубная И.В., Савченко В.Г. (ред.) Алгоритмы диагностики и протоколы лечения заболеваний системы крови. Т. 1. М.; 2018.
3. Лимфомы из клеток мантии у взрослых: Клинические рекомендации. М.; 2018.
4. Bernstein S.H., Epner E., Unger J.M., Leblanc M., Cebula E., Burack R., et al. A phase II multicenter trial of HyperCVAD MTX/Ara-C and rituximab in patients with previously untreated mantle cell lymphoma; SWOG 0213. Ann Oncol. 2013;24(6):1587–93. DOI: 10.1093/annonc/mdt070
5. Hilal T., Wang Z., Almader-Douglas D., Rosenthal A., Reeder C.B., Jain T. Rituximab maintenance therapy for mantle cell lymphoma: A systematic review and meta-analysis. Am J Hematol. 2018;93(10):1220–6. DOI: 10.1002/ajh.25226
6. Lokvenc M., Kalinova M., Forsterova K., Klener P., Trneny M., Fronkova E., et al. Cyclin D1 mRNA as a molecular marker for minimal residual disease monitoring in patients with mantle cell lymphoma. Ann Hematol. 2018;97(3):467–74. DOI: 10.1007/s00277-017-3210-8
7. Dreyling M., Campo E., Hermine O., Jerkeman M., Le Gouill S., Rule S., et al. Newly diagnosed and relapsed mantle cell lymphoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2017;28(Suppl. 4):62–71. DOI: 10.1093/annonc/mdx223
8. Rule S., Dreyling M., Goy A., Hess G., Auer R., Kahl B., et al. Outcomes in 370 patients with mantle cell lymphoma treated with ibrutinib: a pooled analysis from three open-label studies. Br J Haematol. 2017;179(3):430–8. DOI: 10.1111/bjh.14870
9. Воробьев В.И., Гемджян Э.Г., Дубровин Е.И., Нестерова Е.С., Капланов К.Д., Володичева Е.М., и др. Риск-адаптированная интенсивная индукционная терапия, аутологичная трансплантация стволовых кроветворных клеток и поддерживающая терапия ритуксимабом позволяют достигнуть высоких показателей 7-летней выживаемости у больных лимфомой из клеток мантийной зоны. Терапевтический архив. 2019;91(7):41–51. DOI: 10.26442/00403660.2019.07.000322
10. Swerdlow S.H., Campo E., Harris N.L., Jaffe E.S., Pileri S.A., Stein H., et al. (eds) WHO classification of tumours of haematopoietic and lymphoid tissues. Lyon: IARC; 2017.
11. Romaguera J.E., McLaughlin P.W. Mantle cell lymphoma. In: Lichtman M.A., Kipps T.J., Seligsohn U., et al. (eds) Williams hematology. New York: McGraw-Hill; 2014.
12. Dabaja B.S., Zelenetz A.D., Ng A.K., Tsang R.W., Qi S., Allen P.K., et al. Early-stage mantle cell lymphoma: a retrospective analysis from the International Lymphoma Radiation Oncology Group (ILROG). Ann Oncol. 2017;28(9):2185–90. DOI: 10.1093/annonc/mdx334
13. Wang Y., Ma S. Risk factors for etiology and prognosis of mantle cell lymphoma. Expert Rev Hematol. 2014;7(2):23343. DOI: 10.1586/17474086.2014.889561
14. Ruan J., Martin P., Christos P., Cerchietti L., Tam W., Shah B., et al. Five-year follow-up of lenalidomide plus rituximab as initial treatment of mantle cell lymphoma. Blood. 2018;132(19):2016–25. DOI: 10.1182/blood-2018-07-859769
15. Malcikova J., Pavlova S., Kozubik K.S., Pospisilova S. TP53 mutation analysis in clinical practice: lessons from chronic lymphocytic leukemia. Hum Mutat. 2014;35(6):663–71. DOI: 10.1002/humu.22508
16. Воробьев В.И., Лорие Ю.Ю., Мангасарова Я.К., Кравченко С.К., Кременецкая А.М. Возможности терапии рецидивов и резистентного течения лимфомы из клеток мантийной зоны. Гематология и трансфузиология. 2011;(1):34–7.
Об авторах
Канкумашева Эльза Ильдаровна — врач-онколог
450054, Уфа, пр-т Октября, 73/1
Валиахметова Чулпан Хусаеновна — к.м.н., врачонколог, зав. онкологическим отделением противоопухолевой лекарственной терапии
450054, Уфа, пр-т Октября, 73/1
Для цитирования:
Канкумашева Э.И., Валиахметова Ч.Х. Лимфомы клеток мантийной зоны. Новые возможности диагностики и лечения (эпидемиологическое исследование). Креативная хирургия и онкология. 2019;9(4):261-265. https://doi.org/10.24060/2076-3093-2019-9-4-261-265
For citation:
Kankumasheva E.I., Valiakhmetova C.K. Mantle Zone Cell Lymphomas. New Opportunities for Diagnosis and Treatment (Epidemiological Research). Creative surgery and oncology. 2019;9(4):261-265. (In Russ.) https://doi.org/10.24060/2076-3093-2019-9-4-261-265