что такое заместительная терапия при панкреатите
Хронический панкреатит: недостаточность внешнесекреторной функции поджелудочной железы, нарушения полостного пищеварения и заместительная терапия панк
Определение эластазы-1 в кале позволяет лучше диагностировать внешнесекреторную недостаточность поджелудочной железы и оценивать результаты терапии. Формы ферментативных препаратов, где панкреатические ферменты заключены в микрогранулы, позволяют коррегир
The determination of elastaza-1 in the feces makes it possible to properly diagnose the extra-secretory insufficiency of the pancreas and to evaluate the results of therapy. The forms of the fermentative preparations, where the pancreatic ferments are concluded in the micro-granules, make it possible to correct the disturbances of cavity digestion.
Хронический панкреатит (ХП) входит в число важных проблем здравоохранения. За последние тридцать лет отмечен более чем двукратный рост числа хронических и острых панкреатитов. В развитых странах ХП заметно «помолодел» — средний возраст с момента установления диагноза снизился с 50 до 39 лет, на 30% увеличилась доля женщин, доля алкогольного панкреатита возросла с 40% до 75%. Регистрируется также рост заболеваемости карциномой поджелудочной железы (ПЖ), которая развивается на фоне ХП [1, 3, 5].
Хронический панкреатит — прогрессирующий воспалительный процесс ПЖ, который приводит к постепенному замещению паренхимы органа соединительной тканью, изменениям в протоковой системе поджелудочной железы с образованием кист и конкрементов, к развитию недостаточности экзокринной и эндокринной функций железы.
В течении ХП можно выделить два этапа: I этап (чаще до 10 лет) характеризуется чередованием обострений и ремиссий, обострения проявляются болевым синдромом, диспепсия не выражена; на II этапе (чаще после 10 лет) болевой синдром стихает, на первый план выходит диспепсический синдром, связанный с внешнесекреторной недостаточностью ПЖ [1, 2].
Синдром внешнесекреторной недостаточности ПЖ обусловлен уменьшением массы функционирующей экзокринной паренхимы в результате ее атрофии, фиброза либо нарушением оттока панкреатического секрета в двенадцатиперстную кишку в силу блока выводных протоков ПЖ конкрементом, спайками или густым и вязким секретом, что приводит к нарушениям процесса пищеварения.
Участие поджелудочной железы в пищеварении
Под пищеварением понимается переработка с помощью ферментов сложных веществ (белков, жиров, углеводов) в простые для их последующего всасывания.
Основные гидролитические процессы происходят в тонкой кишке, где пищевые вещества расщепляются до мономеров, всасываются и поступают в кровь и лимфу. Процесс переработки пищевых веществ в тонкой кишке проходит в три последовательных взаимосвязанных этапа, объединенных A. M. Уголевым (1967) в понятие «пищеварительно-транспортного конвейера»: полостное пищеварение, мембранное пищеварение, всасывание.
Поджелудочная железа вырабатывает секрет, который содержит ферменты, гидролизующие все виды пищевых веществ: белки, углеводы, жиры. Перечень основных ферментов ПЖ и их участие в пищеварении представлены в табл. 1.
Ферменты, гидролизирующие углеводы и жиры (альфа-амилаза, липаза), секретируются в активном состоянии, протеолитические ферменты (трипсин, химотрипсин, эластаза, карбоксипептидаза) — в виде проферментов, которые активируются в просвете тонкой кишки. В их активации важное место занимает кишечный фермент — энтерокиназа, который переводит трипсиноген в активный трипсин. Трипсин в свою очередь активирует остальные протеолитические ферменты.
В процессе полостного пищеварения углеводы (крахмал, гликоген) расщепляются панкреатической амилазой до дисахаридов и небольшого количества глюкозы. Под действием протеолитических ферментов образуются низкомолекулярные пептиды и небольшое количество глюкозы. Жиры в присутствии желчи гидролизуются панкреатической липазой до ди- и моноглицеридов жирных кислот и глицерина.
Действие панкреатических ферментов уменьшается по мере их продвижения от двенадцатиперстной кишки (ДПК) до терминальных отделов подвздошной кишки. Уровень снижения активности отдельных ферментов различен. Так, липаза наиболее быстро теряет свою активность и в подвздошной кишке в норме определяется лишь в незначительных количествах. Протеазы, особенно амилаза, оказываются более устойчивыми и сохраняют соответственно 30% и 45% своей активности в терминальных отделах тонкой кишки. В основе снижения активности липазы лежит ее протеолиз под воздействием протеаз и, прежде всего, химотрипсина. Неравномерное уменьшение активности ферментов от проксимального к дистальному отделу тонкой кишки наблюдается как у здоровых людей, так, особенно, у лиц с хронической экзокринной панкреатической недостаточностью. Этим объясняется тот факт, что нарушение переваривания жира развивается намного раньше, чем крахмала или белка [1, 3, 4].
Регуляция секреции поджелудочной железы
Секрет поджелудочной железы состоит из двух компонентов — дуктального (неорганического) и ацинарного (органического).
Дуктальный эпителий выделяет секрет, богатый электролитами, особенно бикарбонатами, в составе водного раствора. Функция этого компонента секрета ПЖ — нейтрализация поступающего в ДПК кислого желудочного содержимого и перевод желудочного пищеварения в кишечное. Основным стимулятором секреции неорганического компонента является секретин, вырабатывающийся S-клетками слизистой оболочки ДПК в ответ на поступающее из желудка кислое содержимое.
Гландулоциты панкреатических ацинусов синтезируют и секретируют гидролитические ферменты под влиянием панкреозимина (холецистокинина), который синтезируется J-клетками слизистой оболочки ДПК. Стимулятором освобождения панкреозимина служит главным образом пища.
Клиника и диагностика нарушений полостного пищеварения и внешнесекреторной функции ПЖ
Одним из ранних симптомов нарушения переваривания пищевых веществ является стеаторея. Кал становится жирным, блестящим, липким. Больные с выраженной недостаточностью внешнесекреторной функции ПЖ жалуются на вздутие живота, избыточное газообразование, ощущение переливания и урчание в животе. В более выраженных случаях появляется полифекалия, стеаторея, диарея и похудание.
Наиболее адекватным методом исследования внешнесекреторной недостаточности ПЖ является определение панкреатической эластазы-1 в кале. Основным преимуществом определения фекальной эластазы-1 иммуноферментным методом является то, что эластаза-1 абсолютно специфична для ПЖ; эластаза-1 почти не разрушается при прохождении через кишечный тракт; колебания активности эластазы в кале незначительны, что обеспечивает высокую воспроизводимость результатов; данным методом определяется лишь человеческая эластаза, поэтому результаты теста не зависят от проводимой заместительной ферментной терапии.
Нормальную внешнесекреторную функцию ПЖ определяли при значении эластазы-1 от 200 до 500 мкг в 1 г кала и выше, средней и легкой степени — 100–200 мкг/г, тяжелой степени — менее 100 мкг/г [4, 6].
Коррекция нарушенного полостного пищеварения ферментами ПЖ
Для компенсации нарушения полостного пищеварения широко применяются ферментные препараты ПЖ.
В настоящее время установлено, что препараты, предназначенные для заместительной терапии, должны обладать следующими свойствами:
Этим требованиям отвечают микрогранулированные формы ферментных препаратов. Микротаблетки панкреатина диаметром от 1 до 2 мм, покрытые кислотостойкой, энтеросолюбильной оболочкой, помещают в желатиновую капсулу. Растворяясь в желудке в течение несколько минут, капсула освобождает микрогранулы, которые сохраняют резистентность к действию кислого желудочного сока в течение 2 ч. Микрогранулы равномерно смешиваются с желудочным химусом и эвакуируются в тонкую кишку, где быстро растворяются в щелочной среде, высвобождая ферменты. Таким образом, обеспечивается быстрое наступление действия препарата в тонкой кишке [5, 7].
Липаза наиболее быстро теряет свою активность, что проявляется стеатореей. Поэтому при коррекции экзокринной панкреатической недостаточности, прежде всего, ориентируются на содержание липазы в препарате.
Размер микрогранул является наиболее важным фактором, определяющим скорость и своевременность их эвакуации из желудка. Диаметр микрогранул должен составлять 1,4 ± 3,0 мм, чтобы обеспечить их одновременное прохождение с пищей через пилорический сфинктер. Мини-таблетки (2 мм в диаметре, несферическая форма) не обеспечивают идеальный пассаж.
Характеристика основных микрогранулированных полиферментных препаратов представлена в табл. 2 и 3.
Для большинства больных с умеренным нарушением внешнесекреторной функции ПЖ приема 1–2 капсул (10 000–20 000 МЕ липазы) во время еды вполне достаточно для ликвидации стеатореи. При тяжелых формах недостаточности с выраженной стеатореей число принимаемых капсул увеличивают до 4–5.
Целесообразно при назначении ферментных препаратов ориентироваться на уровень эластазы-1 в кале (табл. 4).
Нами проведена оценка эффективности микрогранулированного ферментного препарата Микразима.
Обследовано 50 больных ХП с внешнесекреторной недостаточностью ПЖ. Группа из 30 больных получала Микразим 10 000 ЕД по 2 капсулы 3 раза в сутки в течение 14 дней и группа контроля (20 пациентов) — Панкреатин по 4 таблетки 3 раза в сутки в течение 14 дней.
Общая эффективность оценивалась как: выраженная, хорошая, удовлетворительная, эффект отсутствует (рис. 1). Учитывалась динамика болевого синдрома (рис. 2), частота дефекаций (рис. 3), консистенция стула (рис. 4).
Проведенное исследование показало, что Микразим более выраженно, чем таблетированный Панкреатин, влияет на улучшение пищеварения, уменьшение боли в животе и нормализацию стула.
Эффективность ферментных препаратов повышается при добавлении к стандартному лечению панкреатином антисекреторных средств (Н2-блокаторы, ингибиторы протонной помпы), поскольку оптимальное действие панкреатических ферментов обеспечивается при рН в просвете тонкой кишки более 5,0.
Причинами неэффективности заместительной терапии может быть следующее:
Заключение
За последние десятилетия отмечается заметный рост числа заболеваний поджелудочной железы и соответственно больных с внешнесекреторной панкреатической недостаточностью, требующей заместительной терапии. Широкое использование нового теста — определение эластазы-1 в кале позволило лучше диагностировать внешнесекреторную недостаточность ПЖ и оценивать результаты заместительной терапии. Появилось большое число ферментативных препаратов с разной степенью энзиматической активности. Современные лекарственные формы, где панкреатические ферменты заключены в микрогранулы (Панцитрат, Креон, Микразим), позволяют корригировать даже тяжелые нарушения полостного пищеварения.
Литература
А. В. Калинин, доктор медицинских наук, профессор
ГУ МОНИКИ им. М. Ф. Владимирского Минздравсоцразвития России, Москва
Влияние заместительной ферментной терапии на течение хронического панкреатита и рака поджелудочной железы
В статье представлены современные данные об эффективности заместительной ферментной терапии (ЗФТ) у больных хроническим панкреатитом (ХП) и раком поджелудочной железы (РПЖ). Дефицит поступающих в просвет двенадцатиперстной кишки пищеварительных ферментов при экзокринной недостаточности поджелудочной железы (ЭНПЖ) приводит к мальабсорбции и мальдигестии, что ухудшает нутритивный статус пациентов. Патогенетическим лечением данного состояния является ЗФТ.
На фоне ЗФТ у пациентов с ЭНПЖ, вызванной ХП и РПЖ, улучшаются всасывание белков и жиров и сывороточные показатели нутритивного статуса, качество жизни, увеличивается масса тела, снижается риск развития остеопороза и остеопоротических переломов, саркопении, сердечно-сосудистых и инфекционных осложнений.
В то же время ЗФТ способствует увеличению выживаемости и снижению выраженности гастроинтестинальной симптоматики, особенно в раннем послеоперационном периоде, у пациентов после операций на поджелудочной железе. ЗФТ представляет собой базовую терапию ЭНПЖ, применение которой до и после оперативного лечения по поводу ХП и РПЖ эффективно и безопасно, что доказано результатами многочисленных исследований и рекомендовано международными консенсусными соглашениями.
В статье представлены современные данные об эффективности заместительной ферментной терапии (ЗФТ) у больных хроническим панкреатитом (ХП) и раком поджелудочной железы (РПЖ). Дефицит поступающих в просвет двенадцатиперстной кишки пищеварительных ферментов при экзокринной недостаточности поджелудочной железы (ЭНПЖ) приводит к мальабсорбции и мальдигестии, что ухудшает нутритивный статус пациентов. Патогенетическим лечением данного состояния является ЗФТ.
На фоне ЗФТ у пациентов с ЭНПЖ, вызванной ХП и РПЖ, улучшаются всасывание белков и жиров и сывороточные показатели нутритивного статуса, качество жизни, увеличивается масса тела, снижается риск развития остеопороза и остеопоротических переломов, саркопении, сердечно-сосудистых и инфекционных осложнений.
В то же время ЗФТ способствует увеличению выживаемости и снижению выраженности гастроинтестинальной симптоматики, особенно в раннем послеоперационном периоде, у пациентов после операций на поджелудочной железе. ЗФТ представляет собой базовую терапию ЭНПЖ, применение которой до и после оперативного лечения по поводу ХП и РПЖ эффективно и безопасно, что доказано результатами многочисленных исследований и рекомендовано международными консенсусными соглашениями.
Поджелудочная железа (ПЖ) – ключевой орган желудочно-кишечного тракта, делающий возможным за счет выработки ферментов и гормонов переваривание пищи и усвоение макро- и микроэлементов организмом человека. Как правило, при прогрессировании заболеваний [1, 2] ПЖ развивается недостаточность ее экзо- и эндокринной функций [3]. Экзокринная недостаточность поджелудочной железы (ЭНПЖ) определяется как снижение активности панкреатических ферментов, особенно липазы, в просвете двенадцатиперстной кишки (ДПК) ниже уровня, необходимого для нормального процесса пищеварения [4].
Выделяют первичную и вторичную ЭНПЖ. Первичная характеризуется снижением синтеза ферментов ПЖ, что иногда наблюдается при врожденных заболеваниях, например муковисцидозе, синдроме Швахмана – Даймонда, Йохансона – Близарда, или утрате ацинарной ткани в течение жизни, например после острого панкреатита [5], при хроническом панкреатите (ХП) [6] и раке поджелудочной железы (РПЖ) [7], а также после резекций ПЖ. Вторичная экзокринная недостаточность является следствием анатомических изменений после оперативных вмешательств на других органах брюшной полости, например после резекций желудка, участков кишки и бариатрических операций [8], либо нарушения активации/дезактивации панкреатических ферментов [9] на фоне сопутствующей патологии.
Согласно панъевропейским [10] и отечественным [11] рекомендациям по диагностике и лечению хронического панкреатита, для выявления ЭНПЖ проводится оценка клинических проявлений мальдигестии, параметров нутритивного статуса и неинвазивное исследование, позволяющее определить функцию ПЖ. Золотым стандартом исследования ЭНПЖ является установление коэффициента абсорбции жира. Данный тест требует сбора кала за 72 часа, в течение которых пациент соблюдает стандартную диету с содержанием 100 г жиров. Однако данный метод трудоемок как для пациентов, так и для медицинского персонала и в клинической практике используется редко. Оптимальным методом определения функции ПЖ в России и за рубежом считается исследование уровня фекальной эластазы 1 с помощью иммуноферментного анализа со специфическими антителами [11, 12]. Существует альтернативный вариант в виде дыхательного теста с 13 С-мечеными триглицеридами, однако в России он пока не используется.
Как известно, клинически ЭНПЖ манифестирует только при снижении до 10% и менее от необходимого количества ферментов, секретируемых в просвет ДПК, для нормального переваривания пищи [13]. Такое снижение ферментной активности ПЖ приводит к синдрому недостаточности пищеварения, или мальдигестии [14], который может сопровождаться абдоминальным болевым синдромом, стеатореей и снижением массы тела [15]. В свою очередь мальдигестия приводит к мальнутриции [16, 17] и снижению показателей нутритивного статуса: гемоглобина, абсолютного числа лимфоцитов [18], холестерина, альбумина, преальбумина [7], ретинол-связывающего белка, трансферрина, жирорастворимых витаминов, кальция, цинка и магния [19]. Результаты многочисленных исследований показали, что данные состояния и дефицит макро- и микронутриентов [20] не только ухудшают качество жизни, но и повышают риск развития остеопороза и остеопоротических переломов [21], саркопении [22], сердечно-сосудистых [23] и инфекционных [24] осложнений. Доказано также, что при ХП ЭНПЖ – независимый фактор, ассоциированный с повышенным риском смерти [25].
Панкреатическая мальдигестия и мальабсорбция наряду с первичным дефицитом нутриентов и гиперметаболизмом являются главными причинами нарушений нутритивного статуса [15, 26]. Патогенетическим лечением данного состояния является заместительная ферментная терапия (ЗФТ). Эта позиция нашла отражение в ряде зарубежных [10, 27–29] и российских [11, 12, 17, 19] консенсусов.
Первое место среди причин развития ЭНПЖ занимает ХП [12]. Систематический обзор и метаанализ 14 рандомизированных клинических исследований (РКИ) эффективности ЗФТ [30] показал, что у пациентов с ХП на ЗФТ улучшалось всасывание белков и жиров, что выражалось в повышении коэффициента абсорбции жира и азота по сравнению с плацебо и исходными данными, а также в стойком снижении фекальной экскреции жира и азота, объема каловых масс и выраженности гастроинтестинальных симптомов. Несмотря на то что исследования, вошедшие в анализ, продолжались не более двух месяцев, два открытых дополнительных исследования – до года [31, 32] продемонстрировали повышение уровней сывороточных показателей нутритивного статуса, качества жизни, увеличение массы тела и снижение выраженности гастроинтестинальных симптомов в более отдаленном периоде наблюдения. В одном из них ЗФТ показала удовлетворительный профиль безопасности [31]: всего у четырех (7,8%) пациентов отмечались нежелательные явления, оцененные исследователями как возможно или вероятно связанные с получаемым лечением.
С ростом хирургической активности на ПЖ возросло внимание к лечению экзокринной панкреатической недостаточности после оперативных вмешательств [33]. Результаты немецкого исследования 2013 г. [34] с участием 147 пациентов после операций по поводу ХП продемонстрировали, что пациенты, получавшие ЗФТ после оперативного лечения, имели более высокую выживаемость (медиана наблюдения составила 5,3 года), а отсутствие ЗФТ и инсулинопотребный сахарный диабет IIIc на момент выписки стали независимыми и статистически значимыми факторами риска смерти в отдаленном периоде наблюдения. Авторы предположили, что положительный эффект на течение ХП ЗФТ может оказать и в случае субклинической ЭНПЖ. Согласно результатам двойного слепого исследования, опубликованного в 2010 г. [35], ЗФТ эффективна у пациентов после хирургического вмешательства по поводу ХП. На фоне ЗФТ отмечались увеличение коэффициентов абсорбции жира и азота, уменьшение выраженности стеатореи и вздутия, улучшение консистенции стула.
В упомянутом открытом дополнительном исследовании [31] у больных с ЭНПЖ вследствие ХП или хирургического лечения ПЖ после шестимесячной ЗФТ достоверно снизилась частота стула (-1,0 ± 1,3 дефекаций в сутки; p 2 ; р
Заместительная ферментная терапия при панкреатической недостаточности
Лечение экзокринной панкреатической недостаточности до сих пор остается сложной задачей, что объясняется многофакторностью ее патогенеза и сложностью выбора оптимальной схемы терапии или наиболее эффективного препарата. В статье освещены патофизиологические и фармакологические аспекты заместительной ферментной терапии, показывающие необходимость индивидуального подхода к каждому пациенту с учетом степени экзокринной недостаточности, уровня желудочного кислотообразования, бактериальной контаминации тонкой кишки и др. Разработанные в последние годы галенические формы ферментных препаратов, существенно улучшающие смешивание и сегрегацию протеаз и липазы непосредственно к их субстратам, значительно повышают качество заместительной терапии при панкреатической недостаточности. Применение таблетированных полиферментных препаратов, покрытых оболочкой, защищающей препарат от соляной кислоты в желудке практически бесполезно; только препараты последних поколений, содержащие минимикросферы панкреатина, покрытые энтеросолюбильной оболочкой, достоверно и дозозависимо уменьшают стеаторею. Знание практикующим врачом принципов заместительной ферментной терапии определяет адекватность назначенного лечения и прогноз течения болезни.
Ключевые слова: панкреатическая недостаточность, хронический панкреатит, лечение, панкреатин
Синдром внешнесекреторной недостаточности поджелудочной железы (ПЖ) обусловлен уменьшением массы ее функционирующей экзокринной паренхимы в результате атрофии, фиброза, неоплазии, либо нарушением оттока панкреатического секрета в двенадцатиперстную кишку (ДПК) в силу блока выводных протоков ПЖ конкрементом, опухолью, густым и вязким секретом. Кроме того, выделяют так называемую вторичную панкреатическую недостаточность, когда панкреатические ферменты не активируются, либо инактивируются в кишечнике (Таблица 1). Важное значение имеет развитие атрофических изменений слизистой проксимального отдела тонкой кишки, когда уменьшается число I-клеток и S-клеток, секретирующих холецистокинин и секретин, соответственно. Дефицит эндогенного секретина вызывает нарушения целого ряда функций органов пищеварения: повышается давление в ДПК и в панкреатических протоках, отмечается спазм сфинктера Одди, снижается объем панкреатического сока и бикарбонатов. В результате уменьшается секреция жидкой части панкреатического сока, что приводит к его сгущению и повышению в нем концентрации белка, а следовательно, к увеличению вязкости и снижению скорости оттока секрета.
Клиническая манифестация экзокринной недостаточности ПЖ зависит от ряда вторичных факторов, включающих особенности гастринтестинальной моторики, желудочной, билиарной и тонкокишечной секреции, абсорбции, секреции гормонов и последствий абдоминальной хирургии (состояние после резекции желудка и гастрэктомии, холецистэктомии, билиодигестивного шунтирования и др.). Коррекция вышеуказанных нарушений может не только способствовать уменьшению проявлений внешнесекреторной панкреатической недостаточности, но и полному ее купированию. Поэтому многие авторы и предпочитают разделение экзокринной недостаточности ПЖ на первичную и вторичную. Следует отметить, что в ряде случаев вторичная панкреатическая недостаточность может развиться как на фоне сохранной экзокринной функции ПЖ, так и не фоне первичной внешнесекреторной недостаточности, значительно усугубляя ее.
Таблица 1
Причины панкреатической недостаточности
| Первичная панкреатическая недостаточность | Вторичная панкреатическая недостаточность |
| – Хронический панкреатит – Муковисцидоз – Липоматоз ПЖ взрослых (при ожирении) – Резекция ПЖ, панкреатэктомия – Изолированная недостаточность липазы – Синдром Швахмана – Синдром Йохансона-Близзарда – Агенезия, гипоплазия ПЖ – Рак ПЖ — инфильтративный рост с субтотальным замещением функционирующей паренхимы без нарушения оттока — локальное поражение ПЖ с развитием блока (прорастание, сдавление) главного панкреатического протока | – Заболевания слизистой оболочки тонкой кишки (уменьшение секретиновой и холецистокининовой стимуляции на ПЖ) – Гастринома (инактивация ферментов ПЖ) – Анастомоз по Бильрот II (плохое перемешивание пищевого комка с ферментами ПЖ) – Врожденная недостаточность энтерокиназы – Недостаточность поступления белков с пищей – Желчнокаменная болезнь, постхолецистэктомический синдром, циррозы печени (дефицит желчных кислот, асинхронизм поступления в ДПК желчи и панкреатического сока) |
Патофизиологические аспекты заместительной ферментной терапии. ПЖ обладает огромной резервной возможностью секреции ферментов, поскольку в физиологических условиях она продуцирует около двух литров панкреатического сока в сутки, содержащего в 10 раз больше ферментов и зимогенов, чем требуется для нормального переваривания пищи (физиологическая гиперсекреция) [13,16]. Значит, для развития синдрома мальабсорбции секреторная возможность должна снизиться существенно, примерно до уровня 5-10% от величины физиологической гиперсекреции, или, другими словами, от «нормы», что и было показано в ряде экспериментальных и клинических исследований [13,19,22,26].
На первый взгляд, лечение синдрома мальабсорбции, возникающего у больных с внешнесекреторной недостаточностью ПЖ, кажется достаточно простым. Действительно, банальный пероральный прием экзогенных панкреатических ферментов с заместительной целью должен быть весьма эффективным. Однако, полная коррекция клинических проявлений панкреатической недостаточности достигается не так часто, что связано с множеством различных факторов, анализ которых мы представим ниже.
Несмотря на широкий спектр различных нозологий, приводящих к экзокринной недостаточности ПЖ, наиболее частой причиной развития данного синдрома является хронический панкреатит (ХП). Патогенез внешнесекреторной недостаточности наиболее изучен именно при ХП, что обусловлено не только частой встречаемостью ХП, но и относительно благоприятным прогнозом течения по сравнению с раком ПЖ, наследственными заболеваниями и аномалиями развития, состояниями после оперативных вмешательств на ПЖ. Именно поэтому в данной статье мы будем говорить преимущественно о внешнесекреторной недостаточности ПЖ у больных ХП.
По мере увеличения длительности ХП секреция ферментов все более уменьшается, причем дефицит липазы выражен в большей степени и развивается раньше, чем дефицит трипсина. Это может быть объяснено следующим:
1. Считается, что у больных ХП в первую очередь снижается панкреатическая секреция именно липазы, а уже в дальнейшем происходит снижение секреции амилазы и протеаз [14,16], однако причины этих нарушений до сих пор не совсем понятны.
2. Липаза по сравнению с амилазой и протеазами в большей степени подвергается инактивации протеолитическим гидролизом [28,30].
3. Недостаточность панкреатических протеаз может быть компенсирована кишечными протеазами и пептидазами, панкреатической амилазы – амилазами слюны и кишечника. Компенсаторные возможности слюнной и желудочной липазы относительно других панкреатических ферментов значительно ниже, и не могут предотвратить появление стеатореи [29,38,45].
4. При экзокринной недостаточности ПЖ наряду со снижением синтеза панкреатических ферментов наблюдается снижение секреции бикарбонатов, что приводит к прогрессирующему падению рН в ДПК. При рН ниже 5,0 липаза разрушается быстрее, чем другие ферменты. Кроме того, при снижении интрадуоденального рН происходит снижение преципитации желчных кислот, нарушается формирование мицелл, вследствие чего дополнительно нарушается всасывание жиров [44,45].
Как было обсуждено ранее, экзогенное поступление липазы в ДПК превышающее 5-10% от нормальной концентрации фермента должно сопровождаться редукцией стеатореи [37]. Однако, в эксперименте у пациентов, коррекция экзокринной недостаточности ПЖ достигалась вне зависимости от принимаемого препарата и его дозы, определяясь только концентрацией липазы в ДПК [23,43]. Можно предположить, что это было обусловлено гиперсекрецией соляной кислоты и инактивацией ферментов в просвете двенадцатиперстной и тощей кишки [31]. Так, после приема ферментов внутрь более активный трипсин противостоит неблагоприятному действию низких значений рН в желудке и ДПК. Поэтому любой препарат панкреатина, принятый в достаточном количестве (более 10% от максимального количества, секретируемого за 4 ч пищеварительного периода), устранит азоторею, но не стеаторею. При таких условиях стеаторея всегда уменьшится, но не исчезнет, если только у больного нет сопутствующей ахлоргидрии [3]. Однако при добавлении к заместительной ферментной терапии антисекреторных средств (с целью повышения рН в двенадцатиперстной кишке) стеаторея исчезает у 40% больных [36].
Таким образом, развитие стеатореи при ХП в большей степени обусловлено нарушением панкреатического липолиза в результате снижения синтеза панкреатической липазы, нарушением секреции бикарбонатов с ацидификацией ДПК и преципитацией желчных кислот.
Краткая характеристика полиферментных препаратов.
Полиферментные препараты – это комбинированные многокомпонентные лекарственные средства, преимущественно животного происхождения, основным действующим субстратом которых является панкреатин в чистом виде или в комбинации с дополнительными компонентами (желчными кислотами, гемицеллюлазой, симетиконом, адсорбентами и др.) [5].
Применение первой группы ферментов у больных панкреатитами показано только при сочетании тяжелой внешнесекреторной недостаточности ПЖ и атрофического гастрита. Препараты 2-4 групп содержат животный панкреатин, но в связи с различным составом и, соответственно, фармакологическим эффектом они не являются взаимозаменяемыми и имеют четкие показания к применению.
Комбинированные препараты наряду с панкреати.ном содержат желчные кислоты, гемицеллюлазу, симетикон, растительные желчегонные (куркума) и др. Введение в препарат желчных кислот существенно из.меняет его действие на функцию пищеварительных желез и моторику желудочно-кишечного тракта. Увеличивается панкреатичес.кая секреция и холерез, стимулируется моторика кишеч.ника и желчного пузыря. В усло.виях микробной контаминации кишечника происходит их деконъюгация, что в некоторых случаях способствует активации цАМФ энтероцитов с последующим развитием осмотической и секреторной диареи. Ферментные препараты, содержащие желчные кислоты противопоказаны больным с отечными и болевыми формами ХП, поскольку они увеличивают секрецию ПЖ, стимулируют перистальтику кишечника и моторику желчного пузыря, увеличивают внутрикишечное осмотическое давление и, следовательно, болевой абдоминальный синдром.
Показания для заместительной ферментной терапии при ХП с внешнесекреторной недостаточностью [7]:
1. стеаторея при потере с калом более 15 г жира в сутки;
2. прогрессирующая трофологическая недостаточность;
3. стойкий диарейный синдром и диспептические жалобы.
Фармакологические аспекты заместительной полиферментной терапии. Основная цель заместительной терапии панкреатическими ферментами заключается в обеспечении достаточной активности липазы в ДПК. Известно, что воздействие соляной кислоты на панкреатические ферменты приводит к разрушению до 90% их количества, поэтому путем преодоления кислотного желудочного барьера явилось создание галенических форм полиферментных препаратов в кислотоустойчивой оболочке. Использование препарата, имеющего такую оболочку, увеличивает всасывание жиров в среднем на 20% по сравнению с сопоставимой дозой панкреатина без оболочки [27].
Если постпрандиальный рН в желудке зависит как от индивидуальных особенностей секреции, так и от количества пищи и времени ее нахождения в желудке, то интрадуоденальный рН зависит от остаточной секреции бикарбонатов ПЖ, секреции бикарбонатов тонкой кишкой, от разведения объемом, а также от количества соляной и желчных кислот. Поэтому при использовании панкреатических ферментов с кислотоустойчивой оболочкой интрагастральный рН не должен превышать 5, так как в этом случае ферменты будут освобождаться от энтеросолюбильной оболочки уже в желудке. Если это произойдет, то часть ферментов у пациентов с нарушенной моторной функцией будет необратимо разрушена при реацидификации. С другой стороны внутрижелудочное высвобождение панкреатических ферментов может сдвигать баланс защиты слизистой оболочки желудка в сторону усиления факторов агрессии, провоцируя эрозивно-язвенные поражения. Этот механизм часто реализуется у пациентов с дуоденогастральным рефлюксом, являющимся самостоятельным агрессивным фактором за счет негативного влияния желчных кислот, лизолицетина и фосфолипаз на слизистую желудка. В то же время, интрадуоденальный рН должен быть не ниже 5,5 для адекватного высвобождения ферментов в ДПК.
Важнейшими факторами, затрудняющими проведение эффективной заместительной ферментной терапии является асинхронный гастродуоденальный транспорт ферментных препаратов и пищевого комка, что наблюдается при нарушениях пассажа (сахарный диабет, стеноз привратника, состояние после ваготомии, автономные нейропатии и т.д.), а также при применении ферментных препаратов сравнительно большого размера.
Большинство ферментных препаратов выпускается в виде драже или таблеток в кишечно-растворимых оболочках, что защищает ферменты от высвобождения в желудке и разрушения соляной кислотой желудочного сока. Размер большинства таблеток или драже составляет 5 мм и более. Тем не менее, известно, что из желудка одновременно с пищей могут эвакуироваться твердые частицы, диаметр которых составляет не более 2 мм при оптимальном размере 1,4 мм [33]. Более крупные частицы, в частности ферментные препараты в таблетках или драже, эвакуируются в межпищеварительный период, когда пищевой химус отсутствует в ДПК. В результате препараты не смешиваются с пищей и недостаточно активно участвуют в процессах пищеварения [8]. Если таблетка или драже длительное время находятся в желудке, энтеросолюбильная оболочка разрушается, а находящиеся внутри ферменты инактивируются [1].
Одним из вариантов возможного решения этой задачи явилось появление на фармакологическом рынке препаратов, содержащих кислотоустойчивые ферменты растительного и грибкового происхождения, не нуждающихся в кислотозащитной оболочке. Однако, эффективность применения кислотоустойчивый липазы грибкового происхождения значительно уступает препаратам панкреатина [40]. По данным A.Suzuki et al. в экспериментах на собаках бактериальная липаза оказалась в 75 раз менее эффективной, чем свиная – стеаторею удавалось устранить назначением 240 мг бактериального фермента или 18 мг фермента свиного происхождения [41].
Поскольку максимальное физиологическое постпрандиальное поступление панкреатической липазы составляет приблизительно 140000 ЕД/час в течение 4 часов после еды [13], а мальабсорбция не развивается, если в двенадцатиперстную кишку попадает более 5% от нормальной максимальной продукции фермента, то для коррекции стеатореи необходимо обеспечить поступление около 28000 ЕД липазы в течение 4 часов постпрандиального периода. В настоящее время имеется большое количество различных полиферментных препаратов, содержание липазы в которых достаточно сильно варьирует (в пределах 0-25000). Соответственно для коррекции стеатореи необходимо использовать препараты только с высоким содержанием липазы [15]. Однако, на практике наиболее часто применяемыми оказываются коммерчески доступные препараты с содержанием липазы в одной таблетке (драже) в пределах 3500-6000 ЕД. Соответственно, минимально эффективной разовой дозой для коррекции стеатореи будет прием по крайней мере 5-8 драже или таблеток. Однако, данные относительные расчеты, несмотря на свою показательность, не учитывают того факта, что большая часть применяемой липазы может быть инактивирована либо не активирована у больных с преимущественно вторичным механизмом панкреатической недостаточности. В этом случае следует говорить не о 5-8 таблетках, а скорее – о 20-30 на прием пищи, что невозможно по психологическим причинам. Таким образом становится понятно, почему традиционно используемое меньшее количество экзогенно принимаемых ферментов уменьшает стеаторею, но не ликвидирует ее.
Поэтому, неоспоримым является мнение, что применение энтеросолюбильных таблетированных полиферментных препаратов панкреатина, особенно в традиционных дозах, и ферментных препаратов растительного происхождения для лечения экзокринной недостаточности ПЖ практически бесполезно [18].
В дополнение к кислотной инактивации панкреатических ферментов была исследована роль протеолитических ферментов в инактивации липазы [15,37], однако клиническое значение этого механизма до сих пор не доказано. В экспериментах in vitro было показано, что быстрая инактивация липазы различными панкреатическими препаратами обратно коррелировала с активацией трипсина, а ингибирование трипсина его ингибитором значительно увеличивало время функционирования липазы [34]. Предположительно протеолитическая инактивация липазы может быть предотвращена при увеличении соотношения липаза/трипсин относительно физиологического уровня и улучшением смешивания панкреатина с белком, содержащимся в пище [34], связывающим трипсин, как в качестве субстрата, так и за счет природных ингибиторов трипсина, в обилии содержащихся в пище, особенно растительной [25]. У пациентов с алкогольным ХП, соотношение активности протеаз к липазе в дуоденальном соке высокое ввиду значительного превалирования трипсина и химотрипсина в панкреатическом секрете. Протеолитическая инактивация липазы у этих пациентов в патогенезе экзокринной недостаточности более важна, чем при нормальной функции ПЖ. Следует отметить, что у больных алкогольным ХП часто используют панкреатические ферменты с высоким содержанием протеаз для купирования боли, однако, при этом усиливается инактивация эндогенной липазы [24,34,42]. Этот факт достаточно часто отмечен в различных публикациях, где анализировались причины низкой эффективности коррекции стеатореи у больных ХП [18,34,40,42].
Для обеспечения быстрого и гомогенного смешивания ферментов с пищевым химусом, предотвращения внутрижелудочной инактивации и адекватного пассажа из желудка в ДПК были созданы ферментные препараты панкреатина нового поколения в виде микротаблеток (панцитрат) и микросфер (креон, ликреаза), диаметр которых не превышает 2 мм. Препараты покрыты энтеросолюбильными оболочками и заключены в желатиновые капсулы. При попадании в желудок желатиновые капсулы быстро растворяются, микросферы или микротаблетки смешиваются с пищей и постепенно поступают в ДПК. При рН дуоденального содержимого выше 5,5 оболочки растворяются, и ферменты начинают действовать на большой поверхности (Рис. 1). При этом, практически воспроизводятся физиологические процессы пищеварения, когда панкреатический сок выделяется порциями в ответ на периодическое поступление пищи из желудка. Препарат Креон также характеризуется оптимальным соотношением активности липазы и колипазы, высоким содержанием карбоксилэстеролипазы и фосфолипазы А2 для наиболее эффективного расщепления жиров.
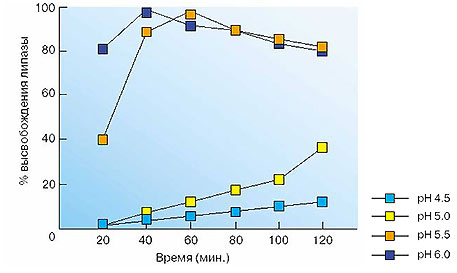
Рис. 1. Характеристики растворимости микросфер Креона, выраженные как процент высвобождения липазы при рН от 4,5 до 6,0.
(По S.N.Atkinson с изм., [11])
Таким образом, именно микрокапсулированные и микротаблетированные препараты можно отнести к самым современным полиферментным препаратам для заместительной ферментной терапии, в том числе отвечающим современным требованиям к данным препаратам, сформулированным на основании экпериментальных, теоретических, биохимических и клинических работ, описанных выше [1, 5, 7]:
Поэтому, препаратами первого выбора при ХП с экзокринной недостаточностью можно считать креон и панцитрат. Широко используемый мезим-форте в дозах 3-6 таблеток в сутки можно использовать только для коррекции дисфункции ПЖ, возникающей при погрешностях в питании. В то время, как креон с активностью 25000 ЕД липазы способен полностью заменить экзокринную функцию ПЖ [10]. Панцитрат – препарат с высоким содержанием трипсина в одной капсуле (от 500 до 1250 ЕД). При этом, как было показано выше, протеазы, прежде всего трипсин, являются главными ингибиторами липазы. Известно, что в препаратах с высоким содержанием протеаз липаза интенсивно разрушается содержащимися в этом же препарате протеазами [7]. Этот эффект несколько ограничивает применение панцитрата для лечения экзокринной недостаточности.
Соответственно, лекарственным средством, полностью удовлетворяющим вышеуказанным требованиям и используемым в последнее время, является высокоактивный полиферментный препарат в виде минимикросфер (Креон 10000 и Креон 25000), покрытых энтеросолюбильной оболочкой. Этот препарат выгодно отличается от своего предшественника креона 8000 и аналогичных препаратов других производителей тем, что средний размер минимикросфер уменьшен до 1 мм. Это обеспечивает иную, чем при применении микросфер и микротаблеток фармакокинетику, способствует оптимальному перемешиванию с пищей и, соответственно, повышает эффективность препарата в среднем на 25% [1]. Решение уменьшить размер микросфер опиралось на результаты исследований J.H.Meyer et al., показавших в эксперименте на здоровых добровольцах, что из желудка быстрее эвакуировались микросферы диаметром 1 мм независимо от количества принимаемой с ферментом пищи [33].
Побочные эффекты полиферментной терапии возникают нечасто и обычно не носят тяжелого характера. Наиболее показательны в этом отношении исследования H.Friess et al. применявших у здоровых добровольцев в течение 4 недель панкреатин в суточной дозе 360000 (!) ЕД липолитической активности. По данным проведенных исследований авторами не только не найдено адаптационных изменений экзо- и эндокринной функции ПЖ, изменений ее размеров, но и не было отмечено существенных побочных эффектов [20], что лишний раз характеризует препараты панкреатина как достаточно безопасные.
К редким возможным побочным эффектам, возникающим при приеме полиферментных препаратов, следует отнести [7]: болезненные ощущения в ротовой полости; раздражение кожи в перианальной области; дискомфорт в животе; гиперурикемию; аллергические реакции; нарушение всасывания фолиевой кислоты (образование комплексов). Наиболее тяжелое осложнение, возникающее при длительном приеме очень высоких доз полиферментных препаратов – фиброз терминальной части подвздошной кишки и правых отделов ободочной кишки, или фиброзная колонопатия.
Хотя ее патогенез до сих пор не известен, появление этой нозологии однозначно связано с длительным приемом высоких доз полиферментных препаратов, превышающих 50000 Ед липазы на 1 кг веса в сутки [12]. До установления данной взаимосвязи было зарегистрировано всего около 60 случаев по всех странах. Фиброзная колонопатия наиболее часто проявляется метеоризмом и болевым абдоминальным синдромом, на рентгенограммах выявляется утолщение стенки кишечника и сужение просвета кишки. При биопсии определяется выраженное разрастание в подслизистом слое зрелой фиброзной ткани. Считается, что это ятрогенное осложнение обусловлено кополимерами метакриловой кислоты, являющихся компонентами энтеросолюбильных оболочек большинства полиферментных препаратов. Поскольку в Креоне кишечнорастворимая оболочка состоит из гидроксипропилметилцелюлозы, его прием является более безопасным [35].
Стратегия заместительной ферментной терапии.
Лечение внешнесекреторной недостаточности ПЖ носит комплексный характер и включает специфическую нутритивную коррекцию, этиотропную и заместительную терапию экзокринной недостаточности, а также симтоматические средства. Этиотропная терапия ХП с внешнесекреторной недостаточностью ПЖ имеет значение только при некоторых этиологических формах ХП. Это обусловлено тем, что при развитии панкреатической недостаточности происходит потеря до 90% функционирующей экзокринной паренхимы ПЖ и этиотропная терапия направлена преимущественно на предотвращение прогрессирования заболевания с максимальным сохранением оставшейся функциональной паренхимы, особенно эндокринного аппарата ПЖ. Классическими примерами этиотропных подходов к терапии является исключение приема алкоголя у больных алкогольным ХП, терапия кортикостероидами при аутоиммунном ХП. Возможно проведение оперативного лечения у больных желчнокаменной болезнью, вентильными конкрементами фатерова соска, рубцовым стенозом сфинктера Одди и другими формами обструктивного ХП. В отношении прочих причин развития ХП этиотропная терапия не разработана, либо не эффективна на данной стадии заболевания.
Нутритивная поддержка складывается из рекомендаций общего характера: исключение алкоголя и табакокурения вне зависимости от этиологии заболевания, высокое содержание белка в рационе (до 150 г/сутки), снижение на 50% от нормы содержания в пище жиров. Рекомендуются преимущественно среднецепочечные триглицериды, моно- и полиненасыщенные жирные кислоты, которые легче перевариваются панкреатической липазой и всасываются без образования мицелл. Пищевой рацион обогащается витаминами, в первую очередь жирорастворимыми. Рекомендуется принимать витаминно-минеральные комплексы, содержащие высокие дозы витаминов и микроэлементов с антиоксидантными свойствами. У больных с развитием трофологической недостаточности в зависимости от тяжести состояния назначается парентеральное, энтеральное, либо комбинированное питание.
Ферментные препараты при ХП с внешнесекреторной недостаточностью назначают пожизненно, однако доза может варьировать в зависимости от многих факторов, в том числе и от соблюдения больным диеты. Таким образом, решение о выборе дозы ферментного препарата должно приниматься индивидуально для каждого больного. Мы считаем, что при выборе концентрации активности ферментов, входящих в состав препарата, можно руководствоваться данными активности фекальной эластазы, снижение содержания которой свидетельствует о выраженности экзокринной недостаточности ПЖ. Эластазный тест в настоящее время самый информативный из неинвазивных методов диагностики внешнесекреторной недостаточности ПЖ и, в то же время он широко доступен. Ряд проведенных нами исследований, где использовалась методика подбора дозы полиферментного препарата у больных ХП, показал клиническую целесообразность ориентации на уровень фекальной эластазы при первичном выборе дозы [5,6]. В зависимости от уровня диагностированной по данным эластазного теста внешнесекреторной недостаточности назначается дифференцированная полиферментная терапия (Таблица 2). Согласно табличным данным, больным ХП с нормальной экзокринной функцией ПЖ можно назначать курсовой прием креона в дозе до 50000 ЕД липазной активности в сутки с целью коррекции симптомов диспепсии, при метеоризме и болевом абдоминальном синдроме. Больным с экзокринной недостаточностью рекомендуются более высокие стартовые дозы полиферментных препаратов.
Таблица 2.
Рекомендации по подбору дозы полиферментного препарата* у больных ХП в соответствии с данными фекальной эластазы
| Состояние экзокринной функции ПЖ | Данные эластазы кала (мкг/г) | Рекомендуемая доза препарата ЕД FIP липазы в сутки |
| Нормальная экзокринная функция ПЖ | Более 200 | 50 000 (1 капсула Креона 10 000 – 5 раз в день) |
| Умеренно выраженная экзокринная недостаточность | 100-199 | 100 000 (2 капсулы Креона 10 000 – 5 раз в день) |
| Выраженная экзокринная недостаточность | Менее 100 | 150 000 (1 капсула Креона 25 000 – 6 раз в день) |
Примечание: * только для микрокапсулированных препаратов панкреатина в энтеросолюбильной оболочке (креон, ликреаза)
Поскольку большинство больных, страдающих панкреатитом с внешнесекреторной недостаточностью, соблюдают диету, придерживаясь рекомендации частого дробного питания, у них, как правило, все приемы пищи равнозначны, и можно принимать ферменты по схеме, указанной в таблице 2. Если же диета пациента состоит из 3 традиционных приемов пищи и 2-3 промежуточных, то рекомендуется прием креона до 30000 ЕД липазы в основные приемы пищи и 10000-20000 ЕД – на промежуточные в зависимости от степени экзокринной недостаточности ПЖ. Для достижения максимального эффекта ферментные препараты должны приниматься в самом начале еды и, по возможности, фракционно во время еды (при приеме более 1 капсулы).
При клинически выраженной панкреатической недостаточности обычно не удается полностью устранить стеаторею даже с помощью высоких доз препаратов, поэтому критерием адекватности подобранной дозы пищеварительных ферментов служит увеличение массы тела, нормализация стула (менее 3 раз в день), уменьшение метеоризма.
Рис. 2. Алгоритм заместительной терапии.
Причины неэффективности заместительной ферментной терапии могут быть следующими:
— неправильно установленный диагноз;
— наличие сопутствующей ХП патологии, утяжеляющей синдром мальабсорбции и требующий специфического лечения (целиакия, воспалительные заболевания кишечника, тиреотоксикоз, глистные инвазии и т.д.);
— назначение препаратов панкреатина, не имеющих кислотозащитной оболочки (панкреаль Киршнера) без блокаторов желудочной секреции;
— назначение таблетированных препаратов панкреатина в энтеросолюбильной оболочке (асинхронный гастродуоденальный транспорт);
— назначение желчьсодержащих препаратов, усиливающих перистальтику и вызывающих осмотическую диарею;
— назначение неадекватно низких доз ферментов (в том числе микрокапсулированных) для снижения общей стоимости лечения;
— нарушение комплайнса (нарушения в диете, произвольное изменение доз, времени и кратности приема полиферментных препаратов),
— недоучет возможных механизмов, приводящих к вторичной панкреатической недостаточности (желудочная гиперсекреция с ацидификацией ДПК, цирроз печени, синдром избыточного бактериального роста, гипермоторные кишечные нарушения, постгастрорезекционные расстройства и т.д.).
У части больных с синдромом внешнесекреторной недостаточности ПЖ ускорен транзит содержимого по кишечнику, что требует назначения препаратов, ослабляющих кишечную перистальтику (имодиум, дюспаталин и др.). С симптоматическими целями могут применяться короткие курсы вяжущих и обволакивающих средств. Следует помнить, что моторика кишечника очень часто нарушена у больных сахарным диабетом и у пациентов, перенесших ваготомию (обе ситуации у пациентов с ХП, к сожалению, не редкость), кроме того, часто встречается синдром избыточного бактериального роста, снижающие эффективность заместительной полиферментной терапии [32]. Поэтому считается, что для наиболее адекватной терапии экзокринной недостаточности необходимо обязательное включение в состав лечебного комплекса препаратов, устраняющих нарушения микробиоценоза кишечника (про- и пребиотики) [9]. Предпочтение следует отдавать препаратам с пребиотическими свойствами, стимулирующим, в отличие от пробиотиков, рост собственной микрофлоры, что не вызывает лишней антигенной нагрузки на организм [2].
Как мы отмечали ранее, низкие значения интрадуоденального рН приводят к инактивации принимаемых с заместительной целью полиферментных препаратов. Даже в случае приема микросфер креона при интрадуоденальных значениях рН менее 4, растворение энтеросолюбильной оболочки произойдет только в проксимальном отделе тощей кишки, что не приведет к адекватной коррекции мальдигестии. Кроме того, при низких значениях дуоденального pH уменьшается концентрация мицелл желчных кислот и липидов, что вызывает преципитацию желчных кислот даже при нормальной постпрандиальной секреции желчи у пациентов с экзокринной недостаточностью ПЖ. Поэтому для достижения максимального терапевтического действия ферментов рекомендуется сочетать их прием с антацидами, блокаторами H2-рецепторов гистамина или ингибиторами протонной помпы, причем дозы и режим приема этих препаратов подбираются индивидуально. Полная редукция стеатореи на фоне применения данных препаратов достигается редко, хотя желудочный и дуоденальный pH поддерживался на уровне pH 5 в течение долгого времени [37]. В случае, если блокаторы Н2-рецепторов гистамина не эффективны в купировании стеатореи, показано применение ингибиторов протонной помпы [21], которые к настоящему времени себя хорошо зарекомендовали в комплексной терапии внешнесекреторной недостаточности ПЖ [4, 17,39]. По данным E.P. DiMagno в случае неэффективности заместительной ферментной терапии (прием до 90 000 ЕД липазы на прием пищи) в отношении стеатореи, введение омепразола в комплексную терапию увеличивает всасывание жиров на 40% [17]. По нашим данным [4] у больных с внешнесекреторной недостаточностью ПЖ тяжелой степени, резистентных к терапии креоном в высоких дозах достаточно эффективным оказался современный ингибитор протонной помпы – рабепразол, назначение которого привело к редукции стеатореи, диарейного синдрома и метеоризма более, чем у 70% больных, причем у части пациентов дозы полиферментного препарата были уменьшены.
В заключение следует отметить, что лечение экзокринной панкреатической недостаточности остается сложной задачей, требует комплексного подхода; при выборе схемы консервативного лечения необходим индивидуальный подход в каждом отдельно взятом случае с учетом степени экзокринной и трофологической недостаточности, выраженности болевого абдоминального синдрома и эндокринных расстройств. Разработанные в последние годы галенические формы ферментных препаратов, существенно улучшающие смешивание и сегрегацию протеаз и липазы непосредственно к их субстратам, значительно повышают качество заместительной терапии при панкреатической недостаточности. Применение таблетированных полиферментных препаратов, покрытых оболочкой, защищающей препарат от соляной кислоты в желудке практически бесполезно; только препараты последних поколений, содержащие минимикросферы панкреатина, покрытые энтеросолюбильной оболочкой, достоверно и дозозависимо уменьшают стеаторею. Знание практикующим врачом принципов заместительной ферментной терапии определяет адекватность назначенного лечения и прогноз течения болезни.
_500.gif)
_500.gif)
_500.gif)