что такое возрастной риск трисомии 21
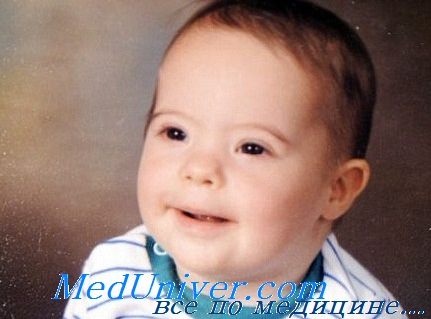
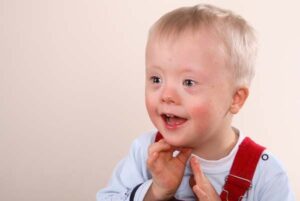
Что такое возрастной риск трисомии 21
Хотя хромосомная основа синдрома Дауна ясна, причина возникновения аномалии все еще недостаточно понята. Большой процент случаев трисомии 21, вызванных аномалией в первом делении материнского мейоза, позволяет предполагать, что это — основная причина. Из-за повышенного риска синдрома Дауна у возрастных матерей одна из возможных причин — гипотеза «старения яйцеклетки»; предполагают, что чем старше овоцит, тем больше шансов, что хромосомы не разойдутся правильно.
Анализ трисомии 21 (а также других аутосомных трисомий) подчеркнул важность количества и положения точек рекомбинации как причины нерасхождения пар хромосом в обоих делениях мейоза. Более «старые» яйцеклетки могут оказаться менее способными преодолевать склонность к нерасхождению, возникающую при рекомбинации.
Примечательная особенность этой модели (а также и фактор, существенно усложняющий исследование) — то, что событие, ведущее к рождению младенца с синдромом Дауна сегодня, произошло 35-40 лет тому назад, когда мать ребенка сама была эмбрионом и первичные овоциты вступали в профазу мейоза I. Несмотря на установление важной ассоциации между рекомбинацией и расхождением хромосом, полного понимания связи нерасхождения хромосомы 21 с эффектом материнского возраста не достигнуто.
Риск рождения ребенка с синдромом Дауна
Оценка риска рождения ребенка с синдромом Дауна — распространенная проблема при генетическом консультировании, особенно в пренатальной генетике. Синдром Дауна может быть обнаружен пренатально цитогенетически или методом CGH при исследовании ворсин хориона или клеток амниотической жидкости. Фактически около 80% процедур пренатальной диагностики выполняют в связи с возрастом матери или изменениями при биохимическом скрининге, выявившими повышенный риск синдром Дауна у плода.
В основном считают, что женщине показана пренатальная диагностика, если риск синдрома Дауна у плода превышает риск выкидыша при процедуре амниоцентеза или БВХ, используемых для получения тканей плода для хромосомного анализа. Риск зависит в основном от возраста матери, а также кариотипов обоих родителей.
Встречаемость в популяции синдрома Дауна у новорожденных в настоящее время оценивают как 1 на 800, с учетом распределения материнского возраста и процента возрастных матерей, проходящих пренатальную диагностику и выборочное прерывание беременности. У матерей старше 30 лет риск начинает быстро увеличивается, достигая 1 на 25 новорожденных у старшей возрастной группы.
Хотя молодые матери имеют значительно более низкий риск, из-за того что рождаемость у них значительно выше, более половины матерей детей с синдромом Дауна моложе 35 лет. Риск синдрома Дауна, вызванного транслокациями или частичными трисомиями, не связан с возрастом матери. Возраст отца влияния на риск синдрома Дауна не имеет.
В Соединенных Штатах и Канаде более 50% беременных старше 35 лет проходят пренатальную диагностику с проведением хромосомного анализа плода, но только у 1% протестированных обнаруживают трисомию 21. В разработке также методы изучения клеток плода, циркулирующих в материнской крови.
Риск повторного рождения ребенка с синдромом Дауна
Риск повторения трисомии 21 и некоторых других аутосомных трисомии после рождения одного ребенка в семье близок к 1%. Риск для молодых матерей (моложе 30 лет) около 1,4%, у более старых матерей равен возрастному риску; т.е. существует значимое увеличение риска для молодых матерей, но не для тех, чей риск уже повышен. Причина повышенного возвратного риска у молодых матерей неизвестна.
Одна из возможных причин — нераспознанный половой мозаицизм с трисомной линией клеток у одного из родителей. Трисомия 21 в семейном анамнезе, хотя часто вызывает беспокойство у матери, существенно не увеличивает риск родить ребенка с синдромом Дауна.
Риск повторения транслокационного синдрома Дауна, как указано ранее, значительно выше.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое возрастной риск трисомии 21
Неинвазивное исследование, которое на основании определенных лабораторных маркеров и клинических данных позволяет при помощи компьютерной программы рассчитать вероятный риск развития хромосомных болезней или других врождённых аномалий плода.
Из-за ограничений в применении расчетных методов определения риска врождённых аномалий плода расчет таких рисков при многоплодной беременности с 3 и более плодами провести невозможно.
Биохимический скрининг I триместра беременности, «двойной тест» 1-го триместра.
Синонимы английские
Maternal Screen, First Trimester; Prenatal Screening I; PRISСA I (Prenatal Risk Calculation).
Твердофазный хемилюминесцентный иммуноферментный анализ («сэндвич»-метод), иммунохемилюминесцентный анализ.
ММЕ/мл (милли- международная единица на миллилитр), МЕ/л (международная единица на литр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Болезнь Дауна – хромосомное заболевание, связанное с нарушением клеточного деления (мейоза) при созревании сперматозоидов и яйцеклеток, которое приводит к образованию дополнительной 21-й хромосомы. Частота в популяции – 1 случай на 600-800 родов. Риск хромосомной аномалии увеличивается с возрастом роженицы и не зависит от состояния здоровья матери ребенка, факторов внешней среды. Синдром Эдвардса (трисомии 18) и синдром Патау (трисомии 13) менее связаны с возрастом матери, а популяционная частота составляет 1 случай на 7000 родов. Для точной пренатальной диагностики генетических заболеваний требуются инвазивные процедуры, которые связаны с большой вероятностью осложнений, поэтому для массового скрининга используются безопасные методы исследования, позволяющие выявить низкий или высокий риск хромосомных аномалий и оценить целесообразность дальнейшего обследования.
Пренатальный скрининг трисомий I триместра беременности выполняют, чтобы определить вероятный риск хромосомной патологии плода – трисомии 21 (синдрома Дауна), а также трисомии 18 (синдрома Эдвардса) и трисомии 13 (синдрома Патау) на сроке между 10-й неделей и 13-й неделей и 6 днями беременности. Его рассчитывают с помощью компьютерной программы PRISCA (Prenatal Risk Calculation), разработанной компанией Typolog Software (Германия) и имеющей международный сертификат соответствия. Для исследования определяется содержание свободной бета-субъединицы хорионического гонадотропина (ХГЧ) и ассоциированного с беременностью белка плазмы А (PAPP-А) в крови беременной.
Фермент PAPP-A обеспечивает полноценный рост и развитие плаценты. Его содержание в крови увеличивается с течением беременности. Уровень РАРР-А существенно не зависит от таких параметров, как пол и масса ребенка. При наличии хромосомной аномалии с пороками развития плода его концентрация в крови значительно уменьшается с 8-й по 14-ю недели беременности. Наиболее резко она снижается при трисомиях по 21-й, 18-й и 13-й хромосомам. При синдроме Дауна показатель PAPP-A на порядок ниже, чем при нормальной беременности. Еще более резкое уменьшение концентрации РАРР-А в сыворотке крови матери наблюдается при наличии у плода генетической патологии с множественными пороками развития – синдроме Корнелии де Ланге. Однако после 14 недель беременности ценность определения PAPP-A в качестве маркера риска хромосомных аномалий утрачивается, так как его уровень тогда соответствует норме даже при наличии патологии.
Для скрининга обязательно учитываются клинические данные (возраст беременной, масса тела, количество плодов, наличие и особенности ЭКО, раса матери, вредные привычки, наличие сахарного диабета, принимаемые лекарственные препараты), данные УЗИ (копчико-теменной размер (КТР) и толщина воротникового пространства (ТВП), длина носовой кости). При наличии данных УЗИ срок беременности рассчитывается по величине КТР, а не по дате последней менструации.
После исследования и расчета риска проводится плановая консультация у врача – акушера-гинеколога.
Результаты скринингового исследования не могут служить критериями для постановки диагноза и поводом для искусственного прерывания беременности. На их основании принимается решение о целесообразности назначить инвазивные методы обследования плода. При высоком риске необходимы дополнительные обследования, в том числе пункция хориона, амниоцентез с генетическим исследованием полученного материала.
Для чего используется исследование?
Когда назначается исследование?
Что такое возрастной риск трисомии 21
Возраст матери как фактор риска врожденных пороков развития
Сотрудники «Научно-исследовательского клинического института педиатрии им. академика Ю.Е. Вельтищева» и «Российской медицинской академии непрерывного профессионального образования» провели анализ возрастной структуры матерей детей с врожденными пороками развития для оценки возрастных рисков врожденных аномалий хромосомной и нехромосомной природы по данным мониторинга.
Врожденные пороки развития – самая частая патология в структуре причин мертворождений, младенческой смертности, младенческой и детской заболеваемости. Это связано как с абсолютным, так и с относительным ростом этой группы заболеваний. Увеличению их числа могут способствовать происходящие в настоящее время изменения демографических характеристик населения. Так, за последние два десятилетия заметно изменился профиль материнского возраста в Европе, причем с каждым годом средний возраст материнства увеличивается. Хорошо известно, что возраст женщины сопряжен с риском развития определенных заболеваний у их детей. Женщины старшего возраста имеют более высокий риск рождения детей с хромосомными аномалиями, такими как синдром Дауна. На другом конце спектра материнского возраста находятся матери-подростки, которые имеют низкий риск рождения детей с хромосомными нарушениями, но более высокий риск возникновения некоторых аномалий нехромосомной этиологии, в частности дефектов брюшной стенки, врожденных пороков сердца у детей.
В связи с этим важно иметь точную информацию о специфических для матерей возрастных рисках рождения детей с врожденными пороками, чтобы оценить последствия наблюдающегося увеличения материнского возраста для общественного здравоохранения, в частности увеличения потребности в медико-генетическом консультировании, пренатальном скрининге и пренатальной диагностике. Однако большинство данных было получено из исследований, выполненных в странах Европы, входящих в систему EUROCAT (Европейская сеть популяционных стандартизованных регистров эпидемиологического надзора за врожденными аномалиями), охватывающей почти треть рождений в Европе или в Америке. Подобное исследование по Российской Федерации стало возможным благодаря длительному мониторингу врожденных пороков развития, что позволяет проводить статистический анализ полученных данных.
Источником данных для изучения ассоциации между возрастом матери и частотой врожденных пороков развития является объединенная база данных мониторинга врожденных пороков регионов Российской Федерации. В основе мониторингового регистра лежит популяционный подход, при котором предусматривается максимально полный сбор данных о новых случаях пороков развития в контролируемом регионе, что достигается использованием множественных источников регистрации. Сведения в региональные регистры поступают из роддомов, детских стационаров, поликлиник и патологоанатомических отделений.
В мониторинговый регистр включаются случаи пороков среди живорожденных, мертворожденных детей и плодов. Материалом для исследования послужили данные из 23 регионов Российской Федерации: Брянская область, Кабардино-Балкарская республика, Калужская, Кировская области, Красноярский край, Курская, Липецкая, Московская, Омская, Оренбургская области, Республика Калмыкия, Республика Саха (Якутия), Республика Северная Осетия–Алания, Рязанская, Самарская, Саратовская, Свердловская, Смоленская, Тамбовская, Тульская области, Удмуртская республика, Ханты-Мансийский автономный округ, Чувашская республика. Период исследования включал с 2011 по 2018 г.
Для анализа были отобраны случаи хромосомной патологии, регистрируемой в системе мониторинга врожденных пороков развития: синдромы Дауна (Q90), Эдвардса и Патау (Q91). В группу пороков нехромосомной этиологии были отобраны следующие врожденные аномалии: анэнцефалия (Q00), энцефалоцеле (Q01), врожденная гидроцефалия (Q03), spina bifida (Q05), расщелина неба (Q35.0–Q35.6, Q35.9), расщелина губы (Q36), расщелина неба и губы (Q37), атрезия пищевода без свища (Q39.0) и с трахеопищеводным свищем (Q39.1), врожденные атрезии и стенозы аноректального отдела (Q42.0–Q42.3), гипоспадия (Q54), агенезия почки двусторонняя (Q60.1), синдром Поттер (Q60.6), эписпадия (Q64.0), экстрофия мочевого пузыря (Q64.1), врожденная диафрагмальная грыжа (Q79.0), экзомфалоз (Q79.2) и гастрошиз (Q79.3).
Оценка частоты заболеваний проводилась в зависимости от возраста матери на момент рождения ребенка. Были выделены следующие возрастные группы матерей: моложе 20 лет, 20–34 года, 35–39 лет, 40–44 года и 45 лет и старше. Частота хромосомных и нехромосомных заболеваний рассчитывалась для каждой возрастной группы на 1000 рождений. Число случаев врожденных пороков развития (числитель) включало случаи анализируемых заболеваний, зарегистрированных среди живорожденных, мертворожденных и у плодов, выявленных пренатально с последующим прерыванием беременности. Для оценки частот использовались сведения обо всех рождениях с распределением по возрастам матерей. Общее число рождений составило за анализируемый период 5 047 468.
Статистические выводы основывались на пуассоновском распределении числа случаев врожденных пороков развития. Интервал значений, в пределах которого с вероятностью 95% находится значение параметра распределения Пуассона, обозначает 95% доверительный интервал (ДИ). Частота врожденных пороков рассчитывалась на 1000 рождений. Расчеты проводились с использованием пакета статистических программ SPSS 13.0.
Для сравнения приведены данные EUROSTAT за 2000–2004 гг. Видно, что структура материнского возраста в настоящем исследовании и по данным EUROSTAT достаточно сопоставима. Абсолютное большинство рождений приходится на возрастной период с 20 до 34 лет (82,1 и 76% соответственно). Эту возрастную группу использовали в качестве основной группы сравнения. Практически нет различий и в доле рождений женщинами молодого (моложе 20 лет) и старшего возраста (старше 40 лет).
С целью анализа изменения возрастного профиля матерей в динамике провели сравнение возрастной структуры женщин в 2011 и 2018 г. Как видно, за 8-летний период увеличилась доля матерей старше 35 лет: в 2011 г. суммарно они составляли 10,03%, а в 2018 г. – 17,79%. Аналогичные тенденции прослеживаются в странах как Европы, так и Азии. Так, согласно данным международного центра по изучению врожденных пороков развития (International Clearinghouse for Birth Defects Surveillance and Research – ICBDSR) в странах Европы доля матерей старше 35 лет увеличилась с 10,9% в 1993 г. до 18,8% в 2004 г. В Южной Корее процент беременных женщин пожилого возраста увеличился более чем в 2 раза за 10-летний период: с 6,2% в 1999 г. до 15,4% в 2009 г. В то же время хорошо известно, что старший возраст матерей связан с повышенным риском возникновения хромосомных аномалий; это касается в первую очередь таких хромосомных нарушений, как трисомии хромосом 13, 18 и 21.
На материале объединенной базы данных мониторинга врожденных пороков развития оценили частоту хромосомных болезней по группе трисомий 13, 18, 21 в зависимости от возраста матери. Всего за период с 2011 по 2018 г. было зарегистрировано 7675 случаев трисомий хромосом 13, 18 и 21 у новорожденных и плодов на 5 047 468 рождений. Суммарная частота составила 1,52 на 1000 рождений. В то же время в разных возрастных группах матерей частоты указанных трисомий значительно различались. Если в возрастном интервале от 20 до 34 лет их частота составила 0,9 на 1000 рождений, то после 40 лет этот показатель увеличился до 13,34 на 1000 рождений, а после 45 лет – до 23,32 на 1000 рождений. Таким образом, возраст женщины старше 35 лет рассматривается как безусловный фактор риска развития анеуплоидий, что объясняется прямой ассоциацией материнского возраста с частотой мейотического нерасхождения хромосом в период оогенеза.
В проведенном исследовании определили возрастной профиль женщин в группе врожденных пороков развития нехромосомной этиологии, включавшей грубые пороки развития ЦНС, пищеварительного тракта, мочеполовой системы и брюшной стенки. Всего за анализируемый период в базе данных мониторинга было зарегистрировано 20 654 таких случаев, что составило 4,09‰ для выбранной группы пороков развития. Анализ распределения частот врожденных пороков нехромосомной этиологии в разных возрастных группах матерей показал, что в группе матерей моложе 20 лет частота таких пороков развития составила 4,56‰, в группе матерей 35–39 лет – 4,64‰, максимальная частота наблюдалась в группе женщин старше 45 лет (7,98‰). Таким образом, начиная с возраста 35 лет наблюдается значительный рост частоты врожденных пороков развития.
Анализ данных мониторинга врожденных пороков развития позволил выявить прямую зависимость частоты хромосомных заболеваний от возраста матери. Для врожденных пороков нехромосомной природы отмечается увеличение риска у матерей младшей и старшей возрастных групп. Таким образом, сдвиг в структуре материнского возраста в сторону увеличения доли женщин старшего возраста может рассматриваться как фактор риска повышения частоты врожденных пороков развития в целом. Необходимы дальнейшие исследования, направленные на выяснение роли возраста женщины для конкретных форм пороков развития, что будет иметь значение для повышения эффективности их профилактики.
Демикова Н.С., Подольная М.А., Лапина А.С.
Российский вестник перинатологии и педиатрии, 2020; 65:(2)
Беременность – пренатальный скрининг трисомий I триместра беременности (синдром Дауна)
Неинвазивное исследование, которое на основании определенных лабораторных маркеров и клинических данных позволяет при помощи компьютерной программы рассчитать вероятный риск развития хромосомных болезней или других врожденных аномалий плода.
Биохимический скрининг I триместра беременности, «двойной тест» 1-го триместра.
Синонимы английские
Maternal Screen, First Trimester; Prenatal Screening I; PRISСA I (Prenatal Risk Calculation).
Твердофазный хемилюминесцентный иммуноферментный анализ («сэндвич»-метод), иммунохемилюминесцентный анализ.
ММЕ/мл (милли- международная единица на миллилитр), МЕ/л (международная единица на литр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Болезнь Дауна – хромосомное заболевание, связанное с нарушением клеточного деления (мейоза) при созревании сперматозоидов и яйцеклеток, которое приводит к образованию дополнительной 21-й хромосомы. Частота в популяции – 1 случай на 600-800 родов. Риск хромосомной аномалии увеличивается с возрастом роженицы и не зависит от состояния здоровья матери ребенка, факторов внешней среды. Синдром Эдвардса (трисомии 18) и синдром Патау (трисомии 13) менее связаны с возрастом матери, а популяционная частота составляет 1 случай на 7000 родов. Для точной пренатальной диагностики генетических заболеваний требуются инвазивные процедуры, которые связаны с большой вероятностью осложнений, поэтому для массового скрининга используются безопасные методы исследования, позволяющие выявить низкий или высокий риск хромосомных аномалий и оценить целесообразность дальнейшего обследования.
Пренатальный скрининг трисомий I триместра беременности выполняют, чтобы определить вероятный риск хромосомной патологии плода – трисомии 21 (синдрома Дауна), а также трисомии 18 (синдрома Эдвардса) и трисомии 13 (синдрома Патау) на сроке между 10-й неделей и 13-й неделей и 6 днями беременности. Его рассчитывают с помощью компьютерной программы PRISCA (Prenatal Risk Calculation), разработанной компанией Typolog Software (Германия) и имеющей международный сертификат соответствия. Для исследования определяется содержание свободной бета-субъединицы хорионического гонадотропина (ХГЧ) и ассоциированного с беременностью белка плазмы А (PAPP-А) в крови беременной.
Фермент PAPP-A обеспечивает полноценный рост и развитие плаценты. Его содержание в крови увеличивается с течением беременности. Уровень РАРР-А существенно не зависит от таких параметров, как пол и масса ребенка. При наличии хромосомной аномалии с пороками развития плода его концентрация в крови значительно уменьшается с 8-й по 14-ю недели беременности. Наиболее резко она снижается при трисомиях по 21-й, 18-й и 13-й хромосомам. При синдроме Дауна показатель PAPP-A на порядок ниже, чем при нормальной беременности. Еще более резкое уменьшение концентрации РАРР-А в сыворотке крови матери наблюдается при наличии у плода генетической патологии с множественными пороками развития – синдроме Корнелии де Ланге. Однако после 14 недель беременности ценность определения PAPP-A в качестве маркера риска хромосомных аномалий утрачивается, так как его уровень тогда соответствует норме даже при наличии патологии.
Для скрининга обязательно учитываются клинические данные (возраст беременной, масса тела, количество плодов, наличие и особенности ЭКО, раса матери, вредные привычки, наличие сахарного диабета, принимаемые лекарственные препараты), данные УЗИ (копчико-теменной размер (КТР) и толщина воротникового пространства (ТВП), длина носовой кости). При наличии данных УЗИ срок беременности рассчитывается по величине КТР, а не по дате последней менструации.
После исследования и расчета риска проводится плановая консультация у врача – акушера-гинеколога.
Результаты скринингового исследования не могут служить критериями для постановки диагноза и поводом для искусственного прерывания беременности. На их основании принимается решение о целесообразности назначить инвазивные методы обследования плода. При высоком риске необходимы дополнительные обследования, в том числе пункция хориона, амниоцентез с генетическим исследованием полученного материала.
Для чего используется исследование?
Когда назначается исследование?
Основные виды трисомии и причины ее возникновения
Трисомия — это числовые нарушения хромосом в результате которых в гомологичной паре присутствует одна лишняя хромосома. В норе у человека 46 хромосом, которые распределены по парам, всего 23 пары. Помимо трисомии могут возникать процессы, при которых наоборот недостает одной хромосомы из пары, моносомии.
Основные причины возникновения хромосомной мутации.
Причины трисомии активно изучаются. В связи с тем, что количество детей, рожденных с анеуплоидией, увеличивается, необходимо до конца понять механизм образования хромосомных патологий на ранних стадиях беременности.
Одна из причин проявляется в анафазе I мейоза, когда одна или несколько паргомологичных хромосом не разойдутся. Далее они направляются к одному и тому же центру клетки. В результате возникает гамета с числовыми нарушениями. Такое явление называется нерасхождение.
Чаще всего числовые мутации связаны с нарушениями в кариотипе яйцеклетки. Если рассматривать риски возникновения аномалий в сперотозоиде и яйцеклетки, то на долю яйцеклеток приходится 75%, против 25% у сперматозоидов. Считается, что после 35 лет у женщины риск родить ребенка с анеуплоидией составляет 1%.
Генетические хромосомные заболевания могут иметь наследственных характер, если кто- то из родителей или родственников является носителем патологий. Сейчас учащаются случаи рождения детей с хромосомными у здоровых родителей. К основными причинам, увеличивающим вероятность возникновения болезни относятся:
Диагностирование аномалий должно протекать в несколько этапов:
Прерывание беременности назначается только врачом и желательно на основании инвазивного анализа.
Какие разновидности бывают?
К основным видам аномалий можно отнести аутосомные и половые трисомии. К первому типу относятся три основных патологии:
В отличие от трисомии 21, 13, 18, с АПХ люди вполне жизнеспособны и могут иметь потомство. Внешний вид не сильно выделяется.
Можно ли вылечить заболевание?
К сожалению, генетические числовые хромосомные нарушения не поддаются лечению. Их можно диагностировать на ранних стадиях беременности и вовремя принять меры. Для профилактики возникновения плода с патологией, рекомендуется пройти полное клиническое обследование перед зачатием. Если женщина и/или мужчина в группе риска (см. выше),то стоит уделить этому вопросу особое внимание.
В отличие от Дауна, Эдвардса и Патау, с АПХ можно вести полноценную жизнь с помощью гормональной терапией