что такое вакцинация и пролонгированная в индонезии
Чем опасна вакцинация от коронавируса
Что известно о COVID-19?
Это РНК-содержащий вирус животного происхождения, относящийся к группе коронавирусов. Согласно данным ВОЗ, он передается от заболевшего человека через мелкие капли, которые выделяются при чихании и кашле из носа и рта. С момента заражения до появления первых симптомов проходит от 1 до 14 дней (в среднем – 7). Носитель вируса еще не знает о своей болезни, но в плане заражения уже представляет опасность для окружающих. По информации коронавирусной эпидемиологии, COVID-19 в 2-3 раза заразнее гриппа, но в 2-3 раза менее заразен, чем корь.
При легком течении болезни ее симптомы сходны с ОРВИ и заканчиваются выздоровлением через 14 дней без каких-либо дальнейших последствий. В тяжелых случаях COVID продолжается до 8 недель. Даже при отсутствии выраженных признаков заболевания у переболевших формируется иммунитет. Но учитывая, пусть и нечастые случаи повторного заражения, сохраняется он не слишком долго. Гораздо большим эффектом обладает вакцина.
Как действует вакцина?
Сегодня в мире используется несколько иммунопрепаратов, разработанных специалистами разных стран и прошедших необходимые клинические испытания. Все они предназначены для формирования иммунитета к возбудителю. После их введения иммунная система:
У человека, прошедшего вакцинацию, формируется стойкий иммунитет к COVID.
Опасна ли вакцинация?
Каждый человек реагирует на иммунопрепарат индивидуально. Поэтому даже самая качественная вакцина может вызвать побочные эффекты. Их появление на непродолжительное время – единственная опасность.
Чем опасна вакцинация от коронавируса:
Эти неприятные симптомы исчезают в течение нескольких дней.
Тяжелые состояния после введения иммунопрепарата могут развиваться у людей, имеющих противопоказания. Нельзя проводить вакцинацию, если наблюдаются:
При этих патологиях прививка может спровоцировать обострение.
Также противопоказанием является возраст (младше 18 и старше 65 лет), беременность, недавно перенесенная тяжелая форма коронавирусной инфекции. У переболевших людей в первое время после выздоровления отмечается высокий уровень антител, а вакцина повысит его еще больше. Последствия могут проявиться бурной иммунной реакцией в форме цитокинового шторма.
Как уменьшить негативные проявления?
Снизить развитие побочных явлений поможет соблюдение всех рекомендаций врача. Чтобы уменьшить риск развития негативных симптомов после вакцинации, нужно:
При отсутствии противопоказаний и соблюдении всех требований, риск побочных эффектов сводится к минимуму.
После прививки от коронавируса врачи советуют соблюдать щадящий режим и выпивать не менее 1,5 литров жидкости в день. При повышении температуры рекомендуется принять жаропонижающее средство. Если слабость не проходит в течение нескольких дней, появились аллергические реакции, нужно немедленно обратиться к доктору.
Когда будет массовая вакцинация?
Массовая вакцинация в США, Канаде и европейских странах началась еще в декабре прошлого года. В это же время стартовала она и в России. Но на начальном этапе мероприятие проводилось только для определенной категории лиц – молодых людей и тех, кто по роду своей профессиональной деятельности не может ограничить число контактов. Сегодня привиться от ковида можно в любом регионе страны.
Что такое ВАКЦИНАЦИЯ
Что такое вакцинация?
Что такое ревакцинация?
Какие существуют виды вакцин?
Курс прививок начат одной вакциной, можно закончить курс другой вакциной?
Да, согласно международным рекомендациям все вакцины взаимозаменяемы, хотя вполне естественно, что несколько более предпочтительно делать весь курс прививок одной вакциной.
Чего можно ожидать в случае отказа от проведения вакцинации?
Ваш ребенок может заболеть теми болезнями, от которых можно сделать прививки. Заболев, ваш ребенок может заразить окружающих (в том числе и членов семьи). Несмотря на действующее законодательство, Вам могут отказать в приеме в детский сад или школу. В поликлинике Вам могут не дать рецепт на молочную кухню для ребенка. При карантине или эпидемии Вам могут временно отказать в приеме в учебное или оздоровительное учреждение (пока не пройдет риск заражения).
Какие существуют противопоказания к проведению вакцинации?
Какие сроки возникновения побочных реакций от вакцинации?
Побочные действия вакцин, как правило, проявляются в пределах 4-недель после иммунизации. Реакции на инактивированные вакцины обычно развиваются рано (в течение нескольких часов) и их проявления являются более кратковременными.
Какие реакции возникают на вакцины в настоящее время?
Число побочных реакций минимально, поскольку современные вакцины как правило на 95% состоят из антигена. В месте введения вакцины крайне редко возникают покраснения и уплотнения. В редких случаях возможно незначительное повышение температуры тела.
В заключении хотелось бы отметить, что решить, прививать ребенка или нет могут только его родители. И никто не в праве их заставить.
Но стоит подумать о том, что в случае возникновения осложнений или побочных реакций от вакцин они все равно гораздо менее опасны, чем заболевания, от которых эти прививки сделаны.
Манипуляция: Искусственный интеллект признал использование вакцин эвтаназией
Следующий
Мажилис одобрил законопроект для развития социального предпринимательства
Автор
Ержан Кенесов
Поделиться статьей
Пользователи Казнета делятся видеороликом, в котором голосовому помощнику «Алисе» задают вопрос о том, что такое «пролонгированная эвтаназия». Искусственный интеллект находит ответ в социальной сети «ВКонтакте» и сообщает, что пролонгированная эвтаназия — это вакцинация. Это сообщение является манипуляцией, передает Toppress.kz со ссылкой на StopFake.kz.
На видео голосовой помощник читает популярный фейк о том, что «вакцинация – это пролонгированное убийство», распространившийся после высказывания фельдшера Марины Корнатовской. О том, что это утверждение ложное, мы уже рассказывали ранее.
Голосовой помощник не способен отвечать на вопросы пользователей самостоятельно. «Алиса» находит наиболее подходящие ответы в Сети, следуя заданному алгоритму. Таким образом, на запрос пользователя о погоде «Алиса» не делает прогноз самостоятельно, а лишь озвучивает найденный в интернете результат.
При этом источник информации выбирает тот, который больше других соответствует запросу. В данном случае, например, он цитирует пост в соцсети. Искусственный интеллект не берет в расчет авторитетность и достоверность озвученных данных.
Термин «пролонгированная эвтаназия» используется относительно недавно и исключительно противниками вакцинации. Поэтому встретить его в контексте, не имеющем отношения к иммунизации, невозможно.
В классическом понимании эвтаназия быть пролонгированной не может, так как по определению является «практикой прекращения жизни человека, страдающего неизлечимым заболеванием и испытывающего вследствие этого заболевания невыносимые страдания». То есть к ней прибегают исключительно для того, чтобы как можно быстрее прекратить мучения неизлечимо больного человека.
В классификации видов эвтаназии термина «пролонгированная» также нет.
Таким образом, расценивать ответ «Алисы» как истину в последней инстанции нельзя. Голосовой помощник лишь прочел пост пользователя социальной сети, который соответствовал запросу.
Теория о том, что вакцинация ведет к смерти, была многократно опровергнута и признана антинаучной.
Индонезия меняет правила въезда в страну
Власти Индонезии приняли решение сократить обязательный карантин для прибывающих иностранцев, а также ввели некоторые другие послабления. Воспользоваться нововведением пока смогут вакцинированные россияне, имеющие бизнес-визу.
ИНДОНЕЗИЯ СОКРАЩАЕТ КАРАНТИН ДО 3 ДНЕЙ И РАЗРЕШАЕТ ВЪЕЗД ПРИВИТЫМ ПЕРВОЙ ДОЗОЙ ДВУКОМПОНЕНТНОЙ ВАКЦИНЫ
Благодаря стабилизации эпидемиологической обстановки власти Индонезии могут продолжать вводить послабления в ограничениях. Вслед за открытием аэропорта на острове Бали для международных рейсов из Китая, Японии, Южной Кореи, Новой Зеландии, Катара и Объединенных Арабских Эмиратов, правительство островного государства приняло решение сократить срок обязательного карантина для полностью вакцинированных туристов с 5 до 3 суток (3 ночи). Соответствующее правительственное решение вступило в силу 2 ноября.
Также было принято решение разрешить въезд в страну иностранцам, привитым только первой дозой двухкомпонентной вакцины. Однако для них будет действовать 5-дневный карантин. Правило распространяется и на вакцинированных первым компонентом «Спутника V». Напомним, Индонезия принимает только одну российскую вакцину – «Спутник V».
РОССИЯНЕ ПОКА НЕ МОГУТ ПРИЛЕТЕТЬ СРАЗУ НА БАЛИ
«Вакцинированные «Спутником V» россияне, имеющие бизнес-визу, как и прежде, должны будут проходить карантин в столичной Джакарте. Прилететь сразу на Бали рейсами из разрешенных стран они пока не смогут», – напомнили в туристическом офисе Индонезии в России (VITO Russia).
КАКИЕ ДОКУМЕНТЫ ПОНАДОБЯТСЯ ДЛЯ ВЪЕЗДА НА БАЛИ
Для въезда в Индонезию россиянам необходимо будет сделать ПЦР-тест за 72 часа до поездки, далее по приезду и еще один тест нужно будет сделать на третий день карантина. Также необходимо иметь при себе сертификат вакцинации, международный полис медицинского страхования с покрытием не менее 100 000 долларов, куда входит и лечение от коронавируса, а также ваучер на проживание в карантинном отеле.
Список отелей в Джакарте, которые можно бронировать для прохождения карантина – тут.
ТУРИСТИЧЕСКИЕ ВИЗЫ В ИНДОНЕЗИЮ ПОКА НЕДОСТУПНЫ
С туристическими целями россияне пока приехать в Индонезию не могут, только с деловыми целями по бизнес-визе.
Бизнес-виза обязательно должна оформляться через турагентство (принимающую компанию) в Индонезии – либо напрямую, либо через российского туроператора. Принимающая компания станет «спонсором» туриста, поручится за него и запросит специальное разрешение на бизнес-визу в столице Индонезии Джакарте.
ИНДОНЕЗИЯ В БЛИЖАЙШЕЕ ВРЕМЯ МОЖЕТ ОТКРЫТЬСЯ ДЛЯ РОССИЙСКИХ ТУРИСТОВ
Российские туроператоры, ссылаясь на информацию, полученную от своих индонезийских партнеров, рассказали «Вестнику АТОР», что решение по туристическим визам для россиян может быть принято в ближайшее время, а это будет означать, что россияне вновь смогут приезжать на отдых в Индонезию.
Однако официальной информации на этот счет пока нет, уточнили в VITO Russia.
ВНИМАНИЕ:
Бесплатные онлайн-курсы, вебинары и электронные каталоги туроператоров вы найдете в «Академии АТОР».
Иммунный ответ на коронавирус SARS-CoV‑2 у больных COVID‑19
Академик Российской академии наук, д.м. н., президент
ФБГУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России
В статье представлен анализ результатов исследований иммунного ответа и памяти к SARS-CoV‑2, включая все ветви адаптивного иммунитета, иммуноглобулины, В-клетки памяти, CD8+- и CD4+-T-клетки у больных в динамике в течение 6–8 месяцев после начала заболевания.
Гуморальное звено
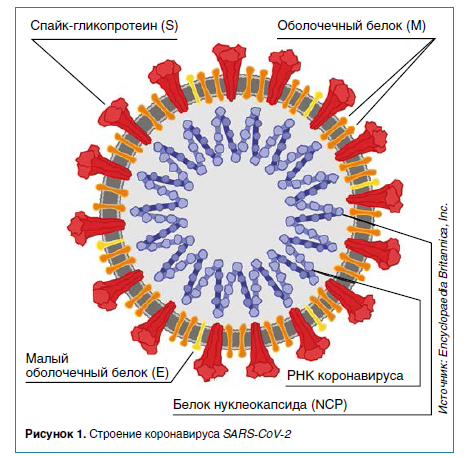
Факт первичного иммунного ответа слизистых на COVID‑19 необычен и требует объяснения. Обсуждаются две гипотезы.
Первая: вирусы контаминируют слизистые дыхательных путей и ЖКТ за 7–14 дней до появления системного ответа и клинических проявлений инфекции, поражая клетки микробиоты — используют их для репродукции вируса.
Вторая: кросс-реактивная продукция антител, предпосылкой которой являются Spike-реактивные CD4+-Т-клетки, обнаруженные у большинства пациентов с COVID‑19 и более чем у 34 % неинфицированных людей. Это подтверждает существование общих эпитопов эндемичных коронавирусов, вызывающих банальные ОРВИ и COVID‑19.
Важно, что изотипы иммуноглобулинов (либо IgG, либо IgA) конкурировали за нейтрализующую активность по отношению к SARS-CoV‑2 в зависимости от локализации. Сывороточные антитела IgG сильно коррелировали с величиной IgG-ответа и тяжестью заболевания. У пациентов, например, с IgA-назальным ответом определялась высокая активность нейтрализации вирусов. Инфекция у таких больных протекала бессимптомно.
Это, с одной стороны, предполагает возможность нейтрализации вируса с помощью IgA слизистых без системного ответа, что имеет отношение к исходам заболевания. А с другой стороны, из-за множества корреляций, наблюдаемых между типами антител и их активностью в разных анатомических участках, клиническая интерпретация гуморального ответа существенно затруднена.
Кроме того, эти данные имеют важное значение для нашего понимания защиты вакцинации, индуцирующей системный ответ на вакцинные гены или белки коронавируса по классическому пути и обеспечивающей иммунный ответ слизистых оболочек на 3–6‑й неделе после вакцинации. В идеале вакцина должна не только защитить реципиента от неизбежной болезни, но и предотвратить бессимптомное носительство, что закрыло бы проблему бессимптомных носителей в популяции.
Титры Spike IgА и RBD IgА сохранялись на стабильном уровне на протяжении всего периода наблюдения t1/2— 210 дней, но у отдельных пациентов уровень специфических IgА-антител достоверно снижался через 90 дней.
Нельзя дать однозначный ответ в отношении серонегативных случаев COVID‑19. По-видимому, кроме протективного эффекта иммунитета слизистых, ответ напрямую связан с уровнем вирусной нагрузки SARS-CoV‑2. С одной стороны, высокие вирусные нагрузки связаны с более ранним ответом антител, в то время как у пациентов с низкой вирусной нагрузкой не может быть сероконверсии. С другой стороны, кинетика иммунного ответа может быть показателем скорости элиминации вируса у больного.
Идентификация специфичных В-клеток памяти к Spike, RBD и NCP с использованием флюоресцентно окрашенных зондов на IgD– и (или) CD27+ c последующей дифференцировкой по изотипам поверхностных IgM, IgG или IgA показала следующее. Количество специфических В-клеток увеличивалось в течение 120 дней после начала заболевания с последующим выходом на плато, в то время как Spike-специфические В-клетки памяти у людей, не заболевших COVID‑19, практически не встречались. RBD-специфические В-клетки появлялись на 16‑й день, и их количество увеличивалось в течение последующих 4–5 месяцев. Интересно, что только 10–30 % Spike-специфических В-клеток памяти было специфично для домена RBD через 6 месяцев после выздоровления больных.
NCP-специфичные В-клетки памяти также стабильно увеличивались в те же сроки и определялись спустя 5–6 месяцев после заболевания. Представленность изотипов иммуноглобулинов Spike-специфических В-клеток имела следующую динамику. В ранней фазе (20–60 дней) после заболевания IgM+ и IgG+ на В-клетках были представлены одинаково. В период после 60 дней до 240‑х суток преобладали IgG+ Spike-специфические В-клетки. Частота IgА+ Spike-специфических клеток составляла примерно 5 %, и они равномерно распределялись в течение всего периода наблюдения в 8 месяцев. Корреляция между сывороточным IgA и IgA слизистых оболочек не проводилась.
Сходная картина динамики наблюдалась и в случае IgG+, IgM+ и IgА+ к эпитопам RBD и NCP коронавируса. В то же время долгосрочное присутствие циркулирующих В-клеток памяти, направленных как против основных SARS-CoV‑2‑нейтрализующих таргетов (Spike и RBD), так и против не нейтрализующего таргета (NCP), свидетельствует о клеточной памяти, сохраняющейся после естественного воздействия вируса. Это может быть использовано для планирования ревакцинации. Тот факт, что почти все RBD- специфические IgG+-В-клетки памяти экспрессировали CD27, свидетельствует о долгосрочной иммунной памяти.
Анализ полученных данных говорит о том, что снижение нейтрализующих и других антител к SARS-CoV‑2 после клинического выздоровления вовсе мунитета. Просто с развитием и сохра- нением памяти В-клеток, способных активизироваться при встрече с новыми штаммами коронавируса, уровень антител в сыворотке снижается, в то время как IgА-ответ слизистых сохраняется на постоянном уровне в течении всего периода наблюдения.
Клеточный ответ
Процент больных с обнаруживаемыми циркулирующими CD8+-Т-клетками памяти через месяц после возникновения симптомов составил 70 %. К 6–9 месяцам клетки обнаруживались у 50 % выздоровевших пациентов. Фенотипические маркеры показали, что большинство SARS-CoV‑2‑специфичных CD8+-Т-клеток представлены терминально дифференцированными клетками памяти.
Циркулирующие SARS-CoV‑2‑специфичные CD4+-Т-клетки памяти через месяц после начала заболевания обнаруживались у 93 % пациентов. Через 6–9 месяцев уровень этих клеток был стабильным, а сами они выявлялись у более чем у 90 % пациентов, перенесших COVID‑19. Причем это касалось как Spike-специфичных, так и мембраноспецифичных CD4+-Т-клеток памяти.
Интересно, что при сравнении параметров иммунного ответа у больных с тяжелым и легким течением инфекции гуморальные показатели были более высокими у тяжелых больных, в то время как CD8+-Т-клетки были стабильными, а CD4+ — более низкими в тяжелых случаях заболевания. Объяснений этому феномену нет, важно, что слабый ответ Т-клеток наблюдается в острой фазе заболевания. Кроме того, важна и методология исследования клеточного им-мунитета.
Нарушения клеточного ответа проиллюстрированы дефицитом интерферонов I и II типов у пациентов с тяжелыми и среднетяжелыми формами COVID‑19 по сравнению с легкими и бессимптомными случаями заболевания. Это может быть связано с подавлением воспаления интерлейкином‑12 (IL‑12) и развитием вторичного дефекта клеточного иммунитета.
Иммунное взаимодействие
Большой интерес представляет изучение взаимодействия гуморального и клеточного ответа на SARS-Cov‑2. В исследованиях RBD-IgG, Spike IgА, RBD-В-клеток памяти, CD8+- и CD4+-Т-клеток в динамике у одних и тех же пациентов установлено, что у большинства из них (64 %) положительные показатели отмечались через 1–2 месяц после начала заболевания. Через 5–8 месяцев число реконвалесцентов, позитивных на пять тестов, снизилось до 43 %. В то же время как минимум три из пяти тестов были положительными спустя 6–9 месяцев. Важно отметить, что IgG на Spike дает на порядок больше положительных ответов, чем на RBD-антиген. Попытки связать гуморально- клеточные взаимодействия не привели к успеху из-за неоднородности участников исследования и методик оценки иммунного ответа.
Неопределенный результат
В метаанализе 22 исследований (4969 пациентов) установлены неблагоприятные признаки тяжелых форм болезни и летальных исходов, такие как лимфопения и нейтрофилез. Поскольку CD4+-Т-клетки необходимы для сбалансированного и эффективного иммунного ответа, неудивительно, что низкий уровень лимфоцитов может отражать гипервоспалительные процессы и способствовать более тяжелому течению заболевания и повышенной смертности.
Нейтрофилы как неотъемлемая часть врожденной защиты контролируют баланс микробиоты и элиминацию продуктов клеточной деструкции за счет производства активных форм кислорода и высвобождения нейтрофильных внеклеточных ловушек в венозном кровотоке. Лимфопения (менее 500 клеток в 1 мкл) указывает на повышение риска тяжелой формы заболевания и смертельных исходов при COVID‑19 в 3 раза. Стойкий нейтрофилез со сдвигом влево свидетельствует об истощении костномозгового резерва, а при сдвиге вправо отражает нарушения выхода клеток в ткани. Этот легко контролируемый анализом крови параметр указывает на более чем семикратное увеличение для пациента риска заболеть тяжело и погибнуть от COVID‑19.
Попытки выявить закономерности иммунного ответа на SARS-CoV‑2 оказались пока безуспешными.
Во-первых, можно сделать вывод, что переболевшие коронавирусной инфекцией сохраняют иммунную память в последующие 6–9 месяцев. Дальнейшие динамические исследования покажут, в какие сроки наступает снижение иммунного ответа, требующее профилактической вакцинации и (или) ревакцинации.
Во-вторых, и это очень интересно, каждый изученный компонент иммунного ответа и иммунной памяти демонстрирует различную кинетику. Это связано с индивидуальным ответом на инфекцию, наличием преморбида и частого превращения моноинфекции в смешанные инфекции SARS-CoV‑2 с активизировавшейся микробиотой больного.
В-третьих, неоднородность ответа может быть центральным признаком, характеризующим иммунную память к SARSCoV‑2. Биологические специфические IgG имеют 21 день периода полураспада, уровень антител с течением времени отражает продукцию короткоживущих, а потом и долгоживущих плазматических клеток. С точки зрения исчезновения возбудителя в течение нескольких дней после появления клиники, процесс наработки антител должен быть снижен к 6 месяцам, но, если SARS-CoV‑2 Spike и RBD IgG сохраняются дольше 8 месяцев, это означает, что вирус персистирует в организме хозяина или его микробиоте. Нельзя исключать и связь с пролонгированным иммунным ответом естественной реиммунизации циркулирующими эпидемическими альфа-коронавирусами, поддерживающими иммунный ответ.
В-четвертых, выявление и анализ SARSCoV‑2‑специфических В-клеток памяти потенциально могут применяться в качестве маркера гуморального ответа при вакцинации. Сейчас исследования поствакцинального иммунного ответа проводятся с использованием иммунофлуоресцентного анализа с оценкой IgM- и IgG-антител в качестве маркеров эффективности вакцины (рис. 3). Методы ИФА-диагностики, к сожалению, не стандартизованы едиными белками S, RBD, NCP, качество которых зависит от очистки антигена. Поскольку количество В-клеток памяти стабильно с течением времени, они могут представлять собой более надежный маркер продолжительности гуморальных иммунных реакций, чем иммуноглобулины сыворотки крови.
Таким образом, из результатов исследований иммунного ответа у больных COVID‑19 невозможно сделать какие-либо выводы о защитном иммунитете при новой коронавирусной инфекции. Ведь изучение антител и клеток памяти при этом заболевании пока еще не завершено. А значит, обсуждаемые механизмы защитного иммунитета против SARS-CoV‑2 у людей окончательно не определены.
Источник: Газета «Педиатрия сегодня» №6, 2021