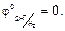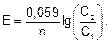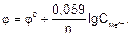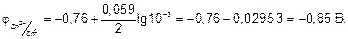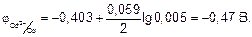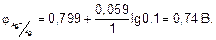что такое потенциал металла
Что такое электродный потенциал
Явления растворения металлов в электролитах используются в химических источниках электроэнергии. Металлическая пластина, опушенная в раствор своей же соли, в той или иной мере стремится в ней раствориться. Это стремление иногда называется упругостью растворения металла.
Эти заряды будут противодействовать дальнейшему переходу металла в раствор — отрицательные пластины удерживают положительный ион металла, а положительный заряд электролита отталкивает ион металла назад на пластину. Иными словами, электрическое поле двойного слоя на границе металл — жидкость противодействует дальнейшему переходу ионов металла в раствор. Устанавливается равновесие между химическими по своей природе силами стремления металла перейти в раствор и электрическими силами, им противодействующими.
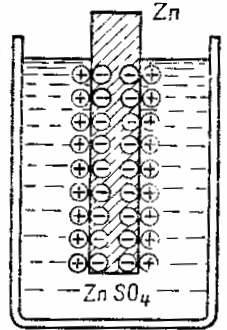
Схема образования двойного электрического слоя на границе металла и электролита
Таким образом, вследствие растворения в электролите металлический электрод приобретает по отношению к электролиту определенный электродный (иначе электрохимический) потенциал, зависящий от материала электрода и состава электролита.
Однако электродные потенциалы могут иметь положительное значение. Это имеет место в тех случаях, когда положительные ионы раствора переходят на электрод, заряжая его положительно, а слой электролита — отрицательно, например, когда медная пластина погружена в достаточно концентрированный раствор сернокислой меди (CuSO4).
Двойной электрический слой можно уподобить конденсатору, одна из обкладок которого представляет собой поверхность металла, а другая — слой ионов в растворе у поверхности металла. Между разноименно заряженными обкладками и возникает разность, или скачок, потенциала.
Скачок потенциала на границе электрод-раствор может служить мерой окислительно-восстановительной способности системы. Однако невозможно произвести измерение такого скачка потенциала или, что то же, разности потенциалов между двумя фазами. Но можно произвести измерение э. д. с. элементов, составленных из интересующих нас электродов и какого-нибудь одного (одинакового во всех случаях) электрода, потенциал которого условно принят за нуль.
Измеренная э. д. с. будет характеризовать окислительно-восстановительную способность интересующего нас электрода относительно некоторого условного нуля. Полученная таким способом величина называется собственным потенциалом металла.
Чтобы измерить электродный потенциал любого металла, необходимо поместить в электролит второй электрод, который и свою очередь будет обладать определенным электродным потенциалом, зависящим от его материала. Следовательно, непосредственно измерить можно только алгебраическую сумму двух электродных потенциалов.
По этой причине электродные потенциалы различных материалов определяются по отношению к стандартному (водородному электроду, потенциал которого условно принимают за нуль.
Для измерения могут применяться и другие электроды сравнения, потенциал которых относительно водородного стандартного электрода известен. Этот потенциал также находят на основании измерения э. д. с. цепи, составленной из выбранного электрода сравнения и стандартного водородного электрода.
Если в соответствующий электролит помещены две пластины из металлов, имеющих различный электродный потенциал, например, в раствор серной кислоты (H2SO4) помещены цинковая (Zn) и медная (С u ) пластины, то вольтметр, присоединенный к этим пластинам, покажет между ними напряжение немного более 1 В.
Это напряжение, называемое в данном случае э. д. с. гальванической пары, будет обусловлено разностью электродных потенциалов меди, обладающей небольшим положительным потенциалам, и цинка, обладающего значительным отрицательным потенциалом. Такое устройство является простейшим гальваническим элементом — элементом Вольта.
В гальваническом элементе происходит превращение химической энергии в электрическую и с его помощью можно совершить электрическую работу за счет энергии химической реакции.
Измерение э. д. с. гальванических элементов необходимо производить при отсутствии тока в цепи элемента. В противном случае измеренная э. д. с. будет меньше, чем величина, определяемая как разность равновесных потенциалов обоих электродов. Действительно, равновесному потенциалу отвечает определенная концентрация электронов на электродах: на более положительном она ниже, на более отрицательном выше. Сообразно с этим различно и строение той части двойного слоя, которая расположена в растворе.
Измерение э. д. с. элемента без протекания тока обычно производится компенсационным методом. Для осуществления его необходимо иметь некоторый эталон э. д. с. Таким эталоном служит так называемый нормальный элемент. Чаще всего пользуются ртутно-кадмиевым нормальным элементом Вестона, э. д. с. которого равна 1,01830 В при 20 °С.
Если Вам понравилась эта статья, поделитесь ссылкой на неё в социальных сетях. Это сильно поможет развитию нашего сайта!
Подписывайтесь на наш канал в Telegram!
Просто пройдите по ссылке и подключитесь к каналу.
Не пропустите обновления, подпишитесь на наши соцсети:
Электродные потенциалы металлов
Существует несколько теорий, объясняющих возникновение тока в гальванических элементах. Наиболее простая из них была выдвинута Нернстом (1888 г.) и позднее подробно развита академиком Л. В. Писаржевским на основе представлений о строении металлов из поло жительно заряженных ионов и свободных электронов.
Лев Владимирович Писаржевский родился в 1874 г.в. г. Кишиневе. Окончив естественный факультет Новороссийского университета (г. Одесса), Писаржевский был оставлен при нем для подготовки к прафессорскому званию. В 1902 г. он защитил магистерскую диссертацию, а в/1913 г. был избран профессором Екатеринославского горного института (г. Днепропетровск). С 1930 г. Писаржевский был действительным членом Академии наук СССР.
Крупный ученый и блестящий педагог, Писаржевский смело использовал достижения физики для изучения и объяснения химических процессов. Важнейшие его работы посвящены исследованию перекисей и надкислот, разработке теории растворов, приложению электронной теории к химии и разработке теории возникновения тока в гальванических элементах.
Возникновение тока в гальваническом элементе происходит следующим образом. Если погрузить любой металл в воду, то ионы его начинают переходить в раствор под влиянием притяжения, испытываемого ими со стороны полярных молекул воды. Вследствие этого металл, в котором остается избыток электронов, заряжается отрицательно, а раствор — положительно. Однако число ионов, которое металл посылает в раствор, как показывает опыт, очень мало. Возникающий на металле по мере ухода ионов отрицательный заряд начинает притягивать обратно ушедшие из металла ионы, так что вскоре наступает состояние равновесия, при котором в единицу времени столько же ионов уходит из металла, сколько и возвращается в него:
металл⇄ионы металла
Перешедшие в раствор ионы не распределяются равномерно по всей массе раствора, а вследствие притяжения к отрицательно заряженному металлу располагаются близ его поверхности, образуя так называемый двойной электрический слой (рис. 127). В результате между металлом и раствором устанавливается определенная разность потенциалов.

Предположим теперь, что мы прибавили к воде, в которую погружен металл, некоторое количество соли того же металла. Вследствие увеличения концентрации ионов металла в растворе равновесие между ними и металлом нарушится и часть ионов перейдет обратно в металл. Следовательно, в раствор своей соли
металл должен посылать меньше ионов, чем в чистую воду, и тем меньше, чем больше концентрация ионов в растворе. При достаточно большой концентрации соли ионы могут совсем не перейти из металла в раствор, так что ни металл, ни раствор не будут заряжены.
Наконец, если концентрация ионов металла в растворе достаточно велика, а активность металла сравнительно мала, то металл не только не посылает ионов в раствор, но, наоборот, часть ионов переходит из раствора в металл. При этом между металлом и раствором тоже возникает разность потенциалов, но теперь уже раствор заряжается отрицательно за счет избытка отрицательных ионов соли, а металл — положительно. Практически дело обстоит так, что одни металлы (более активные) всегда заряжаются в растворах своих солей отри-цательно, другие (менее активные) —положительно.
Следует заметить, что во всех случаях при погружении металла в раствор его соли количество переходящих в раствор или выделяющихся из раствора ионов настолько мало, что не может быть обнаружено химическим путем. Однако заряд их достаточно велик, чтобы создать поддающуюся измерению разность потенциалов.

В гальванических элементах тот электрод, который в процессе работы элемента разрушается, посылая ионы в раствор, называется анодом, а электрод, у которого разряжаются поло жительные ионы, называется катодом.
Гальванический элемент может быть построен из любых двух металлов, погруженных в растворы их солей. При этом совершенно не обязательно, чтобы один металл заряжался «отрицательно, а другой — положительно. Единственным условием для перетекания электронов от одного заряженного тела к другому является существование разности потенциалов между ними. Но последняя должна возникнуть, какие бы металлы мы ни взяли, так как способность отщеплять электроны и переходить в ионы у всех металлов различна. Если, например, составить гальванический элемент из цинка и железа, погруженных в нормальные растворы их солей, то, хотя оба металла заряжаются в растворах отрицательно, между ними все же возникнет некоторая разность потенциалов. При соединении металлов проводником электроны потекут от цинка, как металла более активного, к железу; цинк будет растворяться, а железо — выделяться из раствора. Происходящая в элементе реакция выразится уравнением
Разность потенциалов, возникающая между металлом и раствором его соли, называется электродным потенциалом металла и может служить мерой его способности отдавать электроны или, что то же самое, мерой его химической активности при реакциях в растворах. Поэтому, измерив потенциалы всех металлов при одинаковых концентрациях их ионов, мы могли бы количественно охарактеризовать активность металлов.
К сожалению, прямое измерение этих величин очень затруднительно и не дает точных результатов. Это ясно уже из того, что нельзя, например, присоединить вольтметр к раствору, не погрузив в раствор металлический проводник. Но тогда возникает разность потенциалов между проводником и раствором, так что напряжение, показываемое вольтметром, будет зависеть от двух разностей потенциалов: разности потенциалов между интересующим нас металлом и раствором его соли и разности потенциалов между металлическим проводником и тем же раствором.
Гораздо легче измерить разность потенциалов (разность напряжений электронов) между двумя различными металлическими электродами, погруженными в растворы соответствующих солей, т. е. узнать, насколько потенциал одного металла больше или меньше потенциала другого металла. Если измерить таким образом относительные потенциалы всех металлов, сравнивая их потенциалы с потенциалом какого-нибудь одного из них, то полученные числа будут так же точно характеризовать активность металлов, как и абсолютные величины их потенциалов.
В качестве стандартного электрода, с потенциалом которого сравнивают потенциалы других металлов, принят так называемый нормальный водородный электрод. Последний состоит из платиновой пластинки, покрытой рыхлым слоем платины и погруженной в двунормальный раствор серной кислоты. Через раствор непрерывно пропускают под давлением в 1 ат токчистого водорода, который, приходя в соприкосновение с платиной, в довольно большом количестве поглощается ею. Насыщенная водородом платиновая пластинка ведет себя так, как если бы она была сделана из водорода. При соприкосновении ее с раствором серной кислоты возникает определенная разность потенциалов (потенциал водородного электрода), условно принимаемая при измерениях относительных потенциалов за нуль.
Разность потенциалов между металлом, погруженным в раствор его соли, содержащий 1 грамм ион металла на литр, и нормальным водородным электродом называется нормальным потенциалом металла.
Для измерения нормальных потенциалов обычно пользуются приборами, подобными изображенному на рис. 128. По существу такой прибор представляет собой гальванический элемент, одним из электродов которого служит испытуемый металл, а другим — водородный электрод. Так как потенциал водородного электрода принимается за нуль, то, измерив разность потенциалов на полюсах такого элемента или его электродвижущую силу, мы непосредственно находим нормальный потенциал металла.
Если расположить металлы, включая и водород, по убывающей величине напряжения их электродов, т. е. по убывающим отрицательным нормальным потенциалам (и возрастающим положительным), то получится тот же самый ряд напряжений.
Нормальные потенциалы металлов
| Металл | Ион | Потенциал в вольтах | Металл | Ион | Потенциал в вольтах |
| К | К • | — 2,92 | Ni | Ni •• | — 0,23 |
| Са | Са •• | — 2,84 | Sn | Sn •• | — 0,14 |
| Na | Na • | — 2,713 | Pb | Pb •• | — 0,126 |
| Mg | Mg •• | — 2,38 | н2 | H • | 0,000 |
| Al | Аl ••• | — 1,66 | Сu | Сu •• | + 0,34 |
| Мn | Mn •• | — 1,05 | Hg | Hg2 •• | + 0,798 |
| Zn | Zn •• | — 0,763 | Ag | Ag • | + 0,799 |
| Fe | Fe •• | — 0,44 | Au | Au ••• | + 1,42 |
Зная нормальные потенциалы металлов, легко определить электродвижущую силу любого элемента, состоящего из двух металлов, погруженных в растворы их солей. Для этого нужно только найти разность нормальных потенциалов взятых металлов.
Чтобы величина электродвижущей силы имела положительное значение, всегда вычитают из большего потенциала меньший. Например, электродвижущая сила медно-цинкового элемента:
э. д. с. = 0,34 — (—0,763) = 1,103 вольта
Понятно, что такую величину она будет иметь, если концентрации ионов Zn •• и Сu •• в соответствующих растворах равны 1 граммиону на 1 литр. Для иных концентраций потенциалы металлов, а следовательно, и электродвижущие силы могут быть вычислены по формуле, выведенной Нернстом:
где Е — потенциал металла при данной концентрации ионов; Ео — нормальный потенциал металла; п — валентность ионов металла; с — концентрация ионов в растворе в граммионах на литр.
Так, например, потенциал цинка в 0,001 М растворе его соли будет равняться:
При устройстве гальванических элементов, помимо реакций вытеснения металлов металлами, нередко используются другие окислительно-восстановительные реакции, в которых могут принимать участие и металлоиды. Для некоторых металлоидов также определены их нормальные потенциалы, но ряд напряжений для металлоидов установлен далеко не так полно, как для металлов. В качестве иллюстрации приводим нормальные потенциалы галогенов:
Вы читаете, статья на тему Электродные потенциалы металлов
Похожие страницы:
Понравилась статья поделись ей
Что такое потенциал металла
В электрохимической ячейке (гальваническом элементе) электроны, остающиеся после образования ионов, удаляются через металлический провод и рекомбинируют с ионами другого вида. Т.е.заряд во внешней цепи переносится электронами, а внутри ячейки, через электролит, в который погружены металлические электроды, ионами. Таким образом получается замкнутая электрическая цепь.
Разность потенциалов, измеряемая в электрохимической ячейке, o бъясняется различием в способности каждого из металлов отдавать электроны. Каждый электрод имеет собственный потенциал, каждая система электрод-электролит представляет собой полуэлемент, а любые два полуэлемента образуют электрохимическую ячейку. Потенциал одного электрода называют потенциалом полуэлемента, он определят способность электрода отдавать электроны. Очевидно, что потенциал каждого полуэлемента не зависит от наличия другого полуэлемента и его потенциала. Потенциал полуэлемента определяется концентрацией ионов в электролите и температурой.
В качестве «нулевого» полуэлемента был выбран водород, т.е. считается, что для него при добавлении или удалении электрона с образованием иона никакой работы не совершается. «Нулевое» значение потенциала необходимо для понимания относительной способности каждого из двух полуэлементов ячейки отдавать и принимать электроны.
Потенциалы полуэлементов, измеряемые относительно водородного электрода, называются водородной шкалой. Если термодинамическая склонность отдавать электроны в одной половине электрохимической ячейки выше, чем в другой, то потенциал первою полуэлемента выше, чем потенциал второго. Под действием разности потенциалов будет происходить переток электронов. При сочетании двух металлов можно выяснить возникающую между ними разность потенциалов и направление потока электронов.
Электроположительный металл обладает более высокой способностью принимать электроны, поэтому он будет катодным или благородным. С другой стороны находятся электроотрицательные металлы, которые способны самопроизвольно отдавать электроны. Эти металлы являются реакционноспособными, а, следовательно, анодными:
Al Mn Zn Fe Sn Pb H 2 Cu Ag Au
2 Ag + + Cu → Cu 2+ + 2 Ag
Однако та же самая медь менее реакционноспособна, чем железо. При контакте металлического железа с нонами меди та будет осаждаться, а железо переходить в раствор:
Стандартным электродным потенциалом считается потенциал полуэлемента из полностью отожженого чистого металла в качестве электрода в контакте с ионами при 25 0 С. В этих измерениях водородный электрод выступает в роли электрода сравнения. В случае двухвалентного металла можно записать реакцию, протекающую в соответствующей электро-химической ячейке:
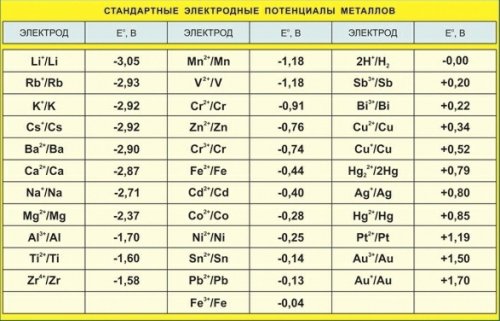
Если упорядочить металлы по убыванию их стандартных электродных потенциалов, то получается так называемый электрохимический ряд напряжений металлов (табл. 1).
Таблица 1. Электрохимический ряд напряжений металлов
Равновесие металл-ионы (единичной активности)
Электродный потенциал относительно водородного электрода при 25°С, В (восстановительный потенциал)
Электродный потенциал. Ряд напряжений. Гальванический элемент
Простейшая модель строения металла следующая: в узлах кристаллической решетки находятся положительные ионы металла, которые прочно связаны подвижными электронами. При погружении металлической пластины в водный раствор соли этого же металла положительные ионы, находящиеся на поверхности металла, гидратируются и переходят в раствор. В результате этого перехода в кристаллической решетке металла оказывается избыток электронов и пластина приобретает отрицательный заряд. Между отрицательно заряженной пластиной и положительными ионами в растворе возникает электростатическое притяжение, в результате которого раствор у поверхности пластины приобретает положительный заряд. Одновременно развивается противоположный процесс: ионы металла из раствора принимают электроны с поверхности пластины и образуют атомы металла, которые становятся частью кристаллической решетки.
Через промежуток времени между металлической пластиной и раствором устанавливается состояние равновесия, при котором скорость перехода ионов из металла в раствор равна скорости разряжения ионов из раствора на поверхности металла:
Me + mH2O « Men+•mH2O + n
Me « Men+ + n
Таким образом, при контакте металла с раствором его соли поверхности этих фаз приобретают противоположные заряды – образуется двойной электрический слой и возникает разность потенциалов.
Система, состоящая из металлического проводника и раствора электролита, в который погружен проводник, называется электродом, а разность потенциалов на границе металл-электролит – электродным потенциалом 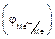
Электродный потенциал зависит от следующих основных факторов:
— концентрации ионов металла в растворе;
Зависимость величины потенциала от указанных факторов выражается уравнением Нернста:
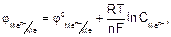
где 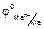
R – универсальная газовая постоянная, равная 8,31 Дж/(моль•К);
Т – абсолютная температура, К;
F – постоянная Фарадея, равная 96500 кл/моль;
n – число электронов, участвующих в электродном процессе;
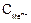
Если в уравнение (1) подставить значения постоянных R и F, стандартную температуру 298 К и перейти от натурального к десятичному логарифму, получим:
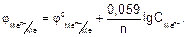
Из уравнения (2) следует, что стандартный потенциал j0 – это потенциал электрода при стандартных условиях: Т=298 К; 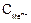
Измерить абсолютную величину электродного потенциала невозможно, поэтому потенциалы металлов выражают по отношению к стандартному водородному электроду (СВЭ), потенциал которого условно принимается равным нулю:
По отношению к потенциалу стандартного водородного электрода потенциалы различных металлов располагаются в ряд стандартных электродных потенциалов или ряд напряжений (приложение, табл.5).
Чем более отрицательное значение имеет потенциал металла, тем более сильной восстановительной способностью он обладает. И наоборот, чем более положителен потенциал электрода, тем большей окислительной способностью обладают его ионы.
Металлы, стоящие в ряду напряжений левее, вытесняют правее стоящие из растворов их солей.
Металлы, расположенные в ряду напряжений до водорода, вытесняют его из некоторых кислот.
Процессы, протекающие на границе металл-раствор, лежат в основе работы гальванического элемента – устройства для превращения энергии химической окислительно-восстановительной реакции в электрическую.
Гальванический элемент представляет собой электрохимическую систему, состоящую из двух металлических пластин, погруженных в растворы солей собственных ионов. Растворы соединяются солевым мостиком – стеклянной трубкой, заполненной электролитом KCl. Солевой мостик препятствует смешиванию растворов и проводит электрический ток.
Рассмотрим гальванический элемент Даниэля-Якоби, состоящий из медной и цинковой пластин, погруженных в растворы солей CuSO4 и ZnSO4, соответственно. Пока цепь разомкнута, на каждой из пластин устанавливается равновесие:
Zn0 « Zn2+ + 2
Cu0 « Cu2+ + 2
Потенциал цинкового электрода имеет более отрицательное значение, чем потенциал медного электрода, поэтому при замыкании внешней цепи, т.е. при соединении электродов металлическим проводником, избыточные электроны будут перемещаться с цинкового электрода на медный. В результате перехода электронов равновесие на цинковой пластине сместится вправо и в раствор перейдут новые количества ионов цинка. В то же время равновесие на медной пластине сместится влево и на поверхности пластины произойдет разряд ионов меди.
Таким образом, при замыкании цепи возникают самопроизвольные процессы растворения цинка на цинковом электроде и осаждение меди на медном электроде.
Движение анионов (SO42–) через солевой мостик замыкает электрическую цепь гальванического элемента.
В гальваническом элементе электрод, на котором идут процессы окисления, называют анодом, ему присваивают отрицательный заряд (–). Электрод, на поверхности которого идут процессы восстановления катионов металла из раствора, называют катодом и ему присваивают положительный заряд (+).
Гальванический элемент принято изображать в виде схемы:
Анодный процесс: А(–): Zn0 — 2 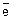
Катодный процесс: К(+): Cu2+ + 2 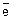
токообразующая Zn0 + Cu2+ = Zn2+ + Cu0
реакция: Zn + CuSO4 = ZnSO4 + Cu
Главной характеристикой гальванического элемента является электродвижущая сила (э.д.с.) Е, равная разности электродных потенциалов катода и анода:
Если э.д.с. измеряют при стандартных условиях, то ее рассчитывают по стандартным электродным потенциалам. Так, для гальванического элемента Даниэля-Якоби
E0 = j0Cu — j0Zn = 0,34 –(-0,76) = 1,1 В
Если условия отличны от стандартных, то величины электродных потенциалов рассчитывают по уравнениям Нернста.
Гальванический элемент из двух электродов, изготовленных из одного металла, но погруженных в растворы солей этого металла с различной концентрацией называют концентрационным.
Анодом в таком элементе будет пластина в растворе с меньшей концентрацией (С1), катодом – пластина в растворе с более высокой концентрацией (С2). Электродвижущую силу такого элемента рассчитывают по формуле:
Таким образом, концентрация первого раствора С1 будет постепенно увеличиваться, а второго раствора С2 – уменьшаться. Через некоторое время концентрации С1 и С2 станут одинаковыми, а э.д.с. – равной нулю.
Пример 1. Определите электродный потенциал цинка, опущенного в раствор его соли с концентрацией ионов Zn2+ 0,001 моль/л.
Решение. Зависимость электродного потенциала металла от концентрации его ионов выражается уравнением Нернста
Пример 2. Составьте схему, анодный и катодный процессы и вычислите э.д.с. гальванического элемента, образованного серебряной и кадмиевой пластинами, погруженными в растворы с концентрацией ионов 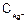
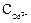
Кадмиевый электрод имеет меньшее значение потенциала, чем серебряный, поэтому он будет анодом. Электродные процессы:
А(–): Cd0 — 2 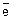
К(+): Ag+ + 1 
реакция Cd0 + 2Ag+ = Cd2+ + 2Ag0
Чтобы определить э.д.с. гальванического элемента, нужно рассчитать потенциалы электродов при данных концентрациях ионов:
Пример 3. Рассчитайте э.д.с. концентрационного гальванического элемента, если железные пластины погружены в раствор соли хлорида железа (III) с концентрацией ионов Fe3+: С1=0,01 моль/л, С2=0,1 моль/л.
Решение. Электродвижущую силу концентрационного гальванического элемента можно рассчитать по формуле