что такое несостоятельность анастомоза
Что такое несостоятельность анастомоза
НИИ онкологии им. Н.Н. Петрова Минздравсоцразвития России; Военно-медицинская академия им. С.М. Кирова, Санкт-Петербург
ФГБУ «НИИ онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург, Россия
ГБОУ ВПО «Первый Санкт-Петербургский медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия
Влияние несостоятельности швов анастомозов на отдаленные результаты лечения больных колоректальным раком
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2018;(8): 42-46
Карачун А. М., Петров А. С., Панайотти Л. Л., Олькина А. Ю. Влияние несостоятельности швов анастомозов на отдаленные результаты лечения больных колоректальным раком. Хирургия. Журнал им. Н.И. Пирогова. 2018;(8):42-46.
Karachun A M, Petrov A S, Panayotti L L, Ol’kina A Yu. Influence of anastomotic leakage on the long-term outcomes in patients with colorectal cancer. Khirurgiya. 2018;(8):42-46.
https://doi.org/10.17116/hirurgia201808242
НИИ онкологии им. Н.Н. Петрова Минздравсоцразвития России; Военно-медицинская академия им. С.М. Кирова, Санкт-Петербург
Несостоятельность швов анастомоза после хирургических вмешательств по поводу колоректального рака — широко известный фактор, который ухудшает непосредственные результаты лечения. При этом ухудшению онкологических результатов лечения уделяется значительно меньше внимания. В настоящем обзоре представлены данные литературы об отдаленных последствиях несостоятельности швов анастомоза, а также предложена гипотеза о механизме реализации негативного эффекта этого осложнения на отдаленные результаты
НИИ онкологии им. Н.Н. Петрова Минздравсоцразвития России; Военно-медицинская академия им. С.М. Кирова, Санкт-Петербург
ФГБУ «НИИ онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург, Россия
ГБОУ ВПО «Первый Санкт-Петербургский медицинский университет им. акад. И.П. Павлова» Минздрава России, Санкт-Петербург, Россия
Несостоятельность швов анастомоза является грозным осложнением и основной проблемой хирургии колоректального рака. Большое внимание уделяется непосредственным последствиям этого осложнения, сопряженного с увеличением внутрибольничной летальности, сроков госпитализации и стоимости лечения таких пациентов, в то время как данных об отдаленных результатах после развития несостоятельности анастомоза представлено гораздо меньше.
Несостоятельность швов анастомоза может приводить к ухудшению качества жизни пациентов даже в отдаленном периоде. При анализе результатов лечения 614 пациентов из CLASSIC trial выявлено отрицательное влияние развития послеоперационных осложнений на отдаленные параметры качества жизни, в особенности физическое и социальное функционирование, образ тела, мобильность, возможность ухода за собой, боль и дискомфорт [1].
Значимый вклад в ухудшение качества жизни вносит перманентный характер стомы вследствие несостоятельности швов анастомоза. Риск формирования постоянной стомы у 297 пациентов, перенесших низкие передние резекции прямой кишки, составил 11% через 1 год и 22% через 10 лет. При анализе установлено, что хирургические осложнения в 3 раза увеличивали риск перманентной стомы [2].
При изучении результатов 341 интерсфинктерной резекции у больных раком нижнеампулярного отдела прямой кишки отмечено, что вероятность закрытия временной стомы уменьшалась в случае несостоятельности швов анастомоза до 78,6% по сравнению с 88,7% в группе контроля. При полной диссоциации анастомоза вероятность закрытия стомы составляла лишь 61,5%. Стриктура анастомоза, встречающаяся в 1,8% случаев при неосложненном течении послеоперационного периода, наблюдалась у 16,7% пациентов с несостоятельностью швов и у 38,5% больных с полной диссоциацией анастомоза. Обращало внимание то, что функция удержания через 2 года была схожей в группе контроля и группе больных с несостоятельностью швов анастомоза, в то время как после полной диссоциации анастомоза даже через 2 года запирательная функция была хуже [3].
Проанализировав результаты лечения 864 пациентов после резекций прямой кишки, J. Ashburn и соавт. [4] пришли к выводу, что несостоятельность швов анастомоза приводит к ранним нежелательным последствиям для функции кишки и качества жизни даже в случае, если анастомоз не был разобщен.
Отрицательное влияние несостоятельности швов анастомоза на качество жизни пациентов практически не вызывает сомнений. Взаимосвязь развития этого послеоперационного осложнения с отдаленными онкологическими результатами не столь однозначна. Имеются данные об отсутствии влияния развития несостоятельности швов анастомоза на онкологические результаты. Так, при анализе отдаленных результатов лечения 584 пациентов после резекции прямой кишки не выявлено связи несостоятельности швов анастомоза и опухолеспецифической выживаемости за 10 лет наблюдения [5]. При анализе результатов лечения 3623 пациентов из регистра PROCARE абдоминальная или тазовая инфекция не приводила к изменению общей выживаемости, встречаемости метастазов или местных рецидивов [6]. Не выявлено изменения частоты рецидивов и общей выживаемости при несостоятельности швов анастомоза после резекций прямой кишки, если проводилась предоперационная химиолучевая терапия [7].
Существуют и противоположные данные об ассоциации несостоятельности швов анастомоза с худшими отдаленными результатами лечения. Первое сообщение о связи несостоятельности швов анастомоза и отдаленных результатов было опубликовано в 1991 г. После 25 мес наблюдения за 135 пациентами без несостоятельности швов анастомоза и 25 пациентами с наличием этого осложнения рецидив у последних выявлен в 46,9% случаев (против 18,5% в группе сравнения; p 10 мг/л и 77% — в группе Dukes C, СРБ 10 мг/л. Таким образом, повышение уровня маркера воспаления ассоциировано с худшей выживаемостью. При изучении группы пациентов с несостоятельностью швов анастомозов выявлено негативное влияние уровня нейтрофилов менее 80% (HR 2,6) и комплексного показателя, получаемого математически из уровня альбумина и лимфоцитов (HR 3,5) на безрецидивную выживаемость [33].
Таким образом, влияние системного воспаления на отдаленные онкологические результаты путем потенцирования опухолевого роста представляется убедительно доказанным. Тем не менее остается не вполне объяснимой причина наличия опухолевых клеток после радикальных резекций с морфологически негативными границами. Кроме того, установлена выраженная связь раневых инфекций и системных рецидивов (HR 2,87) при раке молочной железы, когда такие данные не могут быть объяснены попаданием клеток из просвета органа [34].
Попробуем разобрать этот вопрос более подробно. Имеются данные, подтверждающие наличие клеток в просвете кишки даже после удаления пораженного опухолью участка. Так, при первом промывании культи прямой кишки после удаления препарата 50 мл раствора антисептика наличие опухолевых клеток в смывах установлено у 11 из 14 пациентов, после 10-го промывания опухолевые клетки сохранялись в смывах 4 из 14 пациентов [35]. При исследовании циркулярных краев резекции прямой кишки, остающихся в препарате («бубликов»), в 9 из 10 случаев у пациентов с гистологически негативными границами резекции опухолевые клетки обнаружены при цитологическои исследовании [36].
Опухолевые клетки также могут выделяться из крови пациентов. Имеются данные о наличии циркулирующих опухолевых клеток у 10% больных с Dukes A/B и у 54% пациентов с Dukes С через 12 нед после радикальной операции [37]. В метаанализе [38] показано, что при использовании полимеразной цепной реакции циркулирующие опухолевые клетки могут быть выявлены у 21—71% пациентов с неметастатическим колоректальным раком. Эффективность адъювантной химиотерапии при колоректальном раке даже II стадии после радикальных резекций подразумевает наличие точки приложения для лечения, т. е. наличие опухолевых клеток в органах-мишенях, на которые и нацелено действие адъювантной химиотерапии [39].
Имеющиеся данные свидетельствуют о наличии опухолевых клеток после радикальных резекций в просвете кишки, крае резекции, крови и органах-мишенях. Обеспечением негативных хирургических краев резекции далеко не всегда удается добиться удаления всех опухолевых клеток. Иными словами, с биологической точки зрения R0-резекции хирургическим способом реализовать не удается в большинстве случаев.
Умозрительно возможно предположить наличие некоторого равновесия между остающимися опухолевыми клетками и иммунной системой, которое клинически проявляется как ремиссия. При этом проведение химиотерапии или эффективный противоопухолевый иммунитет способствуют сохранению ремиссии, в то время как иные системные факторы могут сдвигать равновесие не в пользу иммунной системы. Весьма вероятно, что в числе таких факторов присутствует и несостоятельность швов кишечного анастомоза.
Исходя из сказанного, можно объяснить наличие рецидивов после радикальных хирургических вмешательств. Опираясь на данные о наличии опухолевых клеток после радикального лечения и сведения о стимулирующем действии на опухоль провоспалительных цитокинов, можно сформулировать патогенетическую последовательность влияния несостоятельности швов анастомоза на равновесие между опухолевыми клетками и иммунной системой. По-видимому, оно реализуется посредством повышения уровня активности провоспалительных цитокинов, стимулирующих пролиферацию опухолевых клеток.
При таком подходе меняется взгляд на роль хирургического вмешательства в лечении колоректального рака. Задача хирурга в свете подобной концепции состоит не только в том, чтобы любой ценой добиться негативных хирургических краев резекции, но и в том, чтобы, обеспечив «радикализм» вмешательства, способствовать сохранению равновесия между опухолевыми клетками и иммунной системой, в том числе путем снижения числа септических осложнений.
Наше предположение является теоретическим и не может быть подкреплено доказательными данными, так как невозможно организовать и провести исследования, в которых необходимо рандомизировать пациентов на тех, кто будет иметь несостоятельность швов анастомоза, и тех, у кого послеоперационый период будет протекать без осложнений, тех, кому нарочито будет нанесена большая травма, и тех, кому хирургическое вмешательство будет выполняться максимально прецизионно.
Тем не менее у нас есть возможность взглянуть по-новому на результаты уже имеющихся хорошо известных рандомизированных многоцентровых исследований, сравнивающих, по сути, операции с нанесением пациентам травмы разной степени — открытые и лапароскопические вмешательства. В исследовании CLASSIC при изучении результатов резекций прямой кишки получены очень высокие показатели положительного циркулярного края резекции не в пользу лапароскопических вмешательств — 12% в группе с лапароскопическим доступом против 6% в группе с открытым доступом (p>0,05). Несмотря на недостоверность различий, полученные результаты вызвали озабоченность среди хирургов и исследователей лапароскопического доступа при лечении рака прямой кишки [40]. Однако при анализе отдаленных результатов этого исследования через 10 лет медиана выживаемости составила 82,7 мес в группе с лапароскопическим доступом и 65,8 мес в группе открытой хирургии. Данные различия имели тренд к статистической достоверности [41].
При сопоставлении непосредственных и отдаленных результатов лучшая медиана выживаемости выявлена в группе, где наблюдалась меньшая частота негативных хирургических границ и при этом выполнялся менее инвазивный доступ. Одним из теоретических объяснений данных различий может стать именно представление об отсутствии биологических границ опухоли и наличии равновесия между опухолью и иммунной системой на клеточном уровне. Меньшая травматичность доступа, возможно, реализует свой положительный эффект на отдаленные результаты благодаря сохранению этого равновесия и продлению клинической ремиссии.
Таким образом, несостоятельность швов анастомоза не только негативно влияет на непосредственные результаты лечения, но и является важным фактором, ухудшающим качество жизни и онкологические отдаленные результаты. При этом дальнейшее изучение механизма реализации негативного эффекта несостоятельности швов анастомоза может привести к значительному изменению взгляда на требования к хирургической операции как к этапу лечения пациентов с колоректальным раком.
Авторы заявляют об отсутствии конфликта интересов.
Что такое несостоятельность анастомоза
Тщательное консервативное ведение больного при несостоятельности анастомоза, если отсутствуют дистальная обструкция кишки и нарушения кишечного пассажа, более чем в половине случаев обусловливает самостоятельное закрытие послеоперационных тонкокишечных свищей. Не закрывшиеся в течение 6 нед свищи требуют планового оперативного лечения. Эти вмешательства, произведенные при компенсированном SIRS, отсутствии сопутствующего перитонита и под прикрытием анаболиков, восстанавливают целостность ЖКТ с минимальным количеством осложнений. Неблагоприятные исходы встречаются лишь в случаях, когда несостоятельность и свищи решают вести консервативно при наличии перитонита и сепсиса: явный перитонит служит прямым показанием к немедленной операции.
Даже если нет явной клиники перитонита, при четких проявлениях SIRS или сепсиса следует предпринять энергичные усилия для поиска внутрибрюшного скопления гноя и дренирования. Лучше всего это сделать с помощью КТ: абсцесс должен быть дренирован либо путем чрескожного пункционного дренирования (ЧПД), либо с использованием прямого лапаротомного доступа.
Запомните: около трети больных с наружными кишечными свищами погибают, причем преобладающее большинство из них — вследствие внутрибрюшных инфекционных осложнений.
Роль оперативного лечения несостоятельности кишечного анастомоза
Как уже отмечалось, перитонит или сформированный внутрибрюшной абсцесс, не поддающийся ЧПД, служит показанием для лапаротомии.
Но почему бы не оперировать всех таких больных? Как велико искушение поддаться засевшей в вашем мозгу мысли: «Я знаю, откуда происходит утечка кишечного содержимого; если повторно войти в живот, можно несколькими швами решить эту проблему».
Что должно удержать вас от повторного ушивания несостоятельного анастомоза или непредвиденно возникшего кишечного свища?
Повторное ушивание несостоятельного анастомоза обречено на неудачу
Каждый из нас знаком с отдельными успешными случаями повторного ушивания несостоятельных анастомозов, но общий коллективный опыт изобилует рецидивами расхождения швов. Попытки зашить кишечный свищ через несколько дней после его возникновения оказываются тщетными, как и наложение нового анастомоза в условиях послеоперационного перитонита.
Настоящим героем является хирург, который спасает пациента от продолжительной госпитализации и осложнений. Если все же несостоятельность возникает повторно, как это обычно и бывает, она представляет собой тот ужасный «второй удар», которой способен окончательно «добить» уже ослабленного пациента. «Септическая смерть» в этом случае почти неизбежна.
Что такое несостоятельность анастомоза
Прошла неделя после экстренной гемиколэктомии по поводу обтурирующей карциномы слепой кишки у вашей пациентки. Она уже находится дома, чувствует себя неплохо и самостоятельно ест, но вдруг у нее вновь возникает приступ болей в правой половине живота, сопровождающийся рвотой.
Пациентку снова доставляют в приемное отделение. У нее лихорадка, в правой половине живота пальпируется болезненный инфильтрат, на обзорной рентгенограмме брюшной полости — картина, заставляющая заподозрить кишечную непроходимость. Лейкоцитоз повышен. Вы подозреваете несостоятельность анастомоза.
С клинической точки зрения, существуют 3 типа несостоятельности кишечного шва, которые можно идентифицировать.
• Свободная утечка. Анастомоз негерметичен, а утечка не отграничена прилежащими структурами. Состояние пациента обычно ухудшается, появляются симптомы диффузного перитонита. Показана экстренная релапаротомия, как уже указывалось выше.
• Отграниченная утечка. В этом случае вытекающее кишечное содержимое частично отграничивается сальником и прилежащими органами. Клинически симптомы раздражения брюшины локализованы. Последствием этого является формирование околокишечного абсцесса.
• Мини-утечка. Подобное незначительное проникновение кишечного содержимого возникает в поздние сроки после операции, когда анастомоз уже в основном сформирован. Абдоминальные симптомы строго локализованы, и у пациента нет каких-либо проявлений интоксикации. Это действительно перианастомозит — воспалительная инфильтрация вокруг анастомоза. Обычно при этом не происходит формирования какого-либо гнойника.
При отсутствии диффузного перитонита вы должны документировать несостоятельность анастомоза и определить лечебную тактику. Толстокишечый анастомоз лучше всего визуализировать с помощью контрастной клизмы с гастрогра-фином. А для исследования анастомозов верхних отделов ЖКТ гастрографин необходимо давать перорально. Мы обычно сочетаем подобные контрастные исследования с КТ, пытаясь выявить проникновение контрастного вещества в свободную брюшную полость либо зафиксировать формирование гнойника в зоне анастомоза.
При этом также возможно несколько вариантов:
• Свободное проникновение контрастного вещества в брюшную полость; большое его количество и жидкость в животе на КТ. Больного необходимо срочно оперировать. Предварительно мы обсудили, что делать во время операции, — лучше всего резецировать участок кишки с анастомозом.
• Отграниченное скопление контрастного препарата — абсцесс на КТ. Остальные отделы брюшной полости интактны.
• Утечки контрастного вещества не отмечено, выявлена лишь перианастомотическая инфильтрация. Такой перианастомозит обычно разрешается после нескольких дней лечения антибиотиками.
Учтите, что заметная локальная утечка контрастного вещества или его мини-утечка связаны с обструкцией анастомоза воспалительным отеком. Такая обструкция обычно разрешается самостоятельно — примерно за 1 нед, после дренирования гноя и уменьшения отека.
Мы показали вам, что несостоятельность анастомоза не является «одной болезнью». Это спектр состояний, требующих дифференцированного подхода. Чтобы не допускать осложнений, соотносите проводимое лечение с конкретными условиями несостоятельности анастомоза, величиной дефекта и состоянием пациента. Но прежде всего помните, что недренированные скопления в брюшной полости кишечного содержимого или гноя — это убийцы, часто «молчаливые».
Мы склонны лучше помнить тех больных, которых едва не погубили; и мы никогда не забываем тех из них, которых мы действительно довели до гибели.
Хирургическая тактика при несостоятельности пищеводных анастомозов и повреждениях пищевода, осложненных медиастинитом и эмпиемой плевры
Периоперационный период является достаточно непродолжительным, но наиболее ответственным отрезком времени, часто предопределяющим исход оперативного вмешательства. Ошибки здесь недопустимы, а любое решение анестезиолога должно быть взвешенным и обдуманным. Еще в середине 90-х годов XX века анестезиолог-реаниматолог из Дании профессор H. Kehlet заинтересовался патофизиологической природой механизмов осложнений после плановых хирургических вмешательств. В результате проведенного им системного анализа был предложен многокомпонентный комплекс мер, направленных на снижение стрессовой реакции организма на хирургическую агрессию. Нивелирование последствий хирургического стресса стало основанием концепции, получившей название Fast-Track Surgery (быстрый путь в хирургии). В последние годы благодаря общему признанию принципа доказательности подходы к периоперационному ведению пациентов претерпели существенных изменений, позволив снизить частоту и тяжесть послеоперационных осложнений, а соответственно и летальность. О современных аспектах периоперационных мероприятий мы попросили рассказать известных отечественных специалистов в области анестезиологии и интенсивной терапии.
Оперативные вмешательства на органах верхних отделов желудочно-кишечного тракта являются серьезными и тяжелыми ввиду высокого риска развития послеоперационных осложнений, несмотря на большой арсенал современного фармакологического, анестезиологического и хирургического обеспечения.
Развитие несостоятельности швов пищеводно-желудочного анастомоза встречается в 0,5-33% наблюдений. При интраторакальном наложении пищеводно-желудочного анастомоза несостоятельность его влечет за собой развитие таких угрожающих жизни осложнений, как плеврит, эмпиемы плевры, медиастинит, которые, по данным различных авторов, приводят к смерти от 25 до 71% больных. Несостоятельность пищеводно-кишечного анастомоза развивается у 5,9-12% пациентов, перенесших гастрэктомию, и сопровождается высокой летальностью, которая приближается к 100%. При этом основной причиной смерти является развитие гнойно-септических осложнений, возникающих вследствие пенетрации инфекции в участвующие в формировании анастомоза ткани, а затем в окружающие анастомоз ткани и серозные полости. Следует отметить, что в ряде случаев приходится выполнять вынужденную гастрэктомию у больных с перитонитом, развивающимся на фоне перфораций опухолей желудка, что встречается более чем у 14% больных раком желудка.
Причинами развития этих тяжелых осложнений могут служить краевой или более обширный некроз культи пищевода или желудочного трансплантата при эзофагогастропластике вследствие нарушения кровообращения либо из-за плохой репарации тканей. Одной из наиболее веских предпосылок к развитию несостоятельности пищеводных анастомозов являются нарушения нутритивного статуса пациентов, которые нуждаются в проведении операций на верхних отделах желудочно-кишечного тракта. Не следует забывать и о роли технических погрешностей: несопоставление слизистых оболочек, очень частые швы и чрезмерное тугое завязывание узлов, прокалывание иглой слизистых оболочек при формировании второго ряда швов, натяжение сшиваемых органов и др.
Нами проведен анализ результатов лечения больных с несостоятельностью пищеводных анастомозов и перфораций пищевода, осложненных развитием медиастинита и эмпиемы плевры, в период с 1995 по 2015 г. За анализируемый период наши взгляды на данную проблему претерпели кардинальные изменения.
Нами применялись два принципиально отличающихся направления лечения несостоятельности швов внутригрудных пищеводных анастомозов: консервативный и активный хирургический.
С 1995 по 2010 г. мы придерживались нижеприведенной тактики консервативного лечения при частичной несостоятельности швов анастомоза. Она заключалась в следующем: пациенту проводили назогастральный зонд дистальнее анастомоза, перорально назначали антисептические растворы, антибиотики, растительные масла. Установленный зонд использовался для кормления больного. Недостатками описанного способа лечения мы считаем длительность и малоэффективность лечения при развитии гнойных осложнений, так как в раннем послеоперационном периоде отмечается преобладание процессов катаболизма и отрицательного азотистого баланса, с одной стороны, и постоянное поддержание гнойного воспаления плевры микрофлорой желудочно-кишечного тракта.
Описанная методика в исследуемый период применена у 35 больных (52,2%). Летальность больных, которым применялась консервативная тактика, приближалась к 100%.
Второе направление подразумевало активную хирургическую тактику, которая применялась в случае развития полной несостоятельности анастомоза. После проведения интенсивной инфузионной предоперационной подготовки выполняли повторное хирургическое вмешательство – реконструкцию анастомоза или резекцию несостоятельного анастомоза с формированием нового.
К недостаткам такой тактики лечения мы относим трудности наложения повторного анастомоза в условиях инфицирования тканей, а также высокий уровень внутриплевральных гнойно-септических осложнений, что способствует развитию вторичных послеоперационных осложнений, в том числе несостоятельности швов анастомозов.
Такие вмешательства выполнялись у 32 больных (47,8%). Летальность при этом виде операций достигала 60% (умерли 19 пациентов), что сопоставимо с результатами крупных специализированных клиник с большим опытом пищеводной хирургии.
В данный период 3 пациентам (4,5%) с разрывами грудного отдела пищевода применена этапная тактика хирургического лечения, которая заключалась в следующем. На первом этапе выполняли лапаротомию, гастростомию, перевязку абдоминального отдела пищевода для исключения рефлюкса желудочного содержимого в просвет пищевода, дренировали плевральную полость и заднее средостение по Б.С. Розанову. После ликвидации проявлений эмпиемы плевры и медиастинита, а также компенсации состояния пациента, в том числе нутритивного статуса, выполняли второй этап лечения – лапаротомию, «снятие» лигатуры с абдоминального отдела пищевода, закрытие гастростомы. В одном случае снятие лигатуры было выполнено эндоскопическим путем через просвет пищевода. Умер один пациент при нарастании явлений интоксикации и полиорганной недостаточности.
В исследуемый период число развития послеоперационных осложнений составило 43,2%, летальность достигла 86,6%. Среди наиболее частых осложнений следует отметить развитие эмпиемы плевры, медиастинита, продолжающийся перитонит, которые послужили основными причинами смерти.
С 2010 г. до настоящего времени мы придерживаемся активной хирургической тактики лечения.
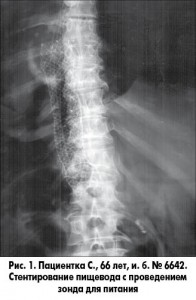
Исключение составили пациенты, тяжесть состояния которых не позволила выполнить хирургическое вмешательство. В таких ситуациях выполнялись эндоскопические стентирования пищеводными стентами Hanarostent производства M.I. Tech (Корея) с антирефлюксным клапаном. Трансназально в отводящую петлю был проведен зонд для питания (рис. 1).
Данная методика за анализируемый период была применена у 13 больных (48,1%). К описанной методике лечения относим высокую частоту (77,2%) миграции стента, что способствует поддержанию явлений эмпиемы плевры и медиастинита. Летальность при использовании указанной методики приближается к 80%.
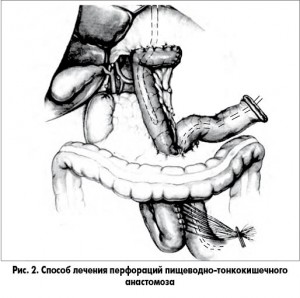
Нами разработан и применен за анализируемый период у 6 пациентов (22,2%) способ лечения перфораций пищеводно-тонкокишечного анастомоза (рис. 2), который заключается в следующем. После проведения релапаротомии выполняют разъединение сращений и оценку состояния пищеводного анастомоза. Выполняют резекцию приводящей петли кишки вместе с заглушкой между эзофагоеюно- и брауновским соустьем. Дистальная ее часть ушивается наглухо. Далее ушивают дефект в зоне пищеводного соустья с «подхватыванием» ножек диафрагмы на желудочном зонде № 30. Затем после удаления зонда трансназально в отводящую петлю заводят зонд № 12 для декомпрессии зоны соустья. Дистальную культю приводящей петли используют для укрепления линии швов. Проксимальный отдел приводящей петли использовали для формирования губовидной или трубчатой еюностомы, через которую осуществляют интубацию тонкой кишки, при этом зонд проводили через брауновское соустье. Выполнение данного способа операции позволяет сохранить ранее наложенное соустье, интубационный зонд используют как для декомпрессии, так и для проведения в послеоперационном периоде зондового питания, при этом снижается риск развития бронхолегочных осложнений.
Среди больных, оперированных с применением описанной методики, умер один при нарастании явлений эндогенной интоксикации и полиорганной недостаточности. Послеоперационные осложнения отмечены в двух случаях: у одного больного диагностирован резидуальный внутрибрюшной абсцесс (выполнено пункционное дренирование под УЗИ-навигацией) и у одного больного развилось нагноение послеоперационной раны.
С 2012 г. в клинике института в случае развития несостоятельности пищеводных анастомозов или перфораций грудного отдела пищевода широко применяют методику трансхиатальной экстирпации пищевода (без торакотомии). Данная методика заключается в следующем.
Абдоминальный этап. После проведения верхнесрединной лапаротомии выполняют висцеролиз, левая доля печени перемещается вправо. При необходимости выполняется сагиттальная диафрагмотомия по А.Г. Савиных. Далее мобилизуется дистальный отдел грудного отдела пищевода на расстоянии 5-10 см в заднем средостении путем тракции пищеводно-желудочного перехода (при его наличии) в брюшную полость за наложенную ранее держалку во время диссекции пищевода вдоль его стенки в средостении второй рукой. Опыт показывает, что выполнение трансхиатальной эзофагоэктомии «вслепую» позволяет мобилизовать меньшую часть дистального отдела пищевода – в отличие от мобилизации пищевода под визуальным контролем с помощью узких ретракторов, когда перевязка и пересечение латеральных перипищеводных связок четко контролируется. В этом случае возможна мобилизация дистального отдела пищевода как минимум до уровня карины трахеи. Мобилизация дистального отдела пищевода считается оконченной, когда пищевод свободно смещается в заднее средостение, отсутствует фиксация его к превертебральной фасции, аорте и другим медиастинальным структурам. Формируется еюностома или гастростома (в зависимости от ситуации), через которую за связку Трейца заводится зонд для кормления.
Шейный этап. Доступ к пищеводу на шее осуществляется косым разрезом параллельно переднему краю левой грудинно-ключично-сосцевидной мышцы от уровня вырезки грудины до перстневидного хряща. Платизма и лопаточно-подъязычная мышца пересекаются, грудинно-ключично-сосцевидная мышца и сосудисто-нервный пучок шеи смещаются латерально, в то время как гортань и трахея смещаются медиально. Средняя щитовидная вена и нижняя щитовидная артерия обычно лигируются и пересекаются.
Диссекцию выполняют путем отделения пищевода от превертебральной фасции вслепую с помощью пальца в верхнем средостении. При диссекции в зоне пищеводно-трахеальной борозды существует опасность повреждения левого возвратного нерва, что можно предупредить тракцией пищевода кзади от трахеи с помощью держалки, наложенной на шейный отдел пищевода, путем аккуратной слепой диссекции передней полуокружности пищевода справа налево. Пищевод свободно подтягивается вверх, когда грудная его часть мобилизована в верхнем средостении. Ладонная поверхность пальцев располагается по направлению к трахее и по средней линии пищевода во время диссекции для предотвращения разрыва мембранозной части трахеи. Использование подобной техники дает возможность мобилизации верхнегрудного отдела пищевода практически до карины трахеи через шейный доступ.
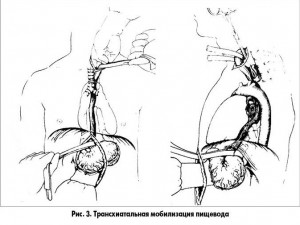
Медиастинальная (трансхиатальная) диссекция. Трансхиатальная диссекция пищевода выполняется аккуратно и последовательно. Одна рука со стороны брюшной полости вводится в средостение через пищеводное отверстие диафрагмы позади пищевода, а через шейный доступ в верхнее средостение вводится тупфер вдоль превертебральной фасции (рис. 3). Далее аккуратно отслаивают тупфером пищевод от превертебральной фасции до тех пор, пока тупфер не достигнет руки введенной через пищеводное отверстие диафрагмы.
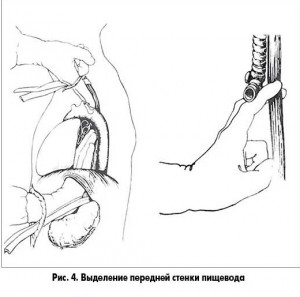
После мобилизации задней стенки пищевода приступают к выделению передней его стенки. С помощью держалки, наложенной в зоне пищеводно-желудочного перехода, пищевод подтягивают книзу, и хирург вводит руку ладонью вниз относительно передней стенки пищевода и продвигает ее в средостении, постепенно отделяя пищевод от перикарда и карины трахеи (рис. 4).
После мобилизации пищевод с помощью верхней держалки выводят в рану на шею на протяжении 8-10 см и пересекают. Затем пищевод выводят в брюшную полость и отсекают. Далее осуществляют дренирование заднего средостения по Б.С. Розанову, в оба поддиафрагмальных пространства устанавливают «улавливающие» перчаточно-трубчатые дренажи.
Гастро- или еюностомическую трубку фиксируют к передней брюшной стенке после окончательного завершения трансхиатальной резекции пищевода.
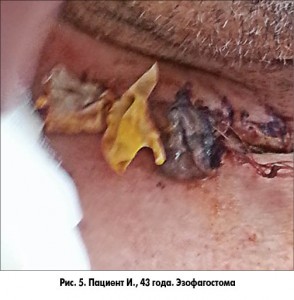
На шее формируют концевую эзофагостому (рис. 5). Лапаротомную рану ушивают.
Описанная методика хирургического лечения применена у 8 больных, умерло 2 пациента; причинами смерти в одном случае стала острая легочно-сердечная недостаточность, один пациент умер на фоне прогрессирования явлений эндогенной интоксикации и полиорганной недостаточности.
Послеоперационные осложнения диагностированы в трех случаях, при этом в двух случаях течение послеоперационного периода осложнилось развитием нагноения послеоперационной раны, в одном случае – развитием острой легочно-сердечной недостаточности, что послужило причиной смерти больного.
Трем выжившим больным, перенесшим экстирпацию пищевода, через 4-6 месяцев после выписки выполнялись реконструктивные операции – проводилась пластика грудного отдела пищевода сегментами кишечника. Двум пациентам, которым накладывались губовидные еюностомы, в плановом порядке производили закрытие стом из локального доступа.
Общая летальность пациентов с несостоятельностью пищеводных анастомозов и перфорациями пищевода в исследуемый период составила 41,8%, послеоперационная – 21,4%, число послеоперационных осложнений достигло 35,7%.
Следует отметить, что у пациентов, к которым применялась активная хирургическая тактика лечения, ни в одном наблюдении развития внутриплевральных осложнений и пневмонии отмечено не было.
На наш взгляд, активная хирургическая тактика лечения оправдывает себя в случаях максимально раннего выполнения оперативного вмешательства после установления факта развития осложнений в виде несостоятельности анастомоза или перфорации.
Таким образом, внедрение в практику лечения больных с несостоятельностью пищеводных анастомозов и разрывов грудного отдела пищевода, сопровождающихся развитием медиастинита, активной хирургической тактики с применением трансхиатальной экстирпации пищевода и разработанного способа лечения несостоятельности пищеводных анастомозов позволило добиться снижения уровня летальности и послеоперационных осложнений (по сравнению с имеющимися литературными данными и собственным опытом), а также исключить возможность развития внутриплевральных осложнений. Предлагаемый лечебно-тактический подход позволяет выполнять реконструктивные вмешательства после стабилизации состояния пациента, что в последующем будет способствовать улучшению качества их жизни.
СТАТТІ ЗА ТЕМОЮ Хірургія, ортопедія та анестезіологія
Традиційна науково-практична конференція з міжнародною участю Ophthalmic Hub, яка цього року відбулася 1-2 жовтня, привернула значну увагу лікарів-офтальмологів, оскільки включала виступи провідних вітчизняних спеціалістів і закордонних спікерів із Білорусі, Єгипту, Іспанії, Казахстану, Нідерландів, Німеччини, Норвегії, Польщі, США та Словенії.