что такое мышечный мостик пмжа
Медицинские интернет-конференции
Языки
Значимость степени стеноза ПМЖВ, обусловленного миокардиальным мостом, в клиническом исходе стентирования проксимального атеросклеротического поражения
Резюме
Ключевые слова
Статья
Введение. Мышечный мост (ММ), частично перекрывающий просвет коронарной артерии, является врожденным анатомическим вариантом и чаще встречается в ПМЖВ. ММ обусловливает развитие ИБС посредством двух независимых механизмов, зависящих от его анатомических особенностей (протяженность, толщина, локализация). Одним из механизмов является прямая механическая компрессия ПМЖВ в момент систолы, способствующая отсрочке диастолической релаксации артерии, снижает резерв кровотока и выраженность перфузии. Второй механизм – усиление прогрессии коронарного атеросклероза, обусловливающего стеноз ПМЖВ проксимальнее ММ, вследствие эндотелиального повреждения на фоне аномальной гемодинамики (ретроградный кровоток к устью ПМЖВ в систолу). Анатомические особенности ММ связаны с выбором тактики и исходом вмешательства у пациентов с ИБС. Так, в случаях стентирования по поводу атеросклеротической бляшки, расположенной проксимальнее ММ, возможно позиционирование части стента в области ММ, что увеличивает частоту отдаленных неблагоприятных исходов, обусловленных, в основном, нарушениями в области стентированного участка ММ. Т.о., анатомические особенности ММ необходимо учитывать при диагностике и выборе тактики лечения ИБС у пациентов, имеющих данную анатомическую особенность.
Цель исследования. Определить влияние степени систолической компресии ПМЖВ, обусловленной ММ, на частоту сердечно-сосудистых событий в ближайшем и отдаленном периоде после стентирования атеросклеротического поражения, расположенного проксимальнее ММ.
Материал и методы. В проспективное исследование было включено 17 пациентов с ИБС, которым в период с января 2012 по август 2013 года было выполнено стентирование ПМЖВ. Критериями включения явились: наличие ММ в средней трети ПМЖВ и стеноза, расположенного проксимальнее ММ. При позиционировании стентов использовалось ВСУЗИ с целью профилактики непреднамеренного стентирования части ММ. Ангиографическая эффективность стентирования оценивалась непосредственно после процедуры, а также по истечении 6 месяцев. Учитывали непосредственные результаты: развитие инфаркта миокарда (ИМ) в ближайшем периоде после стентирования, а также наличие и степень остаточного стеноза. В качестве отдаленных клинических результатов оценивались степень стеноза стента в зависимости от исходной степени систолической компрессией артерии, а также наличие осложнений (инфаркт миокарда, потребность в повторной реваскуляризации в данной локализации, летальные исходы). Наличие и степень остаточного стеноза определяли при контрольной ангиографии и ВСУЗИ непосредственно после стентирования и спустя 6 месяцев. В рамках настоящего исследования были использованы стенты только с лекарственным покрытием.
Неблагоприятных исходов в ближайшем периоде (острых нарушений коронарного кровообращения, диссекций артерии и проч.) в обеих группах зафиксировано не было.
На протяжении 6-месячного наблюдения у пациентов как I, так и II группы, не было отмечено острых коронарных событий или потребности в повторной реваскуляризации миокарда.
В отдаленном периоде частота рестенозов стентов не различалась в группах пациентов с разной степенью систолической компрессии артерии: так, в группе 1 рестеноз имел место у 2 пациентов, а в группе 2 – у 1 пациента (р(c 2 )= 0,55).
Выводы. Обязательным условием при стентировании ПМЖВ, имеющей дистально расположенный ММ, является использование ВСУЗИ для контроля позиционирования стента. Не было выявлено влияния степени систолической компрессии ПМЖВ (более или менее 50%), обусловленной миокардиальным мостом, на частоту неблагоприятных событий после выполнения коронарного стентирования в области проксимально расположенной атеросклеротической бляшки. Необходимо дальнейшее изучение соотношения анатомических параметров ММ и частоты рестенозов стентов, имплантированных по поводу проксимального атеросклеротического поражения ПМЖВ.
Мышечный мостик и фистула коронарной артерии у больной со стенокардией
Полный текст
Аннотация
Сердечно-сосудистые заболевания являются ведущей причиной смерти. В основе развития ишемической болезни сердца лежит атеросклероз коронарных артерий, который обнаруживают у большинства больных, страдающих стенокардией, и у пациентов с инфарктом миокарда. Однако в ряде случаев у лиц с этими клиническими проявлениями коронарные артерии при ангиографии оказываются неизмененными. Это состояние обозначают как синдром Х, или микроваскулярную стенокардию. Наряду с этим в основе развития или усугубления течения ишемической болезни сердца могут лежать врожденные особенности расположения и строения коронарных артерий, к которым относят мышечные мостики и фистулы коронарной артерии, что подтверждено рядом исследований, в которых указывается на роль этих патологий в возникновении стенокардии и инфаркта миокарда. Однако существует и противоположное мнение — часть специалистов признает наличие данных врожденных особенностей строения коронарного русла индивидуальным вариантом нормы. В связи с чем в настоящее время остается спорным вопрос хирургического лечения больных с вышеуказанными аномалиями венечных артерий. В статье приведено описание больной со стенокардией, у которой при коронарной ангиографии не было обнаружено признаков стенозирования коронарных артерий, но выявлены мышечный мостик и фистула коронарной артерии; проанализирован вклад врожденной патологии венечных сосудов в развитие стенокардии напряжения, а также обсуждаются диагностика, тактика консервативного и хирургического лечения больных с данными аномалиями.
Ключевые слова
Полный текст
Сердечно-сосудистые заболевания, и в первую очередь ишемическая болезнь сердца и мозга, являются ведущими причинами преждевременной смертности и инвалидизации лиц различного возраста в промышленно развитых странах. Патоморфологическую основу ишемической болезни сердца составляет атеросклероз коронарных артерий, который обнаруживают у большинства больных, страдающих стенокардией, и у пациентов с инфарктом миокарда. Однако примерно в 5–10 % случаев у лиц с этими клиническими проявлениями коронарные артерии при ангиографии оказываются неизмененными [2]. Это состояние обозначают как синдром Х, или микроваскулярную стенокардию, и указывают на роль в таких случаях эндотелиальной дисфункции [7].
Наряду с этим в основе развития ишемии миокарда могут лежать врожденные особенности расположения и строения коронарных артерий. В норме главные коронарные артерии расположены на поверхности эпикарда. В некоторых случаях короткий участок артерии оказывается погруженным в миокард («туннелизация» артерий), что получило название «мышечный мостик». Мышечные мостики встречаются в 5–12 % случаев и чаще относятся к левой передней нисходящей артерии [9]. Погруженный сегмент артерии имеет нормальный диаметр в диастолу, но резко суживается во время каждой систолы. Коронарные артерии снабжаются кровью во время диастолы, то есть мышечные мостики, казалось бы, не должны способствовать ограничению коронарного кровотока. Тем не менее глубоко расположенные и длинные мостики могут ограничивать коронарный кровоток и в диастолу. Этому способствует ряд факторов: нарушение диастолической функции (гипертрофия миокарда), эндотелиальная дисфункция на фоне факторов риска (артериальная гипертензия, дислипидемия, курение и др.), спазм коронарных артерий. В этих случаях мышечные мостики достоверно взаимосвязаны со стенокардией, инфарктом миокарда, нарушениями ритма и внезапной смертью [5].
Другая аномалия коронарных артерий — это фистула, то есть сообщение артерии с камерами сердца или крупными сосудами (полые вены, легочная артерия и др.) Случаи сообщения с левым желудочком часто бессимптомны, но при значительном сбросе крови сопровождаются повышением давления в левом желудочке, его гипертрофией и дилатацией, а у некоторых больных — развитием ишемии миокарда дистальнее фистулы [12].
В литературе описана тактика ведения больных с синдромом стенокардии на фоне миокардиального мостика. Для объективизации роли миокардиального мостика в генезе болевого синдрома перспективным методом исследования является оценка фракционного резерва кровотока во время коронарной ангиографии (fractional flow reserve, FFR). Метод используют для оценки вероятности ишемии миокарда. Фракционный резерв кровотока определяется как максимальный кровоток в миокарде при наличии стеноза, деленный на теоретический максимальный кровоток в отсутствие стеноза (гемодинамически значимым считается FFR
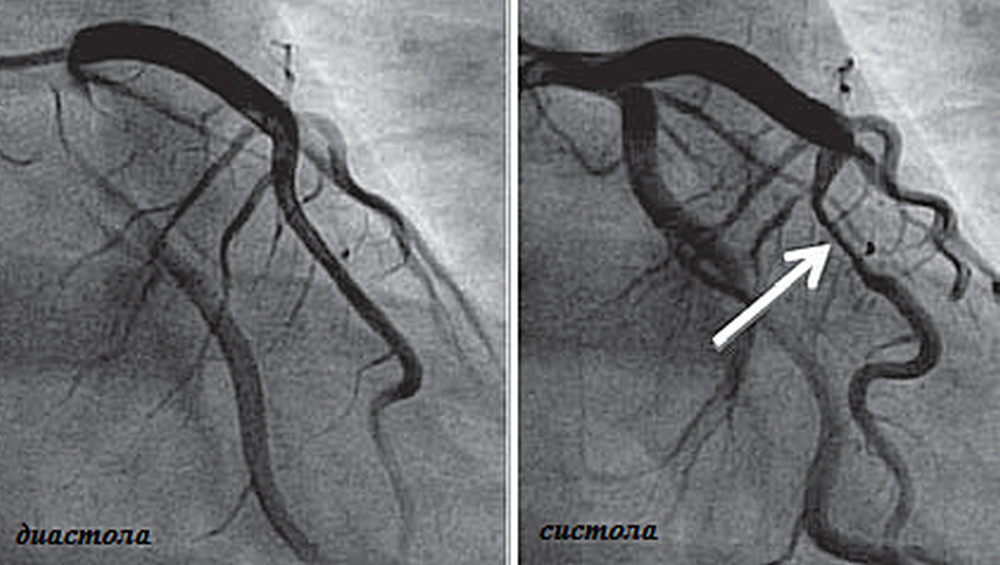
Рис. 1. Мышечный мостик передней нисходящей артерии (коронарная ангиография) в диастолу (a) и в систолу (b)
Fig. 1. Myocardial bridge of the left anterior descending artery (coronary angiography) diastole (a), systole (b)
В период с 20.06.2014 по 04.07.2014 пациентка была планово госпитализирована для дальнейшего обследования. Во время стресс-эхокардиографии ухудшения регионарной сократимости миокарда левого желудочка выявлено не было, однако обнаружен недостаточный коронарный резерв левой передней нисходящей артерии — небольшой прирост максимальной диастолической скорости с 42 до 48 см/с, то есть менее чем в 2 раза (достоверным критерием гемодинамически значимого стеноза является прирост линейной скорости кровотока в зоне стеноза в 2 раза и более). В ходе холтеровского мониторирования ЭКГ в течение суток регистрировался синусовый ритм с тенденцией к умеренной брадикардии и незначительно выраженной наджелудочковой эктопической активностью в виде эпизодов предсердного ритма и одиночных экстрасистол; зарегистрированы паузы за счет синусовой аритмии максимально до 1424 миллисекунд, минимальное количество одиночных желудочковых экстрасистол. Жизнеугрожающих нарушений ритма и проводимости обнаружено не было. После обследования пациентка была проконсультирована кардиохирургом, по заключению которого показания к оперативному лечению отсутствовали, рекомендовано продолжить консервативную терапию; к принимаемым препаратам был добавлен сиднофарм по 2 таблетки на ночь. На фоне терапии значимого клинического улучшения не отмечалось.
Спустя несколько лет пациентка была вновь госпитализирована в связи с усилением болевого синдрома в грудной клетке — для определения тактики дальнейшего ведения. На ЭКГ регистрировались синусовая брадикардия (медикаментозно обусловленная) с частотой 46–57 ударов в минуту, отклонение электрической оси влево, блокада передне-верхнего разветвления левой ножки пучка Гиса, гипертрофия левого желудочка с нарушениями процессов реполяризации по ишемическому типу (отрицательные зубцы Т в области боковой стенки, перегородочной области и верхушки левого желудочка). По результатам госпитализации с учетом недостаточной эффективности полноценной антиангинальной терапии пациентке было рекомендовано выполнить повторную плановую коронарную ангиографию. Возможно, что за три года, прошедшие с момента проведения первой коронарографии, у больной развились стенозы, обусловленные атеросклерозом коронарных артерий, что объясняло бы отсутствие эффекта от терапии. Однако выраженный стенокардитический синдром наблюдался у больной в течение длительного времени до выполнения коронарной ангиографии, в ходе которой стенозов коронарного русла обнаружено не было, поэтому кажется очевидной связь болевого синдрома с миокардиальным мостиком. Отрицательного вклада в гемодинамику со стороны фистулы коронарной артерии по результатам коронарографии не выявлено.
Приведенное наблюдение демонстрирует сочетание двух врожденных аномалий строения коронарных артерий — мышечного мостика и фистулы коронарной артерии у пожилой пациентки с синдромом стенокардии при отсутствии стенозов коронарных артерий по данным ангиографии. Сброс крови из бассейна левой коронарной артерии в левый желудочек оказался незначимым, и очевидно, основное значение в генезе стенокардитического синдрома имеет мышечный мостик. Консервативное лечение больной было неэффективным. Планируется повторить коронарную ангиографию и выполнить диагностические провокационные пробы для решения вопроса об оптимальном методе коррекции мышечного мостика.
В Центре Алмазова внедрено современное оперативное лечение миокардиальных мостиков коронарных артерий
Коронарография с миокардиальным мостиком. В систолической фазе сердечного цикла отмечается сужение диаметра коронарной артерии. В научной литературе данный феномен обозначается как «milking effect» или «step up – step down».
С 2018 года в Национальном медицинском исследовательском центре им. В. А. Алмазова внедрено оперативное лечение миокардиальных мостиков коронарных артерий новым методом супракоронарной миотомии.
За прошедший год кардиохирургами Центра выполнено более двух десятков открытых операций на сердце, в ходе которых проведена коррекция аномального развития коронарных артерий. Миокардиальные мостики — наиболее распространенный вариант данной патологии.
При этом заболевании один из сегментов коронарной артерии (чаще всего средний сегмент передней межжелудочковой артерии) проходит в толще сердечной мышцы, в то время как при нормальном развитии сосудов сердца коронарные артерии располагаются эпикардиально, в толще жировой и соединительной тканей. Такая врожденная аномалия коронарного русла служит одной из причин нарушения кровообращения и приводит к
развитию ишемии миокарда вплоть до некроза.
На рисунке показано интрамиокардиальное расположение коронарной артерии. По результатам многочисленных исследований было выявлено, что миокардиальные мостики способствуют развитию коронарного атеросклероза.
Супрокоронарная миотомия в настоящее время является единственным патогенетически обоснованным и радикальным вариантом лечения миокардиальных мостиков. Суть операции заключается в рассечении мышечных волокон, под которыми располагается артерия, что позволяет исключить компрессию сосуда и изменение его диаметра в зависимости от сердечных сокращений.
Данный вид операций осуществляется лишь в нескольких ведущих медицинских центрах России. В 2018 году в Центре Алмазова их выполнено двадцать три. В шестнадцати случаях применена изолированная супракоронарная миотомия, в пяти — супракоронарная миотомия с коронарным шунтированием и в одном случае потребовалась супракоронарная миотомия с коррекцией клапанной патологии. Однако наибольший интерес вызвал клинический случай супракоронарной миотомии на донорском сердце во время трансплантации сердца.
Важнейшую роль в диагностике и определении показаний к оперативному лечению играют такие исследования, как стресс-эхокардиография, коронарография, позитронно-эмиссионная томография и мультиспиральная компьютерная томография — все эти обязательные методы исследований пациентов с аномальным развитием коронарных артерий в Центре представлены.
Отделения сердечно-сосудистой хирургии тесно сотрудничают с научно-исследовательскими отделами и лабораториями Института сердца и сосудов, а также с НИЛ ядерной медицины. В Центре Алмазова продолжаются исследования, связанные с изучением медикаментозной терапии у данной группы пациентов, информативности различных диагностических подходов, вариантов хирургической
коррекции аномалии. В ближайшее время планируется внедрение миниинвазивных доступов для
выполнения супракоронарной миотомии, а также интраоперационное использование ультразвукового
аппарата нового поколения для облегчения визуализации целевой артерии.
Анализ ближайших и отдаленных результатов хирургического лечения пациентов, прооперированных в Центре Алмазова, подтверждает эффективность и перспективность нового вида лечения миокардиальных мостиков — супракоронарной миотомии
Мышечные «мостики» миокарда.
Мышечными «мостиками» миокарда называется аномалия расположения коронарных артерий, при которой сосуд частично локализуется в толще миокарда, а не непосредственно под эпикардом. Иногда используются другие названия этой аномалии: интрамуральный ход коронарной артерии, «ныряющая» коронарная артерия, глубоко ныряющий ход коронарной артерии.
В норме коронарные артерии располагаются субэпикардиально и окружены рыхлой соединительной тканью и жировой клетчаткой эпикарда, изредка погружаясь в миокард с образованием небольших мышечных «мостиков» длиной 1-2 см. Этим обеспечивается непрерывность кровотока – и в диастолу, и в систолу. Но иногда эти мышечные перемычки становятся весьма выраженными, в результате чего коронарные артерии частично проходят в толще миокарда (интрамурально). Такие значительные мышечные «мостики» могут сыграть роковую роль в изменении коронарного кровотока. Анатомические особенности даже небольших аномалий могут определять их участие в патогенезе различных заболеваний и в прогнозе пациента. Кроме того, динамический стеноз, который во многом зависит от частоты и силы сердечных сокращений и выявляется далеко не всеми методами диагностики, при отсутствии органического поражения коронарных артерий (атеросклероза, тромбоза) существенно затрудняет своевременную диагностику и раннее назначение адекватной терапии.
Хотя это, как правило, доброкачественная патология, ее наличие нередко ассоциировано со стенокардией, инфарктом миокарда, желудочковой тахикардией, а также с внезапной сердечной смертью. Риск того, что наличие «мостика» отразится на клиническом состоянии пациента, определяется длиной и толщиной этого «мостика» и соответственно тяжестью систолической компрессии артерии. При значительном «мостике» на данном участке венечной артерии может полностью прекращаться антероградный кровоток в систолу и даже возникает ретроградный ток крови, что проявляется ишемической симптоматикой и может стать причиной внезапной смерти. Кроме того, в связи с затрудненным или ретроградным кровотоком в указанном сегменте участок коронарной артерии, сдавливаемый мышечным «мостиком», более склонен к эндотелиальной дисфункции, атеросклерозу и тромбозу [2].
Истинная частота встречаемости миокардиальных «мостиков» неизвестна. Многочисленные авторы приводят самые разные данные – от 5 до 87% [2, 5], что зависит от особенностей популяции лиц, подвергшихся аутопсии, и от степени выраженности этих «мостиков». Имеются основания полагать, что мышечные «мостики» в миокарде присутствуют практически у трети взрослых людей [2], хотя далеко не все из них настолько выражены, что могут оказывать влияние на клиническое состояние больного и проявляться симптомами нарушения перфузии сердца. Гемодинамически значимые миокардиальные «мостики» во время коронароангиографии обнаруживаются у 0,5-4,9% больных [2, 5]. Однако было показано, что после использования провокационных тестов, увеличивающих силу и частоту сердечных сокращений, выявляемость мышечных «мостиков» при ангиографии может возрастать до 40% (C. Diefenbach et al., 1994; S. Iversen et al., 1992) [2]. Наибольшее клиническое значение эта аномалия имеет у лиц с гипертрофической кардиомиопатией и у пациентов, перенесших трансплантацию сердца.
Таким больным показано лечение препаратами с отрицательными ино- и хронотропным эффектами, такими как β-адреноблокаторы или антагонисты кальциевых каналов, либо их комбинацией [2, 4, 5]. Антиишемическое действие этих препаратов определяется снижением потребности миокарда в кислороде, уменьшением внутримиокардиального давления и экстрасосудистой коронарной сопротивляемости, особенно в субэндокардиальных слоях.
Важно помнить, что нитраты могут ухудшать состояние таких пациентов, а нагрузка жидкостью, напротив, – увеличивать сопротивление сосудов к компрессии и уменьшать ишемию [2, 5]. Следовательно, классические антиангинальные подходы в случае ишемии, обусловленной интрамуральным прохождением коронарной артерии, не только неэффективны, но и могут усугубить нарушения перфузии миокарда.
В случаях, рефрактерных к фармакотерапии, используется чрескожное коронарное вмешательство (стентирование данного сегмента артерии) или аортокоронарное шунтирование. Возможно проведение миотомии (рассечение «мостика»).
К сожалению, как уже было сказано, при жизни пациентов такие аномалии обычно остаются нераспознанными. Диагностика аномалий коронарных артерий чаще всего бывает случайной находкой, иногда выявляется интраоперационно, а в случаях кардиальной смерти (инфаркт миокарда, острая сердечная недостаточность, внезапная сердечная смерть) обнаруживается при аутопсии. Поэтому особую ценность приобретают современные методы диагностики, которые позволяют оценить не только состояние коронарных артерий, но и особенности их расположения относительно миокарда. В связи с этим наше внимание привлекла заметка немецких ученых Dirk Bose и Sebastian Philipp из West German Heart Center Essen (г. Эссен, Германия) о случае прижизненного распознавания миокардиальных мышечных «мостиков» с помощью визуализационных методов обследования (коронароангиографии и оптической когерентной томографии), который был опубликован в журнале New England Journal of Medicine в январе этого года [1].
В своей публикации D. Bose и S. Philipp приводят описание следующего клинического случая.
Пациент 57 лет поступил в клинику с внезапным приступом боли в грудной клетке, характер которой давал основания подозревать инфаркт миокарда. Коронарная ангиография продемонстрировала наличие сегментарного сужения левой нисходящей коронарной артерии. На рисунке слева (А) изображена соответствующая коронарная ангиограмма, стрелкой указано место сужения артерии. Поскольку причины такого сужения с помощью ангиографии установить невозможно, для уточнения диагноза была проведена оптическая когерентная томография. Этот метод исследования не обнаружил признаков атеросклероза артерии, но показал, что во время систолы диаметр артерии в области данного сужения значительно уменьшался (С), а при диастоле восстанавливался (В).
У данного пациента оказалась успешной терапия β-адреноблокаторами, рапортуют доктора D. Bose и S. Philipp.
Таким образом, хотя в отечественных условиях широкое использование таких визуализирующих методов диагностики с высокими разрешающими способностями, как оптическая когерентная томография, пока недоступно, о вероятности наличия аномалии коронарных сосудов должен помнить каждый врач. Особенно актуальным становится диагностический поиск такой патологии в случае ишемических симптомов вазоспастического характера, при ишемии или инфаркте у лиц молодого возраста, при гипертрофической кардиомиопатии.
Оптическая когерентная томография – новый метод неинвазивной визуализации тканей, основанный на измерении степени светооптического отражения биологических структур. С технической точки зрения метод близок к ультразвуковому исследованию, только для зондирования тканей используются не акустические, а световые излучения (ближнего инфракрасного диапазона). Исследование позволяет получить двухмерное изображение поперечных оптических срезов биологических тканей с разрешающей способностью, приближающейся к клеточному уровню (10-15 микрон). В настоящее время оптическая когерентная томография наиболее интенсивно внедряется в офтальмологическую практику для изучения патологии сетчатки, зрительного нерва и других мелких структур органа зрения. Применение данного метода в кардиологии также оправдано, как можно судить по представленному клиническому наблюдению.
Кроме того, визуализировать интрамуральное прохождение коронарных артерий можно также при помощи интракоронарного ультразвукового допплеровского исследования, трансторакальной допплерэхокардиографии, магнитнорезонансной томографии, многослойной компьютерной томографии, электроннолучевой томографии и других современных методов исследования.
1. Bose D., Philipp S. High-Resolution Imaging of Myocardial Bridging. New England Journal of Medicine 2008; 4: 358-392.
2. Mohlenkamp S., Hort W., Ge J., Erbel R. Update on Myocardial Bridging. Circulation 2002; 106: 2616-2622.
3. Белозеров Ю.М. Инфаркт миокарда у детей // Российский вестник перинатологии и педиатрии. – 1996. – № 3. – С. 36-40.
4. Шляховер В., Берман М., Маневич И., Джафри Д., Рейзин Л. Обморок, желудочковая тахикардия, миокардиальные «мостики». Дефибриллятор? Аортокоронарное шунтирование? Или ничего? // Medicus Amicus. – 2005. – № 2.
По материалам Madicine Review
5. Мазур Н.А. Факторы риска внезапной кардиальной смерти у больных молодого возраста и меры по профилактике // Русский медицинский журнал. – 2003. – Т. 11, № 19. – С. 1077-1079.
Мышечно-тонический синдром
Специалисты реабилитационного центра “Лаборатория движения” помогут в восстановлении функций опорно-двигательного аппарата
Самым частым проявлением дегенеративных патологий позвоночника является мышечно тонический синдром. Длительное и стойкое напряжение мышц, отвечающих за поддержание стабильности позвоночных сегментов, приводит к формированию болезненных «триггерных точек». И только комплексное лечение, направленное на оптимизацию различных звеньев двигательной системы, позволяет существенно облегчить состояние пациента.
Рассказывает специалист ЦМРТ
Дата публикации: 29 Июня 2021 года
Дата проверки: 29 Июня 2021 года
Содержание статьи
Причины мышечно-тонических болевых синдромов
Чрезмерные статические нагрузки и микротравмирование позвоночных структур влечет за собой рефлекторное напряжение мышц, ограничение их подвижности и формирование неоптимального двигательного стереотипа. Основной причиной мышечно-тонического синдрома являются дегенеративно-дистрофические заболевания позвоночника (остеохондроз, межпозвонковые грыжи) и нарушения осанки, связанные с врожденными аномалиями развития и деформацией спинного хребта.
Спровоцировать болезненный мышечный спазм может:
Под воздействием провоцирующих факторов в мышцах происходят биохимические процессы с выделением медиаторов воспаления, вызывающих рефлекторное сокращение мышц.
Симптомы мышечно-тонического синдрома
Основным признаком миотонического синдрома являются глубокие ноющие вертеброгенные боли. Болезненные спазмы, сопровождающиеся уплотнением и отечностью одной или нескольких мышц, существенно ограничивают подвижность. Из-за взаимодействия с нервными рецепторами развивается стойкая болезненность. Та, в свою очередь, усиливает сокращение мышц и замыкает порочный круг: спазм – отек – боль – спазм.
Мышечно-тонический синдром пояснично-крестцового отдела чаще всего становится следствием тяжелых физических нагрузок. Напряжение грушевидной мышцы может повлечь за собой боль в области ягодицы, тазобедренного сустава. В случае сдавливания седалищного нерва возможно онемение одной из конечностей.
Мышечно-тонический синдром шейного отдела проявляется цервикальными болями, болевыми ощущениями в шее, усиливающимися при разгибании и поворотах головы, гиперстезией 4-го и 5-го пальцев руки.
Для мышечно-тонического синдрома грудного отдела характерна болезненность между лопаток и по ходу ребер. Иногда может наблюдаться ощущение жжения и сдавленности в груди, имитирующих проявления сердечных проблем.
Классификация мышечно-тонических синдромов
Существует несколько разновидностей мышечно-тонических болевых синдромов. Они классифицируются в зависимости от локализации:
Помимо вышеперечисленных, патологическим изменениям нередко подвергается трапециевидная, широчайшая грудная, квадратная мышца поясницы, подниматель лопатки. Болевой синдром может быть первичным (охватывающим только спазмированные ткани) и вторичным, локализованным вне зоны повреждения.
Диагностика
Комплекс диагностических мероприятий включает:
Самым информативным, безопасным и безболезненным методом нейровизуализации признана магнитно-резонансная томография. Она дает максимально точную оценку состоянию позвоночника и спинного мозга, позволяет выявить протрузии и межпозвонковые грыжи, определить их размеры и локализацию.