что такое митохондрии и их функции в человеческом организме
Митохондрии: строение и функции
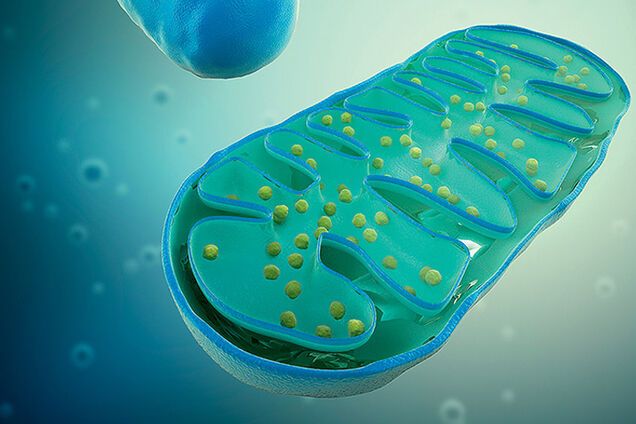
Митохондрии – двомембранний органоид эукариотической клетки. Они являются важными частями наших клеток, поскольку принимают пищу и производят энергию, которую могут использовать клетки.
Животные и растения состоят из многих сложных клеток, которые называются эукариотические клетки. Внутри этих клеток расположены структуры, выполняющие особые функции для клетки, – органеллы. Органеллы, отвечающие за выработку энергии для клетки, – это и эсть митохондрии.
Различные типы клеток имеют разное количество митохондрий. Некоторые простые клетки содержат только один-два митохондрии. Однако сложные животные клетки, которым нужно много энергии, например, мышечные, могут иметь тысячи митохондрий.
Основная функция митохондрий – производить энергию для клетки. Клетки используют специальную молекулу для получения энергии под названием АТФ (аденозинтрифосфат). АТФ для клетки производится внутри митохондрий.
То есть энергетическая функция митохондрий интегрируется с окисления органических соединений, что происходит в матриксе, благодаря чему митохондрии называют дыхательным центром клеток; синтеза АТФ, что осуществляется на кристах, благодаря чему митохондрии называют энергетическими станциями клеток.
Митохондрии вырабатывают энергию в процессе клеточного дыхания. Митохондрии принимают молекулы пищи в виде углеводов и сочетают их с кислородом для получения АТФ. Они используют ферменты для получения правильной химической реакции.
Кроме выработки энергии, митохондрии выполняют и другие функции для клетки, включая клеточный метаболизм, выработки тепла, контроль концентрации кальция и выработки некоторых стероидных гормонов. А о других гормонах можно узнать благодаря онлайн уроку за 8 класс по биологии на тему «Принципы регуляции. Эндокринная система».
Митохондрии имеют четкую структуру, которая помогает им производить энергию.
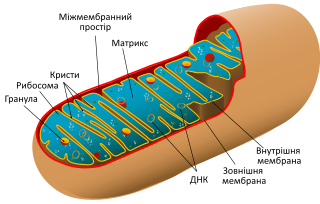
Внешняя мембрана. Защищенная гладкой внешней мембраной, которая имеет форму от круглой палочки до длинного стержня.
Внутренняя мембрана. В отличие от других органелл в клетке, митохондрии также имеют внутреннюю мембрану. Она имеет множество складок и выполняет ряд функций, чтобы помочь сделать энергию.
Кристи. Это складки на внутренней мембране. Наличие всех этих складок способствует увеличению площади поверхности внутренней мембраны.
Матрикс. Это пространство внутри внутренней мембраны. Большинство белков митохондрий находятся в матриксе. Матрикс также содержит рибосомы и ДНК, которые являются уникальными для митохондрий.
Белок синтезирующей системы. В митохондрий есть своя белоксинтезирующая система – ДНК, РНК и рибосомы. Генетический аппарат имеет вид кольцевой молекулы – нуклеотида, точно как у бактерий. Часть необходимых белков митохондрии синтезируют сами, а часть получают из цитоплазмы, поскольку эти белки кодируются ядерными генами.
Интересные факты о митохондриях:
Они могут быстро менять форму и перемещаться по клетке, когда это нужно.
Когда клетке требуется больше энергии, митохондрии могут размножаться, увеличиваясь, а затем делясь. Если клетке нужно меньше энергии, некоторые митохондрии погибнут или станут неактивными.
Митохондрии очень похожи на некоторые бактерии. По этой причине некоторые ученые считают, что сначала они были бактериями, которые поглощались более сложными клетками.
Различные митохондрии вырабатывают различные белки. Некоторые митохондрии могут производить сотни различных белков, которые используются для различных функций.
Кроме энергии в виде АТФ, они также производят небольшие количества углекислого газа.
Нужно выполнить домашнее задание по биологии в учебнике или рабочей тетради? Ищите все готовое в разделе «ГДЗ и решебниики по биологии за 8 класс».
Митохондрии: энергостанции нашего организма
На молекулярном уровне наш организм можно рассматривать как своеобразный биологический механизм. Очень сложную, многогранную, но, тем не менее, машину, принципы работы которой мы сегодня начинаем понимать все лучше и лучше. И один из этих принципов является по-настоящему фундаментальным: никакая машина не сможет работать без притока энергии.
Для более простых механизмов этот принцип нам понятен, что называется, на интуитивном уровне. Двигатель автомобиля получает энергию, сжигая топливо в баке, телевизор использует энергию тока в розетке и так далее. Но вот с нашей собственной биологической машиной – нашим телом – все не так очевидно. То есть, наверняка наш читатель знает, что мы берем энергию из пищи (и об этом мы уже рассказывали более подробно). Но вот как именно это происходит? Где и как в нашем теле условные углеводы или жиры превращаются в ту движущую силу, которая необходима для всех без исключения процессов, протекающих в организме?
Клеточные «электростанции»
Основные объемы энергии в человеческом теле вырабатываются внутри отдельных клеток. Можно сказать, что каждая из них самостоятельно отвечает за собственное энергоснабжение. А это значит, что в каждой клетке (как минимум в тех клетках, которые имеют ядра, эритроциты не в счет), должна быть своя «электростанция». И это действительно так! Более того, нередко таких «электростанций» имеется несколько десятков или даже сотен. Зависит их число от того, насколько интенсивно работает клетка, а значит, и от того, насколько много ей требуется энергии в единицу времени. Научное название таких «электростанций» – митохондрии, а их совокупность именуют митохондриальным пулом клетки.
Как появились митохондрии?
Один из важных вопросов, который давно беспокоил научную общественность: а откуда вообще взялись митохондрии в наших клетках? Самая современная и достоверная теория предлагает крайне необычный ответ: митохондрии – это потомки бактерий.
Давным-давно одноклеточные организмы, которым предстояло стать нашими предками, научились поглощать крохотные бактерии, присутствующие в окружающей среде. Если попросту – они ими питались. Но в один прекрасный день такая протобактерия не разрушилась, попав во внутриклеточную среду. И более того, она сохранила не только целостность, но и кое-какие свои функции. В частности, способность вырабатывать энергию с помощью кислорода. Каков до этого был механизм получения энергии у тех одноклеточных, которые впоследствии станут нами, известно плохо. Но с уверенностью можно сказать, что аэробный путь, предложенный им проглоченной бактерией, был однозначно более выгодным и эффективным.
Результатом этого удивительного события стал внутриклеточный симбиоз. Бактерия вырабатывала много энергии, а одноклеточный организм-хозяин снабжал ее достаточным количеством кислорода и других необходимых соединений. Со временем протобактерия упростилась, видоизменилась и стала необходимой клеточной органеллой. Этот союз оказался настолько успешным, что сейчас на нем построено энергоснабжение практически всех эукариотических клеток растений, грибов и животных. В том числе и нас с вами [1].
Как устроены митохондрии?
Многое в строении митохондрий до сих пор напоминает о том, что когда-то они были самостоятельными бактериями. Так, например, они окружены внешней липидной мембраной – такую мембрану имеют и все остальные клетки нашего организма. Основная функция внешней мембраны – защита митохондрии, отграничение ее от окружающей внутриклеточной среды, а также транспортировка необходимых веществ внутрь и выведение результатов ее работы наружу [2].
Внутреннее пространство митохондрии занимает матрикс. Это жидкая среда, состоящая из смеси жирных кислот, белков, рибосом и других соединений. В матриксе проходит первая стадия кислородного дыхания, то есть, выработки энергии. Кроме того, здесь находится и еще одно свидетельство прошлой самостоятельности митохондрий – митохондриальная ДНК. Да, оказывается, не весь наш генетический материал помещен в клеточное ядро! Эти небольшие кольцевые митохондриальные ДНК (мтДНК) кодируют 13 белков, которые нужны для работы самой митохондрии. В основном это ферменты, участвующие в дыхательной цепи окисления водорода [3].
Что еще интересно: люди наследуют мтДНК исключительно по материнской линии, а мтДНК, полученная от сперматозоида, разрушается сразу после оплодотворения [4]. Эта «женская» мтДНК мутирует по очень четким законам и поэтому можно отследить то, как именно она изменялась с течением времени. Ряд исследований последних лет убедительно доказал, что примерно 200 000 лет назад в Африке жила женщина, от которой свою мтДНК получило все современное человечество. Ученые поэтически назвали эту женщину «митохондриальной Евой» [5].
Наконец, между внешней мембраной и матриксом имеется и вторая, внутренняя мембрана. Она очень неровная и образует кристы – длинные складки, направленные к центру митохондрии. Именно их – как темные полосы – видели первые исследователи XIX века. На внутренней мембране как раз и происходит запасание энергии в виде молекул аденозинтрифосфата (АТФ). В процессе этого потребляется более 80% того кислорода, который попадает в нашу кровь при дыхании [6].
Чем еще заняты наши митохондрии?
Основная функция этих органелл – обеспечение энергией всех протекающих в клетке процессов. Однако, помимо этого митохондрии выполняют и еще целый ряд витальных (жизненно важных) функций. В их числе:
Опираясь на данные современных исследований, можно смело утверждать, что митохондрии, во-первых, активно участвуют во внутриклеточных процессах, а во-вторых, влияют и на физиологию всего организма. Такая «широкая специализация» стала причиной того, что нарушения работы митохондрий сегодня рассматривают как одну из важных причин появления множества заболеваний [12].
Что будет при нарушении работы митохондрий?
Очевидно, что самым первым и самым ярким проявлением дисфункции митохондрий будет уменьшение выработки энергии в клетке. На клиническом уровне такое обстоятельство может проявляться по-разному. И больше всего пострадают те ткани, которые работают максимально активно, а значит, требуют наибольшего притока энергии [13]:
Кроме того, учитывая другие функции митохондрий, о которых мы рассказывали выше, их неправильная работа может становиться фактором риска развития многих нарушений [14]:
Как улучшить работу митохондрий?
На настоящий момент предложены две стратегии того, как улучшить функции митохондриального пула. Первая связана с тем, что митохондрии, как органеллы, не статичны. Они могут сливаться, делиться, увеличиваться и уменьшаться в размерах, а также обмениваться своим генетическим материалом [15]. Это тоже своеобразное «наследие» их бактериального прошлого. В ходе таких слияний и делений поврежденные участки митохондрий и мтДНК отсеиваются и распадаются. Итогом становится образование новых, полноценных митохондрий, которые намного лучше выполняют все свои функции. То есть, благодаря этим процессам происходит обновление всего митохондриального пула клетки [16].
Мы имеем возможность ускорить это обновление. В частности, таким действием обладает функциональный продукт здорового питания под названием T8 ERA MIT UP, который недавно выпустила на рынок компания VILAVI INT LTD. В этом продукте содержится концентрат гранатового сока, который богат веществами под названием эллаготаннины [17]. Попадая в наш желудок, они быстро распадаются с образованием эллаговой кислоты, а ее, в свою очередь, перерабатывают кишечные бактерии, производя уролитин А [18]. Это соединение как раз и стимулирует митохондрии активнее обновляться путем слияния и деления. Уже есть исследования, которые показывают, что дефицит уролитина А – важный фактор преждевременного старения [19]. Помимо этого, доказано, что приток этого вещества увеличивает сопротивляемость физическим и умственным нагрузкам как раз за счет улучшения выработки энергии в митохондриях [20].
Вторая стратегия основана на защите митохондрий от разрушающего воздействия оксидативного стресса. Как мы уже говорили, в ходе выработки энергии они также синтезируют активные формы кислорода. Это молекулы-суперокислители (они же – свободные радикалы), которые играют сигнальную роль. Но, помимо этого, они обладают и немалой химической агрессивностью, являясь основной причиной оксидативного клеточного стресса [21]. А еще один действующий компонент активной формулы T8 ERA MIT UP – комплекс SibXP, содержащий полипренолы, клеточный сок пихты и хвойную пасту CGNC. При этом полипренолы – это многоатомные спирты растительного происхождения, которые обладают выраженной антиоксидантной активностью. Именно это их свойство и важно для улучшения функции митохондрий. Полипренолы химически связывают свободные радикалы, не давая им повреждать митохондриальные мембраны и ферменты. Благодаря этому выработка энергии в клетке и поддерживается на необходимом уровне [22].
Источники
1. Evans A., Neuman N. The Mighty Mitochondria. Molecular Cell. 2016, March, 3, 61 (5): 641.
2. André J. Mitochondria. Biology of the Cell. 1994, 80 (2-3): 103-6.
3. Gaston D., Tsaousis A.D., Roger A.J. Predicting proteomes of mitochondria and related organelles from genomic and expressed sequence tag data. Methods in Enzymology. 2009, 457: 21-47.
4. Al Rawi S., Louvet-Vallée S., Djeddi A., Sachse M., Culetto E., Hajjar C., Boyd L., Legouis R., Galy V. Postfertilization autophagy of sperm organelles prevents paternal mitochondrial DNA transmission. Science. 2011, 334: 1144-1147.
5. Fu Q., Mittnik A., Johnson P.L., Bos K., Lari M., Bollongino R., Sun C., Giemsch L., Schmitz R., et al. A revised timescale for human evolution based on ancient mitochondrial genomes. Current Biology. 21 March 2013, 23 (7): 553–59.
6. André J. Mitochondria. Biology of the Cell. 1994, 80 (2-3): 103-6.
7. Bock F.J., Tait S.W.G. Mitochondria as multifaceted regulators of cell death. Nature Reviews Molecular Cell Biology. 2020, February, 21 (2): 85-100.
8. Kornmann B. The endoplasmic reticulum-mitochondria encounter structure: coordinating lipid metabolism across membranes. Journal of Biological Chemistry. 2020, May, 26, 401 (6-7): 811-820.
9. Liu X., Hajnóczky G. Ca2+-dependent regulation of mitochondrial dynamics by the Miro-Milton complex. International Journal of Biochemistry and Cell Biology. 2009, 41: 1972-1976.
10. Murphy M.P. How mitochondria produce reactive oxygen species. Biochemistry Journal. 2009, 417: 1-13.
11. Clark A., Mach N. The crosstalk between the gut microbiota and mitochondria during exercise. Frontiers of Physiology. 2017, May 19, 8: 319.
12. Annesley S.J., Fisher P.R. Mitochondria in Health and Disease. Cells. 2019. July, 5, 8 (7): 680.
13. van der Giezen M., Tovar J. Degenerate mitochondria. Reports of European Molecular Biology Organization. 2005, June, 6, (6): 525-30.
14. Duchen M.R. Mitochondria in health and disease: perspectives on a new mitochondrial biology. Molecular Aspects of Medicine. 2004, August, 25 (4): 365-451.
15. Youle R.J., van der Bliek A.M. Mitochondrial fission, fusion, and stress. Science (New York, N.Y.), 2012, 337(6098), 1062–1065.
16. Ashrafi G., Schwarz T.L. The pathways of mitophagy for quality control and clearance of mitochondria. Cell Death & Differentiation. 2013, January, 20 (1): 31-42.
17. Johanningsmeier S.D., Harris G.K. Pomegranate as a functional food and nutraceutical source. Annual Review of Food Science and Technology. 2011-02-28, 2 (1): 181–201.
18. Selma M.V., Beltrán D., Luna M.C., Romo-Vaquero M., García-Villalba R., Mira A., et al. Isolation of Human Intestinal Bacteria Capable of Producing the Bioactive Metabolite Isourolithin A from Ellagic Acid. Frontiers in Microbiology. 2017, 8: 1521.
19. D’Amico D., Andreux P.A., Valdés P., Singh A., Rinsch C., Auwerx J. Impact of the Natural Compound Urolithin A on Health, Disease, and Aging. Trends in Molecular Medicine, May 2021, S1471491421001180.
20. Ryu D., Mouchiroud L., Andreux P.A., Katsyuba E., Moullan N., Nicolet-Dit-Félix A.A., et al. «Urolithin A induces mitophagy and prolongs lifespan in C. elegans and increases muscle function in rodents». Nature Medicine. August 2016, 22 (8): 879–88.
21. Lin M.T., Beal M.F. Mitochondrial dysfunction and oxidative stress in neurodegenerative diseases. Nature. 2006, October, 19, 443 (7113): 787-95.
22. Михайлова Е.А., Локошко Д.В., Большакова Е.М. Полипренолы и долихолы, как важный компонент антиоксидантной защиты фосфолипидных мембран. Обзор данных современной научной литературы. Современная Российская наука: актуальные вопросы, достижения и инновации: сборник статей II Всероссийской научно-практической конференции, Пенза, 07 мая 2021 года. С. 97-101.
Митохондриальная патология у детей
Представлены данные о митохондриальных болезнях в детском возрасте. Рассматриваются исторические, этиопатогенетические и генетические аспекты этой группы болезней. Описаны основные виды митохондриальной патологии, подходы к диагностике и современные предс
The article focuses on mitochondrial disorders in infancy and childhood. Authors consider historical, etiopathogenic and genetic aspects of this group of diseases. Main types of mitochondrial pathologies are described, as well as approaches to diagnostics and contemporary ideas of potential treatment methods.
Митохондриальные болезни — это группа наследственной патологии, возникающей в результате нарушений клеточной энергетики, характеризующаяся полиморфизмом клинических проявлений, выражающаяся в преимущественном поражении центральной нервной системы и мышечной системы, а также других органов и систем организма [1].
Альтернативное определение митохондриальной патологии гласит, что это обширная группа патологических состояний, обусловленных генетическими, структурными и биохимическими дефектами митохондрий, нарушением тканевого дыхания и, как следствие, недостаточностью энергетического обмена.
Как указывает A. Munnich, «митохондриальные заболевания могут вызывать любой симптом, в любой ткани, в любом возрасте, при любом типе наследования» [2].
Митохондриальные дыхательные цепи — главный конечный путь аэробного метаболизма. Поэтому митохондриальную патологию нередко называют «болезнями дыхательной цепи митохондрий» (БДЦМ); это сравнительно новый класс болезней.
Исторические аспекты митохондриальной патологии
R. Luft и соавт. (1962) обнаружили взаимосвязь между мышечной слабостью и нарушениями процессов окислительного фосфорилирования в мышечной ткани [3]. S. Nass и M. Nass (1963) открыли существование собственного генетического аппарата митохондрий (обнаружены несколько копий кольцевой хромосомы) [4, 5]. В 1960–1970 гг. появилась концепция митохондриальных болезней, то есть патологии, этиологически опосредованной митохондриальной дисфункцией. В 1980-е гг. были получены точные молекулярно-генетические доказательства митохондриальной природы ряда заболеваний (болезнь Лебера, синдром Пирсона) [6].
Этиопатогенетические аспекты митохондриальной патологии
В зависимости от наличия основного метаболического дефекта принято рассматривать четыре основных группы митохондриальных болезней: 1) нарушения обмена пирувата; 2) дефекты обмена жирных кислот; 3) нарушения цикла Кребса; 4) дефекты электронного транспорта и окислительного фосфорилирования (OXPHOS) [1, 2].
Причинами возникновения митохондриальной патологии являются мутации в генах, кодирующих белки, задействованные в процессах энергообмена в клетках (включая субъединицы комплекса пируватдегидрогеназы, ферменты цикла Кребса, компоненты цепи транспорта электронов, структурные белки цепи транспорта электронов (ЦТЭ), митохондриальные транспортеры внутренней мембраны, регуляторы митохондриального нуклеотидного пула, а также факторы, взаимодействующие с ДНК митохондрий (мтДНК) [2, 6].
Митохондриальные нарушения связаны с большим числом болезней, не являющихся первичными митохондриальными цитопатиями. Тем не менее, при этих болезнях нарушения функций митохондрий вносят значимый вклад в патогенез и клинические проявления заболеваний. Описываемые болезни могут быть метаболическими, дегенеративными, воспалительными, врожденными/приобретенными мальформациями, а также неоплазмами.
Митохондрия является органеллой, которая присутствует практически в каждой клетке, за исключением зрелых эритроцитов. Именно поэтому митохондриальные болезни могут поражать любые системы и органы человеческого организма [6]. В связи с этим правильнее называть эти состояния «митохондриальными цитопатиями» [1, 2].
Основные особенности митохондриальных цитопатий включают выраженный полиморфизм клинических симптомов, мультисистемный характер поражения, вариабельность течения, прогрессирование и неадекватное реагирование на применяемую терапию.
Конечным результатом окислительного фосфорилирования, происходящего в комплексах 1-γ, является производство энергии (АТФ). Аденозин трифосфат — основной источник энергии для клеток.
Митохондриальная ДНК тесно взаимодействует с ядерной ДНК (яДНК). В каждом из 5 дыхательных комплексов основная часть субъединиц кодируется яДНК, а не мтДНК. Комплекс I состоит из 41 субъединицы, из которых 7 кодируются мтДНК, а остальные — яДНК. Комплекс II имеет всего 4 субъединицы; большая их часть кодируется яДНК. Комплекс III представлен десятью субъединицами; кодирование мтДНК — 1, яДНК — 9. Комплекс IV имеет 13 субъединиц, из которых 3 кодируются мтДНК, а 10 — яДНК. Комплекс V включает 12 субъединиц, кодирование мтДНК — 2, яДНК — 10 [2, 6].
Нарушения клеточной энергетики приводят к полисистемным заболеваниям. В первую очередь, страдают органы и ткани, являющиеся наиболее энергозависимыми: нервная система (энцефалопатии, полинейропатии), мышечная система (миопатии), сердце (кардиомиопатии), почки, печень, эндокринная система и другие органы и системы. До недавнего времени все эти заболевания определялись под многочисленными масками других нозологических форм патологии. К настоящему времени выявлено более 200 заболеваний, причиной которых являются мутации митохондриальной ДНК [1, 2, 6].
Митохондриальные болезни могут быть обусловлены патологией как митохондриального, так и ядерного генома. Как указывают P. F. Chinnery и соавт. (2004) и S. DiMauro (2004), мутации мтДНК были выявлены в 1 случае на 8000 населения, а распространенность митохондриальных заболеваний составляет порядка 11,5 случаев на 100 тысяч населения [7, 8].
В каждой клетке находятся от нескольких сотен до нескольких тысяч органелл — митохондрий, содержащих от 2 до 10 кольцевых молекул митохондриальной ДНК, способных к репликации, транскрипции и трансляции, причем независимо от ядерной ДНК.
Генетические аспекты митохондриальной патологии
Митохондриальная генетика отличается от классической менделевской в трех важнейших аспектах: 1) материнское наследование (всю цитоплазму, вместе с находящимися в ней органеллами, потомки получают вместе с яйцеклеткой); 2) гетероплазмия — одновременное существование в клетке нормального (дикого) и мутантного типов ДНК; 3) митотическая сегрегация (оба типа мтДНК в процессе деления клетки могут распределяться случайным образом между дочерними клетками) [1, 2].
Митохондриальная ДНК накапливает мутации более чем в 10 раз быстрее ядерного генома, так как она лишена защитных гистонов и ее окружение чрезвычайно богато реактивными видами кислорода, являющимися побочным продуктом метаболических процессов, протекающих в митохондриях. Пропорция мутантной мтДНК должна превышать критический пороговый уровень, прежде чем клетки начнут проявлять биохимические аномалии митохондриальных дыхательных цепей (пороговый эффект). Процентный уровень мутантной мтДНК может варьировать у индивидов внутри семей, а также в органах и тканях. В этом заключается одно из объяснений вариабельности клинической картины у больных с митохондриальными дисфункциями. Одни и те же мутации могут вызывать различные клинические синдромы (например, мутация A3243G — энцефалопатию с инсультоподобными пароксизмами — синдром MELAS, а также хроническую прогрессирующую наружную офтальмоплегию, сахарный диабет). Мутации в различных генах могут быть причиной одного и того же синдрома. Классическим примером такой ситуации является синдром MELAS [2].
Разновидности митохондриальной патологии
Если перечислить основные митохондриальные болезни, то в их числе окажутся следующие: митохондриальная нейрогастроинтестинальная энцефалопатия (MNGIE), синдром множественных делеций митохондриальной ДНК, липидная миопатия с нормальными уровнями карнитина, недостаточность карнитин пальмитоилтрансферазы, митохондриальный сахарный диабет, болезнь Альперса–Хуттенлохера, синдром Кернса–Сейра, болезнь Лебера (LHON), синдром Вольфрама, синдром MEMSA, синдром Пирсона, синдром SANDO, синдром MIRAS, синдром MELAS, синдром MERRF, синдром SCAE, синдром NARP, синдром Барта, синдром CPEO, синдром Ли и др. [1].
Наиболее часто в детском возрасте встречаются следующие клинические синдромы митохондриальной патологии: синдром MELAS (митохондриальная энцефаломиопатия, лактат-ацидоз и инсультоподобные пароксизмы), синдром MERRF (миоклонус-эпилепсия с рваными красными волокнами), синдром Кернса–Сейра (характеризуется птозом, офтальмоплегией, пигментным ретинитом, атаксией, нарушением сердечного проведения), синдром NARP (нейропатия, атаксия, пигментный ретинит), синдром Ли (подострая некротизирующая энцефаломиелопатия), болезнь Лебера (наследственная оптическая нейропатия) [1, 2].
Имеется большой пул заболеваний, причиной которых является не мутации митохондриальной ДНК, а мутации ядерной ДНК, кодирующей работу митохондрий. К ним относятся следующие виды патологии: болезнь Барта (миопатия, кардиомиопатия, транзиторные нейтро- и тромбоцитопении), митохондриальная гастроинтестинальная энцефалопатия (аутосомно-рецессивное мультисистемное заболевание): птоз, офтальмоплегия, периферическая нейропатия, гастроинтестинальная дисфункция, приводящая к кахексии, лейкоэнцефалопатия. Возраст дебюта последнего заболевания весьма вариабелен — от периода новорожденности до 43 лет.
Диагностика митохондриальной патологии
Клинические критерии диагностики митохондриальных болезней сравнительно многочисленны: 1) миопатический симптомокомплекс (непереносимость физических нагрузок, мышечная слабость, снижение мышечного тонуса); 2) судороги (миоклонические или мультифокальные); 3) мозжечковый синдром (атаксия, интенционный тремор); 4) поражение глазодвигательных нервов (птоз, наружная офтальмоплегия); 5) полинейропатия; 6) инсультоподобные пароксизмы; 7) мигренеподобные головные боли; 8) черепно-лицевая дисморфия; 9) дисметаболические проявления (рвота, эпизоды летаргии, комы); 10) дыхательные нарушения (апноэ, гипервентиляция, тахипноэ); 11) поражение сердца, печени, почек; 12) прогрессирующее течение заболевания [1, 2].
В диагностике митохондриальных болезней используются следующие клинические критерии: 1) признаки поражения соединительной ткани (гипермобильный синдром, гиперэластичность кожи, нарушения осанки и др.); 2) нейродегенеративные проявления, лейкопатии при проведении магнитно-резонансной томографии (МРТ) головного мозга; 3) повторные эпизоды нарушения сознания или необъяснимые эпизоды рвоты у новорожденных; 4) необъяснимая атаксия; 5) отставание в умственном развитии без определенных причин; 6) отягощенный семейный анамнез; 7) внезапное ухудшение состояния ребенка (судороги, рвота, расстройства дыхания, вялость, слабость, нарушения мышечного тонуса — чаще мышечная гипотония, кома, летаргия; поражение печени и почек, не поддающееся обычной терапии) [1, 2].
Лабораторные (биохимические) исследования нацелены в первую очередь на выявление у пациентов лактат-ацидоза и/или пируват-ацидоза. При этом следует помнить, что нормальные показатели молочной кислоты не исключают наличия митохондриального заболевания. Другие биохимические показатели, исследуемые при подозрении на наличие митохондриальной патологии, включают кетоновые тела в крови и моче, ацилкарнитины плазмы крови, а также содержание органических кислот и аминокислот в крови и моче [9].
M. V. Miles и соавт. (2008) предложили оценивать содержание мышечного коэнзима Q10 у детей с дефектом ферментов дыхательной цепи митохондрий [10].
Цитоморфоденситометрические исследования позволяют оценивать активность митохондрий лимфоцитов (снижение количества, увеличение объема, снижение активности).
Из инструментальных исследований (помимо методов нейровизуализации) используется биопсия скелетных мышц с проведением специфических гистохимических реакций — для выявления феномена «рваных красных волокон» (ragged red fibers — RRF) в полученном биоптате. Синдромами с «рваными красными волокнами» являются следующие: MELAS, MERRF, KSS, PEO (прогрессирующая наружная офтальмоплегия), а также синдром Пирсона. Синдромы без RRF: болезнь Leigh, NARP, LHON (наследственная оптическая нейропатия Лебера) [2].
Генетические методы исследований сводятся к определению наиболее частых мутаций и секвенированию митохондриальной ДНК.
Лечение митохондриальной патологии
Терапия митохондриальных болезней, к сожалению, не разработана. С позиций доказательной медицины считается, что эффективное лечение для этой представительной группы болезней отсутствует. Тем не менее, в различных странах мира используются фармакологические средства и биологически активные вещества, нацеленные на нормализацию метаболизма и обеспечение адекватной энергетики митохондрий.
При синдроме MELAS лечение должно быть направлено на лечение судорог, эндокринных расстройств, устранение последствий инсульта.
P. Каufmann и соавт. (2006) указывают, что поскольку уровень лактата часто коррелирует с тяжестью неврологических проявлений, целесообразно применять дихлорацетат для снижения уровня лактата [11]. В нашей стране с аналогичной целью используется диметилоксобутилфосфонилдиметилат (Димефосфон) [12].
В исследованиях японских авторов Y. Koga и соавт. (2002, 2005, 2006, 2007) с хорошим эффектом использовалось внутривенное введение L-аргинина (предшественника NO) — для стимуляции вазодилатации в остром периоде инсульта, а также пероральное его применение для снижения тяжести последующих эпизодов [13–16].
Среди средств, используемых в терапии митохондриальной патологии, фигурируют следующие: витамин В1 (тиамин) — 400 мг/сут, витамин В2 (рибофлавин) — 100 мг/сут, витамин С (аскорбиновая кислота) — до 1 г/сут, витамин Е (токоферол) — 400 МЕ/сут, никотинамид (ниацин) — до 500 мг/сут, коэнзим Q10 — от 90 до 200 мг/сут, L-карнитин — от 10 мг до 1–2 г/сут, янтарная кислота — от 25 мг до 1,5 г/cут, Димефосфон 15% — 1,0 мл на 5 кг массы тела. Применяются также цитохром С (внутривенно), Реамберин (внутривенно) и Цитофлавин (внутривенно и перорально) [17, 18].
В качестве других средств фармакотерапии выступают кортикостероиды, минералокортикоиды (при развитии надпочечниковой недостаточности), антиконвульсанты — при судорогах/эпилепсии (исключая вальпроевую кислоту и ее производные, ограничивая применение барбитуратов). В наших наблюдениях наиболее эффективной противосудорожной терапией являлось использование препаратов леветирацетам (Кеппра), топирамат (Топамакс) или их сочетаний.
Нейродиетология при митохондриальной патологии
Основным принципом диеты при митохондриальной патологии является ограничение нутриентов, оказывающих негативное влияние на механизмы обмена — до формирования метаболического блока (рацион питания одновременно обогащается другими компонентами на обычном или повышенном уровне). Такая терапевтическая стратегия получила название «обхождения блока» (going around the block). Важным исключением в этом плане является группа митохондриальных нарушений, ассоциированных с метаболизмом пирувата (недостаточность пируватдегидрогеназного комплекса с сопутствующими нарушениями со стороны углеводов/гликогена/аминокислот). При этом рекомендуются кетогенная диета и другие виды высокожировых диет [19].
Широко применяются вещества, являющиеся пищевыми кофакторами (коэнзим Q10, L-карнитин, ацетил-L-карнитин, витамин В2, аскорбиновая кислота, витамин Е, витамин В1, никотинамид, витамин В6, витамин В12, биотин, фолиевая кислота, витамин К, α-липоевая кислота, янтарная кислота, Se) [19]. Рекомендуется избегание индивидуальных алиментарных факторов, индуцирующих обострение митохондриальной болезни (голодание, потребление жиров, белков, сахарозы, крахмала, алкоголя, кофеина, мононатрия глутамата; количественные нарушения приема пищи и неадекватное потребление пищевой энергии). При необходимости осуществляется клиническое питание (энтеральное, парентеральное, гастростомия) [19].
Чрезвычайно важными являются своевременная диагностика митохондриальных болезней, поиск клинических и параклинических критериев этих заболеваний на этапе предварительном, догенетическом. Это необходимо для подбора адекватной метаболической терапии и предотвращения ухудшения состояния или инвалидизации больных с этими редкими заболеваниями.
C. S. Chi (2015) подчеркивает, что подтверждение или исключение митохондриальной патологии остается принципиальным в педиатрической практике, особенно когда клинические признаки болезни не являются специфичными, вследствие чего необходим катамнестический подход к оценке симптомов и биохимических показателей [20].
Литература
* ГОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ГОУ ВПО ПМГМУ им. И. М. Сеченова МЗ РФ, Москва