что такое лактоза у ребенка
Терапия лактазной недостаточности у детей первых месяцев жизни
Состояния, связанные с нарушенным кишечным пищеварением и всасыванием, объединенные термином «мальабсорбция», относятся к числу частых нарушений здоровья у детей раннего возраста.
Состояния, связанные с нарушенным кишечным пищеварением и всасыванием, объединенные термином «мальабсорбция», относятся к числу частых нарушений здоровья у детей раннего возраста. Наиболее частой формой синдрома мальабсорбции у детей раннего возраста является непереносимость дисахаридов (лактозы, реже — других углеводов) [1, 2].
Особое значение для детей первых месяцев жизни имеет лактазная недостаточность (ЛН), так как лактоза содержится в грудном молоке, которое является основным питанием ребенка этого возраста. Дисахарид лактоза расщепляется в тонкой кишке ферментом, известным под названием лактаза. Снижение активности этого фермента приводит к развитию симптомокомплекса ЛН, проявляющейся у детей раннего возраста диареей, а также другими диспептическими нарушениями, беспокойством и др. Основным методом лечения ЛН является диетотерапия, направленная на уменьшение или полное исключение лактозы из рациона питания [3, 4]. Особую сложность представляет лечение ЛН у детей грудного возраста, так как в грудном молоке или в современных адаптированных детских молочных смесях углеводный компонент представлен преимущественно лактозой. При искусственном вскармливании детей с лактазной недостаточностью используются низколактозные смеси. Безлактозные смеси в качестве монотерапии используют только при первичной алактазии и при тяжелом течении вторичной гиполактазии [2, 5].
Учитывая, что поддержка естественного вскармливания детей первого года жизни является приоритетной задачей педиатрии, проблема профилактики и лечения ЛН у детей, находящихся на естественном вскармливании, представляется чрезвычайно важной и актуальной. При этом наиболее целесообразным в лечении ЛН является не исключение женского молока, а проведение заместительной терапии в виде назначения детям фермента лактазы. Использование ферментных препаратов лактазы в терапии ЛН позволяет довольно быстро купировать симптомы заболевания, сохранив при этом грудное вскармливание [1, 6, 7].
Учитывая значительные колебания в активности и свойствах препаратов лактазы, выпускаемых различными производителями и выделенных из различных источников, представляется необходимой обязательная клиническая оценка препарата лактазы, впервые выпускаемого в РФ или поступающего из-за рубежа в виде фармацевтического средства или биологически активной добавки (БАД).
Одним из таких БАД, содержащих лактазу, является БАД «Лактазар для детей», выпускаемый ОАО «Фармстандарт — Лексредства» (Россия). Целью настоящей работы явилось изучение эффективности использования в терапии детей первых трех месяцев жизни с ЛН, находящихся на грудном вскармливании, БАД «Лактазар для детей». Исследование проведено ГУ НИИ питания РАМН на базе детской поликлиники г. Химки Московской области.
Краткая характеристика. «Лактазар для детей» предназначен для использования в качестве дополнительного источника фермента лактазы при ЛН у детей с периода новорожденности до 7 лет. БАД «Лактазар для детей» представляет собой твердые желатиновые капсулы с белым порошком со специфическим запахом. Средняя масса содержимого капсул «Лактазар для детей» от 0,135 до 0,165 г. Активность лактазы в БАД «Лактазар для детей» — 700 ЕД на капсулу. Для производства БАД «Лактазар для детей» в качестве сырья используется фермент лактаза (Lactase DS) производства Amano Enzyme Inc. (Япония).
Дизайн исследования. Исследование носило характер открытого проспективного медицинского наблюдения.
Клинические наблюдения проведены у 25 детей в возрасте от 2 недель до 3 месяцев жизни, длительность наблюдения составила 6 недель. Клинико-лабораторные исследования проведены до назначения БАД «Лактазар для детей» и после приема ферментного препарата в течение 1 месяца.
Материалы и методы
Критерии отбора детей для исследования:
Критерии исключения детей из исследования:
Критерии оценки эффективности проводимой терапии:
— изменение кратности и консистенции стула, наличие или отсутствие патологических примесей в кале;
— динамика других диспептических нарушений (срыгиваний, колик, запоров и пр.);
— кожные или иные аллергические проявления при приеме БАД «Лактазар для детей»;
— содержание общих углеводов в кале*;
— копрологические исследования*;
— клинические анализы крови и мочи;
— измерение массы тела 1 раз в 2 недели с использованием стандартизированных весов;
— измерение роста — до и после проведения исследования с использованием стандартного ростомера.
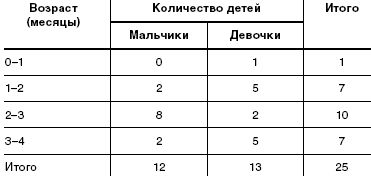
Под наблюдением находилось 25 детей (12 мальчиков и 13 девочек) в возрасте от 2 недель до 3 месяцев жизни. Все дети находились на естественном вскармливании. Под наблюдение дети поступали по обращению матерей к участковому педиатру в детской поликлинике. Дети наблюдались в амбулаторных условиях, еженедельно осматривались врачом-педиатром. Дома матери заполняли специально предложенную им анкету, в которой содержались вопросы о показателях эффективности исследуемого БАД (частота и характер стула, частота и объем срыгиваний и пр.). Дополнительные сведения получали путем телефонного интервью.
Данные о наблюдавшихся детях и их возрастно-половая характеристика представлены в табл.1 и табл.2
Все дети были доношенными, от первых (20), вторых (4) и третьих (1) родов; у 84% матерей имело место патологическое течение беременности (гестозы, анемия, наличие хронических заболеваний, хроническая фетоплацентарная недостаточность и пр.). Все кормящие матери соблюдали предложенную им диету [8]. Из рационов кормящих матерей исключали цельное коровье молоко с целью профилактики развития у детей аллергии к белкам коровьего молока и снижения тем самым возможности формирования вторичной ЛН.
При изучении анамнеза жизни было установлено, что более чем у половины обследованных детей кто-либо из членов семьи не переносит или не любит молоко и молочные продукты. Так, у 60% детей не переносит молоко один из родителей, у 20% — один из членов семьи (сестры, братья, дедушки, бабушки и др.); у остальных детей непереносимости молочных продуктов в семье, со слов матерей, не отмечено.
Диагноз ЛН устанавливали на основании характерных клинических симптомов (типичные изменения частоты и консистенции стула, усиленный метеоризм, болевой синдром и др.) и результатов клинико-лабораторных исследований (повышенного содержания общих углеводов в кале).
Результаты исследования и обсуждение
Дозу БАД «Лактазар для детей» назначали в зависимости от степени выраженности клинических проявлений ЛН (табл. 3), учитывая количество молока, употребляемого ребенком за одно кормление. Большинство детей получали по одной капсуле в каждое кормление, т. е. по 5–7 капсул БАД в сутки. Продолжительность приема БАД «Лактазар для детей» составила 1 месяц. Следует отметить, что ни в одном случае не было рекомендовано прекращение грудного вскармливания и к концу наблюдения все женщины продолжали кормить детей грудью.
Результаты исходного обследования детей
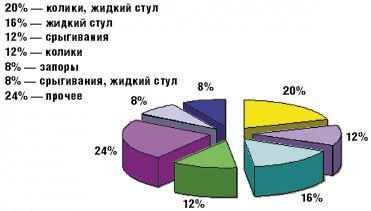
Как видно из табл. 3 и рис. 1 и 2, клинические проявления ЛН у обследованных детей были весьма вариабельны.
Такой наиболее характерный симптом ЛН, как жидкий стул, был обнаружен у 13 детей (52%), причем у 5 из них жидкий стул сочетался с коликами (табл. 3). У остальных детей имели место другие проявления функциональных нарушений пищеварения (срыгивания, метеоризм, запор). Срыгивания разной степени выраженности наблюдались у 7 детей (28%), причем у 2 детей (8%) срыгивания были единственной жалобой. У 4 детей (16%) отмечались запоры, причем как единственная жалоба запоры наблюдались у 2 детей. У 8 детей на момент взятия под наблюдение нарушений частоты и консистенции стула не было, стул у этих детей наблюдался 2–3 раза в день, кашицеобразной консистенции.
У 2 детей отмечалась недостаточная прибавка массы тела (300–400 г в месяц) и снижение аппетита (дети употребляли не весь объем порции молока, необходимый ему из расчета на массу тела и возраст); именно это послужило причиной обращения к педиатру.
Как видно из рис. 1 и 2, у наблюдавшихся детей одинаково часто (в 12% случаев) встречались колики и срыгивания как единственно предъявляемая жалоба; в 8% случаев основной и единственной жалобой были запоры. В группу под названием «прочее» мы объединили 6 детей, которые имели характерное только для них сочетание клинических проявлений ЛН (табл. 3).
Таким образом, полученные нами данные свидетельствуют о том, что клиническая картина ЛН весьма многообразна и часто не совпадает с общепринятым представлением о диарее как ведущем симптоме этого заболевания.
Результаты изучения эффективности БАД «Лактазар для детей»
Проведенные исследования показали хорошую переносимость БАД у всех наблюдавшихся детей (из исследования не был выведен ни один ребенок) и ее эффективность в устранении симптомов ЛН.
Нормализация частоты стула и его консистенции была отмечена уже к концу первой недели, причем положительная динамика имела место в среднем на 5-й день терапии. При этом кратность и консистенция стула изменялись у детей неодинаково. Нормализация консистенции стула у детей с частым жидким стулом отмечалась на 3–5 день применения БАД; а у детей с запорами восстановление регулярного стула с кратностью 3–4 раза в день, имевшего цвет и консистенцию, обычные для детей данной возрастной группы, находящихся на естественном вскармливании, — на 6–8 день. Частота стула у детей с диареей до начала терапии составляла в среднем 5,7 ± 1,2 раза в сутки, а после ее завершения — 3,8 ± 0,9 раза в сутки. У детей с запорами частота стула была равна соответственно 0,8 ± 0,6 и 2,5 ± 1,7.
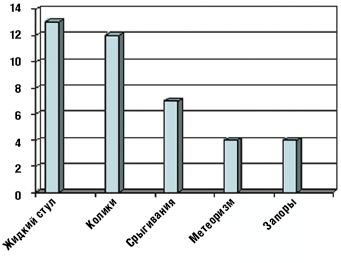
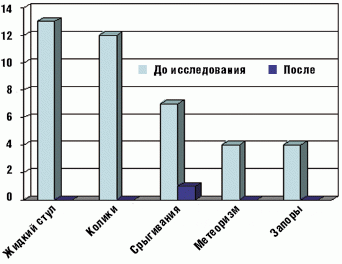
Применение БАД «Лактазар для детей» оказалось эффективным и в устранении других симптомов функциональных нарушений пищеварения, характерных для ЛН у детей раннего возраста (табл. 4 и рис. 3).
Болевой синдром, проявлявшийся кишечными коликами, и метеоризм купировались у всех 25 детей на 3–5 день применения БАД. Частота и объем срыгиваний значительно уменьшились в конце первой недели терапии и полностью исчезли после двух недель приема препарата у большинства детей. Только у одного ребенка к концу исследования изредка отмечались срыгивания.
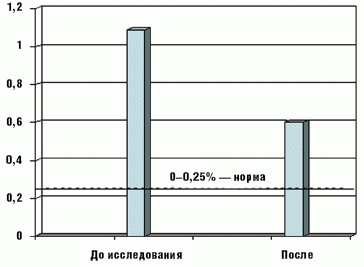
Экскреция углеводов с калом достоверно снизилась у большинства детей с 1,1 ± 0,3% до начала терапии до 0,6 ± 0,1% после ее завершения, разброс значений составил 0,4–1,8% и 0,25–0,6% соответственно (рис. 4).
Однако у 6 детей достоверного снижения уровня экскреции углеводов с калом не отмечено (0,7–0,8% до исследования и 0,5–0,6% — после); хотя клинические симптомы нарушений пищеварения были купированы на первой неделе приема БАД. Полученные нами данные согласуются с литературными данными, указывающими на отсутствие четкой корреляции между выраженностью клинических проявлений ЛН и уровнем экскреции углеводов с калом [1, 3, 4]. В связи с этим необходимо отметить, что в соответствии с современными научными представлениями основным критерием эффективности терапии является устранение клинических симптомов заболевания, а не снижение до нормы экскреции углеводов.
При копрологическом исследовании у большинства наблюдавшихся детей не было выявлено существенных патологических изменений. До проведения терапии у большинства детей каловые массы были жидковатой или кашицеобразной консистенции, светло-желтого или салатового цвета, слегка кисловатого запаха, с pH 5–7, и содержали в умеренном или единичном количестве нейтральный жир, жирные кислоты, лейкоциты (не более 2–3 в поле зрения), небольшие количества прозрачной слизи. Прием БАД «Лактазар для детей» не оказывал влияния на эти минорные изменения в копрологических анализах.
Показатели клинических анализов крови и мочи у обследованных детей до и после проведения терапии были в пределах возрастной нормы. Содержание гемоглобина в крови у детей до и после исследования составило 135,3 ± 1,5 г/л и 132,3 ± 1,2 г/л соответственно.
Наблюдавшаяся динамика массоростовых показателей была в пределах возрастной нормы: средняя прибавка массы тела в сутки составила в среднем 29,7 ± 2,7 г, а прибавка длины тела за месяц — 2,8 ± 0,5 см (средние показатели увеличения массы и длины тела у детей первых трех месяцев жизни составляют 26–30 г/сутки и 2,5–3 см/месяц соответственно). У 2 детей с исходно недостаточной прибавкой массы тела (300–400 г в месяц) прием БАД «Лактазар для детей» привел к значительному увеличению данного показателя (900 и 1000 г в месяц).
Как показали полученные результаты, использование содержащего лактазу БАД «Лактазар для детей» позволило купировать клинические симптомы ЛН и сохранить естественное вскармливание у всех наблюдавшихся детей. Терапия хорошо переносилась, случаев аллергических реакций и непереносимости исследуемого БАД не наблюдалось.
Таким образом, проведенное изучение эффективности использования в терапии детей первых месяцев жизни с ЛН, находящихся на естественном вскармливании, БАД «Лактазар для детей», выпускаемой ОАО «Фармстандарт — Лексредства» (Россия), позволили сделать следующие выводы:
Лактазная недостаточность: происхождение и пути коррекции
Рассмотрена проблема лактазной недостаточности у детей, подходы к коррекции первичной и вторичной лактазной недостаточности. Даются рекомендации по питанию детей грудного возраста с учетом особенностей вскармливания, а также детей старше 1 года и взрослых
The problem of lactase insufficiency correction in children was considered, as well as approaches to primary and secondary lactase insufficiency. The guidelines on nutrition for infants, considering the characteristics of feeding were given, as well as for children over one year old and adults.
Проблема лактазной недостаточности (ЛН) и непереносимости лактозы (как клинического проявления ЛН) стара как мир в самом прямом смысле этого выражения. Непереносимость лактозы была впервые описана Гиппократом, примерно 400 лет до н.э., однако понимание механизмов ее развития пришло лишь в середине XX века [1]. ЛН связана со снижением активности фермента лактазы щеточной каймы энтероцитов тонкой кишки, расщепляющего молочный сахар лактозу. Традиционно ЛН подразделяют на врожденную, проявляющуюся с рождения и обусловленную мутацией в гене LCT на 21-й хромосоме, первичную (ЛН взрослого типа), связанную с генетически детерминированным снижением активности лактазы после прекращения молочного вскармливания, вторичную, связанную с повреждением энтероцитов при заболеваниях кишечника, и транзиторную ЛН недоношенных и незрелых к моменту рождения детей. Наибольшее значение, безусловно, имеет непереносимость лактозы у детей первых месяцев жизни, для которых женское молоко или молочные смеси являются единственными возможными продуктами питания. В то же время самым распространенным и в наибольшей степени привлекающим к себе внимание вариантом является ЛН первичная.
Человечество на протяжении тысячелетий употребляет в пищу молоко и молочные продукты, что привело к формированию мощной индустрии молочного производства. В мире продукция коровьего молока преобладает над продукцией молока других жвачных животных, составляя примерно 85%, на втором месте — молоко буйволицы — около 11%, а козье и овечье молоко составляют 2,4% и 1,4% соответственно. Доля производства коровьего молока меньше в южных регионах, по сравнению с северными, и 80% мировой продукции козьего молока производится в тропической полосе. При этом в последние годы производство коровьего молока в развитых странах снижается, но повышается в странах развивающихся. Особенно обращает на себя внимание большой вклад в производство коровьего молока Индии, страной, в которой значительная часть населения имеет ЛН взрослого типа (табл. 1) [2, 3, 5].
Важность потребления молока в первую очередь определяется тем, что молоко является важным и доступным источником кальция. Из приведенной ниже диаграммы видно, что большая часть потребляемого кальция имеет животное происхождение. При этом в странах с низким потреблением молока отмечается и низкое потребление кальция. В связи с этим коррекция ЛН является необходимым фактором обеспечения здоровья, а при исключении молока и молочных продуктов из питания ребенка и взрослого необходимо компенсировать возникающий при этом дефицит кальция. Лицам, ограничивающим по тем или иным причинам употребление молока и молочных продуктов, следует компенсировать возникающий дефицит кальция из других источников, причем решить эту проблему без назначения препаратов вряд ли возможно (рис.) [5].
Интересны также данные о возможном превентивном эффекте молочных продуктов в отношения ряда онкологических заболеваний, в частности рака толстой кишки, молочной железы, желудка, а также в отношении воспалительных заболеваний кишечника, ожирения и сахарного диабета 2-го типа, однако эта тема требует дальнейшего углубленного изучения [6].
Непереносимость лактозы, снижение активности лактазы после прекращения молочного вскармливания являются нормальным состоянием для всех млекопитающих, и только некоторые представители Homo sapiens сохранили эту способность на протяжении последующей жизни.
Впервые человек стал использовать в своей хозяйственной деятельности жвачных животных в Месопотамии между 11-м и 9-м тысячелетиями до н.э. Это были коровы (Bos primigenius taurus), козы (Capra aegagrus hircus) и овцы (Ovis orientalis aries). В то же время буйволы (Bubalus bubalis) стали домашними животными в Индии и Китае 5000–7000 лет до н.э., а яки (Bos grunniens) — в Тибете примерно 4500 лет до н.э. Домашние жвачные животные уже в те годы использовались не только как источник мяса, но также молока и шерсти. Археологические исследования обнаружили желудки этих животных, в которых хранили молоко, перерабатывающееся в них в сыр под воздействием остаточного количества ренина, желудочного фермента. Сыр получали из молока по крайней мере 6500 лет до н.э. Шумерские клинописные источники периода Третьей династии Ура (примерно 2000 лет до н.э.) указывают на употребление сыра, в тот же период сыр производили в Египте и на Крите. В Древнем Риме сыр был обыденным продуктом питания [7, 9]. Изначально в генотипе человека (как и всех млекопитающих) было заложено снижение активности лактазы после завершения периода грудного вскармливания. Генетические исследования показали, что мутации, ассоциированные с переносимостью лактозы, появились примерно 10000 лет до н.э., параллельно с одомашниванием жвачных животных [11]. Так называемая «культурно-историческая гипотеза» предполагает, что сохраняющаяся высокая активность лактазы у жителей Северной Европы сформировалась в результате процесса отбора, позволяющего популяции полагаться на молоко млекопитающих в качестве важного компонента рациона, особенно в неурожайные годы. Противоположная по своему характеру гипотеза определяет обратные причинно-следственные взаимоотношения, предполагая, что широкое употребление молока привело к закреплению переносимости лактозы в популяции, однако данная гипотеза по данным археологических исследований представляется менее вероятной [12–15].
Помимо источника энергии и воды, употребление молока давало человеку эффективный источник кальция, обеспечивая более высокую костную плотность и профилактику рахита [17]. В большей степени это было актуально для северных регионов (в частности, Северной Европы) в условиях низкой инсоляции и более высокой потребности в кальции при дефиците витамина D. Соответственно, и более высокая частота переносимости лактозы наблюдается в северных регионах Европы, а непереносимости — в южных [5, 17, 19, 20]. Интересно, что переносимость лактозы ассоциируется с устойчивостью к малярии, феноменом, изученным в первую очередь на примере народности Фулани (Африка), однако механизмы этой взаимосвязи остаются неустановленными [21].
Ген LCT, кодирующий лактазу и определяющий расщепление и, следовательно, переносимость лактозы, имеет длину в 49,3 kb, расположен на длинном плече (q) хромосомы 2 в позиции 21 и содержит 17 экзонов (NCBI Reference Sequence NG_008104.1) [23]. Для первичной ЛН описан генетический полиморфизм, затрагивающий репликативный фактор MCM6, один из высококонсервативных белков группы MCM, необходимых для инициации репликации в эукариотических клетках (в первую очередь полиморфизм LCT-13910C.T в интроне 13 и LCT-22018G.A в интроне 9 гена MCM6) [25–27]. Генотипы LCT-13910CT и LCT-13910TT ассоциированы с переносимостью лактозы и, присутствуя в одной аллели в гетерозиготном состоянии, обладают доминантным эффектом, обеспечивая расщепление лактозы, в то время как генотип LCT-13910CC при отсутствии аллели LCT-13910T приводит к лактозной мальабсорбции [26, 27]. Между генотипами LCT-13910C.T и LCT-22018G.A отмечается параллелизм. У лиц с генотипом LCT-13910CC наблюдается вариант LCT-22018GG, тогда как у лиц с LCT-13910CT часто имеет место LCT-22018GA, причем LCT-13910TT ассоциируется с LCT-22018AA, за исключением небольшого числа наблюдений в Финляндии [27], Китае [28] и у бразильцев японского происхождения [29]. Указанные генотипы лактозной мальабсорбции широко распространены в Европе, в то время как в других регионах мира присутствуют иные аллели переносимости/непереносимости лактозы [30].
В Европе распространенность первичной ЛН варьирует от 2% в Скандинавии до 70% в некоторых регионах Италии [31]. Распространенность ее в белой популяции США составляет 20%, в Азии она приближается к 100%. Распространенность ЛН у взрослых в Швеции, Дании составляет около 3%, Финляндии, Швейцарии — 16%, Англии — 20–30%, Франции — 42%, странах Юго-Восточной Азии, среди афроамериканцев США — 80–100%, Европейской части России — 16–18%. Однако коррекция требуется далеко не всем лицам с ЛН.
В лечении нуждаются лишь те пациенты с ЛН, у которых имеют место клинические ее проявления. Отклонение от нормы результатов диагностических методов, не сопровождающееся соответствующими симптомами, также не является основанием для проведения терапии.
При врожденной и первичной ЛН в основе лечения пациента лежит снижение количества лактозы в питании вплоть до полного ее исключения. Параллельно с этим проводится терапия, направленная на коррекцию дисбактериоза кишечника и другое симптоматическое лечение.
При вторичной ЛН основное внимание должно быть уделено лечению основного заболевания, а снижение количества лактозы в диете является временным мероприятием, которое проводится до восстановления слизистой оболочки тонкой кишки.
Снижение количества лактозы в питании может быть достигнуто путем исключения из питания содержащих лактозу продуктов, в первую очередь цельного молока.
Этот способ вполне приемлем для взрослых и детей старшего возраста с ЛН взрослого типа и при вторичной ЛН. При этом часто допускается употребление кисломолочных продуктов, масла, твердых сыров. Следует учитывать возможное снижение потребления кальция при безмолочной диете.
В грудном возрасте, если ребенок находится на естественном вскармливании, оптимальным подходом является использование препаратов лактазы, которые смешиваются со сцеженным грудным молоком и расщепляют лактозу, не влияя на остальные его свойства. Продуцентами лактазы для производства соответствующих препаратов и биологически активных добавок (а в большинстве случаев средства, содержащие лактазу, зарегистрированы как БАДы) являются дрожжи, чаще всего Kluyveromyces fragilis, Kluyveromyces lactis или плесени Aspergillus niger и Aspergillus oryzae.
Детей, находящихся на искусственном вскармливании, следует перевести на полное или частичное питание низколактозными (безлактозными) заменителями грудного молока, подобрав питание с максимальным количеством лактозы, которое не вызывает появления клинической симптоматики и повышения содержания углеводов в кале.
Диета дополняется симптоматической терапией, которая зависит от состояния ребенка и выраженности вторичных нарушений. В случае развития эксикоза требуется терапия, направленная на коррекцию водно-электролитного баланса. Также развитие дисбиоза кишечника может определить показания к назначению пробиотиков.
В дальнейшем после купирования симптомов у детей с ЛН необходимо контролировать содержание углеводов в кале в динамике и при возобновлении симптомов снизить количество лактозы.
У детей на естественном вскармливании при отсутствии препаратов лактазы применяют аналогичную тактику.
Блюда прикорма (каши, овощные пюре) детям первого года жизни с ЛН, естественно, не должны содержать лактозу. Календарь введения прикорма при этом не отличается от такового для детей без ЛН.
У детей старше одного года и взрослых с ЛН из питания исключаются продукты, содержащие лактозу (табл. 2). Целесообразна замена молока и молочных продуктов специализированными низколактозными молочными продуктами: низколактозным молоком, сливками, сметаной и т. п. в количествах, определяемых возрастными потребностями. Кисломолочные продукты (кефир, йогурт) эти больные обычно переносят хорошо.
Проблема умеренно выраженной лактазной недостаточности может быть решена потреблением кисломолочных продуктов с низким содержанием лактозы, за счет высвобождения β-галактозидазы в желудочно-кишечный тракт живыми пробиотическими бактериями, способными выжить в ЖКТ [18]. Уникальным в этом отношении среди других кисломолочных продуктов является йогурт подобно пахте или сладкому ацидофилину. Они хорошо переносятся людьми с лактазной недостаточностью и способствуют расщеплению лактозы благодаря бактериям Lactobacillus bulgaricus и Streptococcus thermophilus [18, 24], освобождающим β-галактозидазу в кишечнике. Назначение пробиотиков улучшает ферментативную активность микроорганизмов кишечника, повышает переваривание лактозы, редуцирует симптомы лактазной недостаточности, замедляя транзит содержимого по пищеварительному тракту. Пастеризация кисломолочных продуктов снижает количество живых бактерий [18, 24]. Клиническое исследование по приему капсул, содержащих Bifidobacterium longum и йогурта, обогащенного Bifidobacterium animalis доказало эффективность в отношении облегчения симптомов непереносимости лактозы [10]. Подобное исследование у детей (возраст с 5 до 16 лет) показало, что потребление молока с Lactobacillus acidophilus или йогурта, содержащего Lactobacillus lactis и Streptococcus thermophilus уменьшает симптомы лактазной недостаточности, по сравнению с группой детей, употреблявших необогащенное молоко [18]. Известно, что методом сбраживания лактозы молочнокислыми микроорганизмами, можно максимально утилизировать до 20% лактозы (до 4% остаточной лактозы), что с точки зрения лактазной недостаточности является малоэффективным. Была изучена возможность получения низколактозных кисломолочных продуктов с использованием ферментного препарата β-галактозидазы, полученного из дрожжей Kluveromyces lactis. Исследовали скорость ферментации, молока гидролизованного β-галактозидазой, как до внесения закваски, так и одновременно с ее внесением. В одном случае закваску вносили в предварительно гидролизованное молоко (процесс ферментации был совмещен с процессом резервирования, в другом — закваску вносили непосредственно с ферментом β-галактозидазой (0,2%, концентрация 2000 НЕЛ/г). Сокращение процесса сквашивания и повышение влагоудерживающей способности в образцах с одновременным внесением фермента и закваски можно объяснить тем, что продукты ферментативного катализа активизируют заквасочную микрофлору. Содержание остаточной лактозы в контрольных образцах (без фермента) составляло 4,0–3,8%; в опытных образцах с предварительным гидролизом лактозы 1,2–1,0%; в образцах с одновременным внесением фермента и закваски — 1,0–0,8% [34, 37].
Следует отметить, что лактоза в последние десятилетия стала широко применяться в пищевой индустрии и фармакологической промышленности. Она используется как подсластитель и как вспенивающий агент, придает продуктам приятный вкус и формирует привлекательную текстуру при производстве хлебобулочных изделий, напитков (как безалкогольных, так и алкогольных, в частности, пива), мясных продуктов (например, при изготовлении бургеров) и др. Важно, что лактоза не ферментируется грибами, и это позволяет избежать избыточной продукции углекислого газа и спиртов. Лактоза может присутствовать в обработанном мясе (сосиски, паштеты и др.), маргарине, хлебе, картофельных чипсах, соусах, плавленых сырах, белковых добавках, пиве. В фармакологической промышленности лактоза широко используется в качестве наполнителя в составе лекарственных препаратов. В связи с этим объемы промышленного производства лактозы растут год от года [5, 32, 33, 35]. Соответственно, список содержащих лактозу немолочных продуктов также расширяется.
Длительность терапии определяется характером заболевания. При врожденной ЛН низколактозная диета назначается пожизненно. При транзиторной ЛН недоношенных многие дети в течение нескольких месяцев постепенно восстанавливают способность переносить лактозу (хотя это не исключает развитие первичной ЛН). Отмена диеты проводится под индивидуальным контролем переносимости лактозы.
При вторичной гиполактазии симптомы ЛН являются транзиторными. Пациентам проводится лечение основного заболевания; наряду с этим назначается низколактозная диета в соответствии с изложенными выше принципами. При восстановлении нормальной структуры и функции слизистой оболочки тонкой кишки активность лактазы восстанавливается. Поэтому при разрешении (ремиссии) основного заболевания через 1–3 месяца диету можно постепенно расширять, хотя и здесь необходим строго индивидуальный подход [36].
С учетом развивающегося при клинически манифестной ЛН дисбиоза кишечника целесообразно в этой ситуации назначение пробиотиков. Они могут быть назначены как самостоятельные препараты, однако некоторые производители вводят их в состав смесей для искусственного вскармливания.
Максилак® и Максилак Бэби в своем составе не содержит казеина (молочного белка) и лактозы (молочного сахара), они гипоаллергенны и их можно применять даже при высокой аллергической чувствительности. В состав Максилак® и Максилак® Бэби входят бифидо- и лактобактерии различных штаммов и могут применяться для поддержания эндогенной флоры при вторичной лактазной недостаточности.
Максилак® выпускается в двух формах:
С. В. Бельмер, доктор медицинских наук, профессор
ФГБОУ ВО РНИМУ им. Н. И. Пирогова, Москва
Лактазная недостаточность: происхождение и пути коррекции/ С. В. Бельмер
Для цитирования: Лечащий врач № 2/2018; Номера страниц в выпуске: 41-46
Теги: грудной возраст, вскармливание, лактоза, непереносимость

_575.gif)
.gif)
.gif)