что такое клинический случай
Клинический случай
Смотреть что такое «Клинический случай» в других словарях:
клинический — КЛИНИЧЕСКИЙ, ая, ое. Излишний, чрезмерный, ненормальный. клинический случай 1. Трудноразрешимая, тупиковая ситуация. 2. То же, что клиника Он идиот? Не то слово, клинический случай … Словарь русского арго
СЛУЧАЙ — В крайнем случае. Разг. При острой необходимости. ФСРЯ, 434. Во всяком случае. Разг. 1. При любых обстоятельствах. 2. Однако, всё таки. ФСРЯ, 435. В случае чего. Разг. Если произойдёт, случится что л., если возникнут какие л. неприятности,… … Большой словарь русских поговорок
Случай — – (как и «лучший», от, вероятно, старославянск. «лукый» случайный, выпавший на долю, назначенный судьбой; англ. оccasion – случай, обстоятельство; повод, основание; событие) 1. в эксперименте – некое событие, происходящее внутри системы под… … Энциклопедический словарь по психологии и педагогике
КЛИНИЧЕСКИЙ — КЛИНИЧЕСКИЙ, ая, ое. 1. см. клиника. 2. Относящийся к лечебному воздействию, требующий или поддающийся лечению (спец.). К. случай. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
КЛИНИЧЕСКИЙ ТИП — Любой частный случай, когда симптомы и поведение соответствуют одному из множества определенных синдромов клинической психологии и психиатрии … Толковый словарь по психологии
BAFTA (премия, 1967) — 20 я церемония вручения наград премии BAFTA Лондон, Англия Лучший фильм: Кто боится Вирджинии Вулф? Who’s Afraid of Virginia Woolf? Лучший британский фильм: Шпион, пришедший с холода The Spy Who Came in from the Cold Википедия
Дирофиляриоз — Dirofilaria immitis … Википедия
ЧЕЛОВЕК-ВОЛК — – имя, данное в психоаналитической литературе пациенту, клинический случай которого описан З. Фрейдом в работе «Из истории одного детского невроза» (1918). Для описания данного случая З. Фрейд использовал псевдоним Wolfsmann, перевод которого… … Энциклопедический словарь по психологии и педагогике
Клинический случай постановки диагноза: «Болезнь Девика»
Оптикомиелит (болезнь Девика) – воспалительное демиелинизирующее заболевание, характеризующееся селективным поражением зрительного нерва (острый и под¬острый неврит) и спинного мозга (обширный поперечный миелит).
Оптикомиелит (болезнь Девика) – воспалительное демиелинизирующее заболевание, характеризующееся селективным поражением зрительного нерва (острый и подострый неврит) и спинного мозга (обширный поперечный миелит). Оптикомиелит часто неправильно диагностируется как рассеянный склероз (РС), но прогноз и лечение этих патологий различны. На сегодняшний день, в связи с особенностями течения и выделением специфического маркера (NMO-IgG), который не встречается при РС, оптикомиелит выделен в отдельную нозологическую единицу. Особый вариант РС описан Девиком (Devic) в 1894 г. и получил название «оптикомиелит Девика». В литературе имеются сообщения о том, что перед возникновением неврологических симптомов имел место продромальный период в виде лихорадки, инфекции и других аутоиммунных состояний, таких как системная красная волчанка, аутоиммунный тиреоидит, синдром Шегрена. Демиелинизирующее поражение зрительных нервов и спинного мозга может происходить одновременно или последовательно. Возникает временная слепота, иногда постоянная, в одном или обоих глазах. Также наблюдаются различная степень пареза или паралича в ногах, потеря чувствительности и/или дисфункция мочевого пузыря и кишечника вследствие повреждения спинного мозга. Полная клиническая картина болезни может проявиться в течение 8 недель. Течение болезни у взрослых чаще многофазное с периодами обострения и ремиссии и, в отличие от РС, более тяжелое. Патоморфологически очаги демиелинизации при этом заболевании близки к РС, но иногда встречаются нетипичные для последнего диффузные воспалительные изменения с выраженным отеком ткани мозга и в редких случаях – с геморрагиями. Данные магнитно-резонансной томографии (МРТ) и аутопсии свидетельствуют о возможности образования бляшек не только в спинном мозге и зрительных нервах, но и в перивентрикулярном белом веществе, редко – в стволе мозга и мозжечке. По данным МРТ, поражения спинного мозга носят больше некротический характер и затрагивают не менее трех сегментов.
Недавнее определение в сыворотке крови больных антител к аквапорину 4 (AQP-4) (специфических IgG) четко дифференцирует оптиконейромиелит от РС. Кроме этого, в клинике, в отличие от РС, начало заболевания приходится на более зрелый возраст, чаще болеют женщины, и в спинномозговой жидкости наблюдается плеоцитоз с повышенным содержанием белка без олигоклональных антител. Повторные исследования уровня специфических IgG позволяют наблюдать ответ на лечение и в целом мониторить заболевание.
Многие аспекты патогенеза до сих пор не ясны. Основной мишенью для иммунной реакции является AQP-4. Сывороточные антитела связываются с церебральными микрососудами, мягкой мозговой оболочкой, пространствами Вихрова – Робина. AQP-4, находящийся в отростках астроцитов или покрывающий участки сосудов, не покрытых астроцитарными ножками, участвует в образовании гематоэнцефалического барьера, при поражении не может справиться со своей функцией. Повреждение астроцитов способствует доступу других иммунных компонентов в ЦНС.
Клинический случай
Пациентка М, 58 лет, поступила на лечение во 2-е неврологическое отделение 20. 01. 2015г.
При поступлении жалобы на слабость в левой ноге, нарушение поверхностной чувствительности в обеих нижних конечностях, области живота, груди.
В плане дообследования повторно проведена нейровизуализация:
МРТ головного мозга: МР картина умеренно выраженной дисциркуляторной энцефалопатии.
МРТ шейного отдела позвоночника с в/в контрастированием: Спинной мозг на уровне С2-Тн2 неоднородной структуры утолщен, с наличием в структуре полостей расположенных на уровне С4 и С7 позвонков размерами 11х6 и 7х5 мм, при этом полость на уровне С7 с нечеткими контурами и неоднородной структуры вокруг которых визуализируются признаки отека. После контрастного усиления 20 мл Омнискана выявляется нечетко очерченное кольцевидно инфильтрирующее накопление контрастного препарата на уровне С7 распространяющееся до уровня С4 позвонка. Пре- и паравертебральные мягкие ткани не изменены. На всех уровнях шейного отдела позвоночника межпозвоночные диски снижены по высоте, МР сигнал от пульпозных ядер выраженно уменьшен, замыкательные пластинки уплощены, заострены с небольшими костными разрастаниями, при этом визуализируются протрузии межпозвонковых дисков выступающие в просвет позвоночного канала до 1, 5-2 мм. На уровнях С4-С7, за счет комплекса изменений: включающих костные разрастания, в том числе и в проекции унковертебральных сочленений, протрузий, гипертрофии желтых и задней продольной связок, утолщения спинного мозга в передне-заднем направлении. кифозирования выявляется и выраженная компрессия эпидуральной жировой клетчатки, сужение, деформация дурального мешка, ликворных пространств и переднего и боковых контуров спинного мозга, кроме того, выявляются признаки деформации дуральных воронок с обеих сторон. Заключение: МР – картину следует дифференцировать между объемным образованием спинного мозга, нарушением спинального кровообращения на фоне выраженных дегенеративно-дистрофических изменений шейного отдела позвоночника либо демиелинизирующему процессу.
МРТ грудного отдела позвоночника с в/в контрастированием: Спинной мозг на уровне (С7-Тн2) и Тн9-11 неоднородной структуры неоднородно-повышенный МР сигнал несколько утолщен. После контрастного усиления 20 мл Омнискана патологического накопления контрастного препарата не выявляется. Заключение: Миелопатия грудного отдела позвоночника на уровне Тн9-11 дифференцировать между МТS отсевом (учитывая изменения на уровне шейного отдела позвоночника) нарушением спинального кровообращения и демиелинизирующим процессом.
Акушерство и гинекология
Разбор типичных клинических случаев
Клинический случай 1
Пациентка А.Г., 22 года. Обратилась с жалобами на нерегулярный менструальный цикл с менархе. Беременность не планирует.
• Из анамнеза: менархе в 16 лет, с задержками менструации до 60–90 дней.
• Наследственная предрасположенность: сахарный диабет 2-го типа у бабушки.
• При осмотре: повышенный рост стержневых волос на молочных железах, по передней линии живота.
• По данным ультразвукового исследования (УЗИ): М-эхо – 4 мм, объем правого яичника – 16 см3, левого яичника – 14 см3, в каждом яичнике более 10 фолликулов диаметром 5–6 мм.
• По данным гормонального обследования: фолликулостимулирующий гормон (ФСГ) – 5,2 МЕ/мл, лютеинизирующий гормон (ЛГ) – 8,8 МЕ/мл, эстрадиол – 11 пмоль/мл, пролактин в норме, тиреотропный гормон (ТТГ) в норме, тестостерон, ДГЭА-сульфат, 17-ОН-прогестерон в норме.
• Фенотип без особенностей, индекс массы тела (ИМТ) в норме.
Выставлен диагноз. Синдром поликистозных яичников (олиго/ановуляция, гирсутизм, поликистоз- ная морфология).
• Рекомендовано исключение инсулинорезистентности (глюкозотолерантный тест).
• Рекомендовано использование КОК-препаратов с антиандрогенным эффектом вплоть до планиро- вания беременности.
В качестве контрацептива был предложен препарат Белара, содержащий этинилэстрадиол 30 мкг и хлормадинона ацетат 2 мг. Выбор контрацептива обусловлен низким риском гиперкоагуляционных нарушений (один из самых безопасных контрацептивов по рискам венозных тромбоэмболических осложнений – ВТЭО) и высокой терапевтической эффективностью. Так, было показано, что хлормади- нона ацетат и ципротерон ацетат обладают одинаковой антиандрогенной активностью в диапазоне терапевтических доз (Terouanne B. и соавт., 2002). 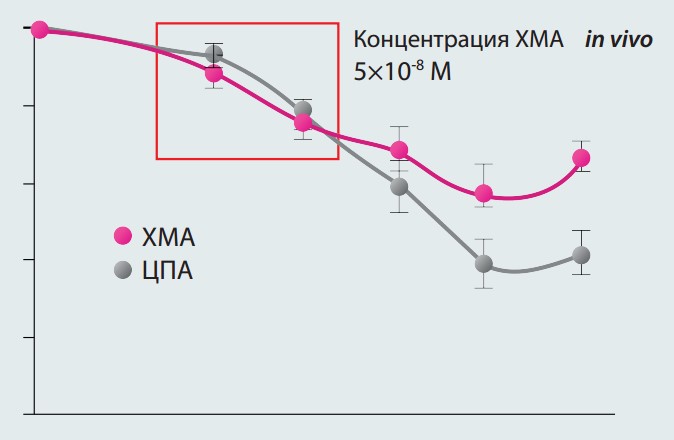
Также крайне важна метаболическая ней- тральность Белары. Так, Р. Урас и соавт. в ходе исследования, в котором приняли участие 48 пациенток, показали, что на фоне применения хлормадинона ацетата не было зафиксировано негативного вли- яния контрацептива с хлормадинона ацетатом на показатели инсулина и глю- козы. Контрацептивы, обладающие отсут- ствием негативного влияния на углевод- ный обмен, низким риском ВТЭО и высо- кой антиандрогенной активностью, явля- ются препаратами выбора для пациенток с синдромом поликистозных яичников.
• При планировании беременности рекомендуется отмена комбинированного орального контра- цептива (КОК), оценка овуляторности цикла, при необходимости – индукция овуляции.
Клинический разбор: тучная пациентка с неалкогольной жировой болезнью печени и дислипидемией
Всовременном обществе проблема ожирения приобрела высокое медико-социальное значение. У тучных пациентов практикующие врачи диагностируют сразу несколько серьезных заболеваний, среди которых сочетание неалкогольной жировой болезни печени (НАЖБП) и атероге
Всовременном обществе проблема ожирения приобрела высокое медико-социальное значение. У тучных пациентов практикующие врачи диагностируют сразу несколько серьезных заболеваний, среди которых сочетание неалкогольной жировой болезни печени (НАЖБП) и атерогенной дислипидемии встречается довольно часто. Согласно нашим данным, у 52% больных НАЖБП и ожирением выявляется атерогенная дислипидемия с повышением уровня общего холестерина, липопротеинов низкой плотности (ЛПНП), гипертриглицеридемией и снижением липопротеинов высокой плотности (ЛПВП) [1].
При лечении данной патологии лекарственные средства должны не только улучшать функциональное состояние печени и предотвращать развитие фиброза печени у больных с НАЖБП, но и параллельно устранять высокий атерогенный потенциал липидного спектра для профилактики развития сердечно-сосудистых катастроф.
В последнее время для лечения НАЖБП все чаще применяются препараты, содержащие эссенциальные фосфолипиды (Эссенциале® форте Н). Наличие у эссенциальных фосфолипидов множественных положительных свойств, таких как мембраностабилизирующее действие, влияние на проницаемость мембран гепатоцитов, способность нейтрализовать реактивные формы кислорода, снижать оксидативный стресс, тормозить развитие фиброза, а также улучшение функции инсулиновых рецепторов и влияние на регуляцию ферментов метаболизма проатерогенных и антиатерогенных липопротеидов, крайне привлекательны при лечении НАЖБП и дислипидемии у больных с ожирением и инсулинорезистентностью [2].
В качестве примера успешного использования такой терапии приводится разбор клинического случая НАЖБП и дислипидемии у тучной пациентки.
Клинический разбор
Пациентка П., 38 лет обратилась с жалобами на снижение работоспособности, повышенную утомляемость; головные боли в височных и затылочной областях на фоне повышения артериального давления (АД) максимально до 200/110 мм рт. ст.; ноющие боли и тяжесть в правом подреберье после приема жареной, жирной пищи.
Из анамнеза заболевания известно, что подъемы АД впервые стали беспокоить пациентку в 31 год во время беременности, осложненной гестозом и артериальной гипертензией (АГ). Цифры АД достигали 160/90 мм рт. ст. В дальнейшем подъемы АД стали беспокоить пациентку все чаще, и АД колебалось от 150/90 до 200/100 мм рт. ст. Постоянной антигипертензивной терапии не получала, лишь эпизодически самостоятельно использовала короткодействующие препараты (Коринфар, Адельфан) для купирования высокого АД.
Напомним, что семья играет особую роль в развитии привычек здорового питания и физической активности. Развитие ожирения у детей связано с образом жизни всех членов семьи в целом, их пищевого поведения. Интересно, что у девочек, чьи матери страдают ожирением, риск стать тучными в три раза выше в сравнении с девочками из семей с нормальной массой тела. У мальчиков такой тенденции не наблюдается, ИМТ их родителей не влияет на развитие у них ожирения во взрослой жизни.
Следует сказать о методике измерении окружности талии. ОТ необходимо измерять по линии, находящейся на середине расстояния между нижним краем реберной дуги и гребнем подвздошной кости. При измерении ОТ пациент принимает вертикальное положение. Руки могут принять одну из двух позиций: 1) опущены вдоль туловища и отведены от тела под углом в 30°; 2) скрещены на груди. Сантиметровая лента не должна перетягивать тело, лишь плотно облегать его. Измерение проводится в конце обычного выдоха для исключения влияния мышц брюшного пресса. Обычно делается два измерения и берется среднее значение, третье требуется, если разница между первым и вторым составляет более 5% (допустимы колебания в 1 см).
Абдоминальное ожирение и повышение АД свидетельствовали о наличии у пациентки метаболического синдрома (МС) или синдрома инсулинорезистентности (табл.) [3].
По данным лабораторного обследования выявлены другие признаки МС: атерогенная дислипидемия с повышением уровня общего холестерина до 284 мг/дл, гипертриглицеридемией до 300 мг/дл, повышением уровня ЛПНП до 172 мг/дл, снижением ЛПВП до 45 мг/дл. Определялась гипергликемия натощак: глюкоза — 105 мг/дл. Результаты глюкозотолерантного теста (глюкоза натощак — 105 мг/дл, через 2 часа после еды — 160 мг/дл) указывали на нарушенную толерантность к глюкозе.
Определялась патология инсулинового обмена: гиперинсулинемия до 20 мкМЕ/мл, повышение уровня С-пептида до 1680 пмоль/л. Были рассчитаны индексы инсулинорезистентности. В реальной клинической практике применяются индексы НОМА (Homeostasis Model Assessment) и QUICKI (Quantitave Insulin sensitivity Check Index). НОМА рассчитывается по формуле: иммунореактивный инсулин натощак (мкМЕ/мл) × глюкоза крови натощак (ммоль/л/22,5); QUICKI: 1/[log (I0) + log (G0)], где I0 — базальное содержание инсулина крови (мкМЕ/мл), G0 — базальное содержание глюкозы в крови (мг/дл). У больной П. значения индекса НОМА составили 5,2 (норма менее 2,5), QUICKI — 0,3 (норма более 0,342), что подтверждало наличие инсулинорезистентности.
Кроме того, сывороточные трансаминазы были повышены в два раза: АЛТ — 76 ед/л, АСТ — 706 ед/л, HCVAb и HBSAg — не обнаружены. С высокой степенью вероятности повышение АСТ, АЛТ у тучной больной указывало на неалкогольный стеатогепатит (НАСГ).
На ЭКГ — синусовый ритм, ЧСС 72 удара в мин, косвенные признаки гипертрофии ЛЖ. При ЭХОКГ умеренная гипертрофия ЛЖ (толщина межжелудочковой перегородки и задней стенки ЛЖ 1,2 см), сохранная фракция выброса 65%, признаки диастолической дисфункции миокарда (Е/А = 1, Е/Еm = 10). При суточном мониторировании АД выявлена систолодиастолическая АГ днем и диастолическая АГ ночью с повышением индексов гипертонической нагрузки и нарушением суточного профиля (non-dipper).
По данным УЗИ брюшной полости у пациентки имелись не только проявления НАЖБП, но и поражение желчевыводящих путей: печень увеличена, паренхима гиперэхогенная, с выраженными явлениями стеатоза. Желчный пузырь: стенки уплотнены, не утолщены, желчь густая, по стенкам — единичные мелкие холестеромы (рис. 2).
Клинический диагноз был сформулирован следующим образом: «Гипертоническая болезнь II стадии, очень высокого риска. Атеросклероз аорты. Абдоминальное ожирение. Атерогенная дислипидемия. Нарушенная толерантность к глюкозе. Неалкогольный стеатогепатит. Холестероз желчного пузыря. Билиарный сладж».
Подробнее остановимся на диагностике НАСГ, который наряду со стеатозом печени является одной из форм (стадий) НАЖБП. В пользу НАСГ у больной говорили: исключение вирусной, алкогольной, аутоиммунной этиологии; наличие ожирения, МС; подтвержденная инсулинорезистентность; УЗИ-признаки жировой инфильтрации печени; повышение биохимических маркеров НАСГ (АСТ и АЛТ). Морфологически диагноз НАСГ верифицируется при выявлении некровоспалительной реакции на фоне крупнокапельного стеатоза печени (рис. 3) [4].
Одновременное наличие у разбираемой больной НАЖБП и сердечно-сосудистых заболеваний (ССЗ) заставляет задуматься о потенциальном влиянии НАЖБП на сердечно-сосудистый риск. Согласно последним научным исследованиям НАЖБП позиционируется как новый предиктор ССЗ. НАЖБП служит предиктором ССЗ независимо от других факторов риска, риск развития ССЗ повышен в 4,12 раза (95% CI, 1,58–10,75, р = 0,004) [5].
Больной была назначена гипохолестериновая гипокалорийная диета со снижением общей суточной калорийности с 3000 ккал до 1800 ккал, увеличена физическая активность. В качестве препарата, улучшающего инсулиночувствительность, больной был назначен метформин 1000 мг/сут.
Для лечения АГ больной назначен комбинированный препарат Коапровель (300/12,5 мг), содержащий гидрохлортиазид и блокатор рецепторов к ангиотензину (БРА) ирбесартан. Наш выбор был обусловлен удобством приема 1 раз в день, содержанием в одной таблетке сразу двух антигипертензивных средств, что несомненно повышает комплайнс больных, доказанным превосходством комбинированной антигипертензивной терапии над монотерапией и возможностью использования Коапровеля при лечении АГ у больных НАЖБП. Клинические исследования доказали не только высокую антигипертензивную эффективность БРА, положительное влияние на диастолическую функцию миокарда, улучшение инсулиночувствительности, профилактику СД 2-го типа, микроальбуминурии, но и возможность уменьшать фиброз печени, воспаление, стеатоз, снижать активность печеночных трансаминаз [14].
Гиполипидемическая терапия осуществлялась симвастатином в дозе 20 мг/сут. Статины безопасны для применения у больных НАЖБП при условии умеренного повышения уровня печеночных трансаминаз. Убедительные данные о связи между увеличением уровня АСТ/АЛТ и гистологически подтвержденным повреждением печени на фоне статинов отсутствуют. Наличие у статинов выгодных для больных НАЖБП механизмов действия (снижение провоспалительных цитокинов фактора некроза опухоли альфа, С-реактивного белка, интерлейкина-6, снижение доставки свободных жирных кислот в печень, влияние на инсулин через адипонектин, торможение фиброгенеза) позволяют назначать статины для коррекции дислипидемии при НАСГ [15].
Терапия НАСГ у больной проводилась препаратом, содержащим эссенциальные фосфолипиды (ЭФЛ), Эссенциале® форте Н в первоначальной дозе: 2 капсулы 3 раза в день в течение 3 недель с переходом на поддерживающую дозу: 1 капсула 3 раза в день в течение 6 месяцев. Препарат Эссенциале® форте Н наиболее широко используется практикующими врачами и представляет собой наилучшую комбинацию эссенциальных фосфолипидов, активным действующим веществом которого является высокоочищенная фракция фосфатидилхолина.
Если рассматривать патогенез НАЖБП с позиции теории множественных ударов (multi-hit), то препараты ЭФЛ воздействуют на многие звенья патогенеза НАСГ. Так, при НАСГ повышается проницаемость мембран гепатоцитов и других клеточных структур, таких как митохондрии. Полиненасыщенный фосфатидилхолин (ПФХ) за счет способности конкурентно замещать эндогенный фосфолипид фосфатидилхолин клеточных мембран и встраиваться в фосфолипидную структуру поврежденных печеночных клеток замещает дефекты и восстанавливает барьерную функцию липидного слоя клеточных мембран, стимулирует синтез эндогенных фосфолипидов, тем самым обусловливая мембраностабилизирующий эффект.
Также ПФХ повышает энзиматическую активность и текучесть биологических мембран, что приводит к нормализации их проницаемости и улучшению обменных процессов. Окислительный стресс при НАСГ возникает в результате невозможности подвергнуть митохондриальному бета-окислению большое количество жирных кислот, содержащихся в гепатоците. В условиях стеатоза функциональные способности митохондрий истощаются, включается альтернативное микросомальное окисление липидов системой цитохрома Р 450 2Е1, что приводит к образованию свободных радикалов и реактивных форм кислорода (РФК). Возникший «окислительный» стресс повышает продукцию провоспалительных агентов, и развивается воспалительная реакция в печени — стеатогепатит.
Препараты ЭФЛ повышают активность фосфолипидзависимых ферментов, в частности цитохромоксидазы, которая способствует нейтрализации свободных радикалов и снижению выраженности окислительного стресса. При окислительном стрессе и повреждении митохондрий наблюдается некроз печеночных клеток или же гибель гепатоцитов по механизму Fas-опосредованного апоптоза [16]. ПФХ понижают синтез противовоспалительных цитокинов, что актуально при НАСГ. В результате повышения активности коллагеназы ПФХ замедляют синтез коллагена, предупреждают трансформацию звездчатых клеток в коллагенпродуцирующие, подавляют трансформацию клеток печени в фибробласты, что крайне тормозит фиброгенез у больных НАСГ (рис. 4).
Кроме того, Эссенциале® форте Н имеет дополнительные «полезные» эффекты для терапии НАЖБП с сопутствующей дислипидемией и МС. Гипогликемический эффект и уменьшение гиперинсулинемии обеспечиваются улучшением функции инсулиновых рецепторов и трансмембранного сигнала в инсулиновых клетках-мишенях. Нормализация липидного обмена (за счет влияния на фосфолипидзависимые ферменты) происходит за счет влияния на ферменты липидного метаболизма. ЭФЛ повышают активность ЛП-липазы, ответственной за внутрисосудистое расщепление липопротеинов очень низкой плотности (ЛПОНП), что приводит к снижению общего холестерина и триглицеридов. Под влиянием ЭФЛ активируется лецитинхолестеринацилтрансфераза, которая участвует в эстерификации холестерина в ЛПВП, что повышает акцепторные свойства ЛПВП [17].
На фоне проводимой терапии через 6 месяцев отмечалось клиническое улучшение: состояние удовлетворительное, головные боли отмечаются редко, масса тела снизилась со 100 кг до 86 кг, ОТ уменьшился на 15 см и составил 98 см, АД 125/80 мм рт. ст. Нормализовался уровень печеночных трансаминаз: АСТ — 22 ед/л, АЛТ — 30 ед/л; липидный спектр: ОХ — 180 мг/дл, ТГ — 150 мг/дл, ЛПВП — 56 мг/дл, ЛПНП — 100 мг/д, глюкоза — 100 мг/дл, индекс НОМА снизился с 5,2 до 3,3.
Заключение
Таким образом, представленный клинический случай демонстрирует пример успешного лечения НАЖБП и дислипидемии у тучной больной. Еще раз хочется подчеркнуть, что у больных ожирением наблюдается множественная сочетанная патология. С учетом новых данных о тесном взаимодействии ССЗ и НАЖБП при лечении таких больных целесообразно применять препараты, воздействующие непосредственно как на этапы формирования НАЖБП, так и благотворно влияющие на другие патогенетические составляющие НАЖБП и ССЗ при ожирении и МС. В этой связи препараты, содержащие эссенциальные фосфолипиды, могут иметь приоритетное значение в терапии НАСГ при ожирении.
Литература
Первый МГМУ им. И. М. Сеченова, Москва






.jpg)
.jpg)
.jpg)