что такое клиническая картина болезни
Современные представления о периодической болезни и клинические рекомендации по диагностике и лечению
В статье представлены современные сведения о патогенезе, клинических проявлениях, диагностике и лечении периодической болезни. Обсуждаются клинические и лабораторные методы оценки активности заболевания и подходы к лечению больных, резистентных к колхицину, на основе подавления эффектов интерлейкина-1.
Периодическая болезнь (ПБ), более известная в англоязычной литературе под названием Средиземноморская лихорадка, является древнейшим заболеванием. Первые наблюдения ПБ были описаны еще на закате средневековья. Так, H. Reimann указывает, что в 1629 г. Aubrey сообщил о своем страдании, которое проявлялось ознобом, тошнотой, рвотой, болями в животе, длящимися до полусуток и возникающими сначала каждые 2 недели, позже ежемесячно, один раз в 3 месяца, один раз в полгода [1].
Как самостоятельная нозологическая единица ПБ была выделена только в середине ХХ столетия. В 1948 г. H. Reimann на основании 6 наблюдений объединил общим термином “периодическая болезнь” ряд синдромов, включающих периодическую лихорадку, доброкачественный пароксизмальный перитонит, циклическую нейтропению и перемежающуюся артралгию [2]. Основными критериями считали периодичность и доброкачественность течения. По этой причине понятие “периодическая болезнь” стало очень широким. Благодаря работам E. S):1–112. ohar и соавт. (1967) [3], а в нашей стране – О.М. Виноградовой (1964, 1973) [4], В.А. Аствацатрян и соавт. [5] клиническая картина ПБ была очерчена более отчетливо. После открытия гена MEFV, мутации которого приводят к развитию клинических проявлений ПБ, были сформулированы окончательные критерии ПБ.
Тем не менее, сохраняет актуальность выделение особого обобщающего термина для всех периодических синдромов, клинические проявления и принципы диагностики которых сходны. Учитывая их наследственный характер, широко применяется термин семейные периодические лихорадки, которые, помимо ПБ, включают в себя криопиринопатии (семейная холодовая крапивница, синдром Макла-Уэллса, NOMID-CINCA синдром), гипериммуноглобулинемию D (дефицит мевалонаткиназы), TRAPS):1–112. (синдром, обусловленный мутацией гена рецептора к фактору некроза опухоли [ФНО]-α) и некоторые другие. Все эти заболевания характеризуются беспричинно повторяющимися приступами лихорадки в сочетании с воспалением кожи, серозных оболочек и суставов [4]. В основе патогенеза ведущую роль играют генетически детерминированные нарушения врожденного иммунитета, а механизмы специфического иммунитета – гуморального, связанного с синтезом аутоантител, и Т-клеточного, не имеют значения [5].
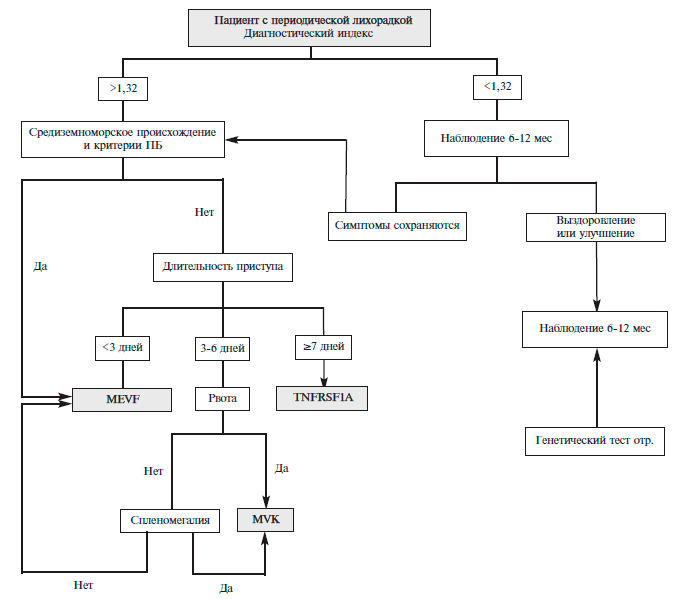
Клиническое предположение о наличии этих синдромов может возникать преимущественно у молодых пациентов с приступами болей в животе, грудной клетке в сочетании с афтозным стоматитом, диареей при наличии подобных признаков у родственников (табл. 1) [8]. Для оценки риска семейных периодических лихорадок предложен специальный индекс [9], автоматизированный расчет которого, предлагается на сайте Eurofever Project (https://www.printo.it/eurofever/index. asp). Паци ен там с высоким риском следует проводить генетическое тестирование для исключения семейных периодических лихорадок. У выходцев из Средиземно морья и Кавказа с непродолжительными приступами (менее 3 дней) в первую очередь следует исключать ПБ, у остальных пациентов с длительностью приступов до недели и эпизодами рвоты следует думать о дефиците мавалонаткиназы с развитием гипериммуноглобулинемии D, приступы длительностью более недели являются основанием для исключения TRAPS):1–112. (рис. 1). У пациентов с низким риском предлагается наблюдение за течением болезни с последующим повторным обсуждением показаний к генетическому исследованию на семейные периодические лихорадки.
Эпидемиология периодической болезни
Одним из признаков наследственной природы ПБ является этноассоциированный характер болезни – ее широкое распространение у народов, проживающих в бассейне Средиземного моря – армян, евреев-сефардов и, реже, арабов, турков, была показана разными авторами на больших группах больных. По данным О.М. Ви но градовой лица других национальностей среди больных ПБ встречались лишь в 2% случаев [4]. Среди 86 носителей гена ПБ, наблюдавшихся J. S):1–112. amuels и соавт. [10], необычно высоким было число итальянцев и евреев-ашкенази. Однако и в этой группе 96% пациентов оказались представителями средиземноморской популяции. В группе из 150 больных ПБ, обследованных О.М. Виноградовой [4], 88,6% составили армяне. В последние годы эту болезнь на территории России широко диагностируют у азербайджанцев, представителей разных народов Северного Кавказа, имеются также отдельные наблюдения ПБ среди русских и украинцев, преимущественно жителей южных регионов России. Болезнь наследуется по аутосомно-рецессивному пути. Это означает, что у родителей симптомы заболевания обычно отсутствуют, однако в больших семьях болезнь может проявиться у родных или двоюродных братьев/ сестер, дяди или дальнего родственника.
Ген, ответственный за ПБ, был клонирован в 1997 году и обозначен аббревиатурой MEFV (MEditerranean FEver) [11,12], в том же году были идентифицированы 8 основных мутаций гена. Ген MEFV располагается на коротком плече 16 хромосомы центромерно к гену гемоглобина- α, рядом с генами, ответственными за аутосомно-доминантный поликистоз почек и туберозный склероз 12. Показано, что среди евреев-сефардов, выходцев из Испании, частота носительства MEFV составляет от 1:16 до 1:8 (при распространенности ПБ в этой популяции от 1:250 до 1:1000) [15]. Частота носительства среди евреев-ашкенази Южной Европы почти на 2 порядка ниже – 1:135 (при распространенности ПБ 1:73000). Частота носительства среди американских армян составляет 1:7 [16].
Причина сохранения в современной средиземноморской популяции высокой частоты носительства MEFV остается неясной, однако сочетание ее с многочисленностью аллелей MEFV может свидетельствовать в пользу благоприятных условий для естественного отбора гетерозигот-носителей этих аллелей, по аналогии с распространенностью гена серповидноклеточной анемии в эндемичных очагах малярии.
Клиническая картина и диагноз
Продуктом MEFV является белок пирин, или маренострин (от латинского Mare Nostrum – Средиземное море) [11,12]. Одним из отличительных свойств пирина является наличие В30.2-домена. Кроме того, в молекуле пирина обнаружены 2 локуса потенциального связывания с ядром, а α-спиральный и В-box-домены могут обеспечивать взаимодействие с другими белками. Все выявленные в настоящее время мутации, ассоциирующиеся с ПБ, касаются изменений в В30.2-зоне пирина.
Экспрессия MEFV происходит почти исключительно в гранулоцитах и не наблюдается в лимфоцитах и моноцитах [11]. Не обнаруживают экспрессию гена и в других тканях. Согласно основной в настоящее время рабочей гипотезе пирин является базовым регулятором воспалительного ответа нейтрофилов. Соответ ственно, структурные изменения в молекуле пирина могут изменить функцию контроля и способствовать постоянному провоспалительному потенциалу нейтрофилов.
Немутантный пирин ингибирует адапторный белок AS):1–112. C, который кроме участия в апоптозе формирует ядро инфламмасомного комплекса путем гомотипического взаимодействия с белком NLRP и каспазой, что ведет к активации интерлейкина (ИЛ)-1 β. Инфламма сома – макромолекулярная платформа в цитоплазме, устойчивая к внутриклеточным механизмам деградации белков и, в силу этого, способная обеспечить реализацию провоспалительной активности клетки. Суще ствует несколько разновидностей инфламмасом. При ПБ и других семейных периодических лихорадках основное значение придают инфламмасоме на основе белка NLRP3 – криопирина. В качестве основной причины развития ПБ рассматривают утрату ингибиторного эффекта мутантного пирина на AS):1–112. C и, как следствие, активацию каспазы-1 [17], либо формирование пирином собственной инфламмасомы [18]. Однако роль мутаций домена B30.2 в развитии ПБ остается спорной; возможно, пирин может проявлять как про-,так и противовоспалительные свойства в зависимости от конкретных условий. Значение мутантного пирина в усилении секреции ИЛ-1 β при ПБ подтверждается купированием приступа ПБ при парентеральном введении ингибиторов ИЛ-1 [19].
Таким образом, в настоящее время несомненным диагностическим критерием ПБ является выявление гомозиготного носительства мутаций пирина. Однако у 20% больных клинические признаки ПБ развиваются при наличии только одной мутации. У таких пациентов сохраняют диагностическое значение клинические критерии болезни, в частности эффективность колхицина. Окончательный диагноз в этом случае может быть установлен только через 6-12 месяцев наблюдения за эффектом колхицина.
Важное значение имеет осмотр пациента во время периодических приступов заболевания, которые проявляются лихорадкой в сочетании с абдоминалгиями, торакалгиями, артралгиями и другими, более редкими, проявлениями. Указанные проявления могут возникать в различных сочетаниях или с разной периодичностью, обычно выделяют абдоминальный, торакальный, лихорадочный, реже суставной варианты ПБ.
Болезнь возникает преимущественно в детском или юношеском возрасте, чаще у мужчин, и характеризуется хроническим течением с обострениями и ремиссиями, возникающими от разнообразных причин и через различные сроки. Между приступами болезненные проявления отсутствуют, а во время приступа болезни многие пациенты сохраняют работоспособность. Приступы продолжаются от 12 ч до 3 суток, а затем самостоятельно разрешаются. Продолжительность межприступного периода у одного и того же пациента составляет от нескольких дней до нескольких месяцев, иногда приступы следуют один за другим с промежутками в 1-3 дня, но возможны и длительные ремиссии до нескольких лет. Характерный признак болезни, имеющий диагностическое значение, – стереотипность приступов. Пациенту, как правило, без труда удается отличить боль и лихорадку, вызванные приступом болезни, от подобных симптомов другого генеза.
Лихорадка, которая у нелеченных больных, как правило, достигает высоких значений и сопровождается потрясающими ознобами, является практически постоянным симптомом приступа. Выделение особой лихорадочной формы болезни обосновывается тем, что другие симптомы, включая абдоминалгии, встречаются реже. Однако В.М. Арутюнян и соавт. полагают, что острый асептический серозит, хотя бы и кратковременный, является облигатным проявлением болезни, в связи с чем нецелесообразно расширять классификацию болезни за счет лихорадочной и суставной форм, а достаточно ограничиться тремя формами – абдоминальной, торакальной и смешанной [20].
Абдоминальный вариант наблюдается у 91% больных [11,12]. В основе абдоминального варианта ПБ лежит рецидивирующее доброкачественное воспаление серозной оболочки брюшной полости с преобладанием экссудативной реакции над пролиферативной, что подтверждается малым количеством спаек, несмотря на частоту приступов. В воспалительный процесс вовлекаются брыжейка, серозная оболочка кишки, печени, селезенки, диафрагмы. Абдоминалгии обычно сопровождаются симптомами раздражения брюшины и вялой перистальтикой, что наряду с лихорадкой и лейкоцитозом периферической крови создает существенные дифференциально-диагностические сложности и ведет к необоснованной лапаротомии.
Торакальный вариант, в основе которого лежит асептический плеврит, наблюдается у 57% пациентов [11, 12]. При рентгеноскопии грудной клетки во время приступа отмечают ограничение подвижности купола диафрагмы, небольшой выпот в синусе над диафрагмой, реже дисковидные ателектазы, все эти явления затем полностью исчезают, но у трети больных возникают спайки.
Артрит и артралгии развиваются у 45% больных [11,12], очень редко как единственное проявление болезни. Суставные проявления имеют характер летучих артралгий, моноартрита, реже полиартрита, чаще вовлекаются коленные и голеностопные суставы. По окончании приступа эти явления полностью исчезают, не оставляя пролиферативных изменений. Ревматоид ный фактор, антистрептококковые антитела не определяются.
Редко (13%) встречается рожеподобная эритема в виде болезненных плотноватых пятен диаметром 10-15 см обычно в области голеностопных суставов [11,12].
Самым тяжелым осложнением является АА-амилоидоз, строящийся из циркулирующего белка-предшественника S):1–112. AA, близкого С-реактивному белку. Частота амилоидоза значительно отличается по данным разных авторов. О.М. Виноградова на примере популяции бывшего СССР указывает частоту амилоидоза 41,3%. Аме риканские авторы, обследовавшие популяцию армян, проживающих в США, сообщают о низкой частоте амилоидоза – 2% [8,21]. В любом случае, прогноз болезни определяется наличием и тяжестью амилоидоза. Клинические проявления амилоидоза характерны для АА-типа, при котором основным органом-мишенью являются почки. В течении амилоидной нефропатии обычно удается выделить три стадии – протеинурическую, нефротическую и стадию почечной недостаточности. Особенностью амилоидоза является сохранение высокой протеинурии на стадии хронической почечной недостаточности [22]. Нелеченный ААамилоидоз в рамках ПБ обычно прогрессирует быстрее, чем при других воспалительных заболеваниях: 5- и 10летняя выживаемость составляет соответственно 48% и 24%, соответственно, а при вторичном АА-амилоидозе другой этиологии – 77% и 44% [23].
Широко распространено мнение о наследственном характере амилоидоза при ПБ. Так, у больных ПБ с отягощенным по амилоидозу семейным анамнезом риск амилоидоза увеличивается в 6 раз [24]. Описан так называемый фенотип II ПБ (некоторые исследователи ставят под сомнение наличие фенотипа II, учитывая его исключительную редкость [25]), при котором клинически выраженных приступов не бывает, однако развивается АА-амилоидоз. При этом у родственников нередко регистрируется клиника несомненной ПБ.
Благодаря обнаружению в последние годы гена ПБ и его продукта – белка пирина показаны различные механизмы наследования ПБ и АА-амилоидоза. Пирин непосредственно не участвует в метаболизме S):1–112. AA, а гены обоих белков располагаются в разных хромосомах (гены S):1–112. AA обнаружены в 11 хромосоме). Таким образом, ПБ в настоящее время, подобно другим хроническим воспалительным процессам, рассматривают в качестве пускового фактора вторичного АА-амилоидоза.
У больных ПБ описаны единичные наблюдения асептического менингита, перикардита, миалгий, узелкового полиартериита, гломерулонефрита, пурпуры Шенлейн-Геноха, клиническое значение которых не вполне ясно [4]. Спленомегалия, как правило, сопутствует амилоидозу [4].
Оценка активности аутовоспалительных заболеваний
Первая попытка создания критериев активности аутовоспалительных заболеваний была предпринята группой ученых из Клиники Шиба (Израиль) в отношении ПБ [26]. В разработанной ими шкале учитываются возраст на момент начала заболевания, частота приступов, наличие артритов, рожеподобной эритемы и доза колхицина, необходимая для достижения ремиссии болезни. В 2005 г. ученые из той же клиники провели дополнительное исследование, в котором показали недостаточность этой шкалы для корректной оценки активности болезни [27]. С использованием статистических методов были разработаны новые критерии тяжести ПБ (модифицированные критерии Тель Хашомер), которые отличаются для больных, принимающих и не принимающих колхицин [27].
Эксперты рабочих групп EUROFEVER и EUROTRAPS):1–112. попытались разработать единые критерии активности семейных периодических лихорадок с использованием дельфийского метода и метода номинальных групп [28]. Для каждого заболевания были выделены симптомы, которые, по мнению экспертов и опрошенных больных, свидетельствуют о его высокой активности. В опроснике для больных содержатся ежедневные сведения о наличии и выраженности симптомов в баллах. По завершении месяца сумма баллов делится на количество дней в месяце (30 или 31): максимальной активности соответствует 13 баллов для криопиринопатий и 16 баллов для ПБ, HIDS):1–112. и TRAPS):1–112.
Традиционными методами подтверждения воспалительной природы заболевания и оценки его активности являются подсчет лейкоцитов крови и измерение показателей острофазового воспаления – СОЭ, уровня С-реактивного белка (СРБ), фибриногена и других.
Нередко при аутовоспалительных заболеваниях развивается анемия, как правило, нормохромная нормоцитарная, которая является следствием хронического воспаления (анемия хронических заболеваний). Веду щую роль в ее патогенезе играют провоспалительные цитокины – ФНО-α, ИЛ-1β, ИЛ-6 и интерферон-g [30,31]. Так, ФНО-α снижает эритропоэз за счет непосредственного блокирующего действия на рост эритроидных клеток-предшественниц и активации их апоптоза в костном мозге [32–34]. ИЛ-6 также подавляет костномозговую пролиферацию эритроидных клеток-предшественниц, снижает синтез эритропоэтина, через стимуляцию печеночной продукции гепсидина блокирует макрофагальное депо железа и его абсорбцию энтероцитами [35].
В последнее время исследователи стали уделять внимание новому показателю активности воспаления – отношению нейтрофилы/лимфоциты – ОНЛ (в норме оно равно 0,78-3,53 с медианой 1,65) [36]. Это надежный маркер, который может быть легко определен по результату клинического анализа крови. В настоящее время показана способность этого показателя отражать активность воспаления при ПБ. А. Ahsen и соавт. определяли ОНЛ и концентрацию СРБ у 62 больных ПБ в стадии ремиссии и 41 здорового человека [37]. Как ОНЛ, так и концентрация СРБ у больных с ремиссией ПБ были выше, чем у здоровых людей. Отмечена умеренная корреляция между этими параметрами (r=0,449, p
Лечение периодической болезни
Несмотря на наследственный характер ПБ в настоящее время существуют эффективные методы ее лечения. С 1970 г. в практику вошел колхицин, который позволил не только предупреждать приступы болезни, но также проводить лечение и профилактику амилоидоза, что существенно улучшило прогноз больных. Механизм противовоспалительного действия колхицина может быть связан с торможением дегрануляции полиморфноядерных лейкоцитов, способностью уменьшать продукцию ИЛ-1, снижать проницаемость сосудистой стенки. Известный цитостатический эффект колхицина в применяемых дозах, по-видимому, незначителен. Ежедневный прием 1-2 мг колхицина позволяет прово дить надежную профилактику приступов ПБ и амилоидоза. Терапевтическая доза при уже развившемся амилоидозе составляет 2 мг/сут. По данным клиники им. Е.М. Тареева колхицин эффективен даже у большинства больных с нефротическим синдромом, однако эффект наступает не сразу, спустя 2-4 года постоянного приема колхицина. Эффективность препарата при амилоидозе почек резко снижается на стадии почечной недостаточности, свидетельствующей о тяжести склеротических изменений.
Указанные дозы обычно хорошо переносятся, в том числе при многолетнем приеме. Нередко развивающаяся в начале лечения диарея носит преходящий характер и, как правило, не требует полной отмены препарата.
Приблизительно у 15-20% больных колхицин оказывается изначально неэффективным. Представление о ПБ как о внешней инфламмасомопатии позволило рекомендовать назначение ингибиторов ИЛ-1 пациентам, резистентным к лечению колхицином. В Рос сийской Федерации зарегистрирован канакинумаб (Иларис®) – человеческие моноклональные IgG1 антитела к ИЛ-1, которые связываются с цитокином и блокируют его взаимодействие с рецепторами. Канакинумаб обладает длительным периодом полувыведения (21-28 дней), что позволяет вводить его подкожно каждые 8 недель. Рекомендуемая стартовая доза у взрослых составляет 150 мг один раз в 4 недели, при необходимости ее можно увеличить до 300 мг.
Эффективность и безопасность канакинумаба изучались у больных с различными аутовоспалитель ными заболеваниями. В двойном слепом, плацебоконтролируемом, рандомизированном исследовании, состоявшем из 3 час тей, 35 пациентов с криопиринассоциированным периодическим синдромом (КАПС; синдром Макла-Уэллса у 33 и синдром NOMID/CINCA у 2) получали канакинумаб в течение 48 недель [52]. Во время части 1 всем пациентам вводили канакинумаб в дозе 150 мг подкожно. Если в течение 15 дней после введения препарата наблюдался полный ответ (отсутствие активности или минимальная активность по оценке исследователя и концентрации СРБ и S):1–112. AA ТАБЛИЦА 1. Эффективность канакинумаба в исследовании CLUSTER
Заключени
Представленная нами проблема ПБ демонстрирует достижения молекулярно-биологических исследований в современной практической медицине, показывает возможности диагностики и лечения на основе знаний о молекулярных механизмах ПБ. Последнее особенно важно с практических позиций, поскольку возможность выделения аутовоспалительных реакций с центральной ролью нейтрофила среди патофизиологических механизмов позволяет определить критерии индивидуального подхода к лечению с выбором патогенетически обоснованного средства подавления активности ПБ. Главным препятствием в диагностике и лечении больных ПБ остается низкая информированность врачей об этом заболевании, хотя в этнических группах высокого риска заболевание встречается с частотой 1-3 на 1000.
Болезнь Иценко-Кушинга
Болезнь Иценко-Кушинга (БИК) — это тяжелое многосимптомное заболевание гипоталамо-гипофизарного генеза, протекающее с проявлениями клинической картины гиперкортицизма, обусловленное наличием опухоли гипофиза или его гиперплазии и характеризующееся повыше
Болезнь Иценко-Кушинга (БИК) — это тяжелое многосимптомное заболевание гипоталамо-гипофизарного генеза, протекающее с проявлениями клинической картины гиперкортицизма, обусловленное наличием опухоли гипофиза или его гиперплазии и характеризующееся повышенной секрецией адренокортикотропного гормона (АКТГ), увеличением продукции гормонов корой надпочечников.
Считается, что при БИК у 85% больных имеется аденома передней доли гипофиза (кортикотропинома), что, по современным представлениям, является первопричиной заболевания. Кортикотропиномы характеризуются небольшими размерами. Это так называемые микроаденомы, располагающиеся внутри турецкого седла. Макроаденомы встречаются при БИК значительно реже. У 15% пациентов с БИК находят диффузную или узелковую гиперплазию АКТГ-продуцирующих клеток (кортикотрофов). Редко у больных БИК обнаруживается первичное «пустое» турецкое седло, либо никаких изменений в этой области на КТ и МРТ не выявляется.
Этиология и патогенез
Причина болезни Иценко-Кушинга точно не установлена. БИК чаще встречается у женщин, редко диагностируется в детском и пожилом возрасте. У женщин заболевание развивается в возрасте от 20 до 40 лет, есть зависимость от беременности и родов, а также от травм головного мозга и нейроинфекций. У подростков БИК часто начинается в период полового созревания.
Установлено, что большинство таких опухолей по своей природе являются моноклональными, что свидетельствует о наличии генных мутаций в исходных клетках.
В онкогенезе АКТГ-продуцирующих опухолей гипофиза важная роль принадлежит аномальной чувствительности гипофиза к гипоталамическим факторам. Усиление стимулирующего действия нейрогормонов или ослабление ингибирующих сигналов имеет значение в процессах образования и роста опухоли гипофиза. Нарушение действия ингибирующих нейрогормонов, таких, как соматостатин и допамин, может сопровождаться усилением деятельности стимулирующих нейрогормонов. Кроме того, имеются данные, свидетельствующие о том, что неконтролируемая клеточная пролиферация опухолей гипофиза может стать результатом нарушения действия ростовых факторов.
Потенциальным механизмом развития кортикотропином может стать спонтанная мутация генов рецепторов КРГ или вазопрессина.
Автономная секреция АКТГ опухолью приводит к гиперфункции коры надпочечников. Поэтому основная роль в патогенезе БИК отводится повышению функции коры надпочечников. При АКТГ-зависимой форме болезни Иценко-Кушинга имеет место повышение функциональной активности всех трех зон коры надпочечников: изменения в клетках пучковой зоны ведут к гиперсекреции кортизола, клубочковой — к повышению альдостерона и сетчатой — к усилению синтеза дегидроэпиандростерона (ДГЭС).
Для болезни Иценко-Кушинга характерно не только повышение функционального состояния коры надпочечников, но и увеличение их размеров. В 20% случаев на фоне гиперплазии надпочечников обнаруживаются вторичные аденомы небольших размеров (1–3 см).
При кортикотропиномах кроме гиперсекреции АКТГ наблюдается нарушение функции гипофизарных гормонов. Так, базальная секреция пролактина у больных с БИК нормальная или незначительно повышена. Соматотропная функция гипофиза у больных с кортикотропиномами снижена. Стимулирующие тесты с инсулиновой гипогликемией, аргинином и L-Допа показали снижение резервов СТГ при болезни Иценко-Кушинга. Уровень гонадотропных гормонов (ЛГ, ФСГ) у больных снижен. Это обусловлено прямым супрессивным действием избытка эндогенных кортикостероидов на секрецию рилизинг-гормонов гипоталамусом.
Клиническая картина
Клиническая картина болезни Иценко-Кушинга обусловлена избыточной секрецией кортикостероидов и, в первую очередь, глюкокортикоидов. Увеличение массы тела характеризуется своеобразным («кушингоидный» тип ожирения) неравномерным перераспределением подкожно-жировой клетчатки в области плечевого пояса, надключичных пространств, в области шейных позвонков («климактерический горбик»), живота, при сравнительно тонких конечностях. Лицо становится круглым («лунообразное»), щеки — багрово-красного цвета («матронизм»). Кроме того, при БИК наблюдаются трофические изменения кожи. При осмотре кожные покровы истонченные, сухие с наклонностью к гиперкератозу и имеют багрово-цианотичную окраску. На бедрах, груди, плечах, животе появляются своеобразные полосы растяжения (стрии) красно-фиолетового цвета. Характер стрий — «минус» ткань. Эти стрии отличаются от бледных или розовых полос растяжения, которые встречаются при ожирении, в период беременности или родов. Появление стрий при БИК связано с нарушением белкового обмена (катаболизм белков), в результате чего кожа истончается. Наличие гематом при незначительных травмах является следствием повышенной ломкости капилляров и истончения кожи. Наряду с этим отмечается гиперпигментация кожных покровов в местах трения (шея, локтевые суставы, подмышечные впадины). У женщин часто наблюдается повышенное оволосение (гирсутизм) на лице (усы, борода, бакенбарды) и груди. Половые расстройства в виде вторичного гипогонадизма являются одним из ранних симптомов при БИК.
В симптомокомплексе БИК наиболее существенным в клинической картине заболевания является поражение сердечно-сосудистой системы. Сочетание артериальной гипертонии с нарушениями метаболизма в сердечной мышце приводит к хронической недостаточности кровообращения и другим изменениям со стороны сердечно-сосудистой системы. Миопатия часто является характерным симптомом гиперкортицизма, который выражается дистрофическими изменениями мышц и гипокалиемией. Атрофические процессы, затрагивающие поперечно-полосатую и мышечную систему, особенно заметны в верхних и нижних конечностях («истончение» рук и ног). Атрофия мышц передней брюшной стенки ведет к увеличению живота.
Содержание калия в эритроцитах и мышечной ткани (в том числе и в миокарде) значительно снижено. Нарушения электролитного обмена (гипокалиемия и гипернатриемия) лежат в основе электролитно-стероидной кардиопатии и миопатии. При БИК нарушения углеводного обмена различной степени выраженности наблюдаются у большого числа больных. При этом у 70–80% пациентов выявляется нарушенная толерантность к глюкозе, а у остальных — сахарный диабет 2 типа. Клинические проявления диабета характеризуются гиперинсулинемией, инсулинорезистентностью и отсутствием склонности к кетоацидозу. Диабет имеет, как правило, благоприятное течение, и для его компенсации достаточно назначения диеты и пероральных сахароснижающих препаратов.
Вторичный иммунодефицит проявляется гнойничковыми (акне) или грибковыми поражениями кожи и ногтевых пластин, трофическими язвами голеней, длительным периодом заживления послеоперационных ран, хроническим и трудно поддающимся лечению пиелонефритом. Энцефалопатия в виде изменения вегетативной нервной системы при БИК ярко выражена и многообразна. Синдром вегетативной дистонии характеризуется эмоционально-личностными сдвигами: от нарушения настроения, сна и до выраженных психозов.
Системный остеопороз представляет собой распространенное и нередко тяжело протекающее проявление гиперкортицизма при БИК в любом возрасте. Остеопороз является причиной болей в позвоночнике, часто приводит к снижению высоты тел позвонков и спонтанным переломам ребер и позвонков.
В зависимости от выраженности гиперкортицизма и формирования клинических симптомов различают несколько степеней тяжести БИК. Легкая форма характеризуется умеренной выраженностью симптомов заболевания; средняя — выраженностью всех симптомов при отсутствии осложнений. Тяжелая форма отличается выраженностью симптомов и наличием осложнений (сердечно-легочная недостаточность, стероидный диабет, прогрессирующая миопатия, патологические переломы, тяжелые психические расстройства). В зависимости от скорости нарастания клинической симптоматики различают быстропрогрессирующее (три–шесть месяцев) и торпидное течение заболевания, которое проявляется сравнительно медленным (от одного года и более) развитием гиперкортицизма.
При подозрении на БИК необходимо проверить, имеется ли у больного гиперкортицизм, затем провести дифференциальную диагностику форм гиперкортицизма (БИК, АКТГ-эктопированный синдром, синдром Иценко-Кушинга), сходных синдромов (ожирение, метаболический синдром, пубертатно-юношеский диспитуитаризм, алкогольное поражение печени) и установить локализацию основного патологического процесса.
Диагноз и дифференциальный диагноз
При подозрении на болезнь Иценко-Кушинга после сбора анамнеза и клинического осмотра у всех больных с помощью методов лабораторной диагностики необходимо подтвердить наличие гиперкортицизма. На первом этапе выявляется повышенная продукция кортизола. С этой целью определяют суточный ритм секреции кортизола в плазме крови утром (8.00-9.00) и вечером (23.00-24.00). Для больных БИК характерно повышение утреннего уровня кортизола в плазме крови, а также нарушение ритма секреции кортизола, т. е. в ночное или вечернее время уровень кортизола остается повышенным. Определение суточной экскреции свободного кортизола в моче является также необходимым методом лабораторной диагностики для подтверждения гиперкортицизма. Уровень свободного кортизола в моче определяется РИА-методом. Для здоровых лиц содержание кортизола колеблется от 120 до 400 нмоль/с. У больных с БИК экскреция кортизола в суточной моче повышена.
В сомнительных случаях для дифференциальной диагностики между патологическим эндогенным и функциональным гиперкортицизмом проводится малая проба с дексаметазоном. Она основана на подавлении продукции эндогенного АКТГ высокими концентрациями кортикостероидов по принципу обратной связи. Если секреция кортизола не снижается на 50% и более от исходного уровня, это свидетельствует о наличии гиперкортицизма.
Таким образом проводится дифференциальная диагностика патологического и функционального гиперкортицизма.
При выявлении повышенной продукции кортизола необходимо провести следующий этап обследования — дифференциальную диагностику между формами эндогенного патологического гиперкортицизма (БИК, СИК, АКТГ-эктопированный синдром), болезнью Иценко-Кушинга, АКТГ-эктопированным синдромом и синдромом Иценко-Кушинга. Этот этап обследования включает в себя определение ритма секреции АКТГ в плазме крови и проведение большой пробы с дексаметазоном.
Для БИК характерны нормальное или повышенное (до 100 –200 пг/мл) утреннее содержание АКТГ и отсутствие его снижения в ночное время. При АКТГ-эктопированном синдроме секреция АКТГ повышена и может колебаться от 100 до 200 пг/мл и выше, и при этом также отсутствует ритм его секреции. При АКТГ-независимых формах гиперкортицизма (синдром Иценко-Кушинга, макро- или микроузелковая дисплазия надпочечников) утреннее содержание АКТГ, как правило, снижено при отсутствии ритма его секреции.
Большая проба с дексаметазоном в настоящее время широко применяется для диагностики патологического гиперкортицизма.
При БИК, как правило, происходит снижение уровня кортизола на 50% и более от исходного уровня, тогда как при АКТГ-эктопированном синдроме это наблюдается лишь в редких случаях. При АКТГ-независимых формах синдрома Иценко-Кушинга указанного снижения уровня кортизола также не отмечается, так как продукция гормонов опухолью не зависит от гипоталамо-гипофизарных взаимоотношений.
В зарубежной литературе для диагностики БИК широко используется проба с кортиколиберином (КРГ). Введение КРГ приводит к стимуляции секреции АКТГ у больных БИК. При БИК содержание АКТГ в плазме крови увеличивается более чем на 50%, а уровень кортизола на 20% от исходного. При АКТГ-эктопированном синдроме концентрация АКТГ практически не меняется.
Методы топической диагностики при БИК используются для выявления патологического процесса в гипоталамо-гипофизарной области и надпочечниках (диагностика микро- или макроаденомы гипофиза и гиперплазии надпочечников). К таким методам следует отнести рентгенографию костей черепа, КТ или МРТ головного мозга, УЗИ надпочечников и КТ или МРТ надпочечников.
Визуализация кортикотропином представляет собой наиболее диагностически сложную задачу, так как размер их бывает очень небольшой (2–10 мм). При этом в поликлинических условиях в первую очередь проводится рентгенография костей черепа (боковая рентгеновская краниограмма) с целью выявления рентгенологических признаков аденомы гипофиза. Существуют следующие явные или косвенные признаки аденомы гипофиза: изменение формы и увеличение размеров турецкого седла, локальный или тотальный остеопороз спинки седла, «двухконтурность» дна, выпрямление передних и задних клиновидных отростков.
В настоящее время магнитно-резонансную томографию и/или компьютерно-томографическое исследование принято считать основными методами диагностики аденомы гипофиза. Методом выбора при визуализации кортикотропином является МРТ или МРТ с контрастированием. Преимуществами этого метода, по сравнению с КТ, можно считать лучшую выявляемость микроаденомы гипофиза и синдрома «пустого» турецкого седла, который может встречаться при болезни Иценко-Кушинга.
Лечение БИК
Лечение БИК должно быть направлено на исчезновение основных клинических симптомов гиперкортицизма, стойкую нормализацию уровня АКТГ и кортизола в плазме крови с восстановлением их суточного ритма и нормализацию кортизола в суточной моче.
Все методы лечения болезни Иценко-Кушинга, которые используются в настоящее время, можно разделить на четыре группы: нейрохирургическое (транссфеноидальная аденомэктомия), лучевое (протонотерапия, γ-терапия), комбинированное (лучевая терапия в сочетании с односторонней или двусторонней адреналэктомией) и медикаментозное лечение. Из них основные виды — нейрохирургическое, лучевое и комбинированное; медикаментозная терапия применяется как дополнение к ним.
В настоящее время во всем мире предпочтение отдается транссфеноидальной аденомэктомии. Этот метод позволяет добиться быстрой ремиссии заболевания с восстановлением гипоталамо-гипофизарных взаимоотношений у 84–95% больных уже через шесть месяцев. Показанием к аденомэктомии служит четко локализованная (на основании данных КТ или МРТ) опухоль гипофиза. Аденомэктомия может быть проведена повторно, если имеется подтвержденный на КТ или МРТ продолженный рост аденомы гипофиза, в любые сроки после операции. Этот метод характеризуется минимальным количеством осложнений (около 2–3%) и очень низкой послеоперационной летальностью (0–1%).
Адреналэктомия — тотальная одно- или двусторонняя — применяется только в комбинации с лучевой терапией. При крайне тяжелой и прогрессирующей форме заболевания осуществляется двусторонняя адреналэктомия в сочетании с лучевой терапией для профилактики развития синдрома Нельсона (прогрессирование роста аденомы гипофиза при отсутствии надпочечников). После тотальной двусторонней адреналэктомии пациент пожизненно получает заместительную гормональную терапию.
Из методов лучевой терапии в настоящее время используются протонное облучение и дистанционная γ-терапия, при этом предпочтение отдается протонотерапии. Протонное облучение наиболее эффективно в связи с тем, что энергия выделяется в области аденомы гипофиза и при этом окружающие ткани затрагиваются минимально. Абсолютным противопоказанием к проведению протонотерапии является опухоль гипофиза более 15 мм в диаметре и супраселлярное ее распространение с дефектом полей зрения.
γ-терапия как самостоятельный метод лечения применяется в последнее время редко и только при невозможности проведения аденомэктомии или протонотерапии. Эффективность действия этого метода следует оценивать не раньше, чем через 12–15 и более месяцев после проведения курса облучения.
Медикаментозная терапия при БИК должна использоваться в следующих случаях: подготовка пациента к проведению лечения основным методом, облегчение течения послеоперационного периода и сокращение срока наступления ремиссии заболевания. Фармакологические препараты, применяемые с этой целью, делятся на несколько групп: производные аминоглютетимида (мамомит 250 мг, ориметен 250 мг, средняя суточная доза — 750 мг/сут, максимальная суточная доза — 1000–1500 мг/сут), производные кетоконазола (низорал 200 мг/сут, суточная доза — 400–600 мг/сут, максимальная суточная доза — 1000 мг/сут) и производные пара-хлорфенила (хлодитан, лизодрен, митотан, начальная доза — 0,5 г/сут, лечебная доза — 3–5 г/сут). Принципы медикаментозной терапии следующие: после определения степени переносимости лекарственного средства лечение надо начинать с максимальных доз. На фоне приема препарата необходимо осуществлять контроль за содержанием кортизола в плазме крови и суточной моче не реже чем один раз в 10–14 дней. В зависимости от уровня снижения кортизола в каждом конкретном случае подбирается поддерживающая доза препарата. Передозировка препаратами, блокирующими биосинтез стероидов в надпочечниках, может приводить к развитию надпочечниковой недостаточности.
Из препаратов, ингибирующих действие АКТГ, преимущественно используются бромокриптин-парлодел (в дозе 2,5 –5 мг) или отечественный препарат абергин, (в дозе 4–8 мг).
Коррекцию электролитного обмена необходимо проводить как до начала лечения основного заболевания, так и в ранний послеоперационный период. Наиболее целесообразно применение препаратов калия (раствор хлористого калия или таблеток ацетата калия 5,0 г и более в день) в сочетании с спиронолактонами, в частности верошпироном. Рекомендуемая доза верошпирона до 200 мг/сут перорально.
Подходы к лечению артериальной гипертонии при гиперкортицизме такие же, как и при артериальной гипертонии без повышения функции надпочечников. Надо отметить, что у большинства пациентов с БИК не удается достичь оптимального АД без снижения уровня кортизола.
Патогенетический подход к терапии сахарного диабета при гиперкортицизме предполагает эффективное воздействие на основные звенья: инсулинорезистентность периферических тканей и неспособность инсулярного аппарата преодолеть эту резистентность. Обычно предпочтение отдается сульфаниламидным препаратам второго поколения, так как они обладают большей активностью и меньшей гепато- и нефротоксичностью.
Начинать лечение сульфонилмочевинными препаратами следует с минимальной дозы. При необходимости дозу увеличивают, ориентируясь на результаты измерений уровня глюкозы в крови. Если лечение не дает желаемых результатов, следует сменить препарат. Во время лечения любыми сахароснижающими средствами больной должен соблюдать диету. Если лечение максимальными дозами производными сульфонилмочевины (ПСМ) оказывается безрезультатным, можно использовать их комбинацию с бигуанидами. Теоретическое обоснование необходимости комбинированной терапии основывается на том, что препараты этих групп имеют различные точки приложения своего основного действия. Метформин — 400 мг (cиофор — 500 и 850 мг, глюкофаж — 500, 850 и 1000 мг) — единственный на сегодняшний день препарат бигуанидов, который снижает инсулинорезистентность. Инсулинотерапия показана при БИК в тех случаях, когда не удается нормализовать уровень глюкозы в крови с помощью пероральных сахароснижающих препаратов или планируется хирургическое вмешательство. Применяется инсулин короткого действия, препараты средней длительности и длительного действия и их комбинация. Операция должна планироваться на первую половину дня: перед операцией вводят инсулин короткого действия или средней продолжительности действия п/к. Во время операции проводят инфузию 5% глюкозы в/в с добавлением инсулина короткого действия из расчета 5 — 10 ЕД/л, скорость инфузии — 150 мл/ч. Инфузию 5% глюкозы с инсулином короткого действия продолжают и после операции, пока больной не начнет самостоятельно принимать пищу. Затем пациент переводится на пероральные сахароснижающие препараты и осуществляется контроль сахара крови.
Лечение стероидного остеопороза (СОП) даже после ликвидации гиперкортицизма длительное. Препараты для лечения СОП условно можно разделить на три группы: средства, влияющие на процессы костной резорбции, препараты, стимулирующие костное формирование, и препараты многопланового действия. К препаратам, снижающим резорбцию костной ткани, относится кальцитонин (миокальцик). Этот препарат используется в двух лекарственных формах: в ампулах и в виде назального спрея. Курсы длительностью два месяца следует проводить три раза в год. Бисфосфонаты (фосамакс, ксидифон) относятся к препаратам, которые снижают резорбцию костной ткани. При терапии бисфосфонатами рекомендуется дополнительный прием солей кальция (500–1000 мг в сутки). Одним из наиболее эффективных препаратов, стимулирующих костеобразование и увеличивающих массу кости, являются соли фтора. Лечение продолжают от шести месяцев до одного года.
Считается, что анаболические стероиды уменьшают костную резорбцию и индуцируют положительный кальциевый баланс благодаря увеличению абсорбции кальция из кишечника и реабсорбции кальция почками. Кроме того, по некоторым данным, они стимулируют активность остеобластов и увеличение мышечной массы. Они назначаются в основном парентерально, прерывистыми курсами по 25–50 мг один-два раза в месяц в течение двух месяцев три раза в год.
Препараты активного метаболита витамина Д (оксидевит, альфа Д3-Тева) широко применяются при БИК. При СОП они используются в дозе 0,5–1,0 мкг/дн как в качестве монотерапии, так и в комбинации с другими препаратами (Д3+кальцитонин, Д3+соли фтора, Д3+бисфосфанаты). При комплексном лечении БИК и СОП также возможно применение препарата остеопан, содержащего кальций, витамин Д3, магний и цинк, назначая по две таблетки три раза в день.
Симптоматическое лечение СОП включает в себя обезболивающую терапию: анальгетики, назначение нестероидных противовоспалительных средств, а также центральных миорелаксантов, так как на генез боли при СОП оказывает влияние и спазм параспинальных мышц. Соли кальция самостоятельного значения при лечении стероидного ОП не имеют, но являются обязательным компонентом комплексной терапии. В клинической практике предпочтение в настоящее время отдается быстрорастворимым солям кальция. Кальций форте содержит в одной растворимой таблетке 500 мг кальция-элемента. Препараты кальция следует назначать в один прием, на ночь. При лечении СОП кальций надо применять ежедневно в суточной дозе 500–1000 мг в комбинации с препаратами патогенетической терапии ОП. Абсолютным показанием для назначения корсета при СОП являются боли в спине и наличие компрессионных переломов тел позвонков.
Прогноз БИК зависит от длительности, тяжести заболевания и возраста больного. При небольшой длительности заболевания, легкой форме и возрасте до 30 лет прогноз благоприятный. После адекватного лечения наблюдается выздоровление. При среднетяжелой форме заболевания и при длительном его течении у больных после нормализации функции гипофиза и надпочечников часто остаются необратимые изменения со стороны сердечно-сосудистой системы и костной системы, которые требуют дополнительного лечения. Вследствие двусторонней адреналэктомии у пациентов развивается хроническая надпочечниковая недостаточность. При стабильной надпочечниковой недостаточности и отсутствии тенденции к росту аденомы гипофиза прогноз благоприятный, хотя трудоспособность больных ограничена.
С. Д. Арапова, кандидат медицинских наук
Е. И. Марова, доктор медицинских наук, профессор
Эндокринологический научный центр РАМН, Москва