что такое каутеризация яичников
Лапароскопическая каутеризация яичников
Лапароскопическая каутеризация яичников (прижигание яичников)
Каутеризация яичников – метод прижигания яичников, посредством лапароскопического доступа.
Показания
Показанием к каутеризации является поликистоз яичников. Это состояние характеризуется образованием множества кистозных образований на его поверхности. Эти образования представляют собой не опухоли, а несозревшие фолликулы. Поликистоз развивается вследствие дисгормональных нарушений с избыточной активностью мужских половых гормонов – андрогенов. Поликистоз – одна из причин женского бесплодия, т.к. при данном состоянии нарушается созревание фолликулов и овуляция (выход яйцеклетки). Еще одна причина бесплодия при поликистозе заключается в том, что наружная капсула яичника уплотняется, и это является механическим препятствием для овуляции. К каутеризации прибегают в случаях неэффективности консервативного лечения поликистоза.
Методика
Каутеризация проводится в стационаре под общим обезболиванием, т.е. под наркозом. В околопупочной области специальным стилетом проделывается отверстие 1см. в диаметре, куда вводится троакар – жесткая металлическая трубка. Через троакар вводится лапароскоп. Затем проделывают 2 отверстия диаметром 5 мм. в подвздошной обл. с обеих сторон для хирургического инструментария. Поликистозный яичник фиксируется в нужном положении специальными щипцами. С помощью игольчатого коагулятора или лазера на его поверхности делают насечки числом 15-20. Глубина каждой насечки – 4-5мм., ширина – 2-3мм. Насечки делают в проекции кистозных образований, из которых через проделанные отверстия изливается жидкость. После этого аналогичные манипуляции проделывают и со вторым яичником. В результате уже к концу оперативного вмешательства яичник уменьшается в размерах.
Эффективность
В ходе каутеризации с одной стороны, уменьшается количество патологической ткани, а с другой – разрушается плотная капсула яичника. Все это создает оптимальные условия для созревания и выхода яйцеклетки из фолликула и для развития нормальной беременности. Каутеризация яичников настолько эффективна, что в ряде случаев беременность может наступить уже на первом месяце после вмешательства. Данный метод лечения имеет ряд преимуществ в сравнении с клиновидной резекцией яичников, к которой также прибегают при поликистозе. Каутеризация менее травматична и болезненна, чем клиновидная резекция. Кроме того, при каутеризации, в отличие от других видов операции на яичниках, риск развития спаечной болезни минимален.
Что такое каутеризация яичников Как современный метод помогает восстановить репродуктивную функцию женщины, особенность процедуры
Такая трагедия женщин как бесплодие, в большинстве случаев вызвана синдромом поликистозных яичников или СПКЯ. Медицина утверждает, что заболевание нельзя вылечить доступными на сегодняшний день средствами, но можно значительно смягчить проявление болезни: восстановить менструальный цикл и овуляцию путем каутеризации яичников. Каутеризация яичников это малоинвазивная, безопасная операция в ходе которой врач прижигает кисты на яичнике.
Каутеризация яичников ― когда потребуется
Несмотря на то что современная официальная медицина достигла большого прогресса в методах диагностики, причина, почему возникает поликистоз яичников до сих пор не ясна.
Предполагается, что заболевание развивается на фоне раннего проявления резистентности тканей к инсулину, который в свою очередь вызван перенасыщением состава крови мужскими гормонами (тестостероном) и андрогенами. Кроме этого на развитие поликистоза влияют аномально высокая выработка гормона ФСГ (фолликулостимулирующего)
Показания к операции
Выделяют три основных показателя, когда каутеризация оказывается единственным вариантом, чтобы женщина смогла выносить и родить ребенка.
Если ваш гинеколог рекомендует проведение каутеризаци необходимо выбрать клинику, поскольку операция проводится под общим наркозом. Вместе с квалификацией хирурга, который будет проводить каутеризацию не менее важным остается и опыт анестезиолога.
Большинство акушеров-гинекологов, опытных хирургов и ученых считают каутеризацию яичников последней мерой, которая должна использоваться при лечении синдрома поликистозного яичника. В большинстве случаев использование адекватных современных средств, в том числе традиционной и нетрадиционной медицины дают положительный эффект. Организм восстанавливает процесс овуляции и женщина беременеет.
Как проходит каутеризация яичников
При процедуре могут использоваться две технологии.
Клиновидная резекция выполняется под общим наркозом, каутеризация проводится методом введения в брюшную полость хирургических инструментов. Именно лапароскопическая каутеризация позволяет провести хирургическое вмешательство практически без шрамов. Кроме стандартной процедуры для лечения синдрома поликистозных яичников используют.
Ультразвук и лазерная терапия считаются сравнительно безопасными методами. После этих вмешательств только в 0,1 % случаев возникают такие осложнения как образование спаек в брюшной полости.
Каутеризация позволяет удалить аномальные кисты с помощью элетрокоагуляции с использованием электрода, который при помощи высокой температуры разрушает кистозные образования.
Когда назначается каутеризация при поликистозе яичников
Как уже было отмечено синдром поликистозных яичников считается заболеванием с невыясненной природой. Существует теория, согласно которой поликистоз является генетическим заболеванием и механизм появления кист запускается в определенном возрасте женщины. Диагноз ставят в том случае, если наблюдается два симптома из трех (могут быть все три).
Кроме бесплодия поликистоз является причиной многих других заболеваний, поскольку в организме развивается тканевая резистентность к инсулину, что приводит к ожирению и развитию диабета 2 типа.
Поскольку сегодня официальная медицина не имеет инструмента чтобы полностью вылечить синдром поликистозного яичника, используют методы, убирающие симптомы заболевания.
Как проходит каутеризация
Поскольку каутеризация использует лапароскопические инструменты и оборудование ее относят к минимально-инвазивной хирургии. Процесс каутеризации можно описать по шагам.
Вводится зонд, через который желудок наполняют от 1 до 5 литров диоксида углерода. Хирург создает пространство для движения инструментов внутри брюшной полости.
Пациентка помещается в операционное положение или позицию Тренделенбурга. Таз поднимается вверх, туловище и голова опущена вниз. Такая позиция заставляет кишечник переместится, освобождая врачу пространство для маневра инструментом.
В брюшной полости делают три надреза. В околопупочной области через надрез вставляют жесткую металлическую трубку ― троакар, через троакар хирург вводит лапароскоп.
Через два других отверстия, диаметром 0,5 см. в брюшную полость вводят хирургический инструмент.
Поликистозный яичник фиксируют щипцами и с помощью игольчатого коагулятора или лазерного луча делают насечки в проекции кистозных образований. Кисты разрезаются и прижигаются.
Уже к концу операции яичник значительно уменьшается в размерах, поскольку происходит избавление органа от патологической ткани и разрушение плотной ткани яичника. Это создает максимально благоприятные условия для формирования здоровой яйцеклетки и ее выхода из яичника. Что в итоге приводит к долгожданной беременности.
Каутеризация ― эффективность процедуры
Лапароскопическая каутеризация относится к наименее травматическим оперативным вмешательствам. Она в несколько раз менее травматична чем клиновидная резекция, кроме этого риск развития спаечных процессов минимален.
Хирургическая картина такова, что в большинстве случаев беременность наступает в первые два месяца после оперативного вмешательства, при отсутствии сопутствующих заболеваний.
Каутеризация яичников ― безопасно или нет?
Большинство лапароскопических процедур имеют минимальное количество противопоказаний. Самым главным недостатком каутеризации считается быстрое высвобождение репродуктивной функции яичника (выработка фолликула), и как следствие быстрый износ яичников и наступление менопаузы.
Следует помнить, что если сперма в организме мужчины воспроизводится постоянно, то количество фолликулов в женском организме, которые развиваются в полноценную яйцеклетку, ограничено. Для наступления беременности в некоторых случаях врач назначает несколько процедур, каждая из которых уменьшает общий репродуктивный возраст женщины.
Второе осложнение, которое можно наблюдать при каутеризации это перфорация (прокол) кишечника, что в свою очередь приводит к перитониту и внутреннему кровоизлиянию. Перфорация кишечника — осложнение всех лапароскопических процедур, поскольку органы в брюшной полости плотно прижаты друг к другу и добраться при к яичнику сложно. К счастью проколы кишечника случаются во врачебной практике редко.
Надеемся, что вы получили ответ на вопрос что такое каутеризация яичника и при каком заболевании ее проводят. Мы очень надеемся, что в вашей жизни будет как много меньше и гинекологических и любых других заболеваний.
Если вы сталкивались с поликистозом яичника или делали каутеризацию, напишите свой опыт и результат, это поможет нашим читательницам.
Прорыв в лечении бесплодия
Прорыв в лечении бесплодия
Овуляция и дальнейшее оплодотворение возможны при наличии в яичниках женщины абсолютно жизнеспособных фолликулов
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Процент женщин, лишенных радости материнства, с каждым годом возрастает. Среди причин бесплодия всё чаще выделяют первичную недостаточность яичников (ПНЯ). Данная патология заключается в отсутствии фолликулов или нарушении их созревания в ответ на гормональную стимуляцию. Решение проблемы эндокринного бесплодия вследствие синдрома истощения яичников предложили ученые из США и Японии. Им удалось активировать фолликулы яичников в условиях in vitro и имплантировать фрагменты ткани в верхний отдел фаллопиевых труб, что дает женщине шанс стать матерью.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучшее новостное сообщение».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Корни проблемы
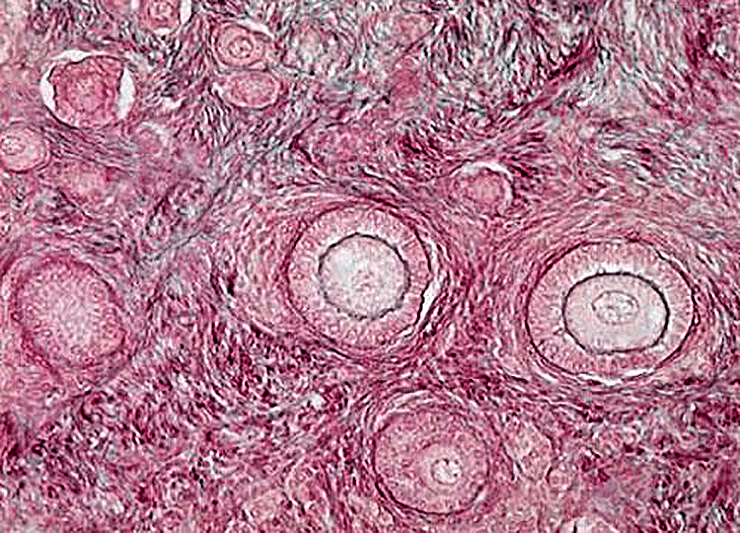
Яичник — уникальная эндокринная система, в которой ежемесячно возникает новая секреторная структура — граафов фолликул (рис. 1). Он развивается из микроскопического примордиального фолликула, потенциальная функциональность которого и определяет регулярность менструального цикла женщины.
Рисунок 1. Фолликулы яичников
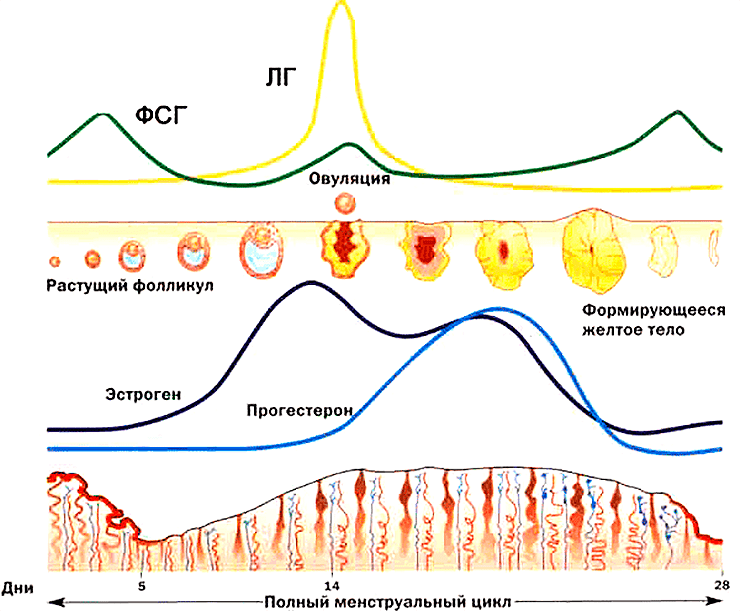
Функция яичников регулируется двумя гормонами гипофиза: фолликулостимулирующим гормоном (ФСГ) и лютеинизирующим гормоном (ЛГ) (рис. 2). В свою очередь, яичники продуцируют гормоны, регулирующие секрецию ФСГ и ЛГ по принципу отрицательной обратной связи: эстрогены, ингибины и прогестерон [1].
Рисунок 2. ФСГ стимулирует рост и созревание фолликула в яичнике. ЛГ стимулирует выход созревшей яйцеклетки из фолликула (овуляцию).
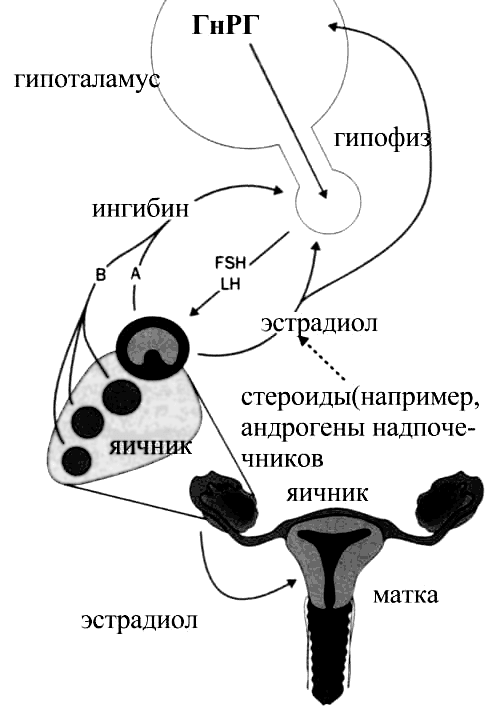
При недостаточности функции яичников для поддержания снижающейся концентрации яичниковых гормонов происходит резкое повышение секреции гонадотропинов. За их выработку отвечает гипоталамус (рис. 3).
Рисунок 3. Связь функционирования яичников с эндокринной системой
Причины, приводящие к развитию первичной недостаточности яичников (ПНЯ), весьма гетерогенны: генетические, ферментативные, аутоиммунные, инфекционно-токсические, психогенные. Кроме того, в эту группу относят и дефекты в структуре гонадотропинов. В последние годы большое внимание исследователей уделяется молекулярно-генетическим аспектам этой патологии яичников, поскольку выявлен определенный набор генов, который может отвечать за развитие ПНЯ.
Стоит отметить, что термин «первичная недостаточность яичников» в настоящее время применяется для определения состояния, которое ранее называли «преждевременной менопаузой». Ключевое различие заключается в том, что термин «ПНЯ», предложенный еще в 1942 году, характеризует нарушение функции яичников в динамике, а не конечное состояние, что наблюдается при менопаузе [1].
Диагностика
Яичниковая недостаточность диагностируется по повышенному уровню ФСГ и ЛГ в крови при сниженном уровне эстрогенов. Самый чувствительный гормон — ФСГ; он является самым ранним маркером преждевременного старения яичников. При двукратном превышении уровня ФСГ (20 Ед/л) наступление и благополучный исход беременности маловероятны.
Клинические характеристики состояния: аменорея (отсутствие менструации) ≥4 месяцев у женщин моложе 40 лет, бесплодие и повышение уровня ФСГ до менопаузальных значений (дважды с промежутком не менее 1 месяца).
Частота спонтанной недостаточности яичников у женщин с хромосомным набором 46 ХХ составляет около 1%; при этом эпидемиологические исследования указывают на тесную связь данного нарушения с возрастом. Так, у женщин в возрасте до 20 лет ПНЯ встречается с частотой 1:10000, а в возрасте от 30 до 40 — 1:1000.
Что происходит на гормональном уровне
Один из половых гормонов — 17β-эстрадиол (рис. 4), который играет важную роль в выполнении репродуктивной функции женщины, — вырабатывается преимущественно в яичниках из мужских половых гормонов — андростендиона и тестостерона [2]; небольшое количество этого гормона также вырабатывается надпочечниками. В процессе угасания функций яичников количество растущих фолликулов в них уменьшается, что приводит к значительному понижению выработки 17β-эстрадиола. Поэтому у женщин с так называемым синдромом истощения яичников наблюдается нехватка этого гормона, которая частично компенсируется большей выработкой 17β-эстрадиола в надпочечниках. Так как менструации становятся нерегулярными, уровень 17β-эстрадиола начинает колебаться, и с прекращением менструаций резко понижается, что приводит к повышению фолликулостимулирующего гормона (ФСГ).
Рисунок 4. β-эстрадиол (кристаллы). Поляризация LM X100.
Механизм активации незрелых фолликулов
Для женщин, страдающих бесплодием по причине рассмотренного заболевания, существует единственная возможность материнства — имплантация оплодотворенной донорской яйцеклетки. Однако группа специалистов из Стэнфордского университета (США) и Медицинского факультета Университета им. Святой Марианны (Япония) предложили альтернативу — метод, позволяющий исключить известные хирургические вмешательства для стимуляции овуляции, такие как клиновидная резекция яичников или лазерное сверление. Врачи удалили яичники у участниц исследования, поделили их на несколько частей, а затем воздействовали на фрагменты яичников препаратами, стимулирующими рост. Спустя несколько дней некоторые из фрагментов ткани были имплантированы в фаллопиевы трубы женщин. Затем специалисты наблюдали за развитием фолликулов. У некоторых участниц исследования сформировались зрелые яйцеклетки, что позволило провести им стандартную процедуру экстракорпорального оплодотворения (ЭКО [3]). Результаты исследования опубликованы в журнале Proceedings of the National Academy of Sciences [4].
Важно отметить, что возможность провести подобное лечение возникла благодаря изучению сигнального клеточного пути под названием Hippo [5], который представляет собой один из ключевых компонентов регуляции таких важных процессов, как контактное ингибирование роста клеток и связанного с ним контроля размера внутренних органов [6]. Первоначально белковый комплекс Hippo был открыт у дрозофил. Мухи, у которых его функционирование было нарушено, буквально увеличивались в размерах (из-за чего регулятор и получил своё название: «Hippo» происходит от слова «гиппопотам»). Затем его обнаружили и у млекопитающих.
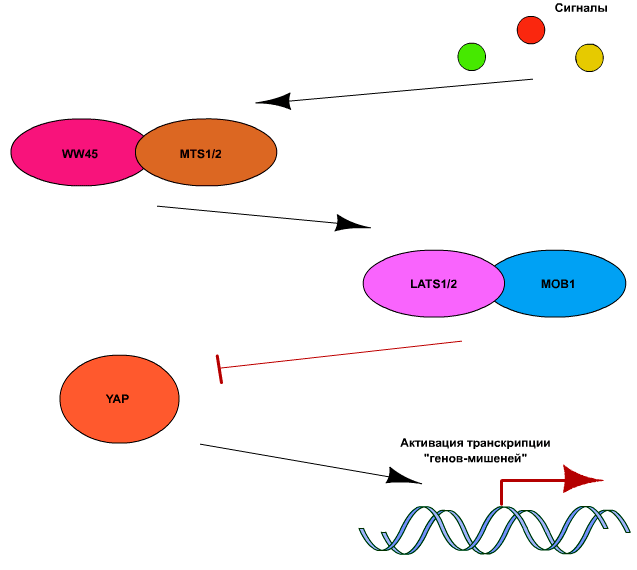
Ключевым компонентом пути Hippo является киназа Yap (Yes-activated protein), которая в активном состоянии способна связывать ряд факторов транскрипции, таких как p73, p53-binding protein-2 (p53BP2), RUNX2, SMAD7, ERBB4, PEBP2а и TEAD/ТЕF [7]. Регуляция активности YAP осуществляется в основном за счет ингибирующего действия киназ LATS1 и 2 (large tumor supressor-1 и −2). Они, в свою очередь, активируются киназами МSТ1 и МSТ2 (mammalian sterile-20-like kinases). Для полной активации LATS и МSТ необходимо также, чтобы они были связаны с адапторными белками WW45 и МОB1, соответственно. Вышеописанная часть сигнального пути Hippo является высококонсервативной у млекопитающих, в то время как сигналы активации или ингибирования LATS и МSТ могут быть достаточно разнообразными. В общих чертах сигнальный путь Hippo представлен на рис. 5.
Рисунок 5. Схематичное изображение работы сигнального белкового регулятора Hippo
Развитие эмбриона, деление эмбриональных клеток и рост тканей и органов эволюционно контролируются работой различных регуляторов. По словам одного из авторов исследования Арона Сюэ (Aaron Hsueh) — акушера-гинеколога из Стэнфордского Университета в Калифорнии — у женщин с синдромом истощения яичников наблюдается повышенная активность регулятора Hippo [8]. Другими словами, он блокирует созревание практически всех фолликулов яичника, что минимизирует возможность наступления овуляции и дальнейшего оплодотворения.
Ученые нарушили работу сигнального пути Hippo в удаленных яичниках и, таким образом, предотвратили преждевременную остановку развития фолликулов. Далее специалисты стимулировали активность другого сигнального пути, называемого Akt, что способствовало ускорению роста фолликулов [9], [10].
Клинические исследования проводились сначала на лабораторных животных. На следующем этапе в эксперименте согласились принять участие 27 женщин, страдающих от первичной дисфункции яичников. В ходе исследования выяснилось, что у некоторых женщин в яичниках не было фолликулов. В яичниках 13 пациенток обнаружили незрелые фолликулы; из них у восьми женщин применение нового метода лечения способствовало росту жизнеспособных фолликулов. Для 14 женщин лечение оказалось неэффективным.
В результате зрелые яйцеклетки были получены у пяти женщин и использованы для ЭКО. Одна из пациенток в возрасте 29 лет во время курса лечения на 37 неделе беременности родила ребенка весом 3,3 кг (рис. 6). Научная группа надеется, что эффективность нового метода лечения достигнет 30%. И, более того, по их словам, этот метод может также помочь женщинам, перенесшим лучевую или химиотерапию, и пациенткам в возрасте лет с нерегулярным менструальным циклом [11].
Рисунок 6. Казухиро Кавамура (Kazuhiro Kawamura) — один из ученых, участвовавший в исследовании — держит на руках новорожденного мальчика, которого родила первоначально бесплодная женщина
Мнения и прогнозы
По мнению Марчелле Цедарса (Marcelle Cedars) — специалиста в области репродуктивной онкологии из Университета Калифорнии в Сан-Франциско — исследователи поторопились апробировать новый метод лечения бесплодия на человеке: «Ученые продемонстрировали рождение здорового потомства при проведении предварительных исследований на мышах, но не было получено доказательств роста, развития и/или плодовитости этого поколения» [12].
Авторы исследования полагают, что метод подходит бесплодным женщинам среднего возраста, а также тем, кому диагностировали первичную недостаточность яичников, вследствие которой в более чем 50% случаев беременность не наступает. Однако не все эксперты разделяют их оптимизм. Руководитель врачебной группы, изучающей оплодотворение, из Университета Южной Калифорнии Ричард Паульсон (Richard Paulson) убежден, что ключевое условие эффективности разработанного механизма лабораторной «активации» фолликула — наличие в нем здоровой яйцеклетки. Кроме того, Паульсон заостряет внимание на том, что неразумно сопоставлять результаты лечения женщины в возрасте 29 лет с результатами лечения женщины в 40 лет, поскольку гормональная стимуляция роста и развития фолликулов в разные возрастные периоды происходит с различной интенсивностью.
Рассмотренный консервативный метод стимуляции овуляции путем блокировки сигнального пути Hippo в отдельных фрагментах ткани яичников может быть полезен женщинам, больным раком или проходящим процедуры стерилизации. Но все же главное достижение ученых — это рождение ребенка у женщины, которая без их участия никогда не смогла бы стать матерью.
Бесплодие
В настоящее время считается, что если при регулярной половой жизни беременность не наступает в течение года, надо ставить вопрос о бесплодии и начинать обследование и лечение супругов.
Бесплодие супружеских пар составляет около 15-20 %.
Для выявления причины проводится обследование. Диагноз бесплодия у женщины может быть установлен только после исключения бесплодия мужчины. Как правило, обследование начинают с общепринятых методов, дальнейший план зависит от результатов предыдущего обследования.
Определение «первичное» и «вторичное» бесплодие относится не только к женщине. Применительно к мужчине первичное бесплодие означает, что от этого мужчины ни у одной из его партнерш не наступала беременность. Вторичным считается бесплодие, когда от данного мужчины была хотя бы одна беременность хотя бы у одной из его партнерш.
К бесплодию приводит целый ряд патологических состояний.
Причиной бесплодия может стать также иммунологическая несовместимость супружеской пары. Кроме того, существует так называемое необъяснимое (идиопатическое) бесплодие, когда при тщательном обследовании не удается выявить нарушения в здоровье как женщины, так и мужчины, при этом в других браках у них также не наступает беременность.
Лечение бесплодия проводят в зависимости от выявленных причин. Оно может быть хирургическим или медикаментозным.
Методы обследования и лечения бесплодия проводимые в отделении:
1) Гистеросальпингография (ГСГ)
ГСГ. Методика проведения
При ГСГ в матку вводят контрастное вещество. Затем делают несколько рентгеновских снимков. При проведении ГСГ возможно возникновение спазма труб в ответ на введение рентгенконтрастного вещества, имитирующее их непроходимость. Для исключения ложной интерпретации результатов ГСГ за 30-40 минут до исследования стоит принять 2 таблетки но-шпы или баралгина. В результате качественно проведенной ГСГ получается серия снимков, характеризующих состояние полости матки, рельеф слизистой матки и маточных труб, проходимость труб.
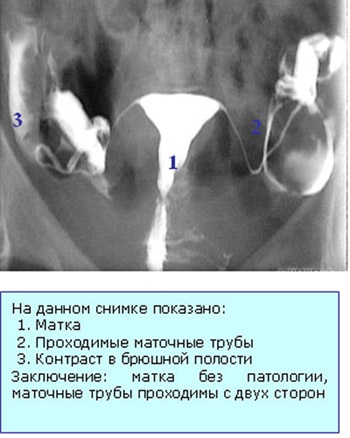
ГСГ хорошо показывает состояние полости матки и маточных труб, но не позволяет оценить спаечный процесс вокруг матки и придатков, выявить очаги эндометриоза. Все это можно увидеть при диагностической лапароскопии. Именно диагностическая лапароскопия является современным способом диагностики состояния внутренних половых органов женщины.
2) Гистероскопия (биопсия эндометрия)
3) Лапароскопия в диагностике и лечении бесплодия:
Дело в том, что при СПКЯ яичники покрываются плотной капсулой, которая препятствует овуляции и высвобождению яйцеклетки. Во время лапароскопии эту капсулу можно рассечь. Проводится так называемый дрилинг (каутеризация) яичников, в их капсуле делается несколько микроотверстий. Процедура весьма эффективна, но лишь в том случае, когда диагноз поставлен верно.
По статистическим данным можно ожидать наступления самопроизвольной беременности у 35% прооперированных пациенток. Если после операции менструальный цикл так и не восстановился и нет овуляции то по истечении 3х месяцев наблюдения следует рекомендовать пациентке проведениестимуляции овуляции. Это позволяет увеличить процент наступивших беременностей до 50%.
Лапароскопия представляет безусловную ценность как диагностический инструмент. Она позволяет получить прямую информацию о состоянии маточных труб и органов малого таза. Ни одно другое исследование, ни гистеросальпингография, ни УЗИ, не позволяет нам с такой точностью это сделать.
Если состояние маточной трубы оценивается как удовлетворительное, а её реконструкция целесообразной, то производится разделение периферических спаек, восстановление её проходимости. Но так бывает крайне редко. Наиболее часто сталкиваемся с тем, что трубы абсолютно не изменены и дело вообще не в них, либо они изменены необратимо. Вопрос этот должен быть обязательно заранее оговорён с пациенткой, но результатом лапароскопии может стать удаление маточных труб с целью её дальнейшей подготовки к ЭКО.
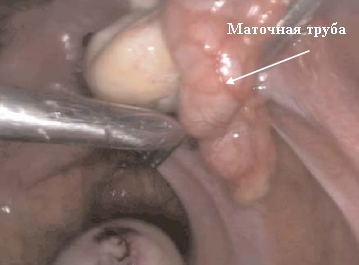
Дело в том, что сохранение такой трубы только затянет время и навредит пациентке.
Функциональность такой трубы утрачена необратимо.
Малые (начинающиеся) формы поверхностного эндометриоза можно определить только во время лапароскопии.
Таким образом, основной целью хирурга во время лапароскопии при бесплодии является:
4. Миома матки не является абсолютным фактором бесплодия, но при росте узла миомы в полость матки (субмукозной миоме) беременность не сохранится. При выявлении миомы с таким расположением, пациентке рекомендовано проведение гистерорезектоскопии и удаление узла. В противном случае узел миомы будет мешать прикреплению уже оплодотворённой яйцеклетки в полости матки.
Независимо от расположения узла миомы рекомендовано оперативное лечение в объёме миомэктомии всем пациенткам накануне планируемой беременности, если его диаметр превышает 4-5см. Естественно проведение операции возможно лапароскопическим доступом.