что такое катионы и анионы в воде
Катионы и анионы в химии, таблица растворимости
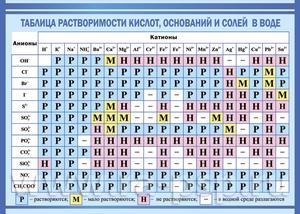
Показатели растворимости в воде
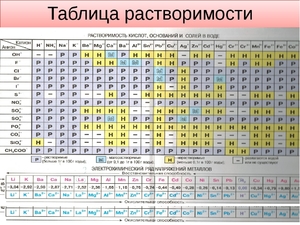
Она помогает при решении химических уравнений, где участвуют ионные реакции. Если результатом будет получение нерастворимого вещества, то реакция возможна. Существует несколько вариантов:
Это интересно: металлы и неметаллы в периодической таблице Менделеева.
Электролиты
Это растворы или сплавы, проводящие электрический ток. Электропроводность их объясняется мобильностью ионов. Электролиты можно поделить на 2 группы:
Теория электролитической растворимости
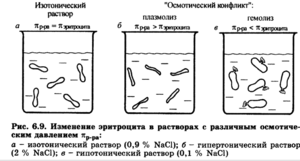
Одновременно с диссоциацией проходит противоположный процесс – соединение ионов в молекулы. Кислоты – это такие электролиты, при распаде которых образуется катион – ион водорода. Основания – анионы – это гидроксид ионы. Щелочи – это основания, которые растворяются в воде. Электролиты, которые способны образовывать и катионы и анионы, называются амфотерными.
Это такая частица, в которой больше протонов или электронов, он будет называться анион или катион, в зависимости от того, чего больше: протонов или электронов. В качестве самостоятельных частиц они встречаются во многих агрегатных состояниях: газах, жидкостях, кристаллах и в плазме. Понятие и название ввёл в обиход Майкл Фарадей в 1834 году. Он изучал воздействие электричества на растворы кислот, щелочей и солей.
Простые ионы несут на себе ядро и электроны. Ядро составляет почти всю атомную массу и состоит из протонов и нейтронов. Количество протонов совпадает с порядковым номером атома в периодической системе и зарядом ядра. Ион не имеет определённых границ из-за волнового движения электронов, поэтому невозможно измерить их размеры.
Отрыв электрона от атома требует, в свою очередь, затрат энергии. Она называется энергия ионизации. Когда присоединяется электрон, происходит выделение энергии.
Катионы
Это частицы, носящие положительный заряд. Могут иметь разную величину заряда, например: Са2+ — двузарядный катион, Na+ — однозарядный катион. Мигрируют к отрицательному катоду в электрическом поле.
Анионы
Это элементы, имеющие отрицательный заряд. А также обладает различным количеством величины зарядов, например, CL- — однозарядный ион, SO42- — двухзарядный ион. Такие элементы входят в состав веществ, обладающих ионной кристаллической решёткой, в поваренной соли и многих органических соединениях.
Химия – наука, где возможно творить практически любые чудеса. Катион вы можете узнать по ссылке.
Что такое катионы и анионы?
Справочные таблицы, в которых дана сероводородная аналитическая классификация анионов 1-3 групп, качественные реакции и групповые реагенты, а также аналитические сигналы на анионы.
Данная аналитическая классификация анионов основана на растворимости солей бария Ba2+ и серебра Ag+, и включает в себя 3 аналитические группы анионов.
Таблица аналитическая классификация анионов
Таблица аналитические сигналы на анионы первой группы
Таблица аналитические сигналы на анионы второй группы
| № | Реагенты | Анионы | ||
| Cl- | Br- | I- | ||
| 1. | AgNO3 в присутствии HNO3 | AgCl белый творожистый растворим в избытке NH4ОН | AgBr желто-белый, частично растворим в избытке NH4ОН, хорошо растворим в Na2S2O3 | AgI светложелтый, растворим в Na2S2O3 и в большом иодида калия |
| 2. | Хлорная вода в кислой среде | — | Свободный бром, окрашивает бензол-толуол в желто-оранжевый цвет | Свободный иод, окрашивает бензол-толуол в малиново-фиолетовый цвет |
| 3. | диоксид марганца MnO2 в кислой среде | Свободный хлор, практически не окрашивает бензол-толуол | Свободный бром, окрашивает бензол-толуол в желто-оранжевый цвет | Свободный иод, окрашивает бензол-толуол в малиново-фиолетовый цвет |
Таблица аналитические сигналы на анионы третьей группы
| № | Реагенты | Анионы | |
| NO3- | NO2- | ||
| 1. | металлический алюминий или цинк (Al,Zn) в щелочной среде | выделяется аммиак NH3 | — |
| 2. | металлическая медь (Cu) | выделяются буро-желтые пары диоксида азота (NO2) | — |
| 3. | дифениламин | раствор окрашивается в синий цвет | раствор окрашивается в синий цвет |
| 4. | сильные кислоты (HCl, H2SO4) | — | выделяются желто- бурые пары окислов азота |
| 5. | перманганат калия(KMnO4) | — | раствор перманганата калия обесцвечивается |
Таблица аналитическая классификация анионов на окислительно-восстановительных свойствах
Эта аналитическая классификация анионов основана на их окислительно-восстановительных свойствах. Она также включает три аналитические группы анионов.
| № группы | Анионы | Групповой реагент | Результат действия реагента |
| 1. Анионы-окислители | BrO3-, AsO43-, NO3-, NO2- | KI в сернокислой среде | Выделение иода I2 |
| 2. Анионы-восстановители | S2-, SO32-, S2O32-, AsO33- | I2 | |
| S2-, SO32-, S2O32-, AsO33-, NO2-, C2O42-, Cl-, Br-, I-, CN-, NCS- | KMnO4 в сернокислой среде | Обесцвечивание раствора KMnO4 | |
| 3. Индифферентные анионы | SO42-, CO32-, PO43-, CH3COO-, B4O72- (BO2-) | Нет реагента | — |
Качественные реакции на неорганические вещества и ионы
Представим себе такую ситуацию: Вы работаете в лаборатории и решили провести какой-либо эксперимент. Для этого вы открыли шкаф с реактивами и неожиданно увидели на одной из полок следующую картину. У двух баночек с реактивами отклеились этикетки, которые благополучно остались лежать неподалеку.
При этом установить точно какой банке соответствует какая этикетка уже невозможно, а внешние признаки веществ, по которым их можно было бы различить, одинаковы.
Данный метод может сработать только в том случае, если различаемые вещества по разному меняют цвет пламени, или же одно из них не меняет цвет вовсе.
Но, допустим, как назло, вам определяемые вещества цвет пламени не окрашивают, или окрашивают его в один и тот же цвет. В этих случаях придется отличать вещества с применением других реагентов. В каком случае мы можем отличить одно вещество от другого с помощью какого-либо реагента?
Возможны два варианта:
Например, нельзя отличить воду от раствора гидроксида натрия с помощью соляной кислоты, не смотря на то, что щелочи с кислотами прекрасно реагируют: NaOH + HCl = NaCl + H2O
Но зато, можно воду от водного раствора щелочи можно различить, например, с помощью раствора хлорида магния – в данной реакции выпадает белый осадок: 2NaOH + MgCl2 = Mg(OH)2 ↓+ 2NaCl
Например, различить раствор карбоната натрия от раствора нитрата серебра можно с помощью раствора соляной кислоты.
Качественные реакции на катионы
Качественные реакции на анионы
Таблица растворимости
Растворимостью называется способность одного или нескольких веществ вступать в реакцию с другими веществами таким образом, чтобы в результате получалась однородная система. При этом оба вещества распадаются на молекулы, атомы или ионы.
Наравне с таблицей периодической системы Д. И. Менделеева, таблица растворимости является основным теоретическим пособием при изучении химии. Не все вещества взаимодействуют между собой одинаково.
Начинающие химики, учащиеся школ, колледжей и вузов не всегда могут запомнить степень растворимости в воде тех или иных веществ. Именно поэтому таблицу периодической системы Менделеева и таблицу растворимости можно увидеть в каждом кабинете или классе химии, каждой лаборатории.
То или иное сочетание веществ из таблицы может вступать в семь различных реакций с водой:
Чаще всего таблица растворимости применяется при решении уравнений с участием ионных реакций. Реакция возможна только в том случае, если конечный продукт малорастворим или нерастворим вообще.
Условные обозначения в таблице растворимости:
| Р | Вещество хорошо растворимо в воде |
| М | Малорастворимо |
| Н | Практически нерастворимо в воде, но легко растворяется в слабых или разбавленных кислотах |
| РК | Нерастворимо в воде и растворяется только в сильных неорганических кислотах |
| НК | нерастворимо ни в воде, ни в кислотах |
| Г | полностью гидролизуется при растворении и не существует в контакте с водой |
| – | вещество вообще не существует |
| Катионы | Анионы | ||||||||||
| OH– | F– | Cl– | Br– | I– | S2- | NO3– | CO32- | SiO32- | SO42- | PO43- | |
| H+ | Р | Р | Р | Р | Р | М | Р | – | Н | Р | Р |
| Na+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |
| K+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |
| NH4+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |
| Mg2+ | Н | РК | Р | Р | Р | М | Р | Н | РК | Р | РК |
| Ca2+ | М | НК | Р | Р | Р | М | Р | Н | РК | М | РК |
| Sr2+ | М | НК | Р | Р | Р | Р | Р | Н | РК | РК | РК |
| Ba2+ | Р | РК | Р | Р | Р | Р | Р | Н | РК | НК | РК |
| Sn2+ | Н | Р | Р | Р | М | РК | Р | Н | Н | Р | Н |
| Pb2+ | Н | Н | М | М | М | РК | Р | Н | Н | Н | Н |
| Al3+ | Н | М | Р | Р | Р | Г | Р | Г | НК | Р | РК |
| Cr3+ | Н | Р | Р | Р | Р | Г | Р | Г | Н | Р | РК |
| Mn2+ | Н | Р | Р | Р | Р | Н | Р | Н | Н | Р | Н |
| Fe2+ | Н | М | Р | Р | Р | Н | Р | Н | Н | Р | Н |
| Fe3+ | Н | Р | Р | Р | – | – | Р | Г | Н | Р | РК |
| Co2+ | Н | М | Р | Р | Р | Н | Р | Н | Н | Р | Н |
| Ni2+ | Н | М | Р | Р | Р | РК | Р | Н | Н | Р | Н |
| Cu2+ | Н | М | Р | Р | – | Н | Р | Г | Н | Р | Н |
| Zn2+ | Н | М | Р | Р | Р | РК | Р | Н | Н | Р | Н |
| Cd2+ | Н | Р | Р | Р | Р | РК | Р | Н | Н | Р | Н |
| Hg2+ | Н | Р | Р | М | НК | НК | Р | Н | Н | Р | Н |
| Hg22+ | Н | Р | НК | НК | НК | РК | Р | Н | Н | М | Н |
| Ag+ | Н | Р | НК | НК | НК | НК | Р | Н | Н | М | Н |
Что означает слово Катионы и анионы?
Катионы и анионы — это типы ионов, то есть атомы, которые приобрели или потеряли электроны через химические связи.
Атом, имеющий одинаковое количество протонов (положительный заряд) и электронов (отрицательный заряд), считается электрически нейтральным. Когда этот атом принимает или передает электроны, он называется ионом, который, в свою очередь, может быть:
Катион
Катион — это атом, который имеет положительный заряд, потому что в нем больше протонов, чем электронов.
Щелочные металлы (литий, натрий, калий, рубидий, цезий и францио), как правило, образуют катионы, поскольку в их валентном слое имеется только 1 электрон. Это означает, что энергия, необходимая для удаления этого электрона, очень мала, что делает эти элементы очень реактивными.
Катион представлен символом +, следующим за именем элемента. Количество потерянных электронов указывает на тип катиона:
Типы катионов также можно определить по количеству знаков +. Таким образом, элемент, представленный только +, является одновалентным катионом, в то время как другой элемент, представленный +++, является трехвалентным катионом.
Примеры катионов
Анион
Анион — это атом с отрицательным зарядом, потому что в нем больше электронов, чем протонов. Элементы семейства азота, калькогенов и галогенов имеют тенденцию образовывать анионы, потому что они легко принимают электроны.
Анион представлен символом — после имени элемента. Количество полученных электронов указывает на тип аниона:
Примеры анионов
Ионные Связи
Ионные или электровалентные связи представляют собой связи, которые возникают между катионами и анионами.
Элементы могут принимать, давать или делить электроны таким образом, чтобы их последний энергетический слой имел 8 электронов. Это известно как теория октетов.
Согласно теории октетов, атомы имеют тенденцию стабилизироваться, когда в валентном слое (последнем электронном слое) находится 8 электронов. Таким образом, будучи положительно заряженными, катионы связываются с отрицательно заряженными анионами. Таким образом, атомы дают или принимают электроны для достижения равновесия.
Связи, образованные между катионами и анионами, очень прочны и имеют тенденцию иметь следующие признаки:
Ионные связи образуют ионные соединения, такие как хлорид натрия (поваренная соль), образованный связью Na + (катион натрия) + Cl- (хлорид-анион) → NaCl.
Примеры ионных соединений
Некоторые примеры ионных соединений:
Катионный стол
Li +Fe + 2Na +Со + 2К +Ni + 2Rb +Sn + 2Cs +Pb + 2(NH 4 ) +Mn + 2Ag +Pt + 2Cu +Би + 3Hg +Al + 3Au +Cr + 3Mg + 2Au + 3Ca + 2Fe + 3Sr + 2Со + 3Ба + 2Ni + 3Zn + 2Sn + 4CD + 2Pb + 4Cu + 2Мн + 4Hg + 2Pt + 4
| литий | железистый |
| натрий | cobaltoso |
| калий | Niqueloso |
| рубидий | содержащий двухвалентное олово |
| цезий | Plumboso |
| аммоний | марганцевых |
| серебро | относящийся к платине |
| медь | висмут |
| Ртути | Нержавеющая сталь |
| Auroso | хром |
| магний | золотоносный |
| кальций | трехвалентного железа |
| стронций | кобальтовые |
| барий | Niquélico |
| цинк | оловянный |
| кадмий | свинцовый |
| двухвалентной | марганца |
| содержащий двухвалентную ртуть | платина |
Таблица анионов
Химический состав воды
Основные (преобладающие) компоненты
Под влиянием климатических и других условий химический состав природных вод изменяется и приобретает характерные черты, иногда специфические для различных видов природных вод (атмосферные осадки, реки, озера, подземные воды).
Не поддаются даже приблизительной оценке громадные количества солевых частиц, поднимаемых с почв, соленых озер, поверхности льда, удобрений и, наконец, выбрасываемых химическими и металлургическими производствами, и выбрасываемые в атмосферу в результате другой деятельность людей, а в дальнейшем вымываемые осадками.
Реки с водой, относящейся к сульфатному классу, сравнительно малочисленны. Они распространены преимущественно в степной полосе и частично в полупустынях. В составе катионов природных вод сульфатного класса, так же как и в водах гидрокарбонатного класса, преобладает кальций. Однако ряд рек сульфатного класса имеет преобладание натрия. По минерализации воды сульфатного класса значительно превосходят воды гидрокарбонатного класса. Речные сульфатные воды с малой (общее количество солей до 200 мг/л) и средней (общее количество солей с 200 до 500 мг/л) минерализацией встречаются сравнительно редко. Наиболее характерна для этих рек повышенная (общее количество солей с 500 до 1000 мг/л), а иногда и высокая (общее количество солей более 1000 мг/л) минерализация воды.
Приведенная характеристика ионного состава речной воды относится к периоду летней межени. До некоторой степени она характеризует состав и в период ледостава. Существенно иная, значительно меньшая минерализация воды наблюдается в период весеннего половодья.

Чем более изолированно море от океана, тем заметнее отличается состав его воды от состава воды в океане. Первостепенное значение имеют условия водообмена с океаном, соотношение объема материкового стока с объемом моря, глубина моря и характер химического состава вод впадающих рек.
Подземные воды отличаются исключительным разнообразием химического состава, в том числе и ионного. Состав воды бывает всех классов, групп и типов. Ионный состав подземных вод прежде всего зависит от условий их формирования и залегания.
Стабилизация pH природной воды
Гидрокарбонат-ионы нейтрализуют кислоты, попадающие в водоём с атмосферными осадками или образующиеся в результате жизнедеятельности организмов. С концентрацией гидрокарбонат-ионов напрямую связана устойчивость водоёмов к кислотным дождям. Наиболее чувствительны к ним реки и озёра Карелии, Финляндии, Скандинавии, в водах которых этих ионов практически нет.
Органические вещества
Общая концентрация органического вещества в природных водах, изменяясь в широких пределах, бывает наибольшей в болотных водах (в которых при большой концентрации гумусовых веществ она иногда достигает 500 мг/л и более) и реках с болотным питанием, причем болотная вода бывает окрашенной в желтый и коричневый цвет до 300° и выше по платиново-кобальтовой шкале цветности (окраску природной воде придают гуминовые кислоты). Высокая концентрация органического вещества иногда встречается в подземных водах, связанных с нефтеносными месторождениями. Еще большая концентрация может быть в природных водах, загрязненных промышленными и хозяйственно-бытовыми сточными водами. Незагрязненные природные воды обычно содержат мало органических веществ. Например, по Б.А. Скопинцеву, в воде океанов концентрация органического вещества составляет только 2,0-5,4 мг/л (в среднем 3,0 мг/л, а в воде рек в среднем 20 мг/л).
В некоторых поверхностных водах, особенно в реках с болотным питанием, вещества гумусового происхождения являются основной частью химического состава воды. После поступления в хорошо аэрируемые реки, а затем озера и моря органические вещества воды подвергаются изменению, и начатый в почвах процесс окисления завершается для большей их части переходом в простые минеральные соединения. Другая, более устойчивая часть остается и накапливается в водных объектах.
В холодных климатических зонах (тундре) очень мало органических остатков, и там водоёмы почти не содержат гуминовых кислот. А в зоне лесов, особенно хвойных, где органических остатков образуется много и они не успевают полностью разложиться, содержание гуминоных кислот составляет несколько десятков миллиграммов на литр. Гуминовые кислоты не только подкисляют воду в водоёме, но ещё и связывают практически все тяжёлые металлы в прочные комплексные соединения.
Газы в природной воде
Кислород (O2) находится в природной воде в виде растворенных молекул. Кислород, являясь мощным окислителем, играет особую роль в формировании химического состава природных вод. Кислород поступает в воду в результате происходящих в природе процессов фотосинтеза и из атмосферы. Расходуется кислород на окисление органических веществ, а также в процессе дыхания организмов. Концентрация растворенного кислорода в природных водах колеблется в ограниченных пределах (от 0 до 14 мг/л, при интенсивном фотосинтезе, в полдень, возможна и более высокая концентрация). Вследствие зависимости концентрации кислорода в поверхностных водах от целого ряда факторов его концентрация значительно меняется в течение суток, сезона и года. Так как потребление кислорода сравнительно мало зависит от суточных изменений солнечной радиации, а фотосинтез всецело определяется ею, то в течение дня происходит накопление кислорода, а в темное время суток расходование его. Кислород необходим для существования большинства организмов, населяющих водоемы. Как сильный окислитель кислород играет важную санитарно-гигиеническую роль, способствуя быстрой минерализации органических остатков.
Диоксид углерода (CO2) находится в воде главным образом в виде растворенных молекул газа CO2. Однако часть их (около 1 %) вступает во взаимодействие с водой, образуя угольную кислоту:
Диоксид углерода расходуется также на растворение карбонатов:
Мезоэлементы
Способствует неустойчивости кремния в растворе и склонность кремниевой кислоты при определенных условиях переходить в гель. В очень мало минерализованных водах кремний составляет существенную, а иногда и преобладающую часть химического состава воды, несмотря на его малое абсолютное содержание. Присутствие кремния в воде является серьезной помехой в технике, так как при продолжительном кипячении воды кремний образует в котлах очень твердую силикатную накипь.
Алюминий поступает в водоёмы в результате действия кислот на глины (каолин):
Микроэлементы
Факторы влияющие на химический состав воды
Почти на всей европейской части России (кроме Карелии и Мурманской области) известняки, а также доломиты MgCO3•CaCO3 залегают довольно близко к поверхности. Поэтому вода здесь содержит преимущественно гидрокарбонаты кальция и магния. В таких реках, как Волга, Дон, Северная Двина, и основных их притоках гидрокарбонаты кальция и магния составляют от 3/4 до 9/10 всех растворённых солей.
Соли попадают в водоёмы и в результате деятельности человека. Так, хлоридами натрия и кальция зимой посыпают дороги, чтобы растапливать лёд. Весной вместе с талой водой хлориды стекают в реки. Треть хлоридов в реках европейской части России привнесена туда человеком. В реках, на которых стоят крупные города, эта доля гораздо больше.
Рельеф местности косвенно влияет на состав воды, способствуя вымыванию солей из толщи пород. Глубина эрозионного вреза реки облегчает поступление в реку более минерализованных грунтовых вод нижних горизонтов. Этому же способствуют и другие виды депрессий (речные долины, балки, овраги), улучшающие дренирование водосбора.
Климат же, создает общий фон, на котором происходит большинство процессов, влияющих на формирование химическою состава природных вод. Климат прежде всего определяет баланс тепла и влаги, от которого зависит увлажненность местности и объем водного стока, а следовательно, и разбавление или концентрирование природных растворов и возможность растворения веществ или выпадения их в осадок.
Огромное влияние на химический состав воды и его изменение с течением времени оказывают источники питания водного объекта и их соотношение. В период таяния снега вода в реках, озерах и водохранилищах имеет более низкую минерализацию, чем в период, когда большая часть питания осуществляется за счет грунтовых и подземных вод. Это обстоятельство используют при регулировании наполнения водохранилищ и сброса из них воды. Как правило, водохранилища наполняют в период весеннего половодья, когда приточная вода имеет меньшую минерализацию.








