что такое кальциевая жесткость
Соли кальция в воде
Источники кальция в воде
Кальций в воде встречается в виде солей сильных и слабых кислот: карбонатов и гидрокарбонатов (CaCO3), сульфатов и сульфитов (CaSO4, CaSO3) фторидов (CaF2), фосфатов (Ca5(PO4)3), а также других солей. Основные источники кальция в воде:
Содержание ионов кальция в воде
В растворенном виде соединения кальция содержатся в морской воде и воде из подземных источников и открытых водоемов. Наибольшее количество кальция присутствует воде из горных рек и источников, артезианских скважин. На высокое содержание кальция в водопроводной воде или воде из скважины указывает:
Как определить количество кальция в воде
Нормы по содержанию кальция в воде
Постоянная жесткость зависит от содержания сульфатов, хлоридов магния и кальция. Эти соли не разлагаются при кипячении. Такая жесткость называется некарбонатной.
По катионному составу различают кальциевую и магниевую жесткость. Вода из источников, залегающих в известняковых породах, имеет высокое содержание ионов кальция. Вода из районов с залежами доломита имеет преимущественно магниевую жесткость.
Но для чего определяют кальций в воде, и как он влияет на наш организм?
Влияние кальция на организм
От 10 до 20% кальция мы получаем из питьевой воды. Недостаток также как и переизбыток этого элемента приводит к ухудшению здоровья, а именно:
В отдельных случаях возникают судороги, проблемы с сердечно-сосудистой системой, желудочно-кишечным трактом. При значительном избытке возникают нарушения сердечного ритма и работы центральной нервной системы. Избыток соединений кальция также является причиной ряда расстройств и заболеваний. Если в воде много кальция возникает:
Превышения кальция в водопроводной воде или воде из скважины приводит к увеличению расхода электроэнергии, снижению срока службы систем и техники. При избыточном содержании кальция и натрия в воде рекомендуются устанавливать ионообменные фильтры. Это поможет избежать проблем со здоровьем и продлит срок службы домашней техники и бытовых систем.
Необходимость дополнительной очистки воды от солей жесткости возникает при содержании солей Мg или Ca от 10 мг-экв./л. Для этого применяют ионообменные фильтры умягчения и установки обратного осмоса.
Определить необходимость установки фильтра для удаления кальция можно после анализа вода и определения химического состава примесей.
Что такое жесткость воды и как ее определить
Жесткость в питьевой воде
Под термином жесткость воды понимается количество растворенных и нерастворенных солей, присутствующих в природных водных залежах. Водица может быть слишком мягкой или слишком жесткой. Вредны оба варианта. Недостаток солей нарушает водно-щелочной баланс в организме, избыток вызывает множественные заболевания важных органов: сердца, почек, кожи, печени. При переизбытке солей жидкость имеет горьковато-металлический вкус, может быть мутной, с разными цветовыми оттенками.
Какие соли обуславливают жесткость природной воды, откуда они берутся
После естественного испарения или после принудительного выпаривания водного раствора соли становятся видимыми, остаются в сосуде. Именно они образуют отложения на дне и стенках посуды, чайников, санприборов. По жесткости воды легко определить, какая соль в ней явственнее присутствует. Примеси магния труднее растворяются, придают напиткам вкус горечи.
От чего зависит присутствие соли жесткости в воде
Степень жёсткости для питьевой воды определяется типом и количеством водных солей. В разной местности показатели различные. Соли проникают в водоносные пласты, вымываясь из залежей горных пород: известняков, гипсов, доломитов.
Показатели жёсткости воды являются величинами переменными, они зависят от разных факторов:
У вод, лежащих близко к поверхности и залегающих на глубине, параметры разные. Они выше там, где водный поток проходит через слои известняков. Весной, при обилии талых потоков, при их попадании в водоемы и при просачивании в подземные водные пласты, количество солей снижается. Зимой концентрация выше.
Классификация воды с солями жесткости
Какие соли жесткости присутствуют в воде? Различают общую, постоянную и временную жёсткость:
При очистке принимаются во внимание все типы: Жо, Жк, Жнк. Предельно допустимая концентрация питьевой воды по жесткости (кратко: ПДК) обычно устанавливается для общей Жо.
Нормы жесткости для воды
Нормирование определяется документами стандартизации: ГОСТ, СанПиН, ТУ. Точные данные получают, проводя испытания проб в аккредитованных лабораториях, в санэпидстанциях. Для фиксирования лабораторных показаний приняты международные единицы измерения жесткости воды:
Измеряемая единица жесткости воды 1°Ж равна 1 мг-экв/л и равна 1/2 миллимоля на литр. Допустимые значения для ионов кальция и магния разные: для Ca2+1°Ж=20,04, для Mg2+1°Ж=12,16 мг/л (примечание: эти показатели вставляются в расчетную формулу, см. далее по тексту*).
По структуре вода может быть мягкой, средней, жесткой. Мягкой считается дистиллированная, кипяченая, дождевая, талая водичка. Жидкость средней жёсткости поступает из централизованных водопроводов. Артезианская и родниковая водица тоже отличаются средними показателями. К сильножесткой относится вододобыча из соленых водоемов, нуждающаяся в опреснении. В таблице показаны концентрации солей в разных размерных единицах.
Предельно допустимое содержание солей жесткости в воде
| Степень жесткости воды | Показатель в мг-экв/л | Показатель в °Ж | Показатель в ppm |
| Слишком мягкая | до 1,5 | до 1-1,5 | 0-70 |
| Мягкая | 1,5-4 | 1,6-4 | 71-140 |
| Среднежёсткая | 5-8 | 5-12 | 141-210 |
| Сильножёсткая | 9-12 | 13-22 | 211-320 |
| Сверхжёсткая | свыше 12 | 23-34 | 321-530 |
Нормы жесткости для питьевой воды
В СанПиН указаны вариативные величины, в зависимости от применения водных растворов. Жесткость воды по ГОСТУ также регламентируется в зависимости от типа и назначения жидкостей:
Если в воде солей жесткости больше, чем предписано стандартами, нужно её очистить до допустимых показателей. В табличке указаны степени солевой концентрации по шкале жёсткости с показателями в промилле.
Шкала жесткости
| Концентрация солей | Величина в ppm (в промилле или мг/л) |
| Представляющая опасность для жизни | свыше 500 |
| Предельно допустимая | 500 |
| Средний показатель вод, добываемых из природныхводоемов | 400 |
| Допустимое значение воды, подающейся из водопровода | 300 |
| После прохождения угольных фильтров | 170 |
| После очистки системой обратного осмоса | 0-50 |
Нормы жесткости для технической воды
ГОСТ по определению жесткости в воде подскажет, какие параметры допустимы:
Раздельно нормируется питьевая вода по жесткости разных категорий: дистиллированная, сетевая, разливная. Для солей железа показатели рассчитываются отдельно.
Как определить жесткость воды
Определить жесткость воды в можно как в лаборатории, так и в домашних условиях. Наличие солей жесткости можно определить визуально:
Повышенная жесткость питьевой воды может причинить ущерб здоровью и нагревательным приборам. Не зная точных показателей концентрации солей, сложно рассчитать дозу средств от накипи для стирально-сушильных агрегатов или запрограммировать на чистку кофемашину. Трудно обеспечить комфортное обитание рыбкам в аквариуме или правильно выбрать фильтры очистки. Помимо визуальной оценки лучше использовать более точные измерительные методы определения жесткости питьевой и технической воды.
Измерение жесткости воды
Перед употреблением в пищу, перед поливом огорода, перед подачей в трубопроводы или перед техническим применением воды для производственных процессов полезно проверить наличие солей жесткости. Такая проверка снимет претензии потребителей к водоснабжающим компаниям, продлит срок службы дорогого промышленного оборудования.
Для измерения жесткости воды используют бытовые и профессиональные приборы:
Полезно заказать исследование в лаборатории, чтобы получить точные результаты с подтверждающей документацией. Тогда не придется думать, чем определить жесткость воды, не нужно покупать измерительные приборы или рассчитывать показатели по косвенным параметрам, используя формулы.
Как определить жесткость воды по формуле
Определить жесткость воды можно по формуле. Для определения общих показателей нужно выполнить расчет:
Жо = [Ca 2+ ] + [Mg 2+ ] = (m(Ca 2+ ))/(Э(Ca 2+ ) x V(H2O)) + (m(Mg 2+ ))/(Э(Mg 2+ ) x V(H2O)),
Далее вычисляют временную или постоянную жёсткость. Рассчитанную величину вычитают из Жо и получают значения всех трёх категорий Ж.
Карбонатная Жк вычисляется по формуле:
Как понизить жесткость в питьевой воде
Понизить жесткость питьевой воды можно бытовыми способами и с помощью профессионального оборудования. Для умягчения водных составов в быту применяют простые и доступные методы: кипячение, отстаивание, заморозка с оттаиванием. Используют дистилляты и бытовые фильтры.
Для загородных домов и промышленного умягчения используют профессиональные установки солеочистки:
На сайте компании Diasel можно купить любые фильтры для удаления из воды солей жесткости. Мы продаем комплектующие к установкам обратного осмоса, соберем для вас комплексные линии очистки, предоставим реагенты для снижения уровня безопасности основного жизненного напитка. Гарантируем консультации по любым вопросам, помощь по монтажным работам, текущему и сервисному обслуживанию. С нашими профессиональными установками жесткость воды всегда будет в норме.
Жесткость воды: воздействие на здоровье и сантехнику
Введение
Жесткость воды — одно из важнейших свойств, имеющее большое значение при водопользовании. Если в воде находятся ионы металлов, образующие с мылом нерастворимые соли жирных кислот, то в такой воде затрудняется образование пены при стирке белья или мытье рук, в результате чего возникает ощущение жесткости. Жесткость воды пагубно сказывается на трубопроводах тепловых сетей, приводя к образованию накипи. По этой причине в воду приходится добавлять специальные «смягчающие» химикаты.
Жесткость воды обусловлена присутствием растворимых и малорастворимых солей-минералов, главным образом кальция (Са2+) и магния (Mg2+). Кроме указанных, к солям жесткости относят также соли стронция (Sr 2+ ), цинка (Zn 2+ ) и др., однако в поверхностных и грунтовых природных водах из перечисленных катионов в заметных концентрациях присутствуют только кальций и магний.
Суммарная жесткость воды, то есть общее содержание растворимых солей кальция и магния, получила название «общей жесткости». Ввиду того, что солями жесткости являются соли разных катионов, имеющие разную молекулярную массу, концентрация солей жесткости, или жесткость воды, измеряется в единицах эквивалентной концентрации — количеством г-экв/л или мг-экв/л.
При жесткости до 4 миллиграмм эквивалент/литр вода считается мягкой; от 4 до 8 миллиграмм эквивалент/литр — средней жесткости; от 8 до 12 миллиграмм эквивалент/литр — жесткой; более 12 миллиграмм эквивалент/литр — очень жесткой.
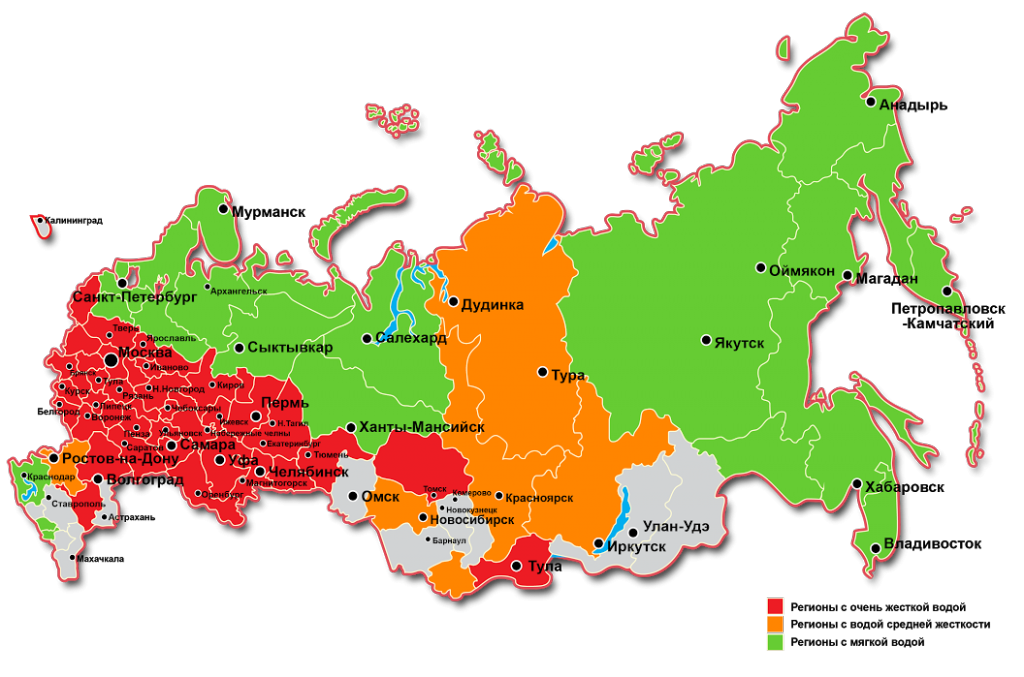
В различных регионах России жесткость поверхностных и грунтовых вод отличается: преимущественно мягкие воды географически приурочены к районам севера Европейской части России, а также Восточной Сибири. В центре и на юге Европейской части России, а также в южных регионах Западной Сибири вода преимущественно жесткая. В естественных условиях ионы кальция, магния и других щелочноземельных металлов, обусловливающих жесткость, поступают в воду в результате взаимодействия растворенного диоксида углерода с карбонатными минералами и других процессов растворения и химического выветривания горных пород. Источником этих ионов являются также микробиологические процессы, протекающие в почвах на площади водосбора, в донных отложениях, а также сточные воды различных предприятий. Различные типы пород, залегающих на территории водосборов, а также взаимосвязанные с ними свойства почвенного покрова непосредственно обуславливают различия в жесткости вод в регионах нашей страны.
Воздействие жесткости на организм
Поиск причинно-следственных связей между жесткостью воды и сердечно-сосудистой патологией был результативным. В ряде исследований установлена статистически достоверная, хотя и не тесная, обратная корреляционная связь между жесткостью воды и частотой инфаркта миокарда. Поскольку в других, не менее тщательно выполненных исследованиях, такой связи не было установлено, считается, что патогенетическим агентом могли быть не сами соли жесткости, а коррелирующие с ними какие-либо другие микроэлементы. Что касается других проявлений вредного влияния жестких вод, то статистическими исследованиями установлено и экспериментально подтверждено их влияние на частоту возникновения мочекаменной болезни. В этом случае не идет речи о прямой детерминированности степени жесткости воды и заболеваний мочекаменной болезнью. Решающую роль играют другие сопутствующие факторы, в частности состояние минерального обмена конкретного человека, потребляющего жесткую воду. Высокое содержание в питьевой воде солей кальция и магния является фактором риска мочекаменной болезни.
Воздействие жесткости на сантехнику
Воздействие повышенной жесткости воды на контактирующие с ней приборы и сантехнику приводят к следующим последствиям:
Жёсткость воды из-за образующихся отложений негативно влияет на котельное оборудование. В России введены строгие требования к качеству воды по жёсткости для котлов ТЭЦ, электростанций, промышленных водонагревателей. Поэтому умягчение воды (водоподготовка) является в этом случае обязательным условием.
Способы умягчения воды
Умягчение воды может быть осуществлено следующими основными способами:
Нередко представляется целесообразным комбинировать эти способы, удаляя часть солей жесткости реагентным способом, а остаток их — катионированием, либо применять реагентный способ в комбинации с термическим способом умягчения воды.
Из реагентных способов умягчения наиболее распространен известково-содовый способ. Сущность его состоит в переводе растворенных в воде солей Са 2+ и Mg 2+ в малорастворимые СаСОз и Mg(OH)2, выпадающие в осадок.
Катионитовый способ умягчения воды заключается в фильтровании жесткой воды через мелкозернистую загрузку некоторых веществ (сульфоуголь, искусственные смолы). Эти вещества обладают способностью обменивать катионы содержащегося в них натрия Na + или водорода Н + на катионы кальция Са 2+ или магния Mg 2+ солей жесткости, растворенных в воде. Таким образом, различают процесс Na-катионирования и Н-катионирования.
Когда обменная способность катионитового фильтра исчерпана, производят регенерацию катионитовой загрузки. Na-катионитовые фильтры регенерируются раствором поваренной соли NaCl, а Н-катионитовые — растворами серной H2SO4 или соляной HCl кислот.
Вода после Na-катионитовых фильтров обычно имеет повышенную щелочность (рН>7), а после Н-катионитовых — повышенную кислотность (рН
Что такое жесткость в воде
Что такое жесткость воды
Термин общая жесткость воды возник в результате наблюдений за состоянием тканей после стирки. Особая структура материала, состоящего из отдельных нитей, способствует накоплению упомянутых солей металлов. При большом их содержании ткань, становится жесткой и грубой. Позже было замечено, что высокая концентрация таких соединений существенно снижает эффективность моющих средств.
Основные причины образования жесткости воды
Фактически эта жидкость является универсальным растворителем, который при контакте с почвой и минералами насыщается содержащимися в ней веществами и химическими соединениями. Отвечая на вопрос о жесткости воды, и чем она обусловлена, необходимо выделить основные источники солей щелочноземельных металлов:
Помимо естественных причин повышенное содержание ионов жесткости в воды обусловлено также и техногенными. В составе стоков промышленных, строительных и коммунальных предприятий имеется большое количество примесей. В результате происходит вторичное загрязнение водоемов и водоносных слоев.
Естественные процессы химического выветривания горных пород и техногенные факторы определяют параметры жесткости воды питьевой или технической. Эти показатели неодинаковы для различных источников и постоянно изменяются:
Виды жесткости воды
Уровень содержания солей и их состав для разных источников водоснабжения как открытых, так и закрытых различаются и существенно. Возникает закономерный вопрос, а какова жесткость воды, и какой она может быть в зависимости от происхождения. Существует классификация по уровню насыщенности химическими веществами и соединениями, для удобства сведенная в таблицу:
| Наименование | мг∙экв/л | Градусы °dH | ppm |
| Очень мягкая | не более 1,5 | 0-4° | 0-70 |
| Мягкая | от 1,5 до 4,0 | 5-8° | 70-140 |
| Средней жесткости | от 4,0 до 8,0 | 9-12° | 140-210 |
| Жесткая | от 8,0 до 12,0 | 13-22° | 210-320 |
| Очень жесткая | свыше 12,0 | 23-34° | 320-530 |
Приведенная шкала наглядно показывает уровни жесткости воды, и в чем она измеряется в системах, принятых в разных государствах. Данная классификация отображает методические подходы к определению означенного показателя в соответствии с нормативными документами следующих стран:
При сравнительно невысоком уровне жесткости воды содержание ионов кальция в ней может достигать 70-80%, в тоже время насыщенность ионами магния редко превышает 50-60%. При увеличении уровня минерализации картина резко меняется: концентрация первых сильно уменьшается и редко доходит до 1 г/л; содержание же ионов магния часто превышает показатель 10 г/л. Такое соотношение особенно характерно для соленых озер, не имеющих стока.
Классификация вод осуществляется не только по уровню жесткости, но и с учетом ее гидрохимического состава. По данному признаку различают следующие разновидности:
Для каждого типа характерно определенное соотношение содержания солей кальция, магния и других. Соответственно методы уменьшения жесткости воды зависят от ее вида, и состав оборудования для конкретного случая определяется с учетом реальных показателей. Рассмотрим этот вопрос подробнее.
Общая жесткость воды
Перечисленные соли, определяющие общую жесткость воды, при кипячении не разлагаются и их удаление из жидкости требует иных методов. Для численного выражения этого показателя используют специальную физическую единицу 1 ммоль-экв./л, которая соответствует содержанию 20,04 мг/л катионов кальция либо 12,16 мг/л катионов магния.
Общая жесткость подземных вод (в некоторых регионах), а также морских и океанских может достигать 80 и даже 100 ммоль-экв/л, что делает их непригодными для использования. В тоже время в реках и озерах, находящихся в таежных районах данный показатель находится на уровне от 0,1 до 0,2 ммоль-экв/л. Такой водой практически невозможно смыть мыльный раствор.
Временная жесткость (карбонатная)
Постоянная жесткость (некарбонатная) воды
Помимо гидрокарбонатов кальция и магния в источниках водоснабжения присутствуют в значительных количествах соли азотной, серной и соляной кислоты. Под некарбонатной жесткостью воды подразумевается суммарное содержание этих химических соединений. Последние при нагревании остаются в растворенном состоянии и не выпадают в осадок.
Некарбонатная жесткость воды именно поэтому и называется постоянной, а для ее устранения необходимо специальное оборудование. Существенно уменьшить концентрацию этих растворимых соединений возможно при использовании ионообменных технологий и деминерализации. Особенно высока эффективность у современных систем умягчения.
Действующие нормативы жесткости воды
Жесткость общая воды в части гигиенических норм устанавливается требованиями СанПиН 2.1.4.1075-01, утвержденным Постановление от 26.09.2001 года. Суммарный показатель содержания солей щелочноземельных металлов не должен превышать предельно-допустимых концентраций, которые определены в размере 7,0 и 10,0 мг-экв./л. Второе значение может быть установлено только по решению главного санитарного врача с учетом используемой технологии водоподготовки для конкретного населенного пункта.
Расчет жесткости воды
При определении общей жесткости воды допускается применение вычислительных методов. Этот показатель измеряется в ммоль/дм 3 или моль/м 3 и описывается следующей формулой:
Данное уравнение позволяет вычислить среднюю жесткость воды, в ней приняты следующие обозначения:
Для того чтобы рассчитать общую жесткость воды необходимо знать молярную масса катионов кальция и магния, а также анионов сернистой кислоты. Результаты вычислений могут быть использованы для определения наиболее подходящего метода ее очистки. Подобные расчеты проводятся специалистами профильных лабораторий на основании опытных данных.
Методы определения уровня жесткости воды
Как определить жесткость воды? Точная оценка количественных параметров содержания солей производится специализированными лабораториями. В соответствии с ГОСТ 31954-2012 общая жесткость воды определяется комплексонометрическим методом в такой последовательности:
Обработка результатов, полученных с использованием описанного метода определения общей жесткости воды, выполняется по следующей формуле:
Результат испытаний согласно данному методу определения общей жесткости в питьевой воде, а также технической, вычисляется как среднеарифметическое от двух полученных значений. Это позволяет минимизировать погрешность расчетов.
Бытовые способы умягчения воды
Высокая соленость и жесткость воды, используемой в пищу и в хозяйственно-бытовых целях, может принести вред здоровью и привести к выходу из строя бытовой техники. В домашних условиях уменьшить этот показатель можно путем термической и химической обработки исходной жидкости.
Химическая обработка в целях снижения жесткости исходной воды выполняется при помощи извести и соды. Первый реагент обеспечивает умягчение жидкости с незначительным содержанием некарбонатных и высокой насыщенностью карбонатными соединениями. Для повышения эффективности данного метода дополнительно применяются реагенты коагулянты.
Комбинирование извести и пищевой соды позволяет уменьшить общую жесткость речной или колодезной воды до значений 1,4-1,8 мг экв./л. Химическая обработка обеспечивает улучшение качества жидкости по данному показателю, но требует очень точной дозировки реагентов. Кроме того она непригодна для приготовления пищи и питья.
Профессиональные методы снижения жесткости воды
При выборе установки для снижения жесткости воды, прибором для ее определения устанавливают точный гидрохимический состав и количественное содержание солей. Оборудование подбирается по результатам испытаний и с учетом требований заказчика к качеству обработанной воды.
Фильтры умягчения
Процесс уменьшения общей жесткости воды должен быть достаточно эффективным и недорогим. В настоящее время основным способом умягчения является метод натрий-катионирования (фильтры умягчения), который применяется и в быту, и в промышленных масштабах. Поток воды пропускается через ионообменные колонны, где происходит замещение кальция и магния катионами натрия. На поверхности полимерных смол происходят следующие химические реакции:
Ca 2+ + 2RNa = 2Na + + R2Ca
Mg 2+ + 2RNa = 2Na + + R2Mg
В результате общая жесткость доводится до уровня питьевой воды по ГОСТу, что делает возможным ее применение для приготовления пищи и хозяйственно-бытовых нужд.
Такие фильтрующие колонны применяются в составе многоступенчатых систем, в которых вода сначала очищается от механических примесей и железа. Это позволяет повысить ресурс основных картриджей, который естественным образом уменьшается в процессе расходования ионов натрия и накопления ионов жесткости. Для восстановления свойств ионообменных смол в системе предусмотрены баки с раствором поваренной соли, клапаны и блоки управления.
Когда датчик фиксирует повышение жесткости воды в ppm, подача ее перекрывается и производится обратная промывка содержимого колонны солевым раствором. После восстановления характеристик полимерных гранул, подача реагента прекращается. Открывается клапан и возобновляется процесс умягчения.
Управление работой такого фильтра, обеспечивающего уменьшение общей жесткости природной воды, в зависимости от комплектности осуществляется в автоматическом или в ручном режиме. В первом варианте используются электронные датчики и электроклапаны. Во втором случае переключение установки в режим регенерации выполняется человеком по истечении определенного периода времени.
Ионообменные фильтры
Данный метод умягчения по принципу действия в значительной мере аналогичен описанному выше. Замещение ионов, обуславливающих жесткость воды, в них происходит с помощью многокомпонентных смол типа Ecomix или Ecotar. В состав этих фильтрующих загрузок входят следующие материалы:
Применение многокомпонентных составов для фильтрующих установок позволяет снизить общую жесткость воды за счет реакции замещения катионов кальция и магния. Данная технология более универсальна в сравнении с фильтрами умягчения, однако и менее эффективна. При этом финансовые затраты на ее приобретение и содержание выше нежели у специализированных элементов.
Обратный осмос
Использование полупроницаемых мембран обеспечивает высочайший уровень очистки жидкости от всех видов примесей. В современных системах обратного осмоса показатели общей жесткости воды после кондиционирования на мембранах типа DRO-4040 или DRO-8040 снижаются более чем на порядок. Такие установки применяются для опреснения соленых воды (океанских, морских, озерных и подземных).
Мембраны имеют пористую структур, пропускающую только молекулы воды и задерживающую соединения кальция и магния (гидрокарбонатные и соли кислот). В результате происходит снижение общей жесткости воды до значений, делающих возможным ее применение в фармацевтике и микроэлектронике. Пермеат практически не содержит микроэлементов и нуждается в минерализации для питья и приготовления пищи.
Такие показатели, существенно превосходящие ГОСТ для питьевой воды по общей жесткости, явно избыточны. С учетом высоких начальных затрат на приобретение, монтаж и последующее обслуживание использовать установки обратного осмоса в быту экономически невыгодно. Гораздо эффективнее для таких целей применять традиционные фильтры умягчения.
Что такое общая жесткость воды
Получив представление о жесткости воды, и как она влияет на организм, а также на бытовую технику и другое оборудование, приходим к выводу о необходимости ее нормализации. Кустарные методы (кипячение или химобработка) не обеспечивают надлежащего качества воды. Кардинальное решение проблемы возможно только при использовании современных фильтрационных установок.
Компания Diasel Enginereeng предлагает высокоэффективные системы водоподготовки: фильтры умягчения и ионообменные, а также обратноосмотические. Мы предоставляем полный комплекс услуг по проектированию установок, подбору, монтажу и запуску оборудования. Наши специалисты обеспечивают их сервисное и гарантийное обслуживание. Перейти в раздел «Контакты».