что такое интервиллузит очаговый
Опыт исследования развития фетоплацентарной недостаточности при герпесвирусной инфекции
Ташкентский институт усовершенствования врачей, Узбекистан
Внутриутробная инфекция (ВУИ) представляет собой серьезную проблему современной перинатальной медицины, так как данное осложнение может быть причиной перинатальной патологии и смертности матери и ребенка [1-3, 6, 9].
ВУИ играет важную роль в генезе различных патологических процессов при беременности, оказывает вредное влияние на исход беременности и состояние новорожденного. В подавляющем большинстве случаев ВУИ является причиной антенатальной патологии: 32% самопроизвольного выкидыша, 24% внутриутробной задержки развития плода и преждевременных родов. Наиболее распространенным представителем нативных вирусов является герпесвирусная инфекция, частота обнаружения вируса простого герпеса (ВПГ) составляет 98,9% среди взрослого населения земного шара [1, 2, 4, 7].
В последние годы отмечается тенденция к увеличению инфицирования беременных ВПГ. Генитальной герпетической инфекции уделяется большое внимание, так как ее способность активно размножаться в плаценте и эмбриональных тканях, проникать через плацентарный барьер и вызывать внутриутробное поражение плода приводит к формированию плацентарной недостаточности и развитию пороков развития плода [1-3, 6].
Возрастающая роль внутриутробных инфекций среди причин неблагоприятных перинатальных исходов определяет актуальность всестороннего изучения этой проблемы.
Цель исследования: изучение роли ВПГ в генезе плацентарной недостаточности и определение специфических изменений в плаценте женщин с генитальной герпетической инфекцией.
Материалы и методы исследования. Под нашим наблюдением находилось 204 женщины с диагностированной вирусной инфекцией, Возраст больных составлял от 18 до 37 лет. У всех пациенток в анамнезе (1,2±0,4 года назад) были перинатальные потери, хронические воспалительные заболевания репродуктивной системы, что и послужило основанием для проведения детального клинико-лабораторного, в том числе серологического, обследования на наличие вирусной инфекции. Также проводилось ультразвуковое исследование плода и плаценты в 16-17, 24-28 недель гестации и накануне родов с осуществлением допплерометрии и ультразвуковой фетометрии плода.
Макроскопическое, морфометрическое, гистологическое и иммуногистохимическое исследование плаценты, пуповины и околоплодных оболочек.
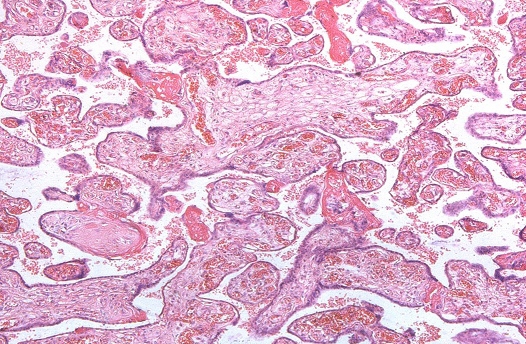
Во всех наблюдениях при наличии доношенной беременности в плаценте отмечались различной степени выраженности нарушения дифференцировки структур. При этом выявлялись поля ворсин, находящихся на разных стадиях развитая. Преобладали терминальные ворсины. Наряду с ними определялись участки, содержащие незрелые и зрелые промежуточные, хаотичные, склерозироваиные и единичные эмбриональные ворсины. Незрелые промежуточные ворсины характеризуются неправильной формой, крупными размерами (диаметр 110-180 мкм), единичными отходящими от них мелкими ветвями, рыхлой стромой, слабой васкуляризацией (5-8 центрально расположенных мелких капилляров), присутствием клеток Кащенко-Гофбауэра. Наличие значительного количества таких ворсин в плаценте при доношенной беременности свидетельствует о нарушении развития ворсинчатого хориона при сроке гестации 19-25 недель. Зрелые промежуточные ворсины имеют округлую форму, диаметр 60-80 мкм, малое количество ответвлений. В рыхлой строме центрально и субэпителиально видны 5-6, иногда 6-8 гиперемированных капилляров. Доминирование таких ворсин характерно для 26-31 недель беременности. Во всех случаях наблюдаются в различном количестве эмбриональные ворсины. Крупные (диаметром 120-140 мкм), многопластные, бессосудистые, покрытые тонким синцитиотрофобластом, они имеют рыхлую строму, систему стромальных каналов и свободно лежащие клетки Кашенко-Гофбауэра. Преобладание таких ворсин характерно для 8-12 нед. гестации. Таким образом, во всех наблюдениях отмечалось диссоциированное развитие ворсинчатого хориона с преобладанием терминальных ворсин.
Рис. 1. Патологическая незрелость ворсин хориона при герпесвирусной инфекции у беременных
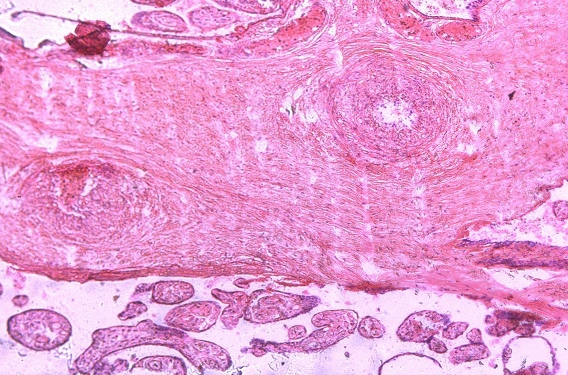
В ткани плаценты с помощью флюоресцирующих моноклональных антител выявлялись антигены вируса простого герпеса 1-го и 2-го типа. Причем 1-й тип у 15%, 2-й у 40%, сочетание 1-го и 2-го типов у 45%. Светооптически в плаценте пораженных только вирусом простого герпеса 1-го или 2-го типа, изменения идентичны. Характерным является наличие ограниченного продуктивного очагового воспаления с вовлечением в патологический процесс плодовой и материнской частей плаценты. При этом в эпителии амниона, синцитиотрофобласте, эндотелии сосудов, клетках базальной пластинки и септ выявляются гигантские одноядерные клетки с крупными гиперхромными ядрами, содержащими базофильное включение. Последние отделены от кариолеммы полоской просветления и содержат антиген вируса простого герпеса. Часть клеток эпителия амниона и трофобласта претерпевает некротические изменения. Во всех случаях наблюдаются распространенные поражения стенок сосудов ворсин в виде очагового эндоваскулита, иногда с некрозом части внутренней выстилки и формированием тромбов. Интервиллезит встречается нечасто и носит очаговый характер. Более типичными являются кровоизлияния или очаги тромбоза в межворсинчатом пространстве. Базальный децидуит различной степени выраженности имеется во всех наблюдениях. Некротические изменения встречаются как в отдельных клетках, так и в виде очагов. Постоянно выявляются участки склероза, диффузные отложения солей кальция, фибриноида в ворсинах и базальной пластинке.
Рис. 2. Отложение фибриноида в прилежащем межворсинчатом пространстве
Изменения в плаценте во многом зависят от времени возникновения рецидивов и их количества. Степень деструкции более выражена у пациенток, имевших 4 рецидива и более.
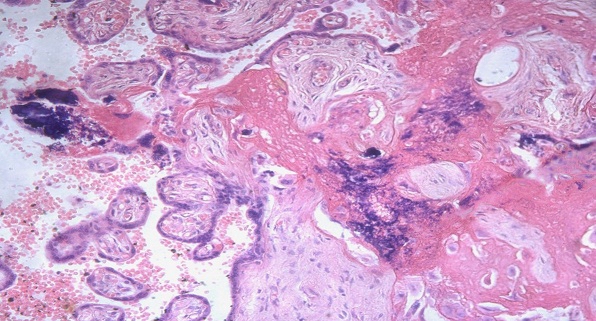
Возникновение рецидивов герпетической инфекции в III триместре беременности сочетается с альтеративными процессами в структурах последа. В базальной пластинке, септах, крупных и мелких ворсинах, амнионе, гладком хорионе обнаруживаются резко выраженные дистрофические изменения, некробиоз, очаги фибриноидного некроза. При этом имеется лимфоидно-плазмоцитарная и лимфоидно-макрофагальная воспалительная реакция, нередко с гигантоклеточным метаморфозом и очаговыми кровоизлияниями.
Рис. 3. Некроз и лимфоидная инфильтрация стромы базальной пластины у беременных с герпесвирусной инфекцией
При морфологическом исследовании последов детей, родившихся с явлениями гипотрофии, наряду с характерными изменениями и различной степени выраженности компенсаторно-приспособительными реакциями, имелось явная редукция сосудистого русла ворсинчатого хориона. Это сочеталось с повышением коэффициента плотности ворсин, который составил 4,09±0,06 и, как следствие этого, объем материнской крови в межворсинчатом пространстве был уменьшен. Эти изменения соответствовали относительно субкомпенсированной форме плацентарной недостаточности.
При морфологическом исследовании плаценты после самопроизвольного выкидыша наряду с выраженными альтернативными и воспалительными изменениями отмечалась резкая задержка развития ворсинчатого хориона, выраженный продуктивный васкулит, что сочеталось со слабовыраженными компенсаторно-приспособительными процессами и свидетельствовало о тяжелом герпетическом поражении плаценты с явлениями декомпенсированной формы хронической плацентарной недостаточности.
Заключение. Генитальная герпетическая инфекция приводит к развитию хронической плацентарной недостаточности, степень тяжести которой зависит от времени, частоты и длительности рецидивов заболевания. Изменения в плаценте характеризуются наличием как деструктивных, так и компенсаторных процессов, степень сохранности которых определяет дальнейшее развитие и состояние плода.
Беременных с данной патологией следует отнести к группе высокого риска по возможности развития плацентарной недостаточности. В план обследования пациенток с данной патологией должны быть включены современные методы диагностики состояния фетоплацентарного комплекса и морфологическое исследование последа. Выявленные морфологические изменения последа позволяют своевременно начать патогенетически обоснованную терапию новорожденных, что способствует снижению частоты тяжелых форм неонатального герпеса.
Список использованных источников:
Что такое интервиллузит очаговый
ФГБУ «Ивановский НИИ материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России; ГБОУ ВПО «Ивановская государственная медицинская академия» Минздрава России
ФГБУ «Ивановский НИИ материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России
Патоморфологические особенности плацент у женщин с угрожающими преждевременными родами в зависимости от исхода беременности
Журнал: Российский вестник акушера-гинеколога. 2016;16(5): 4-9
Малышкина А. И., Назарова А. О., Кулида Л. В., Козырина А. А., Назаров С. Б., Жолобов Ю. Н. Патоморфологические особенности плацент у женщин с угрожающими преждевременными родами в зависимости от исхода беременности. Российский вестник акушера-гинеколога. 2016;16(5):4-9.
Malyshkina A I, Nazarova A O, Kulida L V, Kozyrina A A, Nazarov S B, Zholobov Iu N. Pathomorphological placental characteristics in women with threatened premature birth in relation to the outcome of pregnancy. Russian Bulletin of Obstetrician-Gynecologist. 2016;16(5):4-9.
https://doi.org/10.17116/rosakush20161654-9
ФГБУ «Ивановский НИИ материнства и детства им. В.Н. Городкова» Минздрава России
Цель исследования — выявление патоморфологических особенностей плацент у женщин с угрожающими преждевременными родами. Материал и методы. Проведен анализ социальных и клинико-анамнестических данных 117 беременных женщин с угрожающими преждевременными родами в 22—36 нед гестации. У всех беременных прослежены течение и исходы беременностей, у 60 родильниц проведено патоморфологическое исследование последов. Результаты. К основным патоморфологическим изменениям в плацентах при преждевременных самопроизвольных родах в сроки беременности 24—36 нед относятся гипоплазия плацент I—II степени, обусловленная нарушением инвазии сосудистого цитотрофобласта и гестационного ремоделирования спиральных артерий с развитием гипоперфузии плаценты, крупноочаговые, центрально локализованные хронические геморрагические инфаркты, тромбоз межворсинчатого пространства общей площадью более 35%, а также поствоспалительная гиповаскуляризация и нарушение дифференцировки сосудисто-стромального компонента терминальных отделов ворсинчатого дерева на фоне недостаточного развития компенсаторных процессов. Гипоплазия плацент I степени, суммарная площадь хронических нарушений материнского и плодового кровообращения не более 23% от площади материнской поверхности плаценты, базальный, париетальный децидуит и компенсаторная гиперплазия сосудистого компонента промежуточных и терминальных ворсин являются основными признаками структурной перестройки в плацентах у женщин с угрожающими преждевременными родами, родившими своевременно. Заключение. Анализ неблагоприятных медико-социальных факторов и патоморфологических изменений в плацентах позволит разработать персонифицированный подход к профилактике преждевременных родов и проведению прегравидарной подготовки последующей беременности. Авторы информируют об отсутствии конфликта интересов.
ФГБУ «Ивановский НИИ материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России; ГБОУ ВПО «Ивановская государственная медицинская академия» Минздрава России
ФГБУ «Ивановский НИИ материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России
ФГБУ «Ивановский научно-исследовательский институт материнства и детства им. В.Н. Городкова» Минздрава России
В современном акушерстве одной из наиболее актуальных проблем остается невынашивание беременности. В экономически развитых странах мира число случаев преждевременных родов составляет от 5 до 9%, а в различных регионах Российской Федерации — от 6 до 15% [1]. Преждевременные роды определяют высокую перинатальную заболеваемость и смертность. В структуре ранней неонатальной смертности недоношенные дети составляют 60—70%, из них 50% имеют различную степень выраженности неврологических расстройств [2, 3].
Выявление изменений в плаценте может иметь большое значение для установления причины преждевременных родов [4]. Среди многочисленных факторов, способствующих развитию преждевременных родов, ведущее место занимают системные и внутриутробные инфекции, стресс и перерастяжение матки, маточно-плацентарный тромбоз, внутриматочные сосудистые поражения и децидуальные кровоизлияния. Развивающиеся при этом повреждения в фетоплацентарном комплексе проявляются в виде патологических преобразований спиральных артерий, артериального тромбоза и маточно-плацентарной ишемии [5, 6].
Исход беременности при угрозе преждевременных родов, помимо этиологических и патогенетических факторов, тесным образом связан с морфофункциональным состоянием плаценты как связующего звена элементов функциональной системы мать—плацента—плод [7, 8]. Новые взгляды на механизмы регуляции маточно-плацентарного кровотока и возникновение плацентарной недостаточности дадут возможность оказать своевременную персонифицированную помощь женщине и ее ребенку, а также улучшат раннюю диагностику нарушений плацентации при последующих беременностях [4].
Цель исследования — выявление патоморфологических особенностей плацент у женщин с угрожающими преждевременными родами.
Материал и методы
Проведен анализ социальных и клинико-анамнестических данных 117 беременных с угрожающими преждевременными родами в 22—36 нед гестации, которые были разделены на две группы: 1-ю группу составили 62 женщины, родившие своевременно; 2-ю группу — 55 женщин, у которых произошли самопроизвольные роды до 37 нед беременности. Критериями включения в исследование являлись одноплодная самопроизвольно наступившая беременность у женщины молодого репродуктивного возраста без тяжелых соматических заболеваний, добровольное информированное согласие женщины. Исследование одобрено локальным этическим комитетом. Диагноз угрожающих преждевременных родов устанавливался при наличии у беременной абдоминального болевого синдрома и структурных изменений шейки матки (размягчение, укорочение менее 20 мм и раскрытие шейки матки) — код по МКБ-10 O47.0. Обследование и лечение женщин, включенных в исследование, проводились согласно клиническим рекомендациям Минздрава России «Преждевременные роды» № 15−4/10/2−9480 от 17.12.13, в акушерском стационаре ФГБУ «Ивановский НИИ материнства и детства им. В.Н. Городкова».
Социальные и клинико-анамнестические данные беременных регистрировались в специально разработанных акушерских картах.
Патоморфологическое исследование последов проведено у 60 родильниц: у 29 пациенток 1-й группы и 31 пациентки 2-й группы. Морфологическая оценка структурных изменений плацент включала макроскопическое описание, органометрию и обзорное гистологическое исследование. После осмотра последа и освобождения его от сгустков крови определяли линейные параметры (два диаметра и толщину плаценты), массу плаценты без оболочек с культей пуповины не более 0,5 см, а также площадь материнской поверхности и объем макропатологии (участки инфарктов, кровоизлияния, петрификаты и гематомы).
Взятие и последующая фиксация биологического материала проводились с учетом топографических особенностей плаценты: из центральных, парацентральных и краевых отделов плаценты. Дополнительно исследовались патологически измененные участки плаценты, пуповина и фрагменты плодных оболочек, закрученные в виде спирали. Для обзорного гистологического исследования материал из плацент помещался в 10% раствор нейтрального формалина. С фиксированного материала после осуществления стандартной парафиновой проводки готовились срезы, окрашиваемые гематоксилином Эрлиха с докраской эозином.
Математические методы обработки полученных данных включали статистический анализ c использованием программы Statistica 10.0, методы клинической эпидемиологии (расчет отношения шансов — ОШ и 95% доверительных интервалов — ДИ с использованием системы OpenEpi). Различия относительных показателей определяли с использованием непараметрических критериев Стьюдента, Фишера, χ 2 и считали достоверными при p 
Средние масса и длина тела при рождении самих пациенток 2-й группы были достоверно ниже этих показателей пациенток 1-й группы (масса тела 3000±70,7 и 3289±57 г, р 

Для плацент 2-й группы была характерной центральная локализация хронических геморрагических инфарктов и тромбоза межворсинчатого пространства, что является прогностически неблагоприятным для исхода данной беременности [10]. Суммарная площадь хронических нарушений кровообращения в плацентах данной группы составила более 35% от площади материнской поверхности и была достоверно больше, чем в группе со своевременными родами (p 
При этом пролиферативный виллузит в 41,9% (р 
Выраженность указанных компенсаторных процессов в плацентах у женщин со своевременными родами связана с меньшей, чем в плацентах родильниц 2-й группы, распространенностью воспаления в ворсинчатом дереве и гестационной зрелостью структурных элементов, составляющих основу обменных процессов между материнским и плодовым кровотоком в плаценте.
При сопоставлении патоморфологических изменений с процессами адаптации и компенсации в сравниваемых группах была диагностирована хроническая плацентарная недостаточность, компенсированная форма которой достоверно чаще определялась в 1-й группе (68,9%; p
Что такое интервиллузит очаговый
Младенческая смертность в России, несмотря на снижение, остается достаточно высокой и составляет 7,5%, причем перинатальные причины в ее структуре достигают 40—60%. Внутриутробные инфекции (ВУИ) являются одной из ведущих причин перинатальных потерь и достигают 30% [1—4]. Частота невынашивания беременности, связанная с наличием очагов инфекции у матери, особенно в урогенитальной системе, остается стабильно высокой — от 10 до 15% [5—7]. В России каждый год рождаются около 11 000 недоношенных детей, выхаживание которых требует от государства значительных затрат, связанных с применением дорогостоящих медицинских технологий [7—9]. В связи с этим проблема планирования семьи, прегравидарной подготовки, своевременной диагностики, лечения и профилактики плацентарной недостаточности имеет не только медицинское, но и социальное значение. Не менее актуальной является экспертная оценка случаев перинатальных потерь.
Цель работы — определение роли внутриутробных инфекций в генезе перинатальных потерь, а также причинно-следственной связи неблагоприятного исхода беременности с действиями медицинских работников.
Материал и методы
В ГБУЗ С.К. Бюро судебно-медицинской экспертизы за период 2011—2016 гг. проведены комиссионные судебно-медицинские экспертизы 28 случаев перинатальной смерти плодов и новорожденных, связанных с ВУИ. Выделили две группы: 1-ю основную и 2-ю — контрольную, в которую вошли 11 практически здоровых женщин, сопоставимых по полу, возрасту, паритету, социальному положению, с физиологическим течением беременности и родов. Изучали медицинскую документацию (карты амбулаторного наблюдения беременных, истории родов и развития новорожденных, протоколы патологоанатомических заключений). Принимали во внимание данные анамнеза, социальный статус пациенток, результаты клинико-лабораторных исследований, особенности течения беременности, родов, периода новорожденности. Производили измерения массы, площади и объема плацент, массы тела и длины живо- и мертворожденных, оценивали состояние новорожденных по шкале Апгар. Изучали особенности терапии, проводимой беременным, роженицам и новорожденным. На основании существующих судебно-медицинских критериев [10, 11] определяли предотвратимость наступления смерти, степень тяжести вреда, причиненного здоровью матери и ребенку. Гистологические препараты внутренних органов мертворожденных и умерших детей, а также последов подвергали судебно-медицинской экспертизе. Препараты окрашивали гематоксилином и эозином, стекла исследовали в проходящем свете под микроскопом Микмед-5 с ув. 40. Микрофотосъемку проводили с помощью цифровой фотокамеры Сanon. Числовые данные подвергали статистической обработке по методу Ойвина.
Результаты и обсуждение
Все женщины проживали на территории Ставропольского края, состояли в браке, социально-бытовые условия были хорошими, беременности желанными. Средний возраст пациенток основной группы составил 26,6±1,1 года, контрольной — 25,9±1,1 года (p≥0,05). Преобладали жительницы села — 60,7%. Все пациентки состояли на учете в женской консультации. В 1-й группе преобладали повторно беременные — 19 (68%) женщин, у 17 (61%) был отягощенный гинекологический анамнез: аборты, воспалительные заболевания женских половых органов, бесплодие, неразвивающаяся беременность. В контрольной группе повторно беременных было 7 (63,6%) без отягощающих факторов в анамнезе.
Гинекологические заболевания во время настоящей беременности выявили у 26—93% обследованных 1-й группы. Преобладали воспалительные заболевания нижнего отдела гениталий. Спектр патогенной микрофлоры был разнообразен. Мико- и уреаплазменная инфекция в клинически значимых титрах обнаружена у 8 (28,6%), хламидийная у 6 (21,4%), микстинфекции с участием бактерий и грибов у 8 (28,6%) женщин.
Экстрагенитальные заболевания диагностировали у 24 (85,7%) женщин 1-й группы. В структуре заболеваний внутренних органов преобладали воспалительные процессы в почках и мочевыводящих путях, легких и ЛОР-органах, их обнаружили у 57% обследованных. Ведущим симптомом патологического течения гестационного процесса у 26 (93%) женщин 1-й группы явилась клинически доказанная угроза прерывания беременности на различных сроках. Патологию амниона в виде мало- и многоводия диагностировали у 14 (50%) женщин в каждой группе. Токсикоз беременных и преждевременную отслойку нормально расположенной плаценты отметили у 4 (14,3%) беременных. В основной группе хроническую плацентарную недостаточность и синдром задержки развития плода диагностировали у 16 (57%) женщин, преждевременное прерывание беременности в срок 28—37 нед произошло у 13 (46,4%), роды в срок 38—40 нед — у 11 (39,3%), пролонгирование беременности и запоздалое родоразрешение в срок 41—42 нед — у 4 (14,3%) обследованных. В контрольной группе все женщины родили в 38—40 нед. Общая продолжительность родов у лиц основной группы составила 455±30,2 мин, контрольной — 560±37,4 мин (p≤0,05); длительный безводный период, превышающий 12 ч, отметили у 7 (25%), аномалии родовой деятельности у 5 (17,86%) рожениц 1-й группы. Объем кровопотери в родах в 1-й и 2-й группах составил 332±25,4 и 259±9,1 мл (p≤0,02) соответственно. Кровотечение в раннем послеродовом периоде, превышающее 1000 мл, с развитием геморрагического шока зарегистрировали у 3 (10,7%) родильниц основной группы. Всем пациенткам этой группы во время беременности, в родах и в послеродовом периодах проводили различные акушерские операции и пособия: родовозбуждение 3 (10,7%), длительную эпидуральную анестезию 4 (14,3%), эпизиотомию 12 (42,8%), кесарево сечение 5 (18%), кесарево сечение и перевязку внутренних подвздошных артерий с последующей гистерэктомией по поводу матки Кувелера 1 (3,6%) женщине. Роды закончились вакуум-экстракцией плода у 2 (7,2%), плодоразрушающей операцией — краниотомией также у 2 (7,2%) пациенток. Ручное обследование полости матки выполнили 6 (21,4%) родильницам.
В 1-й группе у 15 (53,6%) живорожденных детей оценка по шкале Апгар составила на 1-й минуте 5,3±0,5 и 6,7±0,6 балла на 5-й минуте, в контрольной — соответственно 8,0±0,1 и 8,8±0,1 балла (р≤0,01). Четверо (14,3%) новорожденных от матерей 1-й группы родились в состоянии тяжелой асфиксии с оценкой по шкале Апгар менее 4 баллов.
Мертворожденных было 13 (46,4%), причем антенатально погибли 8 (61,5%), а интранатально 5 (38,5%) детей. В контрольной группе наблюдали только вагинальные роды без осложнений для матери и плода.
Данные новорожденных и плацент представлены в таблице.

Из данных таблицы видно, что масса рожденных от матерей 1-й группы достоверно ниже. Это объясняется большим числом преждевременных родов у матерей 1-й группы, хронической плацентарной недостаточностью с развитием синдрома задержки развития плода, который диагностировали у 16 (57%) пациенток. По этим же причинам масса и объем плацент у родильниц 1-й группы достоверно ниже, чем в контрольной. Вместе с тем у женщин 1-й группы, инфицирование которых произошло в 36 нед и позже или незадолго до родоразрешения, отмечали достоверное увеличение массы и объема плаценты, чем в контрольной группе. Так, масса плаценты в 1-й группе составила в среднем 669±60,6 г, во 2-й — 523±19,6 г (p≤0,05), объем плаценты 907±54,7 и 777±14,2 см 3 (p≤0,05), а плацентарно-плодовый индекс массы увеличился до 0,19±0,01 и 0,15±0,01 (p≤0,01) соответственно. Это объясняется относительно «свежими» воспалительными изменениями в плацентах в виде отека тканей, пролиферации и тромбозов.
Основной причиной мертворождения и неонатальной смертности детей, рожденных от матерей 1-й группы, явилась внутриутробная инфекция. Причиной смерти в перинатальный период явились сепсис у 12 (42,8%), двусторонняя пневмония у 5 (17,86%), синдром дыхательных расстройств у 7 (25%), асфиксия у 4 (14,3%), врожденный порок сердца, не совместимый с жизнью, у 1 (3,6%) ребенка. Геморрагический синдром присоединялся у каждого третьего новорожденного — 10 (35,7%) случаев.
Всем мертворожденным и умершим детям провели вскрытие, последы были подвергнуты морфометрии и патогистологическому исследованию. Непосредственной причиной смерти детей явилась полиорганная недостаточность с вовлечением в системный воспалительный процесс от 3 до 7 органов. Обнаружили дистрофические и некротические изменения в головном мозге и его оболочках, легких, миокарде, печени, почках, селезенке, поджелудочной железе, фиброз стромы органов; нарушения кровообращения в виде паралитического расширения капилляров, стазов крови, эритроцитарных сладжей, артериальных и венозных тромбозов, кровоизлияний. У 2 (7,2%) детей, умерших от менингоэнцефалита, выявили синдром Уотерхауза—Фридериксена — множественные кровоизлияния в надпочечники, у 7 (25%) детей диагностировали патологию в виде гипоплазии и дисплазии органа (6 наблюдений) и тимомегалии — 1, а также опустошение лимфоидных зон в селезенке. Патолого-анатомические изменения в тимусе и селезенке расценивали как проявление иммунодефицита.
В последах воспалительные изменения были локальными (очаговый фиброзно-серозный центральный интервиллузит) или имели диффузный характер в виде флегмонозного париетального хориоамнионита, фибринозно-гнойного субхориального интервиллузита, базального децидуита, гнойного флебита пупочной вены, тромбозов артериальных и венозных сосудов, межворсинчатого пространства (рис. 1, 2). Диффузное поражение последов наблюдали в 10 (35,7%) случаях. Тромбоз сосудов плаценты, межворсинчатого пространства и сосудов пуповины диагностировали также в 10 (35,7%) наблюдениях. Инфаркты плаценты выявили у 3 (10,7%), кровоизлияния в межворсинчатое пространство, вартонов студень и децидуальную оболочку у 4 (14,3%) обследованных. Кальцинаты в плацентах обнаружили более чем в половине наблюдений.


Все беременные посещали женские консультации. Родоразрешение 25 (89,3%) пациенток 1-й группы произошло в центральных районных больницах (ЦРБ), 3 (10,7%) были госпитализированы в перинатальный центр. После обследования все женщины во время беременности получали антибактериальную и антисептическую терапию с учетом характера патогенной микрофлоры, обнаруженной в урогенитальном тракте, пре- и пробиотики, препараты, улучшающие маточно-плацентарный кровоток, токолитические средства, витамины; по показаниям при наличии плацентарной недостаточности применялись производные прогестерона. Каждая вторая пациентка во время гестации была неоднократно госпитализирована в стационар для проведения курсов лечения по поводу плацентарной недостаточности и угрозы прерывания беременности. Тем не менее диагноз внутриутробного инфицирования во время гестационного периода не поставлен ни одной пациентке 1-й группы. Лечение живорожденных от матерей 1-й группы начинали в родильном блоке: проводили реанимационные мероприятия — ИВЛ тугой маской, 4 детям произведена интубация трахеи. Проводили интенсивную антибактериальную, инфузионную терапию в условиях ИВЛ и пребывания новорожденного в кувезе. Продолжительность жизни новорожденных составила 3,0±0,5 сут.
Комиссионные судебно-медицинское экспертизы и расследования по материалам уголовных дел и проверок производились с участием профильных специалистов в отношении всех пациенток 1-й группы. Вследствие трудности диагностики ВУИ во время беременности у 25 (89,3%) из них неблагоприятные исходы беременности были отнесены к категории непредотвратимых и условно предотвратимых. Только у 3 (10,7%) женщин с пролонгированной беременностью и запоздалыми родами действия врачей находились в прямой причинно-следственной связи с анте- и интранатальными потерями плода. Члены комиссии акцентировали внимание руководителей служб охраны здоровья матери и ребенка и практических врачей акушеров-гинекологов на своевременное и результативное решение вопросов профилактики и ранней диагностики ВУИ.
Комиссионные судебно-медицинские исследования показали, что в группе женщин, беременность у которых закончилась мертворождением или смертью новорожденного в неонатальном периоде от ВУИ, чаще встречались пациентки среднего репродуктивного возраста, большинство составляли жительницы сельских территорий. Преобладали повторно беременные женщины с отягощенным гинекологическим анамнезом. Социально-экономические условия в семьях были хорошими. При обследовании беременных обнаружили многочисленные очаги инфекции в организме, включая урогенитальный тракт. При бактериологическом исследовании выделений из канала шейки матки, уретры и влагалища выявили различную патогенную микрофлору, чаще микстинфекции. Беременность у большинства женщин протекала на фоне первичной плацентарной недостаточности, мало- и многоводия, с явлениями угрозы прерывания во всех семестрах. Практически у каждой второй пациентки, несмотря на проводимую терапию, произошли преждевременные роды. Рождались дети с малой массой тела, требующие реанимации и интенсивной терапии. Анте- и интранатальные потери отметили у половины пациенток. Родоразрешение большинства женщин происходило в ЦРБ вследствие недооценки факторов риска перинатальной патологии, связанных с ВУИ, диагностика которой представляет определенные трудности. Патолого-анатомическое исследование умерших и мертворожденных детей показало, что непосредственная причина их смерти — полиорганная недостаточность, обусловленная ВУИ. Патоморфологические исследования последов подтвердили наличие восходящего инфицирования. Полученные результаты не противоречат данным, приводимым в доступной литературе [3, 7—9]. В ходе комиссионной судебно-медицинской экспертизы в большинстве случаев не выявили прямой причинно-следственной связи неблагоприятных исходов беременности с действиями медицинских работников. Основными факторами в танатогенезе признаны характер и тяжесть трудного для диагностики патологического процесса.
Выводы
1. Беременные с очагами инфекции в организме, особенно в урогенитальной системе, и отягощенным гинекологическим анамнезом относятся к группе высокого риска по ВУИ.
2. Главные синдромы и симптомы ВУИ — первичная фетоплацентарная недостаточность, синдром задержки развития плода, угроза или прерывание беременности на различных сроках, что приводит к мертворождению и смерти в раннем неонатальном периоде.
3. Источником инфекции для плода всегда является его мать. Основной путь распространения инфекции — восходящий.
4. Перинатальные потери вследствие ВУИ в большинстве наблюдений обусловлены характером и тяжестью патологического процесса, трудностями в диагностике, а не действиями медицинских работников.