что такое глс в фармацевтике
Что такое глс в фармацевтике
GLS PHARMACEUTICALS РОССИЙСКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПАНИЯ
Современные технологии для создания уникальных продуктов
GLS PHARMACEUTICALS РОССИЙСКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПАНИЯ
Инновационные разработки собственного производства
GLS PHARMACEUTICALS РОССИЙСКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПАНИЯ
Новый взгляд на актуальные проблемы
КОМПЛЕКСНОЕ СРЕДСТВО ДЛЯ ЗАЩИТЫ ОТ ИНФЕКЦИЙ МОЧЕВЫВОДЯЩИХ ПУТЕЙ
ЗАЩИТА ОТ ЦИСТИТА ДЛЯ БЕРЕМЕННЫХ И КОРМЯЩИХ ЖЕНЩИН
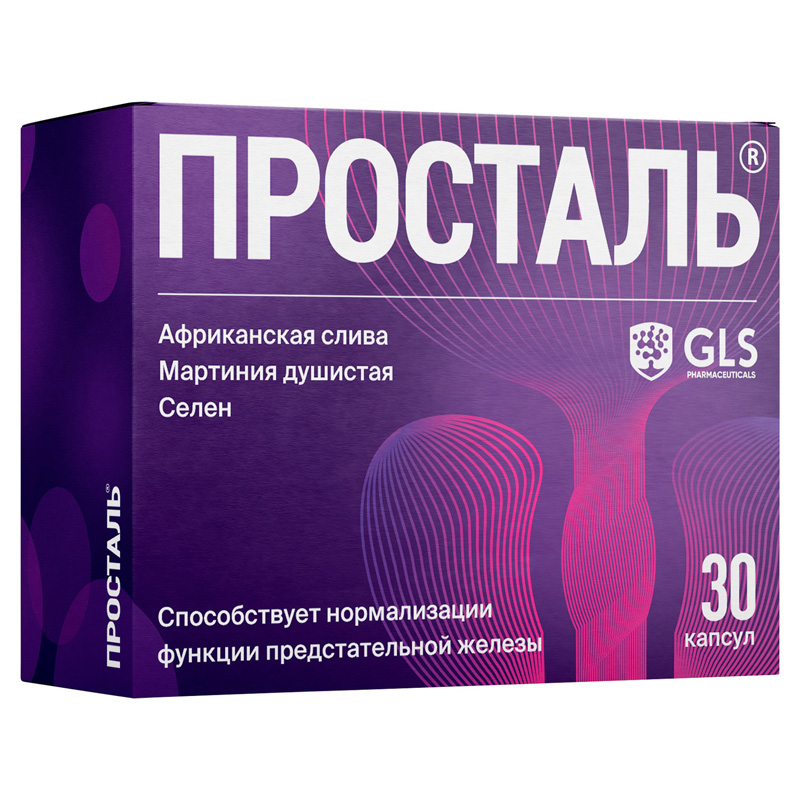
КОМПЛЕКСНОЕ РАСТИТЕЛЬНОЕ СРЕДСТВО, НАПРАВЛЕННОЕ НА УЛУЧШЕНИЕ ФУНКЦИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
ПОДДЕРЖКА ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ МОЧЕВЫДЕЛИТЕЛЬНОЙ СИСТЕМЫ ПРИ УРОЛИТИАЗЕ И ОБЛЕГЧЕНИЕ СИМПТОМОВ ЦИСТИТА
НАТУРАЛЬНЫЙ БУСТЕР ТЕСТОСТЕРОНА
Коллаген придает тканям упругость и эластичность. С возрастом выработка коллагена уменьшается. В связи с этим снижается упругость кожи, появляются морщины, ломкость ногтей, ослабевают волосы, ощущается мышечная слабость, кости и суставы становятся хрупкими.
Коллаген, полученный из рыбы, легко усваивается и является основным типом коллагена во всем организме.
Гиалуроновая кислота удерживает воду, помогая тем самым коллагену поддерживать упругую структуру кожи. Кроме того, она входит в состав синовиальной жидкости, которая смазывает сустав, предохраняя его от повреждений.
БАД. Не является лекарственным средством.
Треонин необходим для образования зубной эмали, он участвует в синтезе коллагена и эластина, в белковом и жировом обмене, стимулирует иммунитет и помогает работе печени, препятствуя отложению в ней жиров.
В суточной дозе Треонина содержится 500 мг.
БАД. Не является лекарственным средством.
Аргинин – это условно незаменимая аминокислота, имеет важное значение для организма.
Аргинин показан к применению у спортсменов для развития выносливости, способствует росту и развитию мышц, увеличивает физическую силу. Ускоряет метаболизм, участвует в жировом обмене, помогает сжечь лишний жир и улучшить формирование мышечной массы.
Кроме того, Аргинин нормализует артериальное давление и уровень холестерина в крови, способствует улучшению функций печени и репродуктивной системы.
БАД. Не является лекарственным средством.
Орнитин — незаменимая аминокислота, необходимая для синтеза гормона роста.
В суточной дозе Орнитина содержится 800 мг.
БАД. Не является лекарственным средством.
Триптофан – это незаменимая аминокислота, необходима для создания белков.
Помимо участия в белковом синтезе, триптофан является источником образования в головном мозге серотонина, мелатонина, дофамина, играющих важную роль в регуляции поведения, настроения, когнитивных функций и сна. Триптофан помогает бороться с тревожностью, агрессией, стрессом, бессонницей и депрессией.
УПАКОВКА ГЛС метода
ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«САНКТ-ПЕТЕРБУРГСКАЯ ГОСУДАРСТВЕННАЯ ХИМИКО-ФАРМАЦЕВТИЧЕСКАЯ АКАДЕМИЯ»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
Кафедра промышленной технологии лекарственных препаратов
Упаковка готовых лекарственных средств
Учебное пособие для самостоятельной работы студентов
Санкт-Петербург «Изд-во СПХФА»
Зав. кафедрой ПАХТ СПХФА, профессор, д. т. н. Е. В. Иванов Ведущий инженер-технолог ЗАО «Вертекс» О. Ю. Романова Зав. кафедрой химии Северо-Западного Государственного заочного технического университета, проф. д. х. н. В. Е. Каган
Упаковка готовых лекарственных средств : учебное пособие для самостоятельной работы студентов к изучению курса «Технология готовых лекарственных средств» / под ред. Л. И. Громовой. — СПб. : Изд-во СПХФА, 2011 — 102 с.
Учебное пособие содержит основные сведения о таре и упаковке готовых лекарственных средств в дополнение к курсу «Технология готовых лекарственных средств». Приведена классификация видов упаковки, описаны различные упаковочные материалы, их свойства и основные требования. Уделено внимание современному оборудованию для упаковки различных лекарственных форм, рассмотрены основные требования к проведению процесса упаковки.
Предназначено для студентов факультета промышленной технологии лекарств.
Л. М. Маркова, Е. М. Пучкова, М. В. Палечкина
Рекомендовано методической комиссией факультета промышленной технологии лекарств
© Санкт-Петербургская государственная химико-фармацевтическая академия, 2011
Список аббревиатур и сокращений……………………………………………. 4
1. Основные понятия о таре и упаковке………………………..……………. 7
2. Основные требования к упаковке и таре…………………………………. 8
2.1. Требования к упаковке и таре для готовых лекарственных средств. 8
2.3. Укупорочные средства для лекарственных препаратов………. 16
2.4. Характеристика и требования к материалам упаковки…………..…. 23
2.5. Требования к внешнему оформлению упаковки………. ……. 32
3. Оборудование для упаковки готовых лекарственных средств………. 35
3.1. Требования к упаковочному оборудованию……………. …………. 35
3.2. Упаковка жидких лекарственных препаратов……………………. 37
3.3. Упаковка твёрдых лекарственных форм……………………………. 46
3.4. Упаковка медицинских мазей……………………………………. 56
3.5. Упаковка парентеральных препаратов………………………………. 64
3.6. Специальные виды упаковок………………………………………. 86
4. Организация процесса упаковки готовых лекарственных средств………. 89
4.1. Требования к помещениям для упаковки лекарственных средств…. 89
4.2. Требования к проведению процесса упаковки………………………. 90
4.3. Постадийный контроль процесса упаковки………………………. 92
4.4. Аттестация (испытания) процесса упаковки………………………..…..92
4.5. Документирование процесса упаковки………………………………. 95
6. Тесты для самоконтроля………………………………………………………. 98
Список аббревиатур и сокращений
ГЛС — готовое лекарственное средство ЛП — лекарственный препарат ЛС — лекарственное средство
МТО — медицинское тарное обесцвеченное АБ — ампульное безборное НС — нейтральное стекло ОС — оранжевое тарное стекло
СНС — светозащитное нейтральное стекло ПЭ — полиэтилен ПП — полипропилен
ПВХ — поливинилхлорид ПЭГ — полиэтиленгликоль
ЖНЛП — жидкие нестерильные лекарственные препараты КЯУ — контурная ячейковая упаковка
КБЯУ — контурная безъячейковая упаковка
Одним из важных показателей при сертификации лекарственных средств является показатель «Упаковка».
Упаковка для лекарственных средств должна гарантировать сохранность их количества и качества в пределах, установленных нормативными документами (НД) на лекарственные средства
в течение установленных сроков их годности на всем пути их обращения, в условиях производства, транспортирования, хранения и использования.
Многообразие лекарственных форм, сложный состав препаратов, защитные свойства упаковочных материалов, укупорочных средств, условия производства, транспортирования и хранения
в течение всего процесса обращения ЛС требуют комплексного, системного подхода при выборе упаковки (ее конструкции и материала). Процессы упаковки и маркировки готовых лекарственных средств являются одними из наиболее мобильных, быстро развивающихся процессов: расширяются функции упаковки, появляются новые упаковочные материалы, новые нормативные документы, ужесточаются требования к упаковке.
Вопросы качества упаковки и упаковочных материалов неотделимы от требований GMP. Требования GMP к упаковке в широком понимании этого термина сформулированы в «Руководстве Всемирной организации здравоохранения. Надлежащая производственная практика для фармацевтических продуктов», в нормативном документе Конвенции фармацевтических инспекций PLC/S — «Руководстве по надлежащей производственной практике лекарственных средств», «Европейском Руководстве по надлежащей производственной практике» — нормативном документе для фирм-производителей лекарственных средств стран ЕС, ГОСТ Р 52249-2009 — отраслевом стандарте РФ. Кроме этого, существует большое количество отраслевых стандартов, методических указаний, руководящих документов, касающихся вопросов организации производства упаковки, упаковочных материалов, маркировки продукции.
Настоящее учебное пособие имеет целью способствовать усвоению курса технологии готовых лекарственных средств, самостоятельному изучению вопросов, касающихся упаковки
лекарственныхсредств,атакжелучшеориентироватьсясредибольшого количества информации, посвященной этим проблемам.
Учебное пособие содержит главы, раскрывающие основные понятия и определения, современные требования к упаковке. Дана классификация упаковочных материалов, рассмотрены примеры наиболее употребляемых материалов, требования к внешнему оформлению упаковки.
Приведена основная информация об организации процесса упаковки, применяемом современном упаковочном оборудовании для различных видов лекарственных форм.
В конце пособия приведены контрольные вопросы и тесты
с правильными ответами к ним, дающие возможность проверить усвоение студентом изложенного материла.
Освоение материала, изложенного в методическом пособии, позволит использовать полученные знания в выполнении курсовых и дипломных проектов, а также в дальнейшей профессиональной работе.
1. Основные понятия о таре и упаковке
Лекарственные препараты, выпускаемые фармацевтической промышленностью, доходят до потребителя в готовом к употреблению виде или в виде так называемого готового лекарственного средства (ГЛС). Таким образом, готовое лекарственное средство представляет собой комплекс, состоящий из непосредственно лекарственного средства в определённой лекарственной форме, упаковки и информационных сведений о препарате. Для каждого вида лекарственной формы требуется свой способ упаковки и определённый упаковочный материал.
Под термином «упаковка» понимают средство или комплекс средств, обеспечивающих защиту лекарственных препаратов от повреждений и потерь, защиту окружающей среды от загрязнений, процесс обращения продукции медицинского назначения, транспортирование, хранение и реализацию. Упаковка, соответствующая требованиям соответствующей нормативной документации на лекарственное средство, называется стандартной упаковкой.
Под термином «упаковка» понимают также технологические стадии и операции, в том числе нанесение маркировки, в результате которых создаётся лекарственное средство, предназначенное для реализации потребителю.
Основным элементом упаковки, представляющим собой изделие для размещения лекарственного средства, является тара.
Если тара образует самостоятельную транспортную единицу, то она называется внешней или транспортной тарой. В транспортной таре продукция доставляется до места распределения или реализации. Транспортная упаковка, как правило, не доходит до потребителя. Тара, поступающая к потребителю с лекарственным средством и не выполняющая функции транспортной тары, называется внутренней или потребительской тарой. Так, банка, бутылка, картонная коробка, короб из гофрокартона, бочка, ящик — это тара.
Упаковка — это комплекс, состоящий из тары и вспомогательных средств, определяющих потребительские и технологические свойства упаковываемого продукта. Различают первичную и вторичную тару. Первичная тара представляет собой индивидуальную упаковку, непосредственно контактирующую с продукцией.
Вторичная или групповая упаковка объединяет определённое количество первичных упаковок лекарственных средств.
Перемещение, складирование и хранение сырья, вспомогательных материалов, лекарственных средств в производственных помещениях осуществляется в производственной (цеховой) таре (контейнеры, ёмкости, бины).
В качестве транспортной тары часто используется бочка
с корпусом цилиндрической или параболической формы с обручами или зигами катания. Контейнер представляет собой ёмкость, многократно используемую на различных видах транспорта для перевозки и временного хранения грузов, с приспособлениями механизированной упаковки и снятия с транспортных средств, с внутреннимобъёмом 1 м 3 и более. Врядеслучаевиспользуетсямешок (мешкотара), представляющий собой мягкую транспортную тару
с корпусом в форме рукава с дном и открытой горловиной.
В большинстве случаев для упаковки готовых лекарственных средств используется транспортная тара с корпусом формы прямоугольника, с дном, двумя торцевыми и боковыми стенками,
с крышкой или без неё, называемая ящик или короб.
Для транспортирования, например, вытяжекизлекарственного растительного сырья используют фляги или бидоны.
12. 2. Основные требования к упаковке и таре. 23. 2.1. Требования к упаковке и таре для ГЛС
Использованиеразнообразныхпосвойствамидействиюна организм человека действующих веществ, сырья и продуктов, сильнодействующих и ядовитых веществ, активных, легколетучих, пожаро- и взрывоопасных, с одной стороны, особые требования к чистоте, стерильности, точностиималойдозировкеиряддругих специфических требований — с другой, выделяют производство ГЛС в особую отрасль промышленности, продукция которой доходит до потребителя в готовом для употребления виде. К упаковке такой продукции предъявляется ряд требований. Первичная упаковка ГЛС должна обеспечить длительную сохранность лекарственной формы. Исходя из этого к материалу первичной упаков-
ки, контактирующему с лекарственным препаратом, предъявляются особые требования газо- и паронепроницаемости, химической индифферентности, прочности, стойкости к температурным воздействиям, светонепроницаемости, барьерной устойчивости к микроорганизмам и др.
Обеспечение максимального срока годности препарата является важным условием выбора вида и конструкции упаковки, т. к. является наиболее важным технико-экономическим показателем ГЛС. Так, нестойкость препарата при хранении может потребовать создания специальной упаковки, которая может сделать нерентабельным производство препарата.
Не менее важным является обеспечение необходимых потребительских свойств упаковки: она должна быть удобной для ношения, содержатьинформациюохранениииприёмесредства,иметьпривлекательный внешний вид, предусматривать возможность повторного использования и ряд специальных требований, таких, как контроль первоговскрытияупаковки,особоеразмещениелекарственногосредства, позволяющее его многократно использовать без нарушения герметичности, стерильности и контроль за его использованием.
К вторичной упаковке предъявляются требования по обеспечению сохранности первичных упаковок, а также по обеспечению информативных требований.
Выбор вида упаковки в первую очередь диктуется свойствами лекарственного препарата, в зависимости от которых определяют вид и конструктивные признаки упаковки. Существуют и особые требования к упаковке, связанные, например, с созданием упаковок для лекарств, которые затрудняли бы доступность препарата для детей. Важной задачей, особенно в педиатрической практике, является расширение выпуска лекарственных средств упаковке с дозой однократного приёма.
Широкоеприменениевмедицинскойпрактикенаходятлекарственные формы в виде аэрозолей. Однако аэрозольные упаковки должны иметь предохранительные устройства, препятствующие вскрытию и использованию их детьми. Наблюдаются случаи передозировки лекарственных препаратов при приёме их чайной или столовой ложкой. Доза при этом может превышать требуемую в два и более раз. Поэтому созданиеспециальныхдозирующихустройствявляетсяважнойзадачей.
Актуальной задачей в последнее время является охрана окружающей среды от использованных упаковок для лекарственных средств. Если такие упаковочные материалы как бумага, картон, металлы и дерево могут повторно использоваться в качестве сырья при соответствующей переработке или уничтожаться путём сжигания, то отходы полимерных материалов являются самыми вредными с экологической точки зрения.
Классификация видов упаковок и применяемой тары зависит от группы лекарственных средств и вида лекарственной формы. Различные виды упаковок и тары, используемые в производстве готовых лекарственных средств приведены в таблице 1.
О компании
GLS PHARMACEUTICALS — российская инновационная фармацевтическая компания, использующая современные технологии для создания уникальных продуктов.
Мы расширяем возможности современного, безопасного, эффективного ухода за здоровьем и внедряем инновационные решения для улучшения качества жизни.
Компания обладает широким портфелем продуктов в областях женского и мужского здоровья, и непрерывно стремится к расширению возможностей современной науки, сохраняя бесценный ресурс здоровья каждого человека.
За короткое время компания вывела на рынок портфель уникальных продуктов, которые завоевали заслуженное доверие как у потребителей, так и у профессионального сообщества специалистов.
ОСНОВНЫЕ ПРИОРИТЕТЫ:
Уникальность — вывод на рынок принципиально новых продуктов, не имеющих аналогов, в которых фармацевтический рынок испытывает острую потребность.
Качество продукции — вся продукция компании разрабатывается и производится с обязательным контролем качества на всех этапах:
— разработка рецептуры
— закупка качественного сырья у проверенных поставщиков
— получение заключений экспертов и регистрация
— производство готового продукта
Признание эффективности продукции специалистами — чрезвычайно важна поддержка и заинтересованность во всех выпускаемых средствах у профессионального сообщества, на всех этапах жизни каждого продукта — от формирования идеи до реализации готового продукта.
Компания высоко ценит доверие потребителей и специалистов, поэтому производит продукцию высочайшего качества и дорожит своей репутацией производителя высококачественных и эффективных средств.
ПРОИЗВОДСТВО
С 2018 года наша компания выпускает продукцию на современном заводе в Московской области — GLOBAL HEALTH CARE.
GLOBAL HEALTH CARE — предприятие полного цикла выпуска пищевой продукции, а также биологически активных добавок, основано в 2017 году.
Деятельность компании GLOBAL HEALTH CARE полностью соответствует международному стандарту ХАССП-ISO 22000:2005.
Производство оснащено новейшим оборудованием высокой производительности, которое также соответствует всем необходимым стандартам и регулярно проходит тщательный контроль и оценку внешних экспертов.
Выпуск безопасной продукции является обязательным условием работы компании, контролируемым Федеральными законами, Техническими регламентами, ГОСТами, гарантирующим высокое качество производимого товара и соответствие всем необходимым требованиям.
Смотри на упаковке: Что такое GMP и зачем обращать на это внимание при покупке лекарств?
Informburo.kz совместно с компанией SANTO рассказывает, зачем фармацевтическим компаниям нужен стандарт GMP, и что всё это значит для покупателя.
Покупая лекарства, хочется быть уверенным, что они помогут решить проблемы со здоровьем, ну или хотя бы, не навредят. Стандарт GMP – самая проверенная и надёжная система обеспечения качества фармацевтических препаратов в мире. Она гарантирует наилучшее качество продукта, его постоянную проверку и соответствие мировым стандартам производства.
№1. Что такое GMP?
GMP (Good Manufacturing Practice; Надлежащая производственная практика) – это международный стандарт, определяющий требования к производству лекарственных препаратов, БАДов, пищевых добавок и некоторых продуктов питания. В международный стандарт GMP включены все требования, которым должно отвечать предприятие-производитель: от температуры в производственном цехе до одежды работников. Стандарты GMP – это не просто пожелания к производству препаратов, а строгие требования. Употребляя лекарства или продукты компаний, имеющих сертификат GMP, потребитель может быть спокоен за своё здоровье.
№2. Зачем нужен этот стандарт, и чем он отличается от других?
GMP – принципиально новый подход к соблюдению технологий производства. Обычный контроль качества предполагает исследование только некоторых, причём уже готовых, образцов продукции и гарантирует лишь их качество или качество партии, выпущенной в то же время. По стандартам GMP производится комплексная лабораторная проверка и регулирование всех параметров производства, а значит – обеспечение качества всей продукции. Правила GMP вводятся, чтобы снизить риск ошибок на производстве до минимума.
№3. Какие правила есть в своде GMP?
Кроме GMP в мировой практике распространены и другие стандарты надлежащих практик исследования, производства, дистрибьюции, хранения и лекарственного обеспечения:
Читайте также:
№4. GMP – это какой-то новый тренд?
Нет, это не очередной скоропортящийся тренд. Мировая история GMP стандартов берёт своё начало с 1963 года в США, где группой ученых были разработаны специальные правила для регламентирования условий качественного и безопасного производства лекарственных препаратов – стандарт Good Manufacturing Practice (GMP). Начиная с 70 годов, GMP получил широкое распространение во всем мире, за исключением Советского Союза. Уже после распада СССР страны СНГ начали подстраивать существующие нормативные базы к правилам GMP.
№5. А Казахстан принял стандарт GMP?
Стандарты надлежащих фармацевтических практик, в том числе GMP, были утверждены в системе Госстандарта Республики Казахстан ещё в 2006 году. Тогда они носили рекомендательный, добровольный характер. Но уже с марта 2014 года все иностранные компании, экспортирующие продукцию в Казахстан, должны были подтвердить, что работают по стандарту GMP, иначе ввоз их продукции в страну запрещался. В 2015-м стандарты GMP актуализировали с учётом требований ЕС и ЕАЭС. С января 2016 года начал функционировать общий рынок лекарств для стран Евразийского экономического союза. На территории ЕАЭС должны производиться и распространяться только медицинские препараты стандарта GMP, который подтверждает эффективность, безопасность и качество продукции.
С 1 января 2018 года стандарты GMP сделали обязательными для казахстанских производителей. Те из них, кто ещё не внедрил GMP, могут подавать заявку на проведение оценки безопасности и качества продукции и реализовывать препараты до истечения сроков действия их регистрационных удостоверений.
№6. Какие производители имеют сертификат соответствия GMP?
Производители продукции, изготовление которой регламентировано стандартом GMP, должны пройти процедуру сертификации. Наличие сертификата GMP у производителя подтверждает, что:
Сертификаты GMP в Казахстане уже получили 58 предприятий. Одним из первых отечественных производителей, активно внедряющих этот стандарт, стала компания SANTO. Компания получила первый сертификат GMP по производству мягких лекарственных форм в 2011 году. В 2012-м SANTO получила сертификат GMP на производственный участок асептической рассыпки порошковых антибиотиков. В 2013-м – сертификат на действующий ампульный цех, в 2014-м – на производство инъекционных растворов в цехе по производству инъекционных растворов и инфузий. В 2015-м SANTO был выдан сертификат GMP на производственный участок инфузионных растворов, а в 2018-м – на производственные площадки по производству инъекционных растворов и инфузий, производству твёрдых пероральных лекарственных средств. Также SANTO – обладатель сертификата на соответствие аптечного склада стандарту надлежащей дистрибьютерской практики (GDP). Обладание такими сертификатами – веское подтверждение того, что система обеспечения качества и условия производства в компании отвечают правилам надлежащей производственной практики Республики Казахстан.
№7. Я пришёл в аптеку. Как узнать, что нужное мне лекарство произведено по правилам GMP?
Некоторые производители указывают это прямо на упаковке, ведь знак GMP – гарантия качества. Но даже если вы не нашли этой аббревиатуры на коробочке, важно помнить, что с 2014 года все иностранные лекарства, продающиеся в Казахстане, соответствуют GMP. Другие зарубежные лекарственные препараты в нашей стране не регистрируются.
Отечественные производители также постепенно внедряют стандарт в производство. Полный список компаний, уже имеющих сертификат соответствия GMP, можно посмотреть на сайте Министерства здравоохранения РК.
Читайте также:
№8. В Казахстане производят много лекарств?
Да, в Казахстане производят многие лекарства. Всего на казахстанском фармацевтическом рынке представлено больше 700 компаний. Один из лидер ов казахстанской фарминдустрии – компания SANTO – производит более 200 генерических препаратов и оригинальных лекарственных препаратов 12 фармакологических групп. Производственные мощности компании позволяют ежегодно выпускать 1 млрд. 283 млн. таблеток, капсул и гранул, 294 млн. ампул, 6 млн. инфузий, 40 млн флаконов порошков антибиотиков (цефалоспорины ) и 13 млн. флаконов порошков антибиотиков (пенемы/мицины) и 4,5 млн. флаконов жидких пероральных лекарственных средств. 90% продукции реализуется на внутреннем рынке страны, 10% экспортируется в Россию, Кыргызстан, Таджикистан, Монголию и Туркменистан.
№9. Как GMP влияет на казахстанскую фармацевтическую индустрию?
Внедрение GMP гарантирует обычным покупателям, что отечественные препараты ничем не уступают иностранным, потому что произведены по единому стандарту. Подтверждение стандартов способствует более свободному продвижению казахстанских препаратов на внешних рынках. По данным Казахстанского института развития индустрии за 2017 год в Казахстане было произведено фармацевтической продукции на 73,4 млрд тенге. На три региона – Южно-Казахстанскую и Алматинскую области и город Алматы – пришлось 92,3% прибыли от произведённой продукции. Старейшее предприятие ЮКО – АО «Химфарм» с торговой маркой SANTO – лидер среди казахстанских производителей лекарственных средств и часть международной фармацевтической группы Polpharma. Это одно из первых казахстанских предприятий, которое подтвердило соответствие государственному стандарту Надлежащей производственной практики (GMP) и получило сертификаты соответствия.