что такое гламированный нефрит почек
Гломерулонефрит: причины, симптомы, диагностика, лечение
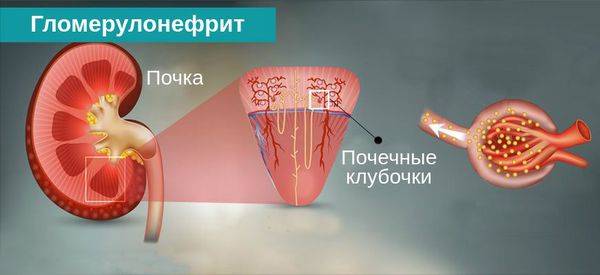
Гломерулонефрит занимает третье место среди заболеваний почек и чаще всего встречается у людей в возрасте 30-40 лет. Это иммуновоспалительное заболевание почечных клубочков протекает в острой, хронической или быстропрогрессирующей форме с поражением обеих почек.
Чаще всего причины гломерулонефрита и его патогенез неизвестны. Из-за поражения клубочков почки теряют способность фильтровать кровь, в организме задерживаются вода и токсины. На конечной стадии заболевания наступает почечная недостаточность, которая требует пожизненного диализа или пересадки почки, поэтому очень важно выявить гломерулонефрит на ранних стадиях.
Причины гломерулонефрита
Причины острого гломерунефрита
Причины хронического гломерунефрита
Симптомы гломерулонефрита
Диагностика гломерулонефрита
Клинические признаки гломерулонефрита в большинстве случаев не позволяют определить характер изменений в клубочках, а при латентной форме у пациента нет никаких жалоб, и заболевание выявляется случайно при обращении в клинику по другим причинам. Также учитываются ранее перенесенные и хронические инфекции и системные заболевания.
Для определения степени поражения почек и оценки течения гломерулонефрита используют лабораторные анализы и инструментальные исследования.
Общий анализ мочи при гломерулонефрите проводится для обнаружения крови (эритроцитов), белка, цилиндров, которые указывают на поражение почечных клубочков, а также учитывается снижение удельного веса мочи [3].
Проба Зимницкого используется для оценки суточного объема мочеиспускания и концентрации мочи. Этот метод помогает определить способность почек концентрировать и выделять мочу.
Общий анализ крови помогает выявить наличие воспалительного процесса в организме.
Биохимический анализ крови показывает повышенный уровень мочевины, креатинина, электролитов. Эти параметры характеризуют фильтрационную способность почек и степень их поражения [4].
Иммунологическое исследование крови на наличие антистрептококковых антител выявляет перенесенную стрептококковую инфекцию и, следовательно, риск развития постинфекционного гломерулонефрита.
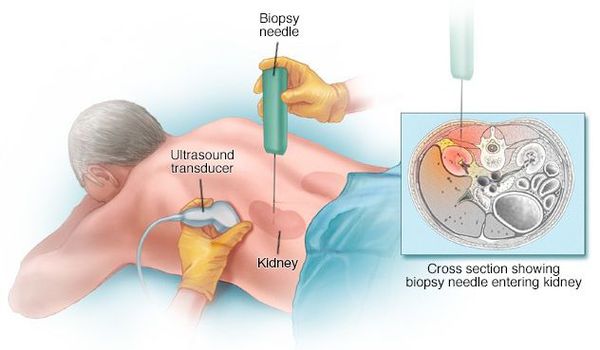
Биопсия (микроскопическое исследование образца почечной ткани) проводится, когда диагностика и классификация гломерулонефрита затруднены.
Ультразвуковое исследование почек выявляет участки воспаления, расширение и сужение почечных клубочков и сосудов, изменения положения и размеров почек. Также проводится доплерографическое исследование сосудов почек для оценки кровотока в органе.
Рентгенограмма и КТ почек (получение изображения тонких срезов почек) используются для выявления участков воспаления и других изменений структуры почек.
Нефросцинтиграфия за счет накопления в тканях почек специального препарата, введенного внутривенно, позволяет оценить состояние тканей почек, локализацию и особенности патологических процессов.
Экскреторная урография выявляет патологии почек и мочевыводящих путей. На рентгеновских снимках можно выявить нарушения при выведении почками контрастного вещества.
Измерение артериального давления систематически в течения дня имеет значение при гипертензивной форме гломерулонефрита.
ЭКГ и ЭхоКГ позволяют оценить работу сердца.
УЗИ грудной клетки (легкие и плевральные полости) проводят при одышке.
Дифференциальная диагностика проводится для исключения нефротического синдрома, пиелонефрита, почечно- и мочекаменной болезней, поликистоза почек, артериальной гипертензии [3].
Гломерулонефрит у детей часто протекает вяло или атипично и требует наблюдения у нефролога.
Лечение и профилактика гломерулонефрита
Из-за тяжести заболевания лечение проводится в условиях стационара. Это особенно касается случаев выраженной симптоматики или почечной недостаточности.
Пациентам с гломерулонефритом противопоказаны физические нагрузки, в частности работа на открытом воздухе и в условиях низкой температуры или высокой влажности.
При почечной недостаточности назначают диализное лечение. С его помощью заменяют две основные функции почек: выведение избыточной воды из организма и удаление токсинов из крови. При тяжелом гломерулонефрите проводят пересадку почки.
Острая фаза гломерулонефрита купируется в течение 1-3 недель с возможными рецидивами. Показатели мочи нормализуются более года. Наблюдение пациентов, перенесших острый гломерулонефрит, ведется в течение 2 лет, а при хронической форме рекомендовано проходить регулярное обследование 2-3 раза в год.
Клинические рекомендации направлены на снижение риска гломерулонефрита, а также его рецидивов. Они включают обязательное полное излечение стрептококковых, бактериальных и других инфекций, избегание переохлаждения и высокой влажности, ограничение потребления соли, соблюдение здорового образа жизни, а также регулярное медицинское наблюдение у специалистов.
Что такое гломерулонефрит хронический? Причины возникновения, диагностику и методы лечения разберем в статье доктора Болгарова О. Г., педиатра со стажем в 11 лет.
Определение болезни. Причины заболевания
Гломерулонефрит — это двустороннее диффузное иммунное воспалительное заболевание почек, при котором в первую очередь поражаются их клубочки — гломерулы.
Хронический гломерулонефрит включает в себя группу различных заболеваний почек, отличных по своей причине, морфологической структуре и подходам к лечению, но объединённых первичным поражением гломерулов. [3]
В России заболеваемость хроническим гломерулонефритом достигает 13–50 случаев на 10 000 населения. Данные патологии чаще наблюдаются у мужчин. Они могут развиться в любом возрасте, однако наиболее часто возникают у детей 3–7 лет и взрослых 20–40 лет. [17]
На заболеваемость гломерулонефритом влияют популяционные, климатические и социально-экономические факторы. Так, фокально-сегментарный гломерулосклероз чаще встречается у афроамериканцев, ИГА-нефропатия более распространена на азиатском континенте, инфекционно-зависимые гломерулонефриты — в тропиках и развивающихся странах. [16]
Причины возникновения хронического гломерулонефрита зачастую неизвестны. В развитии части болезней установлена роль бактериальной и вирусой инфекции, в частности вирусов гепатита В и С, ВИЧ-инфекции, вирусов кори и Эпштейна — Барра. По существу, каждая редкая и новая инфекция может вызвать гломерулонефрит. [3] Также на появление хронического гломерулонефрита оказывают влияние лекарственные препараты, опухоли и другие внешние и внутренние факторы. [2]
Симптомы хронического гломерулонефрита
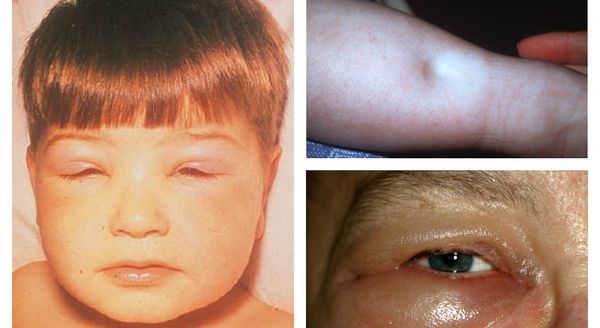
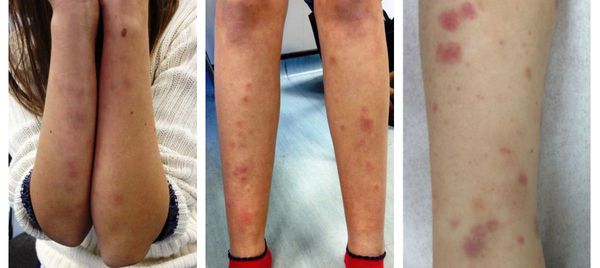
Первые клинические проявления хронического гломерулонефрита могут быть скудными, поэтому зачастую болезнь подкрадывается незаметно. В этом случае заподозрить заболевание можно только по изменению состава мочи: появление в ней белка (протеинурия) и изменение мочевого осадка — появление эритроцитов и лейкоцитов в моче.
Иногда болезнь дебютирует как острый нефрит. В таком случае она проявляется несколькими синдромами:
Сочетание нефротического и нефритического синдрома является наиболее неблагоприятным вариантом.
Помимо данных проявлений для гломерулонефрита характерны следующие симптомы:
Все формы хронического гломерулонефрита способны периодически обостряться, при этом клиническая картина напоминает или полностью повторяет проявления острой формы заболевания. При подостром или быстро прогрессирующем гломерулонефрите функции почек снижаются на 50% меньше чем за три месяца.
Патогенез хронического гломерулонефрита
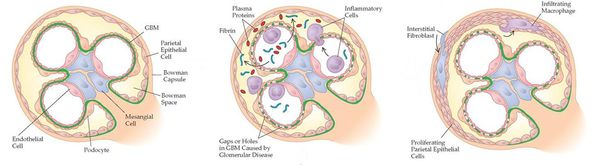
Инфекционные и другие стимулы способствуют появлению иммунного ответа с формированием и отложением антител и/или иммунных комплексов в клубочках почек (или их образованием сразу в клубочках), а также усилению клеточно-опосредованной иммунной реакции. В ответ на возникающие иммунные нарушения в почечных клубочках развиваются изменения, претерпевающие ряд стадий. Сегодня с достаточной уверенностью можно говорить о конкретных механизмах только некоторых из них.
Начало иммуновоспалительного процесса связано с активацией медиаторов тканевого повреждения, прежде всего с активацией хемотаксических факторов, способствующих миграции лейкоцитов. Одновременно активируются факторы коагуляции (сгущения), в результате чего образуются депозиты фибрина и происходит выброс факторов роста и цитокинов — гормоноподобных веществ, вырабатываемых клетками иммунной системы.
На первых этапах заболевания иммунное воспаление преобладает. Поэтому чем раньше начато иммуносупрессивное лечение, тем лучше прогноз заболевания. При стихании воспалительного процесса на первый план выходят неиммунные механизмы прогрессирования болезни:
При дальнейшем прогрессировании заболевания происходят вторичные изменения: процесс распространяется на другие структуры почки — канальцы и интерстиций (вид соединительной ткани).
Исход воспаления — фиброз и склероз почечной ткани, т. е. потеря почечной функции.
Классификация и стадии развития хронического гломерулонефрита
По причинам возникновения гломерулонефриты делятся на две группы:
По клиническим проявлениям выделяют пять форм заболевания:
По морфологическим изменениям выделяют три хронических гломерулонефритов:
Осложнения хронического гломерулонефрита
Гломерулонефрит может осложниться инфекцией, в том числе связанной с иммунодепрессивной терапией (пиелонефрит, туберкулёз), нарушениями фосфорнокальциевого гомеостаза и остеопорозом. Причиной тому — острый воспалительный процесс или же осложнения иммунносупрессивной терапии.
Осложнения нефротической формы хронического гломерулонефрита:
Нефротический криз возникает внезапно. Его развитие может спровоцировать активная диуретическая терапия. К характерным проявлениям относятся интенсивные боли в животе, перитонитоподобный синдром, повышенная температура тела. В дальнейшем это осложнение может привести к развитию гиповолемического шока и смерти. [15]
Частые осложнения гипертонической форм связаны с гипертрофией миокарда левого желудочка (сердечная астма, отёк лёгких). Также может возникнуть острая сердечная недостаточность. [1]
Диагностика хронического гломерулонефрита
Для диагностики гломерулонефритов прежде нужно исключить целый ряд заболеваний со схожими симптомами:
Лабораторное или визуальное наличие крови в моче требует исключения других урологических проблем, опухолей, феномена сдавления левой почечной вены у детей, наследственных заболеваний почек — болезни тонких мембран, синдрома Альпорта (наследственного нефрита).
Для дифференциальной диагностики с системными заболеваниями необходимо исследовать их маркеры в крови:
При обострении любой формы хронического нефрита скорость оседания эритроцитов увеличивается, а также уровень иммунологических показателей, сиаловых кислот, фибрина и серомукоида в крови. При развитии хронической почечной недостаточности независимо от формы хронического нефрита уровень креатинина и мочевины в крови увеличивается. [1] [11]
Основные аспекты диагностики гломерулонефритов:
Постановка диагноза многих гломерулярных заболеваний невозможна без пункционной биопсии почки.
Показания к биопсии:
Противопоказания к биопсии:
Биопсию проводит опытный нефролог или хирург в условиях стационара. Сама процедура длится примерно 15-20 минут. Осложнения при биопсии возникают редко, кровотечение возможно всего в 5-10% случаев. [5]
Проведение биопсии почки и верификация морфологического варианта поражения почек показаны даже в тех случаях, когда имеется связь макро- гематурии с ангиной и напрашивается диагноз «острый гломерулонефрит». Исследования показали, что под маской острого «постстрептококкового» гломерулонефрита могут скрываться такие тяжёлые поражения почек, как экстракапиллярный гломерулонефрит, исход и прогноз которого зависят от своевременного начала лечения. [6]
Лечение хронического гломерулонефрита
Лечение хронических гломерулонефритов сводится к трём целям:
Этиотропная терапия проводится только при выявленной причине хронического гломерулонефрита, например, при лептоспирозе, БГСА-инфекции, вирусных гепатитах, ВИЧ-инфекции и других). В подобных случаях применяются антибиотики и противовирусные препараты.
Иммуносупрессивная терапия включает применение следующих лекарств:
Однако ГКС имеют множество побочных эффектов. Поэтому их стараются назначать коротким курсом в больших дозах, постепенно переходя на поддерживающую терапию минимальными дозам.
У пациентов со стероидрезистентным фокально-сегментарным гломерулосклерозом и непереносимостью циклоспорина предлагается применение другого цитостатика — микофенолата мофетила в комбинации с высокими дозами дексаметазона. [2]
Одна из методик лечения резистентных к стандартной терапии форм является пульс-терапия — высокодозное введение лекарств коротким курсом. [12] Такой способ эффективно купирует обострения гломерулонефритов и относительно хорошо переносится пациентами.
Как правило, пульс-терапия проводится с использованием метилпреднизолонома, циклофосфамида или обоих препаратов:
В последние десятилетия для торможения прогрессирования хронического гломерулонефрита применяется нефропротективная стратегия лечения. Так как при стихании иммунно-воспалительного процесса на первый план выходят неиммунные факторы прогрессирования заболевания (прежде всего гемодинамические), а также обменные (гиперлипидемия, дислипидемия, гиперурикемия) и коагуляционные, применяются ингибиторы АПФ и блокаторы рецепторов ангиотензина. Эти препараты восстанавливают системную и внутриклубочковую микроциркуляцию, обладают противовоспалительным и цитопротективным действием (защита клеток от вредных факторов). Они применяются для лечения всех форм гломерулонефритов и замедляют прогрессирование болезни. При некоторых формах латентных и гематурических вариантов заболевания, когда не показано иммуносупрессивное лечение, они являются препаратами выбора.
Плазмаферез (способ очищения крови) применяется для лечения быстро прогрессирующего гломерулонефрита, а также нефритов, протекающих на фоне системных заболеваний.
Гемосорбция и гемодиализ (способы внепочечного очищения крови) относятся к методам заместительной почечной терапии. К ним прибегают во время острого периода почечной недостаточности.
Посиндромная терапия диуретиками, антикоагулянтами, дезагрегантами, антигипертензивными препаратами, статинами, гиперлипидемическими и другими средствами проводится по показаниям. Также уделяется внимание устранению очагов хронической инфекции, лечению кариеса, профилактике вирусных инфекций, на фоне которых чаще всего возникают обострения заболевания.
При лечении нефротического синдрома у детей показана инициальная терапия в течение 4-6 недель, а также приём преднизолона, доза которого со временем снижается до поддерживающей. При благоприятном течении болезни преднизолон постепенно отменяют. В случае выявления стероидзависимости (когда на фоне снижения дозы преднизолона возникает рецидив заболевания) используются алкилирующие препараты — циклофосфамид или хлорамбуцил, а также применяется левамизол, микофенолат мофетил или такролимус.
Прогноз. Профилактика
Течение хронического гломерулонефрита зависит от причины заболевания и морфологической формы. Наиболее неблагоприятным является подострый быстро прогрессирующий вариант.
Без лечения все формы гломерулонефрита заканчиваются хронической почечной недостаточностью, разница заключается лишь в срок её наступления. А осложенения ухудшают и без того тяжёлый прогноз заболевания.
Смерть при гломерулонефрите может наступить в результате развития отёка легких, нефротического синдрома, инсульта, острой почечной недостаточности, гиповолемического шока и венозных тромбозов. Летальность при хроническом гломерулонефрите на III-V стадиях хронической болезни почек связана с сердечно-сосудистыми патологиями. [17]
Всем пациентам с хроническим гломерулонефритом важно помнить о следующих мерах профилактики обострения заболевания:
Публикации в СМИ
Гломерулонефрит хронический
Хронический гломерулонефрит (ХГН, медленно прогрессирующая гломерулярная болезнь, хронический нефритический синдром) — групповое понятие, включающее заболевания клубочков почки с общим иммунным механизмом поражения и постепенным ухудшением почечных функций с развитием почечной недостаточности.
КЛАССИФИКАЦИЯ
Клиническая (Тареев Е.М., Тареева И.Е., 1958, 1972) • По формам •• Латентная форма •• Гематурическая форма (см. Болезнь Берже) •• Гипертоническая форма •• Нефротическая форма •• Смешанная форма • По фазам •• Обострение (активная фаза) — нарастание изменений в моче (протеинурии и/или гематурии), появление остронефритического или нефротического синдрома, снижение функции почек •• Ремиссия — улучшение или нормализация экстраренальных проявлений (отёков, артериальной гипертензии), функций почек и изменений в моче.
Морфологическая (Серов В.В. и соавт., 1978, 1983) включает восемь форм ХГН • Диффузный пролиферативный гломерулонефрит (см. Гломерулонефрит острый) • Гломерулонефрит с полулуниями (см. Гломерулонефрит быстропрогрессирующий) • Мезангиопролиферативный гломерулонефрит • Мембранозный гломерулонефрит • Мембрано-пролиферативный (мезангиокапиллярный) гломерулонефрит • Фокально-сегментарный гломерулосклероз • Фибропластический гломерулонефрит.
Статистические данные. Заболеваемость — 13–50 случаев заболевания на 10 000 населения. Первичный ХГН возникает в 2 раза чаще у мужчин, чем у женщин, вторичный — в зависимости от основного заболевания. Может развиться в любом возрасте, но наиболее часто у детей 3–7 лет и взрослых 20–40 лет.
Этиология
• Один и тот же этиологический фактор может вызвать разные морфологические и клинические варианты нефропатий и, наоборот, разные причины могут вызвать один и тот же морфологический вариант повреждения.
• Диффузный пролиферативный — см. Гломерулонефрит острый.
• Гломерулонефрит с полулуниями (см. Гломерулонефрит быстропрогрессирующий).
• Мезангиопролиферативный гломерулонефрит — геморрагический васкулит, хронический вирусный гепатит В, болезнь Крона, синдром Шёгрена, анкилозирующий спондилоартрит, аденокарциномы.
• Мембранозный гломерулонефрит — карциномы лёгкого, кишечника, желудка, молочных желёз и почек (паранеопластический гломерулонефрит), неходжкенская лимфома, лейкозы, СКВ (см. Нефрит волчаночный), вирусный гепатит В, сифилис, филяриатоз, малярия, шистосомоз, воздействие ЛС (препараты золота и ртути, а также триметадион и пеницилламин).
• Мембрано-пролиферативный гломерулонефрит — идиопатический, а также вторичный при СКВ, криоглобулинемии, хронических вирусных (HCV) или бактериальных инфекциях, ЛС, токсины.
• Фокально-сегментарный гломерулосклероз — идиопатический, а также серповидноклеточная анемия, отторжение почечного трансплантата, циклоспорин, хирургическое иссечение части почечной паренхимы, хронический пузырно-мочеточниковый рефлюкс, применение героина, врождённая патология (дисгенезия нефронов, поздние стадии болезни Фабри), ВИЧ-инфекция.
Патогенез
• В развитии и поддержании воспаления участвуют иммунные механизмы •• Иммунокомплексный •• Антительный (аутоантигенный) •• Активизация комплемента, привлечение циркулирующих моноцитов, синтез цитокинов, освобождение протеолитических ферментов и кислородных радикалов, активизация коагуляционного каскада, продуцирование провоспалительных Пг.
• В прогрессировании ХГН участвуют кроме иммунных и неиммунные механизмы •• Внутриклубочковая гипертензия и гиперфильтрация •• Протеинурия (доказано нефротоксическое воздействие протеинурии) •• Гиперлипидемия •• Избыточное образование свободных радикалов кислорода и накопление продуктов перекисного окисления липидов •• Избыточное отложение кальция •• Интеркуррентные рецидивирующие инфекции мочевыводящих путей.
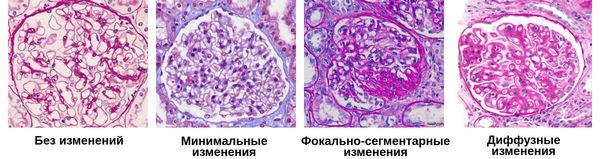
Патоморфология зависит от морфологической формы ХГН. При любой форме выявляют признаки склероза различной степени в клубочках и интерстиции — синехии, склерозированные клубочки, атрофия канальцев. Пролиферация и активация мезангиальных клеток играют ключевую роль в процессах накопления и изменения структуры внеклеточного матрикса, что заканчивается склерозированием клубочка. Патоморфологические изменения имеют исключительное значение для диагностики гломерулонефритов, т.к. постановки диагноза практически всегда необходимо проведение биопсии почечной ткани.
• Диффузный пролиферативный — диффузное увеличение числа клеток клубочка вследствие инфильтрации нейтрофилами и моноцитами и пролиферации эндотелия клубочков и мезангиальных клеток.
• Гломерулонефрит с полулуниями (быстропрогрессирующий) — см. Гломерулонефрит быстропрогрессирующий.
• Мезангиопролиферативный — пролиферация мезангиальных клеток и матрикса.
• Мембрано-пролиферативный — диффузная пролиферация мезангиальных клеток и инфильтрация клубочков макрофагами; увеличение мезангиального матрикса, утолщение и удвоение базальной мембраны.
• ХГН с минимальными изменениями — световая микроскопия без патологии, при электронной микроскопии — исчезновение ножек подоцитов.
• Фокально-сегментарный гломерулосклероз — сегментарное спадение капилляров менее чем в 50% клубочков с отложением аморфного гиалинового материала.
• Мембранозный — диффузное утолщение базальной мембраны клубочков с формированием субэпителиальных выступов, окружающих отложения иммунных комплексов (зубчатый вид базальной мембраны).
• Фибропластический гломерулонефрит — исход большинства гломерулопатий, характеризуется выраженностью фибротических процессов.
Клинические проявления • Симптомы появляются через 3–7 дней после воздействия провоцирующего фактора (латентный период), также они могут быть выявлены случайно при медицинском осмотре • Рецидивирующие эпизоды гематурии • Отёки, мочевой синдром, артериальная гипертензия в различных вариантах — нефротический или остронефритический синдром (нефротическая форма, смешанная форма — до 10%, гипертоническая форма — 20–30%) • Возможно сочетание проявлений остронефритического и нефротического синдромов • Жалобы на головную боль, потемнение мочи, отёки и снижение диуреза • Объективно — пастозность или отёки, повышение АД, расширение границ сердца влево • Температура тела нормальная или субфебрильная.
Клинические проявления при различных клинических формах
• Латентный ХГН (50–60%) •• Отёки и артериальная гипертензия отсутствуют •• В моче протеинурия не более 1–3 г/сут, микрогематурия, лейкоцитурия, цилиндры (гиалиновые и эритроцитарные) •• Может трансформироваться в нефротическую или гипертоническую формы •• Развитие ХПН происходит в течение 10–20 лет.
• Гипертонический ХГН •• Клинические проявления синдрома артериальной гипертензии •• В моче небольшая протеинурия, иногда микрогематурия, цилиндрурия •• ХПН формируется в течение 15–25 лет.
• Гематурический ХГН •• В моче — рецидивирующая или персистирующая гематурия и минимальная протеинурия (менее 1 г/сут) •• Экстраренальная симптоматика отсутствует •• ХПН развивается у 20–40% в течение 5–25 лет.
• Нефротическая форма — клинико-лабораторные проявления нефротического синдрома.
• Смешанная форма •• Сочетание нефротического синдрома, артериальной гипертензии и/или гематурии •• Обычно её отмечают при вторичных ХГН, системных заболеваниях (СКВ, системные васкулиты) •• ХПН формируется в течение 2–3 лет.
Клиническая картина в зависимости от морфологической формы
• Мезангиопролиферативный ХГН •• Изолированный мочевой синдром •• Остронефритический или нефротический синдром •• Макро- или микрогематурия — болезнь Берже •• ХПН развивается медленно.
• Мембранозный ХГН проявляется нефротическим синдромом (80%).
• Мембрано-пролиферативный ХГН •• Начинается с остронефритического синдрома, у 50% больных — нефротический синдром •• Изолированный мочевой синдром с гематурией •• Характерны артериальная гипертензия, гипокомплементемия, анемия, криоглобулинемия •• Течение прогрессирующее, иногда быстро прогрессирующее.
• Гломерулонефрит с минимальными изменениями •• Нефротический синдром, в 20–30% случаев с микрогематурией •• Артериальная гипертензия и почечная недостаточность возникают редко.
• Фокально-сегментарный гломерулосклероз •• Нефротический синдром •• В моче эритроцитурия, лейкоцитурия •• Артериальная гипертензия •• Закономерно развитие ХПН.
• Фибропластический гломерулонефрит •• Нефротический синдром (до 50%) •• ХПН •• Артериальная гипертензия.
Лабораторные данные
• В крови — умеренное повышение СОЭ (при вторичном ХГН возможно выявление значительного повышения, что зависит от первичного заболевания), повышение уровня ЦИК, антистрептолизина О, снижение содержания в крови комплемента (иммунокомплексный ХГН), при болезни Берже выявляют повышение содержания IgA.
• Снижение СКФ, повышение уровня мочевины и креатинина, анемия, метаболический ацидоз, гиперфосфатемия и др. (ОПН на фоне ХПН или ХПН).
• В моче эритроцитурия, протеинурия (массивная при нефротическом синдроме), лейкоцитурия, цилиндры — зернистые, восковидные (при нефротическом синдроме).
Инструментальные данные • При УЗИ или обзорной урографии размеры почек нормальны или уменьшены (при ХПН), контуры гладкие, эхогенность диффузно повышена • Рентгенография органов грудной клетки — расширение границ сердца влево (при артериальной гипертензии) • ЭКГ — признаки гипертрофии левого желудочка • Биопсия почек (световая, электронная микроскопия, иммунофлюоресцентное исследование) позволяет уточнить морфологическую форму, активность ХГН, исключить заболевания почек со сходной симптоматикой.
Диагностика. При уменьшении диуреза, появлении тёмной мочи, отёков или пастозности лица, повышении АД (может быть норма) проводят комплекс исследований: измерение АД, общий ОАК, ОАМ, определение суточной протеинурии, концентрации общего белка и оценивают протеинограмму, содержание липидов в крови. Углублённое физикальное и клинико-лабораторное обследование направлено на выявление возможной причины ХГН — общего или системного заболевания. УЗИ (рентгенография) почек позволяет уточнить размеры и плотность почек. Оценка функции почек — проба Реберга–Тареева, определение концентрации мочевины и/или креатинина в крови. Диагноз подтверждают биопсией почки.
Дифференциальная диагностика: с хроническим пиелонефритом, острым гломерулонефритом, нефропатией беременных, хроническими тубуло-интерстициальными нефритами, алкогольным поражением почек, амилоидозом и диабетической нефропатией, а также поражением почек при диффузных заболеваниях соединительной ткани (в первую очередь СКВ) и системных васкулитах.
ЛЕЧЕНИЕ
Общая тактика • Госпитализация в стационар при обострении ХГН, впервые выявленном ХГН, впервые выявленной ХПН • Диета с ограничением поваренной соли (при отёках, артериальной гипертензии), белка (при ХПН, обострении ХГН) • Воздействие на этиологический фактор (инфекция, опухоли, ЛС) • Иммунодепрессивная терапия — ГК и цитостатики — при обострении ХГН (показана и при азотемии, если она обусловлена активностью ХГН) • Антигипертензивные препараты • Антиагреганты, антикоагулянты • Антигиперлипидемические препараты • Диуретики.
Иммунодепрессивная терапия
• ГК показаны при мезангиопролиферативном ХГН и ХГН с минимальными изменениями клубочков. При мембранозном ХГН эффект нечёткий. При мембрано-пролиферативном ХГН и фокально-сегментарном гломерулосклерозе ГК малоэффективны •• Преднизолон назначают по 1 мг/кг/сут внутрь в течение 6–8 нед с последующим быстрым снижением до 30 мг/сут (по 5 мг/нед), а затем медленным (2,5–1,25 мг/нед) вплоть до полной отмены •• Пульс-терапию преднизолоном проводят при высокой активности ХГН в первые дни лечения — по 1000 мг в/в капельно 1 р/сут 3 дня подряд. После снижения активности ХГН возможно ежемесячное проведение пульс-терапии до достижения ремиссии.
• Цитостатики (циклофосфамид по 2–3 мг/кг/сут внутрь или в/м или в/в, хлорамбуцил по 0,1–0,2 мг/кг/сут внутрь, в качестве альтернативных препаратов: циклоспорин — по 2,5–3,5 мг/кг/сут внутрь, азатиоприн по 1,5–3 мг/кг/сут внутрь) показаны при активных формах ХГН с высоким риском прогрессирования почечной недостаточности, а также при наличии противопоказаний для назначения ГК, неэффективности или появлении осложнений при применении последних (в последнем случае предпочитают сочетанное применение, позволяющее снизить дозу ГК). Пульс-терапия циклофосфамидом показана при высокой активности ХГН либо в сочетании с пульс-терапией преднизолоном (или на фоне ежедневного перорального приёма преднизолона), либо изолированно без дополнительного назначения преднизолона; в последнем случае доза циклофосфамида должна составлять 15 мг/кг (или 0,6–0,75 г/м 2 поверхности тела) в/в ежемесячно.
• Одновременное применение ГК и цитостатиков считают эффективнее монотерапии ГК. Общепринято назначать иммунодепрессивные препарата в сочетании с антиагрегантами, антикоагулянтами — так называемые многокомпонентные схемы: •• 3-компонентная схема (без цитостатиков) ••• Преднизолон 1–1,5 мг/кг/сут внутрь 4–6 нед, затем 1 мг/кг/сут через день, далее снижают на 1,25–2,5 мг/нед до отмены ••• Гепарин по 5000 ЕД 4 р/сут в течение 1–2 мес с переходом на фениндион или ацетилсалициловую кислоту в дозе 0,25–0,125 г/сут, или сулодексид в дозе 250 МЕ 2 раза/сут внутрь ••• Дипиридамол по 400 мг/сут внутрь или в/в •• 4-компонентная схема Кинкайд–Смит ••• Преднизолон по 25–30 мг/сут внутрь в течение 1–2 мес, затем снижение дозы на 1,25–2,5 мг/нед до отмены ••• Циклофосфамид по 200 мг в/в ежедневно или двойная доза через день в течение 1–2 мес, затем половинная доза до снижения ремиссии (циклофосфамид можно заменить на хлорамбуцил или азатиоприн) ••• Гепарин по 5000 ЕД 4 р/сут в течение 1–2 мес с переходом на фениндион или ацетилсалициловую кислоту, или сулодексид ••• Дипиридамол по 400 мг/сут внутрь или в/в •• Схема Понтичелли: начало терапии с преднизолона — 3 дня подряд по 1000 мг/сут, следующие 27 дней преднизолон 30 мг/сутки внутрь, 2-й мес — хлорамбуцил 0,2 мг/кг •• Схема Стейнберга ••• Пульс-терапия циклофосфамидом: 1000 мг в/в ежемесячно в течение года ••• В последующие 2 года — 1 раз в 3 мес ••• В последующие 2 года — 1 раз в 6 мес.
Симптоматическая терапия
• Антигипертензивная терапия •• Ингибиторы АПФ обладают антипротеинурическим и нефропротективным действием, т.к., снижая внутриклубочковую гиперфильтрацию и гипертензию, замедляют темпы прогрессирования ХПН: каптоприл по 50–100 мг/сут, эналаприл по 10–20 мг/сут, рамиприл по 2,5–10 мг/сут •• Блокаторы кальциевых каналов негидропиридинового ряда: верапамил в дозе 120–320 мг/сут, дилтиазем в дозе 160–360 мг/сут, исрадипин и др.
• Диуретики — гидрохлоротиазид, фуросемид, спиронолактон.
•Антиоксидантная терапия (витамин Е), однако убедительные доказательства её эффективности отсутствуют.
• Гиполипидемические препараты (нефротический синдром): симвастатин, ловастатин, флувастатин, аторвастатин в дозе 10–60 мг/сут в течение 4–6 нед с последующим снижением дозы.
• Антикоагулянты (в сочетании с ГК и цитостатиками, см. выше) •• Гепарин по 5000 ЕД 4 р/сут п/к (под контролем международного нормализованного отношения [МНО]) не менее 1–2 мес; перед отменой за 2–3 дня дозу снижают •• Низкомолекулярные гепарины: надропарин кальция в дозе 0,3–0,6 мл 1–2 р/сут п/к, сулодексид в/м 600 МЕ 1 р/сут 20 дней, затем внутрь по 250 МЕ 2 р/сут.
• Антиагреганты (в сочетании с ГК, цитостатиками, антикоагулянтами; см. выше) •• Дипиридамол по 400–600 мг/сут •• Пентоксифиллин по 0,2–0,3 г/сут •• Тиклопидин по 0,25 г 2 р/сут •• Ацетилсалициловая кислота по 0,25–0,5 г/сут.
В лечении ХГН также используют следующие лечебные мероприятия (эффект которых в контролируемых исследованиях не доказан).
• НПВС (альтернатива преднизолону при малой клинической активности ХГН): индометацин по 150 мг/сут 4–6 нед, затем по 50 мг/сут 3–4 мес (противопоказаны при артериальной гипертензии и почечной недостаточности).
• Производные аминохинолина (хлорохин, гидроксихлорохин) назначают при отсутствии показаний к активной терапии при склерозирующих формах по 0,25–0,2 г внутрь 2 р/сут в течение 2 нед, затем 1 р/сут.
• Плазмаферез в сочетании с пульс-терапией преднизолоном и/или циклофосфамидом показан при высокоактивных ХГН и отсутствии эффекта от лечения этими препаратами.
Лечение отдельных морфологических форм
• Мезангиопролиферативный ХГН •• При медленно прогрессирующих формах, в т.ч. при IgA-нефрите, необходимости в иммунодепрессивной терапии нет •• При высоком риске прогрессирования — ГК и/или цитостатики •• 3- и 4-компонентные схемы •• Влияние иммунодепрессивной терапии на отдалённый прогноз остаётся неясным.
• Мембранозный ХГН •• Сочетанное применение ГК и цитостатиков •• Пульс-терапия циклофосфамидом по 1000 мг в/в ежемесячно •• У больных без нефротического синдрома и нормальной функцией почек — ингибиторы АПФ.
• Мембрано-пролиферативный (мезангиокапиллярный) ХГН •• Лечение основного заболевания •• Ингибиторы АПФ •• При наличии нефротического синдрома и снижения функций почек оправдана терапия ГК и циклофосфамидом с добавлением антиагрегантов и антикоагулянтов.
• ХГН с минимальными изменениями •• Преднизолон по 1–1,5 мг/кг в течение 4 нед, затем — по 1 мг/кг через день ещё 4 нед •• Циклофосфамид или хлорамбуцил при неэффективности преднизолона или невозможности его отменить из-за рецидивов •• При продолжающихся рецидивах нефротического синдрома — циклоспорин по 3–5 мг/кг/сут (детям по 6 мг/м 2 ) 6–12 мес после достижения ремиссии.
• Фокально-сегментарный гломерулосклероз •• Иммунодепрессивная терапия недостаточно эффективна •• ГК назначают длительно — до 16–24 нед •• Больным с нефротическим синдромом назначают преднизолон по 1–1,2 мг/кг ежедневно 3–4 мес, затем через день ещё 2 мес, затем дозу снижают вплоть до отмены •• Цитостатики (циклофосфамид, циклоспорин) в сочетании с ГК.
• Фибропластический ХГН •• При очаговом процессе лечение проводят согласно той морфологической форме, которая привела к его развитию •• Диффузная форма — противопоказание к активной иммунодепрессивной терапии.
Лечение по клиническим формам проводят при невозможности выполнения биопсии почек.
• Латентная форма •• Активная иммунодепрессивная терапия не показана. При протеинурии >1,5 г/сут назначают ингибиторы АПФ.
• Гематурическая форма •• Непостоянный эффект от преднизолона и цитостатиков •• Больным с изолированной гематурией или/или небольшой протеинурией — ингибиторы АПФ и дипиридамол.
• Гипертоническая форма •• Ингибиторы АПФ; целевой уровень АД — 120–125/80 мм рт.ст •• При обострениях применяют цитостатики в составе 3-компонентной схемы •• ГК (преднизолон 0,5 мг/кг/сут) можно назначать в виде монотерапии или в составе комбинированных схем.
• Нефротическая форма — показание к назначению 3- или 4-компонентной схемы.
• Смешанная форма — 3- или 4-компонентная схема лечения.
Хирургическое лечение • Трансплантация почки в 50% осложняется рецидивом в трансплантате, в 10% — реакцией отторжения трансплантата.
Особенности течения у детей • Чаще, чем у взрослых, постстрептококковые нефриты с исходом в выздоровление • Нефротический синдром до 80% обусловлен ХГН с минимальными изменениями.
Особенности течения у беременных • Влияние беременности на почки: функция снижается, увеличивается частота присоединения вторичного гестоза • Влияние ХГН на беременность — три степени риска (Шехтман М.М. и соавт., 1989): •• I степень (минимальная) — беременность можно разрешить (латентная форма) •• II степень (выраженная) — риск высокий (нефротическая форма) •• III степень (максимальная) — беременность противопоказана (гипертоническая и смешанная формы, активный ХГН, ХПН).
Осложнения • Почечная недостаточность, левожелудочковая недостаточность, острое нарушение мозгового кровообращения, интеркуррентные инфекции, тромбозы.
Течение и прогноз. Частота прогрессирования в ХПН зависит от морфологической формы ХГН • Диффузный пролиферативный — 1–2% • Мезангиопролиферативный — 40% • Быстропрогрессирующий — 90% • Мембранозный — 40% • Очаговый и сегментарный гломерулосклероз — 50–80% • Мембранозно-пролиферативный — 50% • IgA-нефропатия — 30–50%.
Сокращение. ХГН — хронический гломерулонефрит.
МКБ-10 • N03 Хронический нефритический синдром