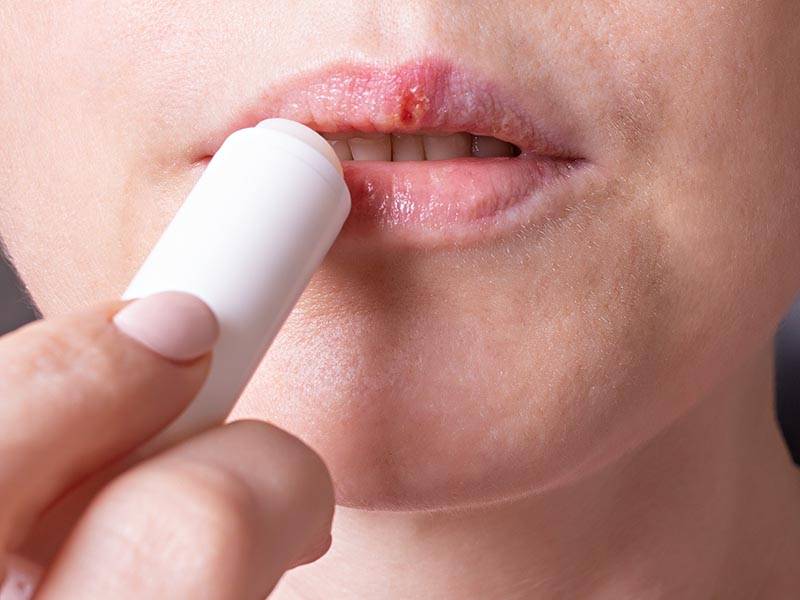
что такое герпес лабиалис
Герпес на губах
Лабиальный герпес (герпес на губах, простой герпес) — заболевание, которое вызывается вирусом герпеса 1 типа. Вирусов герпеса выделяют 8 типов, но в том, что называется простудой на губах, виновен чаще всего 1 тип.
Как происходит заражение вирусом?
Вирусом можно заразиться разными путями: воздушно-капельным, контактным (через общие полотенца, столовые приборы, через поцелуи), половым путем, самовыражением (когда из язвочек вирус попадает на здоровые слизистые и заражает их). Заразиться можно при переливании крови и ребенок может получить вирус от матери внутриутробно.Инкубационный период (от момента контакта до появления первых признаков) составляет 2-14 дней.Человек становится заразным, как только появляются болячки на губе, и заразен для окружающих пока корочки не отпадут.
Фото: Один из самых распространенных путей передачи герпеса — контактный.
Где скрывается вирус?
Если человек заразился однажды, то герпес останется с ним на всю жизнь. Вирус попадает в организм через трещинки на коже губ. Дальше он проходит в клетки нашего организма и размножается, выделяя всё новые вирусы, которые разрушают клетки. Так протекает обострение с пузырьками. А потом вирус никуда не исчезает. Он попадает в нервные окончания и там хранится до следующего обострения.
Почему появляется простуда на губах?
Те, кто болеют герпесом заметили, что обострения начинаются вместе с ОРВИ. Герпес возникает при снижении иммунитета, защитные силы которого идут на подавление ОРВИ. Еще простуда на губах появляется, когда защитные силы организма ослабли: при хронической усталости, недосыпании, частых стрессах, неправильном питании, злоупотреблении алкоголем и активном курении, у женщин в начале беременности и в первые 5-7 дней после родов.
Фото: Простуда на губах может появляться только в случае снижения иммунитета
Как проявляется герпес?
В медицине принято выделять 5 статей развития простого герпеса:
1. Первая стадия возникает при появлении пузырьков. Проявляется жжением и зудом в области губы, ее отеком.
2. Вторая стадия начинается с появлением пузырьков. Сначала маленькие, они растут, заполняются прозрачной жидкостью. Через пару дней жидкость мутнеет.
3. Для третьей стадии болезни характерен разрыв пузырьков. На месте лопнувших пузырьков образуются язвочки с отеком. Эта стадия опасна развитием осложнений. Человек в этот момент очень заразен.
4. В четвертой стадии язвочки покрываются плотной корочкой.
5. На пятой стадии корочки подсыхают, отпадают. Симптомы проходят. Человек становится не заразен.
Как часто могут быть обострения?
Выделяют три формы течения заболевания:
• тяжелая: 6-8 рецидивов в год, часто сопровождаются высокой температурой, головной болью, слабостью, рвотой, воспалением лимфоузлов;
• средней тяжести с обострениями 3-4 раза в год;
• легкая форма: 1-2 рецидива в год.
Чем может быть опасен герпес?
Герпес может вызывать множество осложнений. Некоторые их них опасны для жизни.
Фото: Воизбежание осложнений приступать к лечении герпеса нужно своевременно.
Как лечить герпес?
Полостью и навсегда вылечить герпес нельзя, но можно уменьшить частоту рецидивов и снизить тяжесть симптомов
Есть три группы препаратов для лечения герпеса:
• противовирусные препараты;
• иммуномодуляторы;
• инактивированные вакцины.
При местных формах герпеса с нечастыми обострениями используются препараты с дезинфицирующим действием и препараты для ускорения заживления. К ним относятся примочки из хлоргексидина, гель алломедин, мазь декспантенол. При обострениях реже 1 раза в 6 месяцев лечение, направленное на уменьшение количества вирусов в организме (вирусной нагрузки) не требуется. Просто нужно заниматься спортом, высыпаться и хорошо питаться, чтобы иммунитет был крепким.
Фото: Лечение герпеса
Если герпес появляется 1 раз в 3 месяца и чаще, тогда назначаются противовирусные препараты, выбор отдается ацикловиру и валацикловиру. Препараты применяются в таблетках внутрь ( 5 раз в день по 1 таблетке не менее 5 дней) и в виде мази на сами пузырьки (тонким слоем 5 раз в день 5 дней, даже при исчезновении проявлений болезни). Существуют противовирусные препараты растительного происхождения, например, алпизарин. Выпускается в двух формах: в виде таблеток и свечей ( при генитальном герпесе).
Еще одно направление лечения герпеса — иммуномодуляторы и индукторы интерферонов.
Иммуномодуляторы — препараты, которые воздействуют на иммунитет и укрепляют его. Есть растительные и синтетические препараты. Растительные (женьшень, элеутерококк, эхинацея, лимонник, девясил, родило розовая), которые обладают общетонизирующим действием. Содержат небольшое количество стимулирующих веществ и поэтому единственным их противопоказанием является наличие аллергии. Могут применяться курсами на протяжении всей жизни. Синтетические в таблетках и капсулах (интерферон, ликопид, арбидол) и уколах (тимолин, тимоген, альтевир, неовир)повышают защитные силы организма, снижают количество и тяжесть обострений. Применяются только после консультации с врачом.
Используются и индукторы интерферонов (циклоферон). Препарат стимулирует образование своего интерферона, который не позволяет вирусу попасть в клетку и снижает риск заражения здоровых соседних клеток.
В последние годы активно разрабатывалась и проходила доклинические испытания вакцина против герпеса. Она содержит фрагменты ДНК вируса. Вакцина позволит увеличить интервал между обострениями простуды на губах, а в некоторых случаях и полностью излечить пациента от вируса герпеса.
Существует множество эффективных методов лечения симптомов герпеса, снижения и тяжести частоты обострений, но правильное и действенное лечение может подобрать только врач.
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
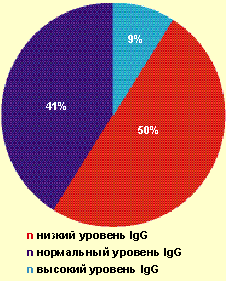 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
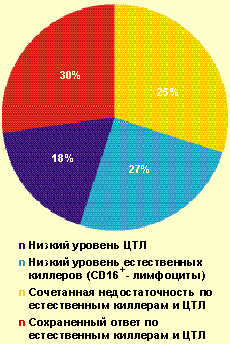 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва
ЭФФЕКТИВНОЕ И БЫСТРОЕ ЛЕЧЕНИЕ ГЕРПЕСА
Герпес – вирусное заболевание, поражающее кожный покров и слизистые оболочки. Его возбудителем является ВПГ (вирус простого герпеса). Он имеет высокую заразность и присутствует в организме 90% населения планеты. На сегодня не существует методов лечения герпеса для полного устранения вируса. Носитель живет с ним всю жизнь, однако в 60% случаев ВПГ никак не проявляется, хотя остается вероятность его передачи другим людям.
Опасность заболевания
Необходимость лечения герпеса у взрослых и детей возникает только при создании благоприятных условий для жизнедеятельности вируса. До этого он находится в «спящем» состоянии, а к активизации приводит ослабление иммунитета на фоне:
Если лечение герпеса на губах требуется человеку не более 3-4 раз в год, это считается вариантом нормы и подразумевает только симптоматическую терапию. Обязательно пройти подробное иммунологическое обследование нужно при рецидивах болезни 4-5 раз в год с высыпаниями на обширных участках тела.
Сложность лечения опоясывающего герпеса у взрослых
Заболевание проявляется в виде пузырьков с прозрачным содержимым, которое трансформируется в кровянистое или гнойное. Лечение опоясывающего герпеса сопряжено с рядом сложностей, так как пораженный участок вызывает сильную болезненность. Однако главной проблемой становятся невралгические боли на продолжении длительного периода. Некоторых пациентов они тревожат несколько месяцев, других – несколько лет.
Симптоматика лабиального герпеса
Главным признаком болезни являются пузырьки с прозрачной жидкостью, образующиеся на губах. Как правило, заболевание вызывает дискомфорт только из-за покалывания и зуда, однако у некоторых больных наблюдается повышение температуры и головная боль. Как и в случае с опоясывающим герпесом, возможно только симптоматическое лечение. Для полного заживления требуется 1-1,5 недели. Данная форма болезни склонна рецидивировать на одном и том же участке губ.
По окончании острой фазы вирусного поражения (с лечением герпеса или без него) пузырьки лопаются с формированием корки. При умывании она размокает и отслаивается, открывая влажную поверхностную язвочку. Это самая заразная стадия заболевания, поскольку содержимое ранки контактирует с окружающей средой. В данный период человеку нужно тщательно следить за гигиеной, пользоваться отдельной посудой, полотенцами и пр.
Передача лабиального герпеса происходит контактным, воздушно-капельным и бытовым путем, поэтому большинство людей заражается в возрасте 3-4 лет. Как правило, необходимость лечения этого типа герпеса возникает при появлении таких симптомов, как:
Современная диагностика и лечение герпеса в «Медикал Он Груп – Люберцы»
Лечение герпеса в «Медикал Он Груп – Люберцы» проводится дерматологом, который собирает анамнез и подбирает ряд диагностических мероприятий. Диагноз ставится после осмотра и подтверждается с помощью методов ПЦР, РИФ (реакции иммунофлюоресценции), ИФА (иммуноферментного анализа), цитологического исследования.
При появлении симптомов герпеса необходимо комплексное лечение, которое может включать:
Дерматологи нашей клиники используют современные методы лечения герпеса на теле и губах у взрослых, что позволяет уменьшить дискомфорт и значительно ускорить выздоровление. Врач в обязательном порядке дает рекомендации по укреплению иммунитета и профилактике рецидивов.
ЛАБИАЛЬНЫЙ ГЕРПЕС: что необходимо знать стоматологу
Вступление Боль и зуд в области губы, покраснение, возникновение болезненных пузырьков, которые через несколько дней лопаются и сменяются «корочками». Многим знакомы эти неприятные симптомы заболевания, фигурирующего в медицине под названием «лабиальный герпес».
Проявления лабиального герпеса обычно исчезают в течение 1-2 недель, даже при отсутствии лечения. Поэтому большинству людей эта болезнь не представляется опасной, хотя и вызывает дискомфорт с точки зрения неприятных ощущений и эстетики. Как в профилактической медицине, так и в классической, мало внимания уделяется предупреждению заражения вирусом герпеса и возникновению повторных рецидивов, в том числе связанных с посещением медицинских учреждений и непосредственным контактом врач — пациент. Насколько такая позиция справедлива, можно судить по данным, приведенным в статье.
Cреди огромного числа вирусных заболеваний герпетическая инфекция является наиболее распространенной. Она охватывает до 90% взрослого населения земного шара и примечательна тем, что всегда становится персистентной. После заражения вирусом герпеса и последующего выздоровления с симптоматической точки зрения вирус не исчезает из организма, а переходит в латентную форму. В таком виде он может существовать постоянно, никак не проявляя себя, или периодически «просыпается» и начинает размножаться, снова вызывая сходное заболевание. Заразными для человека являются 8 типов вирусов герпеса, включенных в подсемейства альфа, бета и гамма-вирусов. Из них особенно часто у человека встречаются представители альфа-вирусов — вирусы простого герпеса (Herpes simplex) 1 и 2 типов, а также вирус ветряной оспы (herpes zoster virus). Главными особенностями альфа-вирусов, способствующими их широкому распространению среди людей, являются: 1) размножение в покровных оболочках, где вирусные частицы легко доступны для передачи другому человеку; 2) переход в латентное («спящее») состояние в телах чувствительных нейронов, куда вирус может легко проникнуть через периферические нервные окончания; 3) быстрое размножение вируса и высокая скорость транспорта по нервным волокнам. Лабиальный герпес (ЛГ) — одно из часто встречающихся заболеваний, связанных с реактивацией вируса герпеса из латентного состояния.
РАСПРОСТРАНЕННОСТЬ ЛАБИАЛЬНОГО ГЕРПЕСА. ГРУППЫ РИСКА
ЛГ проявляется в виде однократного или рецидивирующего поражения эпителия в области губ. Это заболевание вызывает вирус простого герпеса 1-го или (реже) 2-го типа [4; 13].
В среднем по популяциям разных стран вирусом простого герпеса 1-го типа (ВПГ-1) инфицировано 70-80% людей [8; 12; 15], в отдельных популяциях до 90% [10; 11; 17] по крайней мере однократное проявление ЛГ. Для проявления симптомов лабиального герпеса необходимо сочетание трех факторов: 1) наличия вируса (первичное инфицирование или латентное состояние); 2) стрессовых воздействий или повреждений периферических нервных ганглиев; 3) генетической предрасположенности [8].
Первичное заражение часто происходит в детском возрасте. Так, в Великобритании к 12 годам 40% детей имеют антитела к ВПГ-1. Первичное инфицирование более чем у 80% детей протекает бессимптомно [1], а у остальных, как правило, вызывает герпетический гингивостоматит [10]. Симптомы первичной ВПГ-1 инфекции разнообразны, могут не распознаваться или быть ошибочно интерпретированы. Только у 5% людей наблюдаются характерные, ярко выраженные клинические признаки — наличие язвочек в полости рта, гингивит, лихорадка и цервикальная лимфаденопатия. У людей с нормальным иммунным статусом проявления первичной инфекции исчезают через 10-14 дней. Однако проникший в организм вирус не уничтожается иммунной системой до конца, а проникает в нервные клетки, где переходит в неактивное (латентное) состояние. Позже вирус может снова стать активным и вызвать неприятные локальные симптомы в области кожи или слизистых — гингивостоматит, лабиальный герпес, офтальмогерпес и др.
Таким образом, чаще всего люди не замечают ситуации первичного заражения ВПГ-1 и не подозревают о том, что стали носителями вируса, пока у них не возникнет острый эпизод, связанный с реактивацией вируса из латентного состояния.
Иногда возможны случаи, когда первичное инфицирование ВПГ-1 может возникать в области пальцев и глаз, что имеет прямое отношение к работе стоматологов. При приеме пациента с реактивированным вирусом основным путем заражения ВПГ-1 для врача становится контакт с пораженными зонами и/или со слюной. Герпетический стоматит у стоматолога при первичном инфицировании возникает редко, однако зафиксированы случаи поражения кожи пальцев и роговицы глаз. В первом случае у врача развивается воспаление мягких тканей пальца (рис. 1), во втором, как правило, воспаление роговицы — кератит [10]. Оба заболевания сопровождаются неприятными ощущениями, снижают работоспособность, могут продолжаться несколько недель. Все это время заболевший доктор является заразным и не должен принимать пациентов. Профилактикой подобного инфицирования является использование перчаток и защитных очков. Воспаление (панариций) тканей пальца стоматолога, вызванное ВПГ-1 (из Lewis, 2004) [10].
С другой стороны, прием у стоматолога с активной формой лабиального герпеса представляет угрозу заражения для пациента. Особенно важно предотвратить передачу ВПГ-1 от врача к иммунокомпрометированным, восприимчивым пациентам. С этой целью важно оценить наличие такого риска еще до начала лечения, поскольку связанные со стоматологическими манипуляциями микротравмы могут способствовать развитию лабиального герпеса.
Еще одним важным путем первичного инфицирования ВПГ-1 является заражение ребенка от матери. Первичное инфицирование беременных женщин ВПГ-1 обычно не имеет последствий для плода [5]. Носительство ВПГ-1 беременной женщиной в некотором смысле может быть даже благоприятным вследствие присутствия антител к ВПГ-1 в крови. Это делает детей менее восприимчивыми к вирусу в первые 6 месяцев жизни. Однако наличие у матери ЛГ в острой фазе, особенно при грудном вскармливании, представляет угрозу заражения для новорожденного ребенка. Результатом первичного инфицирования малыша не всегда является гингивостоматит. Так, в литературе описан случай возникновения у ребенка в возрасте 5 мес. тяжело протекающего генитального герпеса, вызванного полученным от матери ВПГ-1 [1].
Проникновение ВПГ-1 в слизистую полости рта при заражении от матери не всегда ограничивается латентностью вируса в близлежащих нервных клетках. Согласно особенностям жизненного цикла вируса (см. ниже) после первичного инфицирования ВПГ-1 может распространяться не только по тем нервным волокнам, куда он попал первоначально, но и далее, по цепочке нейронов. В результате вирусные частицы могут проникать не только в чувствительные ганглии, но и в центральную нервную систему, а также в головной мозг [7; 9]. В этом случае при реактивации ВПГ-1 возможно возникновение поражений не только в области губ, но и в других частях лица, в области глаз (офтальмогерпес, герпетический ретинит), в других областях кожи (по типу экземы, сходной с атопическим дерматитом), а также существует риск энцефалита [2; 15]! Каждый год фиксируется около 1 эпизода развития энцефалита, вызванного ВПГ-1, на 250 тыс. — 500 тыс. людей. Вероятность развития энцефалита выше в ситуации реактивации вируса и у людей в возрасте от 6 мес. до 20 лет и старше 50 лет. При энцефалите смертность составляет 70%, у 97% выживших людей возникают нейрологические нарушения.
ПОЧЕМУ ЛГ ПОВТОРЯЕТСЯ?
Примерно у трети инфицированных людей (от16% до 35% популяции, у пожилых около 20%) ВПГ-1 рано или поздно реактивируется из латентного состояния [10].
Чаще всего вторичная инфекция проявляется в виде лабиального герпеса на границе между красной каймой губ и кожей (mucocutaneous) нижней или верхней губы. Кроме того, сходные повреждения могут возникать на других частях лица, в области носа, на шее. Также могут наблюдаться эпизоды изъязвлений в слизистой полости рта, особенно на твердом нёбе. У некоторых людей, особенно детей, ВПГ-1 периодически появляется в слюне без клинических проявлений.
Частота рецидивов ЛГ сильно варьирует — от единичных случаев за 5-10 лет до ежемесячных эпизодов или более частых (у небольшого количества людей) [8]. Основными факторами, коррелирующими с частотой рецидивов, являются женский пол, низкий социоэкономический статус, пожилой возраст (наибольший риск в 65-74 года), частые инфекции верхних дыхательных путей, пониженное число лимфоцитов [4]. Реактивации вируса способствует ряд провоцирующих факторов: 1) системные — лихорадка, менструация и другие сопровождающиеся гормональными изменениями состояния, стресс, действие препаратов, подавляющих иммунитет; 2) местные — повреждения губ, воздействие холода, солнечное излучение, а также зубоврачебные манипуляции и хирургические операции в полости рта [2; 10].
В частности, описаны случаи рекуррентного герпеса после удаления зуба с обширным распространением повреждений в области носа, подбородка, губ, полости рта (рис. 2). Более выраженными были поражения на той стороне лица, где производилось удаление зуба. Повреждение нерва при стоматологическом лечении повышает риск реактивации герпеса. Среди пациентов с хирургическими вмешательствами, затрагивающими ветви тройничного нерва, реактивация ВПГ-1 возникает у 50% людей. Фактором риска является также использование анестезии, так как она временно нарушает функционирование нервных волокон в зоне действия [6].
Важную роль в возобновлении активности вируса играет иммунный статус человека, в частности реактивность Т-лимфоцитов к разным иммуностимулирующим участкам (эпитопам) вирусных белков [3]. Показано, что у людей с регулярными симптоматическими проявлениями ЛГ (5% среди иммунокомпетентных пациентов) и у инфицированных ВПГ-1 лиц с отсутствием симптомов герпеса частота реактивации вируса одинакова, однако поражения тканей наблюдаются только у первой группы. Есть данные о различиях в величине и природе Т-клеточных иммунных реакций у «симптоматических» и «асимптоматических» пациентов: у первых при реактивации вируса образуются неэффективные Т-лимфоциты (Тхелперы CD4+ и Ткиллеры CD8+), в то время как у вторых имеются Т-лимфоциты с высокой степенью противовирусной защиты. Надо отметить, что при реактивации вируса «асимптоматические» пациенты тоже являются источником распространения вируса, несмотря на отсутствие внешних заметных проявлений [3].
ЖИЗНЕДЕЯТЕЛЬНОСТЬ ВПГ-1
Особенности молекулярной биологии ВПГ-1 позволяют ему после первичного заражения оставаться в организме до конца жизни, периодически возобновляя свою активность при нарушении баланса между защитными силами иммунитета и жизнедеятельностью латентной формы вируса. Частица ВПГ-1 представляет собой линейную двухцепочечную молекулу ДНК, покрытую многослойной оболочкой. Внутренняя часть оболочки — это белковая капсула (капсид), затем следует слой белков (тегумент) и далее — внешняя фосфолипидная оболочка с встроенными белками (рис. 3). Белки внешней оболочки являются главными маркерами (антигенами), позволяющими иммунной системе распознать вирус.
Жизненный цикл ВПГ-1 состоит из нескольких стадий [7]. На первом этапе происходит заражение организма зрелой формой вируса. Он передается от носителя воздушно-капельным или контактным способом. В зоне контакта вирус проникает в эпителиальные клетки и быстро размножается в них (рис.4). Взаимодействие вирусной частицы с клеткой-мишенью происходит путем прикрепления белков фосфолипидной оболочки вируса (гликопротеинов gC и gB) к рецепторам клеточной мембраны. После этого другой белок вирусной оболочки (гликопротеин gD) запускает процесс ее слияния с мембраной клетки-мишени. Внутрь клетки вирусная частица попадает уже без оболочки в виде капсида (рис. 5). Капсид транспортирует вирусную ДНК к ядру клетки, где и происходит размножение вируса путем многократного дублирования вирусной ДНК (репликации). При этом с ДНК вируса считываются молекулы мРНК, которые выходят из ядра в цитоплазму. В цитоплазме на их основе синтезируются необходимые вирусу белки (в том числе белки оболочки) с использованием белоксинтезирующей машины самой клетки. Каждая копия ДНК вируса опять упаковывается в капсид, выходит из ядра, снова покрывается оболочкой, и сформированная вирусная частица покидает клетку. Такие дочерние вирусные частицы достигают окончаний дендритов нервных клеток (в основном, чувствительных нейронов ганглиев тройничного (V) нерва) и проникают в них. Затем вирусы транспортируются от нервных окончаний к телам нейронов (путем ретроградного аксонного транспорта), где переходят в латентную форму существования (рис.4). Вирус, находящийся в латентной форме, невозможно обнаружить. Во время латентного состояния геном вируса в виде множества копий кольцевых фрагментов ДНК находится в ядрах нервных клеток. Состояние латентности возникает в результате стабилизации вирусной ДНК и ограничения «считывания» (экспрессии) генов вируса. В латентном состоянии экспрессируется только один ген вируса — LAT (Latency Associated Transcript). Белок, кодируемый LAT, отвечает за регуляцию состояния генома клетки-хозяина, предотвращает уничтожение зараженного нейрона лейкоцитами (Т киллерами) и, таким образом, поддерживает вирус в консервированном состоянии.
Традиционное место локализации латентной формы ВПГ-1 — чувствительные нейроны периферических ганглиев тройничного нерва. Однако в зависимости от очага первичного заражения ВПГ-1 может персистировать и в нейронах других периферических ганглиев головы и шеи (чувствительных и эфферентных вегетативных) — спинальных, вестибулярных, спиральных, ресничных, лицевого нерва, верхних шейных, узловатых (nodose) блуждающего нерва [9; 13]. Кроме того, ВПГ-1 может транспортироваться и дальше — по аксонам пораженных нейронов к их синаптическим окончаниям. Через синапсы вирус способен проникать в клетки центральной нервной системы, где также возможен его переход в латентное состояние.
Через некоторое время (от нескольких недель до месяцев и лет) происходит реактивация вируса из латентного состояния и репликация его ДНК, достаточная для образования нескольких новых вирусных частиц. Новые вирусные частицы в виде капсидов с помощью антероградного аксонного транспорта перемещаются от тела нейрона к окончаниям его нервных волокон. Выделяясь из периферических окончаний дендритов, вирус проникает в клетки первичного очага заражения (эпидермиса), что вызывает местное повреждение тканей, в случае ЛГ — соединения между кожей и слизистой в области губ. Это часто сопровождается классическими симптомами, описанными ниже [15].
У иммунокомпрометированных людей вирус может распространяться не только по дендритам нейрона-хозяина к периферическим тканям, но и по аксону к мозгу. В случае проникновения вируса в мозг возникает риск энцефалита, однако у взрослого человека частота таких случаев невысока [18].
ПРОТЕКАНИЕ ЛАБИАЛЬНОГО ГЕРПЕСА: СТАДИИ И СИМПТОМЫ
Максимальное количество вирусных частиц наблюдается через 24 часа после начала повреждения ткани, что соответствует стадии образования пузырьков, и далее происходит прогрессирующее снижение числа вирусных частиц [4]. Таким образом, вирус инициирует начальное повреждение клеток, в то время как дальнейшие симптомы болезни связаны с физиологическими процессами иммунной защиты и восстановления целостности тканей, в том числе с активацией ноцицепторов (боль, ощущение жжения). В зараженных вирусом клетках происходят процессы, в итоге вызывающие их лизис: изменение свойств мембраны, снижение синтеза клеточных белков, замедление деления и атака со стороны иммунитета. Надо отметить, что у иммунокомпрометированных пациентов болезнь протекает дольше и тяжелее, может затрагивать полость рта и область лица [4].
ДИАГНОСТИКА ВИРУСА ПРОСТОГО ГЕРПЕСА 1 ТИПА
Выявление ВПГ-1 особенно необходимо при симптомах инфекционных проявлений в области лица и полости рта — в первую очередь с целью постановки правильного диагноза и назначения оптимального лечения. Особенно часто с такими проявлениями сталкиваются врачи-стоматологи — при наличии стоматита, гингивита или поражений покровных оболочек в области лица после лечения или удаления зуба.
Обнаружить присутствие ВПГ-1 в организме можно двумя способами. Первый — это определение наличия в клетках или жидкостях вирусных белков (антигенов) или ДНК, что возможно только в активную фазу жизни вируса. Второй способ заключается в выявлении присутствия антител к ВПГ-1 в сыворотке крови вне зависимости от формы существования вируса в текущий момент. Этот метод более универсален, он неэффективен только при оценке крови сразу после первичного инфицирования, поскольку антитела появляются на 4-8-й день после заражения. Преимуществом данного метода является возможность по соотношениям антител первичного и вторичного иммунного ответов (соответственно — иммуноглобулинов М и G) сделать заключение о характере инфекции — является ли она первичной или рецидивирующей.
ПОДХОДЫ К ЛЕЧЕНИЮ ЛАБИАЛЬНОГО ГЕРПЕСА
При лечении ЛГ используют несколько видов воздействий: 1) противовирусное, направленное на подавление размножения вирусных частиц; 2) иммуномодулирующее, направленное на активацию защитных механизмов иммунитета (интерфероны, индукторы интерферона и пр.); 3) симптоматическое, направленное на снижение выраженности неприятных симптомов и более быстрое заживление повреждений (антигистаминные, противоспалительные, обезболивающие препараты, регенерирующие вещества); 4) профилактическое, направленное на предупреждение вторичных инфекций (антисептики) и рецидивов в последующем (вакцинация, улучшение иммунного статуса). Поскольку естественный процесс выздоровления начинается уже в первые сутки заболевания, терапию необходимо начинать как можно раньше [4]. Блокада репликации вируса в начале заболевания позволяет уменьшить длительность симптомов и ускорить процесс заживления.
Главными противовирусными веществами, используемыми в современной медицине, являются аналоги нуклеозидов — ацикловир и пенцикловир или их предшественники — валацикловир и фамцикловир соответственно [15]. Эти вещества оказывают селективное действие на пораженные клетки. Принцип их биохимических преобразований и избирательного действия сходен: под действием фермента ВПГ-1 тимидин-киназы исходное вещество фосфорилируется и затем подвергается дальнейшему фосфорилированию двумя молекулами фосфата под действием киназ зараженной клетки. Трифосфатная форма вещества является активной. Она ингибирует вирусную ДНК-полимеразу, вызывая обрыв цепи ДНК вируса, что в итоге предотвращает дальнейшую ее репликацию. Таким образом, активация противовирусного вещества происходит только в тех клетках, где присутствует вирус и его фермент тимидин-киназа.
Показано, что при остром протекании ЛГ противовирусные препараты ускоряют процесс заживления и уменьшают продолжительность негативных ощущений — зуда, жжения, боли. Так, согласно клиническим исследованиям, местное применение ацикловира в виде мази ( 5%, аппликация 5 р в день) уменьшало время заживления на несколько дней — по разным данным от 0,5 до 2,5 суток, не влияя на выраженность болевых ощущений [12; 15]. Применение мази, содержащей комплекс ацикловира (5%) с гидрокортизоном (1%) укорачивало этот срок на 0,2 дня [15]. Мазь, содержащая пенцикловир, оказывала сходное c ацикловиром действие и, кроме того, уменьшала продолжительность болевых ощущений в среднем на 0,5 дня [12]. Однако использование этой мази с практической точки зрения менее удобно, так как требует аппликации каждые 2 часа. Оральная противовирусная терапия с использованием ацикловира, фамцикловира или валацикловира уменьшала распространение вируса, время заживления и продолжительность болевых ощущений — в зависимости от схемы лечения от 1 дня до 4-5 дней [4; 15].
Различные результаты по применению противовирусной терапии могут быть связаны не только с разными схемами лечения и дозами препаратов, но и развитием резистентности к ним. Резистентность может возникать вследствие как спонтанных мутаций в вирусной ДНК, так и гомологичной ее рекомбинации в процессе репликации [11; 15]. В этом отношении значимыми являются мутации, изменяющие функции объектов действия препарата — вирусных ферментов тимидин-киназы (90% случаев развития резистентности) и ДНК-полимеразы, снижая ее сродство к активному ацикловир-трифосфату [14; 15; 16]. Показано, что у людей с нормальным иммунным статусом резистентность к ацикловиру наблюдается довольно редко (
Похожие статьи
ЧЕМ ОПАСЕН ПРОСТОЙ ГЕРПЕС
Герпетическая инфекция входит в число наиболее распространенных, плохо контролируемых, трудно поддающихся лечению инфекций человека. 90% населения страдает от периодических высыпаний на губах и коже вокруг рта, сопровождающихся легким недомоганием, повышением температуры и прочими признаками острой вирусной инфекции. У ослабленных людей вирус герпеса может поражать нервную систему, кожу, слизистые оболочки и внутренние органы.
ЧТО ТАКОЕ ЛАБИТАЛЬНЫЙ ГЕРПЕС И КАК ЕГО ЛЕЧИТЬ?
Лабиальный герпес (ЛГ), или «простуда на губах» — это вирусное заболевание, проявляющееся в виде однократного или повторяющегося поражения эпителия в области губ, вызванного вирусом простого герпеса (ВПГ) 1 или 2 типа.
«ГЕРПЕНОКС» — активные компоненты и их действие
На сегодняшний день на фармацевтическом рынке России представлено большое количество противовирусных средств — аналогов нуклеозидов (ацикловир, пенцикловир, валацикловир, фамцикловир и пр.), иммунных препаратов (препараты интерферона, индукторы интерферона, герпетическая вакцина).
123592, Москва, ул.Кулакова, дом 20, строение г. Тел.: + 7 (495) 781 9203, info@globaldrc.com
© 2012-2015 Distribution Retail Company.
Все права защищены.