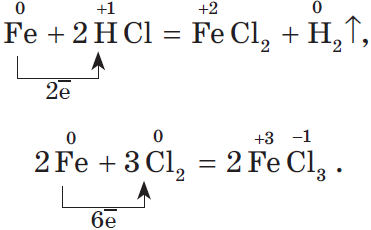что такое генетический ряд
Основные классы неорганических соединений
Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ
Генетическая связь – это связь между веществами, которые относятся к разным классам.
Основные признаки генетических рядов:
1. Все вещества одного ряда должны быть образованы одним химическим элементом.
2. Вещества, образованные одним и тем же элементом, должны принадлежать к различным классам химических веществ.
3. Вещества, образующие генетический ряд элемента, должны быть связаны между собой взаимопревращениями.
Таким образом, генетическим называют ряд веществ, которые представляют разные классы неорганических соединений, являются соединениями одного и того же химического элемента, связаны взаимопревращениями и отражают общность происхождения этих веществ.
1. Генетический ряд металлов, гидроксиды которых являются основаниями (щелочами):
металл → основный оксид → основание (щелочь) → соль.
Например, генетический ряд кальция:
2. Генетический ряд металлов, которые образуют амфотерные гидроксиды:
соль
металл → амфотерный оксид → (соль) → амфотерный гидроксид
cоль
Оксид цинка с водой не взаимодействует, поэтому из него сначала получают соль, а затем гидроксид цинка. Так же поступают, если металлу соответствует нерастворимое основание.
3. Генетический ряд неметаллов (неметаллы образуют только кислотные оксиды):
неметалл → кислотный оксид → кислота → соль
Например, генетический ряд фосфора:
Переход от одного вещества к другому осуществляется с помощью химических реакций.
Например:
Генетический ряд металла объединяет:
— основные оксиды
-основания
-соли
Генетический ряд неметалла объединяет:
— кислотные оксиды
— кислоты
— соли
Например:
Химия. 11 класс
Конспект урока
Урок № 16. Генетическая связь неорганических и органических веществ
Перечень вопросов, рассматриваемых в теме: урок посвящён изучению взаимосвязи неорганических и органических соединений: свойствам органических и неорганических веществ, взаимосвязи различных классов соединений, уравнениям химических реакций, отражающих её.
Генетическая связь – это связь между классами соединений, отражающая возможность превращения вещества одного класса в вещество другого класса.
Генетический ряд – это цепочка превращений веществ, которые имеют в составе один и тот же химический элемент.
Витализм – это устаревшее учение о существовании сверхъестественной «жизненной силы», которая наполняет органическую природу и определяет её свойства.
Фридрих Вёлер – великий немецкий врач и химик, синтезировал мочевину и щавелевую кислоту из неорганических соединений, первым получил карбид кальция, из которого под действием воды синтезировал ацетилен.
Синтез-газ – это смесь монооксида углерода и водорода, получают паровой конверсией или частичным окислением метана, газификацией угля. Используется для синтеза метанола, синтеза Фишера-Тропша.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
1. Рябов, М.А. Сборник задач, упражнений и тесто по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
До девятнадцатого века в химии господствовал витализм – учение о «жизненной силе». Виталисты считали, что «жизненная сила» отличает живое вещество от неживого. Поэтому синтез органических соединений из неорганических казался им принципиально невозможным.
В начале девятнадцатого века немецкий врач и химик Фридрих Вёлер опроверг теорию витализма. Из неорганических веществ он получил мочевину и щавелевую кислоту.
В 1828 году Ф. Вёлер при нагревании цианида аммония неожиданно для себя получил мочевину – вещество, которое образуется при метаболизме белков у млекопитающих и рыб. Ранее, в 1824 году, Ф. Вёлер получил щавелевую кислоту из дициана. Дициан – бесцветный ядовитый газ со слабым запахом. Его получают в электрической дуге при взаимодействии углерода с азотом. При гидролизе дициана в кислой среде образуется щавелевая кислота.
В промышленных масштабах получают метанол из неорганических веществ – смеси монооксида углерода, углекислого газа и водорода. Эта смесь носит название синтез-газ. Процесс ускоряют катализаторы из оксида цинка или меди.
Вышеприведенные синтезы иллюстрируют генетическую связь между классами органических веществ. Термин генетическая связь означает, что вещество одного класса может превращаться в вещество другого класса.
Генетическая связь записывается в виде генетических рядов – цепочек превращений веществ, имеющих в составе один и тот же химический элемент. Генетические ряды органических веществ очень разветвленные и сложные, в чем вы убедились на примере ацетилена, метанола, метана.
Генетические ряды неорганических веществ намного проще, потому что неорганические вещества делятся на меньшее число классов.
Генетический ряд металлов, образующих растворимые гидроксиды, представлен последовательностью реакций: из простого вещества получают основный оксид, затем гидроксид, затем соль. Помните, что у металлов, образующих нерастворимые в воде гидроксиды, генетический ряд выглядит несколько иначе: за оксидом следует соль, и только затем гидроксид.
Генетический ряд неметаллов аналогичен таковому металлов. Простое вещество образует кислотный оксид, затем кислоту и, наконец, соль.
Теперь вы знаете, что между генетическими рядами органических и неорганических соединений нет чётких границ, и можете обосновать это на примере синтеза мочевины, щавелевой кислоты, метана, ацетилена, метанола.
В клетках живых организмов постоянно происходит синтез и распад органических соединений. В ходе фотосинтеза в хлоропластах растений из воды и углекислого газа образуется глюкоза. В клетках млекопитающих углеводы и жиры окисляются до воды и углекислого газа, а белки распадаются с образованием мочевины.
ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ ТРЕНИРОВОЧНОГО МОДУЛЯ
1. Решение задачи на множественный выбор.
Условие задачи: Выберите верные генетические ряды и запишите их номера.
Первый вариант неверный, потому что гидроксид меди нерастворим в воде и может быть получен только реакцией обмена соли меди и щелочи.
Второй вариант верный.
Третий вариант верный.
2.Решение задачи на вписывание формул.
Условие задачи: Введите формулы пропущенных веществ в генетическом ряду.
Химия. 11 класс
Конспект урока
Урок № 16. Генетическая связь неорганических и органических веществ
Перечень вопросов, рассматриваемых в теме: урок посвящён изучению взаимосвязи неорганических и органических соединений: свойствам органических и неорганических веществ, взаимосвязи различных классов соединений, уравнениям химических реакций, отражающих её.
Генетическая связь – это связь между классами соединений, отражающая возможность превращения вещества одного класса в вещество другого класса.
Генетический ряд – это цепочка превращений веществ, которые имеют в составе один и тот же химический элемент.
Витализм – это устаревшее учение о существовании сверхъестественной «жизненной силы», которая наполняет органическую природу и определяет её свойства.
Фридрих Вёлер – великий немецкий врач и химик, синтезировал мочевину и щавелевую кислоту из неорганических соединений, первым получил карбид кальция, из которого под действием воды синтезировал ацетилен.
Синтез-газ – это смесь монооксида углерода и водорода, получают паровой конверсией или частичным окислением метана, газификацией угля. Используется для синтеза метанола, синтеза Фишера-Тропша.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
1. Рябов, М.А. Сборник задач, упражнений и тесто по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
До девятнадцатого века в химии господствовал витализм – учение о «жизненной силе». Виталисты считали, что «жизненная сила» отличает живое вещество от неживого. Поэтому синтез органических соединений из неорганических казался им принципиально невозможным.
В начале девятнадцатого века немецкий врач и химик Фридрих Вёлер опроверг теорию витализма. Из неорганических веществ он получил мочевину и щавелевую кислоту.
В 1828 году Ф. Вёлер при нагревании цианида аммония неожиданно для себя получил мочевину – вещество, которое образуется при метаболизме белков у млекопитающих и рыб. Ранее, в 1824 году, Ф. Вёлер получил щавелевую кислоту из дициана. Дициан – бесцветный ядовитый газ со слабым запахом. Его получают в электрической дуге при взаимодействии углерода с азотом. При гидролизе дициана в кислой среде образуется щавелевая кислота.
В промышленных масштабах получают метанол из неорганических веществ – смеси монооксида углерода, углекислого газа и водорода. Эта смесь носит название синтез-газ. Процесс ускоряют катализаторы из оксида цинка или меди.
Вышеприведенные синтезы иллюстрируют генетическую связь между классами органических веществ. Термин генетическая связь означает, что вещество одного класса может превращаться в вещество другого класса.
Генетическая связь записывается в виде генетических рядов – цепочек превращений веществ, имеющих в составе один и тот же химический элемент. Генетические ряды органических веществ очень разветвленные и сложные, в чем вы убедились на примере ацетилена, метанола, метана.
Генетические ряды неорганических веществ намного проще, потому что неорганические вещества делятся на меньшее число классов.
Генетический ряд металлов, образующих растворимые гидроксиды, представлен последовательностью реакций: из простого вещества получают основный оксид, затем гидроксид, затем соль. Помните, что у металлов, образующих нерастворимые в воде гидроксиды, генетический ряд выглядит несколько иначе: за оксидом следует соль, и только затем гидроксид.
Генетический ряд неметаллов аналогичен таковому металлов. Простое вещество образует кислотный оксид, затем кислоту и, наконец, соль.
Теперь вы знаете, что между генетическими рядами органических и неорганических соединений нет чётких границ, и можете обосновать это на примере синтеза мочевины, щавелевой кислоты, метана, ацетилена, метанола.
В клетках живых организмов постоянно происходит синтез и распад органических соединений. В ходе фотосинтеза в хлоропластах растений из воды и углекислого газа образуется глюкоза. В клетках млекопитающих углеводы и жиры окисляются до воды и углекислого газа, а белки распадаются с образованием мочевины.
ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ ТРЕНИРОВОЧНОГО МОДУЛЯ
1. Решение задачи на множественный выбор.
Условие задачи: Выберите верные генетические ряды и запишите их номера.
Первый вариант неверный, потому что гидроксид меди нерастворим в воде и может быть получен только реакцией обмена соли меди и щелочи.
Второй вариант верный.
Третий вариант верный.
2.Решение задачи на вписывание формул.
Условие задачи: Введите формулы пропущенных веществ в генетическом ряду.
Взаимосвязь неорганических веществ
Теория к заданию 10 из ЕГЭ по химии
Взаимосвязь различных классов неорганических веществ
Материальный мир, в котором мы живем и крохотной частичкой которого мы являемся, един и в то же время бесконечно разнообразен. Единство и многообразие химических веществ этого мира наиболее ярко проявляется в генетической связи веществ, которая отражается в так называемых генетических рядах. Выделим наиболее характерные признаки таких рядов:
1. Все вещества этого ряда должны быть образованы одним химическим элементом. Например, ряд, записанный с помощью следующих формул:
$Br_2 → HBr → NaBr → NaNO_3$,
$NaBr + AgNO_3 = AgBr↓+ NaNO_3$.
Этот ряд мог бы считаться генетическим рядом элемента брома, если бы его завершили, например, так:
$Br_2 → HBr → NaBr → AgBr$.
2. Вещества, образованные одним и тем же элементом, должны принадлежать к различным классам, т.е. отражать разные формы его существования.
3. Вещества, образующие генетический ряд одного элемента, должны быть связаны взаимопревращениями. По этому признаку можно различать полные и неполные генетические ряды.
Например, приведенный выше генетический ряд брома будет неполным, незавершенным. А вот следующий ряд:
$Br_2 → HBr → NaBr → AgBr → Br_2$
уже можно рассматривать как полный: он начинался простым веществом — бромом и им же закончился. Обобщая сказанное выше, можно дать следующее определение генетического ряда.
Генетическим называется ряд веществ — представителей разных классов, являющихся соединениями одного химического элемента, связанных взаимопревращениями и отражающих общность происхождения этих веществ или их генезис.
Генетическая связь — понятие более общее, чем генетический ряд, который является пусть и ярким, но частным проявлением этой связи, реализующейся при любых взаимных превращениях веществ. Тогда, очевидно, под это определение подходит и первый приведенный в тексте ряд веществ.
Для характеристики генетической связи неорганических веществ мы рассмотрим три разновидности генетических рядов.
Генетический ряд металла.
Напомним, что для окисления железа в хлорид железа (II) нужно взять более слабый окислитель, чем для получения хлорида железа (III):
Генетический ряд неметалла.
Затруднение может вызвать лишь последний переход. Руководствуйтесь правилом: чтобы получить простое вещество из окисленного соединения элемента, нужно взять для этой цели самое восстановленное его соединение, например, летучее водородное соединение неметалла. В нашем случае:
По этой реакции в природе из вулканических газов образуется сера.
Аналогично для хлора:
Генетический ряд металла, которому соответствуют амфотерные оксид и гидроксид, очень богат связями, т.к. они проявляют в зависимости от условий то кислотные, то основные свойства.
Например, рассмотрим генетический ряд цинка:
Что такое генетический ряд
Единство и многообразие химических веществ наиболее ярко проявляется в генетической связи веществ, которая отражается в генетических рядах. Наиболее важными признаками генетических рядов являются:
Генетический ряд металла
Генетический ряд железа со степенями окисления +2 и +3.
Fe 







Ряд завершен, начинается и заканчивается простым веществом – железом. Уравнения реакций, при помощи которых можно получить все вещества ряда:
Генетический ряд неметалла
Генетический ряд серы со степенями окисления +4 и +6.
S 







Ряд завершен, начинается и заканчивается простым веществом – серой. Уравнения реакций, при помощи которых можно получить все вещества ряда:
Генетический ряд амфотерного элемента
Генетический ряд амфотерного металла – алюминия, который в зависимости от типа превращения может проявлять свойства кислоты и основания.
Уравнения реакций, при помощи которых можно получить все вещества ряда:
Генетическим называют ряд веществ – представителей разных классов неорганических соединений, являющихся соединениями одного и того же химического элемента, связанных взаимопревращениями и отражающих общность происхождения этих веществ.