что такое дросселирование газа пара
Дросселирование газов
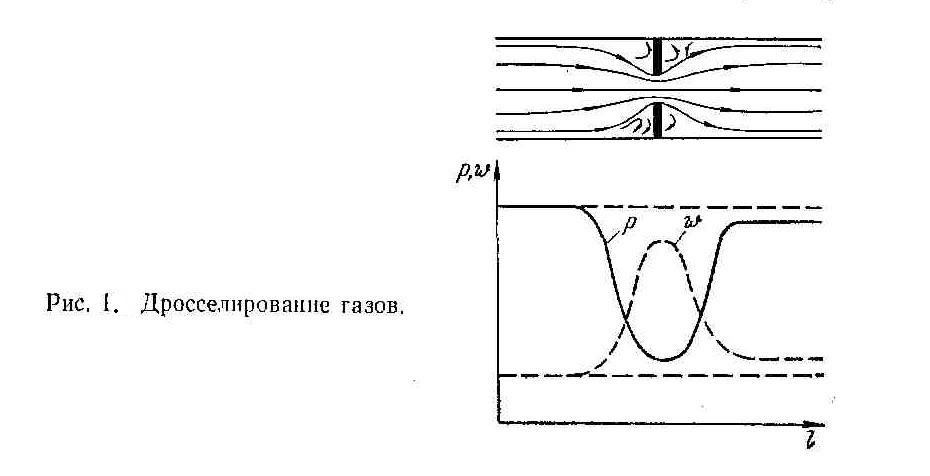
Здравствуйте! При движении газа на пути потока могут встречаться различные сопротивления, имеющие уменьшенные проходные сечения (задвижки, вентили, диафрагмы). Как показывает опыт, после прохождения через сопротивление происходит расширение газа и уменьшение его давления (рис. 1.).
При этом кинетическая энергия газа, затраченная на преодоление сил трения, превращается в теплоту трения. Процесс неравновесного расширения газа без совершения внешней работы при прохождении через местное сопротивление принято называть дросселированием.
Если дросселирование происходит при адиабатном течении, то, согласно уравнению первого закона термодинамики для потока,
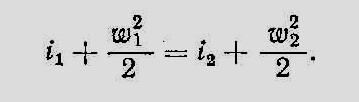
Обычно вторые члены в обеих частях этого уравнения малы по сравнению с первыми и, кроме того, скорости до дросселирования ω1 и после дросселирования ω2 мало отличаются друг от друга, поэтому вторыми слагаемыми можно пренебречь. Тогда из уравнения (1) получим i1 — i2. Следовательно, при дросселировании с достаточной для технических расчетов точностью энтальпию газа можно считать постоянной.
Так как энтальпия идеального газа зависит только от температуры: di = cpdT то при дросселировании конечная и начальная температуры равны: Т1 = Т2.
Дросселирование реального газа обычно сопровождается изменением его температуры. Это явление было экспериментально установлено в 1852 г. Джоулем и Томсоном и получило название эффекта Джоуля — Томсона.
Характер изменения температуры в процессе дросселирования определяется начальной температурой газа. При некоторой температуре, которая называется температурой инверсии, температура реального газа в процессе дросселирования, как и идеального, остается постоянной. Если температура реального газа перед дросселированием меньше температуры инверсии, то при дросселировании газ будет охлаждаться. При начальных температурах, превышающих точку инверсии, газы в процессе дросселирования нагреваются.
Температура инверсии зависит от давления, и для каждого значения давления имеются две температуры инверсии, расположенные соответственно в области перегретого пара и в области жидкости. Температуры инверсии всех газов, за исключением водорода и гелия, выше 0° С, поэтому дросселирование газов приводит к снижению их температуры. Это явление используется для сжижения газов с помощью машины Линде, в которой осуществляется многократное сжатие и охлаждение газа с последующим его дросселированием. Для сжижения водорода и гелия требуется предварительно охладить их ниже температуры инверсии.
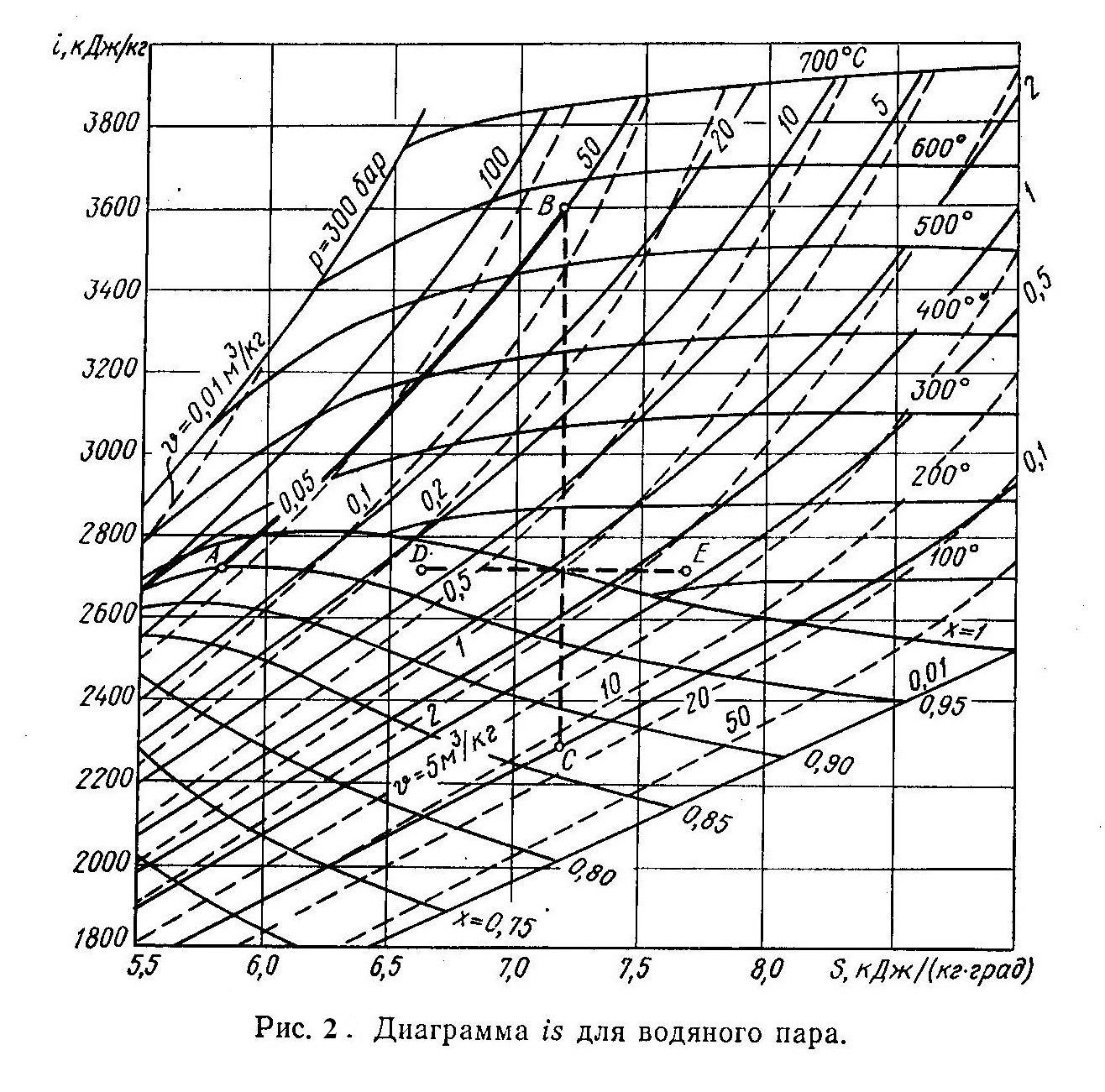
Процесс дросселирования водяного пара удобно рассчитать с помощью is-диаграммы. Построив на диаграмме линию, соответствующую условию i = const (изоэнтальпу), можно определить конечные и промежуточные значения параметров пара. Процессу дросселирования на рис.2. соответствует линия DE i = const.
Из этого примера видно, что при дросселировании влажного насыщенного пара низкого давления (точка D) его степень сухости x повышается и при большом снижении давления в процессе дросселирования пар становится перегретым. Исп. литература: 1) Теплотехника, под редакцией А.П.Баскакова, Москва, Энергоиздат, 1982. 2) Теплотехника, Бондарев В.А., Процкий А.Е., Гринкевич Р.Н. Минск, изд. 2-е,»Вышейшая школа», 1976.
Сущность процесса дросселирования газов и паров и изменение параметров рабочего тела при дросселировании.
Сущность процесса дросселирования газов и паров и изменение параметров рабочего тела при дросселировании.
Дросселирование газов и паров широко используется в редукционных клапанах, применяемых в системах тепло и парогазоснабжения, а также в холодильной технике для получения низких температур и снижения давления газов путем их многократного дросселирования.
Дросселирование является необратимым процессом.
При дросселировании идеального газа выполняется условие h2-h1=Ср(Т2-Т1), что свидетельствует о постоянстве температуры рабочего тела как до диаграммы, так и после нее. Обычно, дросселирование потока осуществляется диафрагмой.
Цикл поршневого ДВС с изобарным подводом теплоты (цикл дизеля) и его термический КПД
Термодинамический цикл (цикл Дизеля) с подводом теплоты при постоянном давлении (p= const) – реализуемой в компрессорных дизелях состоит из следующих обратимых процессов: 1-2 – адиабатное сжатие воздуха, 2-3- изобарный подвод теплоты, 3-4 – адиабатное расширение, 4-1 – отвод теплоты по изохоре.
Термодинамический к.п.д. цикла
Для этого цикла принимают ε = 12…14, l=1, r=1,1…1,5.
Цикл Ренкена парасиловой установки и его изображение в П1В-у-ТС-диаграммах и термический КПД
Теплота в цикле подводится в процессах 45, 56 и 61 и может быть определена как разность энтальпии в начале и конце процесса подвода теплоты:

Теплота 

Если пренебречь работой, расходуемой для привода насоса, величина которой незначительна, то работа цикла 


Так как 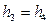

Термический КПД данного цикла может быть определен по формуле:
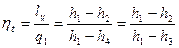
Из формулы (7.5) видно, что термический КПД цикла Ренкина зависит от значений энтальпий пара до и после турбины, а также от значения энтальпии воды, находящейся при температуре кипения 

Способы повышения КПД цикла парасиловой установки?
Теплопроводность через плоскую стенку. уравнение теплового потока и понятие термического сопротивления стенок
Теплоотдача при свободном движении жидкости (см 44)
Передача теплоты через ребристую стенку.
Основные схемы движения и теплообмена потоков теплоносителей.
Сущность процесса дросселирования газов и паров и изменение параметров рабочего тела при дросселировании.
Дросселирование газов и паров широко используется в редукционных клапанах, применяемых в системах тепло и парогазоснабжения, а также в холодильной технике для получения низких температур и снижения давления газов путем их многократного дросселирования.
Дросселирование является необратимым процессом.
При дросселировании идеального газа выполняется условие h2-h1=Ср(Т2-Т1), что свидетельствует о постоянстве температуры рабочего тела как до диаграммы, так и после нее. Обычно, дросселирование потока осуществляется диафрагмой.
Учебный вопрос № 1. Сущность процесса дросселирования



Лекция № 1. ДРОССЕЛИРОВАНИЕ ГАЗОВ.
Тема № 3. РАСШИРЕНИЕ ГАЗОВ.
Дросселированием называют необратимый процесс, в котором давление при прохождении газа через ссуженное отверстие уменьшается без совершения внешней работы.
Всякое сопротивление в трубопроводе (вентили, задвижка, шайба кран, клапан и др.) вызывает дросселирование газа и, следовательно, падение давления.
Величина падения давления зависит от природы рабочего тела, его состояния, величины сужения газопровода и скорости движения газа.
В большинстве случаев дросселирование, сопровождающееся уменьшением работоспособности тела, приносит безусловный вред, Но иногда оно является необходимым и создается искусственно, например, при регулировании паровых двигателей, в холодильных установках, в приборах, замеряющих расход газа и т.д.
Газ при прохождении через отверстие, представляющее известное сопротивление, кинетическая энергия газа и его скорость в узком сечении возрастают, что сопровождается падением температуры и давления (рис. 1).
Примером процесса дросселирования является выпуск сжатого газа из баллона. Температура газа на выходе из баллона резко понижается и вентиль обмерзает.
Процесс дросселированияподчиняется обшей теория газового потока,
| Р1, V1, Т1 Сжатый газ |
| Р2, V2, Т2 Расширенный газ |
| Рис. 1. Принципиальная схема дросселирования. |
основные положения которого были изложены Д.Бернулли, Н.Е.Жуковским и Чаплыгиным. Особое значение имеют работы Жуковского «Истечение газа под большим напором» и «О трении газов».
Большинство реальных газов (воздух, кислород, азот, углекислота и др.) при дросселировании в обычных условиях понижают свою температуру.
В основе этого процесса лежит эффект охлаждения, обнаруженный Джоулем и Томсоном в 1852 г. при адиабатномдросселировании реального газа. Этот процесс протекает как без теплообмена» так и без совершения полезной внешней работы.
Эти ученые произвели опыт с пропусканием сжатого газа через пористую пробку, вставленную в трубку, и установили, что при расширении газа во время прохождения через пробку происходит охлаждение его.
Дросселирование протекавшего газа или жидкости возникает в том случае, когда поток внезапно сужается вследствие уменьшения сечения, а затем опять получает возможность двигаться в большем сечении.
В ссуженном сечении скорость потока возрастает, что одновременно вызывает понижение температуры потока и, следовательно, уменьшение его внутренней энергии.
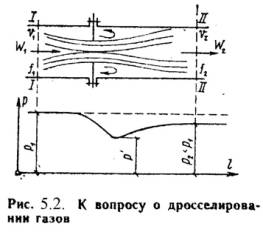
Процесс дросселирования можно рассмотреть с помощью схемы, изображенной на рисунке 2.
При прохождении газа через отверстие, представляющее известное сопротивление, кинетическая энергия газа и его скорость в узком сечении возрастают, что сопровождается падением температуры и давления.
| Рис. 2. Схема процесса дросселирования |
Газ, протекая через отверстие, приходит в вихревое движение. Часть кинетической энергии затрачивается на образование этих вихрей и превращается в теплоту, кроме этого, как было указано выше, в теплоту превращается и работа, затраченная на преодоление сопротивлений (трения).
Вся эта теплота воспринимается газом, в результате чего температура его изменяется и может как уменьшаться, так и увеличиваться.
В отверстии скорость газа увеличивается. За отверстием, когда газ течет по полному сечению, скорость его вновь понижается, а давление увеличивается, но до начального значения оно не поднимается; некоторое изменение скорости произойдет в связи с увеличением удельного объема газа от уменьшения давлении.
Дросселирование, как указывалось выше, является необратимым процессом, при котором всегда происходит увеличение энтропии и уменьшение работоспособности рабочего тела.
Для перемещения I кг газа необходимо затратить работу P1S1F1 или P1Q1.
Часть этой работы P2S2F2 или P2V2 будет израсходована на преодоление давления P2, а разность работ P1V1–P2V2 вызовет изменение энергии рабочего тела.
| w2 2 – w1 2 |
Если начальная скорость газа W1 и внутренняя энергия W2 то будем иметь
Р1V1 – P2V2 = U2 – U1 +
| w1 2 |
| w2 2 |
При условии, что скорости W1 и W2 мало отличаются друг от друга, изменением внешней кинетической энергии можно пренебречь и считать
(U1 – P1V1) – (U2 – P2V2) = 0
Полученное равенство показывает, что энтальпия в результате процесса дросселирования не изменяется. Этот вывод к промежуточным состояниям газа неприменим.
Энтальпия идеального газа является однозначной функцией температуры. Отсюда следует, что в результате дросселирования идеального газа температура его не изменяется Т1 = Т2.
В результате процесса дросселирования реального газа энтальпия для начальных и конечных давлений остается одинаковой, энтропия и объем увеличиваются, давление падает, а температуре может увеличиваться, уменьшаться или же, в частном случае, остаться без изменений.
Изученное ранее уравнение состояния Клапейрона PV = RT справедливо только для идеальных газов, которые в природе не существуют. Объем реальных газов, особенно в условиях высокого давления и низкой температуры, уменьшается при сжатии больше или меньше, чем это следует из уравнения состояния.
Уравнение Клапейрона для 1 кг реального газа имеет следующий вид: РV=ZRT,
Сущность явления сжимаемости заключается в следующем.
Между молекулами реального газа существуют силы сцепления и отталкивания. При сжатии газа до давлений 10-20 МПа силы сцепления возрастают в большей степени, нежели силы отталкивания. За счет этих повышенных сил сцепления объем газа при сжатии уменьшается в большей степени, чем это следует по закону Бойля-Мариотта, на величину «самосжимаемости».
Зная коэффициент сжимаемости данного реального газа, можно по уравнению Клайперона для идеального газа определить изменение давления или объема реального газа. Кривые, по которым можно определить коэффициенты сжимаемости для некоторых газов при разных абсолютных давлениях и температурах (0 и 50°С) приведены на рисунке.
Если коэффициент сжимаемости при данной температуре и давлении меньше единицы, такой газ сжимается в большей степени, чем идеальный газ; наоборот, если z >1, газ сжимается в меньшей степени, чем это следует из уравнения Клапейрона. Для идеального газа коэффициент сжимаемости z =1.
В момент дросселирования газа давление понижается и газ расширяется. Температура идеального газа остается постоянной, но для всех реальных газов при дросселировании температура изменяется. Данное явление обусловлено присущей реальным газам большей или меньшей степени сжимаемости по сравнению с идеальным газом.
0 40 80 120 160 200 0 40 80 120 160 200
Абсолютное давление, кгс/см2 Абсолютное давление, кгс/см2
Рис. 3. Коэффициент сжимаемости реальных газов при разных абсолютных давлениях и температурах
Оно было установлено английскими учеными Джоулем и Томсоном (Кельвином).
При дросселировании реальный газ совершает два вида работы – внешнюю и внутреннюю.
Внешняя работа заключается в перемещении некоторого объема газа при том давлении, которое действует после дросселя, а внутренняя – в преодолении сил взаимного притяжения между молекулами газа в процессе его расширения. Внешняя работа может быть как положительной, так и отрицательной. Если реальный газ сжимается сильнее, чем это следует по уравнению Клапейрона, то внешняя работа будет положительной. Она производится за счет части внутренней энергии газа, вследствие чего его температура понижается, т.е. газ охлаждается.
Когда реальный газ сжимается в меньшей степени, чем следует по уравнению Клапейрона, то внешняя работа отрицательна. В этом случае используется часть работы компрессора, и газ после дросселя нагревается, так как эта избыточная работа идет на увеличение внутренней энергии газа. Внутренняя работа, производимая газом при дросселирования, всегда положительна, т.е. вызывает охлаждение газа.
Общий эффект дросселирования для каждого реального газа определяется соотношением внешней и внутренней работы и зависит от начальных условий дросселирования (начального давления и температуры газа), а также физической природы газа.
Внешняя работа для воздуха, кислорода, азота в областях давлений и температур, обычных при их дросселировании в установках глубокого холода, положительна и по своей абсолютной величине незначительна по сравнению с внутренней работой. Поэтому эти газы при дросселировании всегда охлаждаются.
Однако существуют условия, когда эти газы при дросселировании могут не охлаждаться, а наоборот нагреваться. Например, Фогель установил, что при начальной температуре 28З°Кпроцессыдросселирования воздуха с давлением выше 36,8 МПа и кислорода с давлением свыше 31,1 МПа сопровождаются нагреванием этих газов.
Учебный вопрос № 2. Эффекты дросселирования
В термодинамике низких температур различают дифференциальный, интегральный и охлаждающий эффекты Джоуля-Томсона.
Теплосодержание газа в процессе дросселирования остается постоянным (i = сonst). Уменьшение теплосодержания газа происходит всегда до начала дросселирования, т.е. в процессе сжатия газа в компрессоре до начального давления перед дросселем. При этом затрачиваемая на сжатие механическая работа переходит в тепло сжатия, которое отводится от газа водой в холодильнике. Расширившийся затем в дросселе газ будет иметь вследствие этого меньшее теплосодержание и его температура после расширения будет ниже начальной на величину интегрального эффекта. Дифференциальный эффект αi = δТ/δР.
Принимая αР = 0,1 МПа, получим αi равной изменению температуры при дросселировании, приходящейся на 0,1 МПа падения давления.
Если αi > 0, то эффект положительный;
| Рис. 4. Значения дифференциального эффекта Джоуля-Томсона для воздуха при различных температурах и абсолютных давлениях |
| Температура Т, ˚К |
температуры увеличивается до линии насыщения. При давлениях выше критического этот эффект с понижением температуры сначала возрастает до максимума, а затем уменьшается, и тем более резко, чем ближе давление к критическому.
Дифференциальный эффект Джоуля-Томсона при высоких давлениях и низких температурах отрицательный. Точки пересечения изобар с горизонталью 0-0 являются инверсионными, так как в них αi = 0. Как видно из диаграммы изобары в правой части также где-то пересекаются с горизонталью 0-0; это соответствует вторым инверсионным точкам для воздуха в области очень высоких температур. Между двумя инверсионными точками значение дифференциального эффекта Джоуля-Томсона для воздуха всегда положительно.
Практически для приближенных подсчетов дифференциальный эффект считают равным ¼ °С при понижении давления на 1 ат.
Эффект, наблюдающийся при больших изменениях давления, называется интегральным.
Интегральный эффект Δ Тi показывает суммарное изменение температуры при данном конечном перепаде давлений.
Величину интегрального эффекта Джоуля-Томсона вычисляют для различных начальных давлений и температур дросселирования. Кроме того величина Δ Тi может быть определена:
— непосредственным измерением температур газа в начале и конце процесса как разность Δ Тi = Т2 – Т1;
Δ Тi = di (Р1 – Р2)(273/Т1)2,
где: (Р1–Р2) – перепад давлений;
273/Т1 – температурная поправка с учетом начальной температуры ;
по диаграммам i – Т; i – S и др.
| Рис. 5. Графики i – Т иi – S для определения интегрального эффекта |
Изотермический (охлаждающий) эффект
Изотермический эффект ΔIт показывает количество холода в кдж, расширившегося в дросселе с начального до конечного давления.
Для расчета процессов глубокого охлаждения исключительно важное значение имеет выражение джоуль-томсоновского эффекта в кдж или так называемый изотермический эффект дросселирования, представляющий собой разность теплосодержания сжатого состояние до дросселирования и расширенного газа при одной и той же температуре начала дросселирования.
ΔIт – это величина, численно равная разности энтальпий, полученных в процессах, предшествовавших дросселированию, т.е. в результате изотермического сжатия в компрессорной установке. Между изотермическим эффектом и интегральным существует следующая зависимость
Изотермический эффект характеризует холодопроизводительность процесса дросселирования. Он равен работе межмолекулярных сил газа при его сжатии и, следовательно, количеству холода, полученному при дросселировании:
5.3. Дросселирование
Любой кран, вентиль, задвижка, клапан и прочие местные сопротивления, уменьшающие проходное сечение трубопровода, вызывают дросселирования газа или пара, следовательно падения давления. В большинстве случаев это явление приносит безусловный вред. Но иногда оно является необходим и создается искусственно (регулирование паровых двигателей, в холодильных установках, в приборах для измерения расхода газа и т.д.).
При прохождении газа через отверстие, кинетическая энергия газа и его скорость в узком сечении возрастают, что сопровождается падением температуры и давления.
Газ, протекая через отверстие, приходит в вихревое движение. Часть его кинетической энергии затрачивается на образование этих вихрей и превращается в теплоту. Кроме того, в теплоту превращается и работа, затраченная на преодоление сопротивлений (трение). Вся эта теплота воспринимается газом, в результате чего температура его изменяется (уменьшается или увеличивается).
В отверстие скорость газа увеличивается. За отверстием газ опять течет по полному сечению и скорость его вновь понижается. А давление увеличивается, но до начального значения оно не поднимается; некоторое изменение скорости произойдет в связи с увеличением удельного объема газа от уменьшения давления.
Дросселирование является необратимым процессом, при которм происходит увеличение энтропии и уменьшение работоспособности рабочего тела.
Это равенство показывает, что энтальпия в результате дросселирования не изменяется и справедливо только для сечений, достаточно удаленных от сужения.
Для идеальных газов энтальпия газа является однозначной функцией температуры. Отсюда следует, что при дросселировании идеального газа его температура не изменяется (Т1 = Т2).
При дросселировании реальных газов энтальпия газа остается постоянной, энтропия и объем увеличиваются, давление падает, а температура изменяется (увеличивается, уменьшается или остется неизменной).
Изменение температуры жидкостей и реальных газов при дросселировании называется эффектом Джоуля-Томсона. Для идеального газа эффект Джоуля-Томсона равен нулю. Различают дифференциальный температурный эффект, когда давление и температура изменяются на бесконечно малую величину, и интегральный температурный эффект, при котором давление и температура изменяются на конечную величину.
Интегральный температурный эффект определяется из следующего уравнения:
Для реальных газов D T ¹ 0 и может иметь положительный или отрицательный знак.
Состояние газа, при котором температурный эффект меняет свой знак, называется точкой инверсии, а температура, соответствующая этой точке, называется температурой инверсии — Тинв.