что такое детский лейкоз
Лейкоз у детей
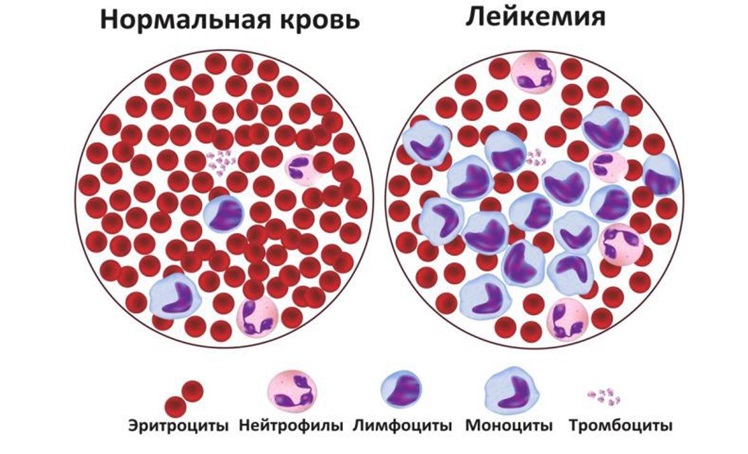
Лейкоз у детей (лейкемия) – заболевание, которое сопровождается нарушением костномозгового кроветворения и замещением нормальных клеток крови незрелыми бластными клетками лейкоцитарного ряда. Из ста тысяч детей болеет около 4-5. Среди детских онкологических заболеваний удельный вес случаев лейкоза составляет 30%, рак крови поражает наиболее часто малышей от 2 до 5 лет.
В последние годы заболеваемость пациентов маленького возраста растет, высокая летальность всё еще сохраняется.
Формы лейкоза у детей:
В 97 случаях из 100 у детей диагностируют острый лейкоз. Особая его форма – врожденная.
Виды острого лейкоза:
Касательно течения заболевания, исследователи выделяют 3 стадии, от которых зависит тактика терапии:
Что провоцирует / Причины Лейкоза у детей:
Сегодня доказанной является роль онкогенных вирусных штаммов, радиационного излучения, наследственной предрасположенности, химических факторов, эндогенных нарушений на возникновение лейкоза у детей. Лейкоз вторичный может появиться в результате лучевой или химиотерапии, которые были проведены для лечения другого заболевания (окнологического).
У детей с диагнозом «болезнь Дауна» лейкоз бывает примерно в 15 раз чаще, чем у детей без такой болезни. Также в группе риска дети с такими заболеваниями:
Факторы риска при лейкозах у детей
Факторами риска считаются любые влияния, которые увеличивают вероятность заболевания ребенка лейкозом. Сюда относят вредные привычки, нездоровое питание, многочасовое пребывание на солнце. Важную роль играют генетические факторы риска, которые были перечислены выше.
Если у одного из сиблингов в возрасте до 6 лет возник острый лейкоз, то вероятность 20-25%, что лейкоз обнаружат со временем и у второго сиблинга.
Больные, которые получают интенсивную терапию с целью угнетения иммунных функций, имеют повышенный риск развития опухолей, особенно лимфоидной системы, в том числе острого лимфобластного лейкоза.
Патогенез (что происходит?) во время Лейкоза у детей:
У нормальной кроветворной клетки снижается резистентность и повышается чувствительность к действию различных канцерогенов и коканцерогенов. Далее клетка мутирует. Кроветворная клетка превращается в опухолевую. Далее следует опухолевая прогрессия. Причем сначала длительный период происходит безграничная моноклональная пролиферация — так называемая доброкачественная прогрессия.
Следующий этап патогенеза – повторная мутация опухолевых клеток, которые приводят к появлению субклонов-поликлонов. Как итог – происходит злокачественная опухолевая прогрессия. Для всех лейкозных клеток, как было доказано исследователями, характерны выраженные расстройства их структуры, метаболизма, гистохимических особенностей и функций.
Продолжительность существования бластных клеток удлиняется, а функциональная активность (фагоцитарная, двигательная, ферментативная, регуляторная) снижается.
Симптомы Лейкоза у детей:
Лейкоз проявляется неспецифическими симптомами:
В некоторых случаях первым проявлением лейкоза у детей будет геморрагический или интоксикационный синдром.
В части случаев проявляются и такие симптомы лейкоза у детей:
Типичные проявления острого лейкоза в детском возрасте:
При остром лейкозе у детей может быть выявлен анемический синдром, который возникает как следствие угнетения эритропоэза и кровотечений. Кардиоваскулярные расстройства при лейкозе у ребенка могут проявляться аритмией, тахикардией, диффузными изменениями миокарда (могут быть выявлены по ЭКГ), расширением границ сердца (видно на рентгенограмме), снижением фракции выброса.
Интоксикационный синдром при лейкозе (лейкемии) у детей проявляется так:
Проявлениями иммунодефицитного синдрома при лейкозе у детей служит наслоение инфекционно-воспалительных процессов, которые могут принимать тяжелое, угрожающее течение. Дети с диагнозом «лейкоз» умирают в части случаев от тяжелой пневмонии или сепсиса.
Среди осложнений лейкемии у детей выделяют лейкемическую инфильтрацию головного мозга, мозговых оболочек и нервных стволов. Нейролейкоз проявляется головными болями, головокружением, диплопией, тошнотой, ригидностью затылочных мышц. При инфильтрации вещества спинного мозга возможно развитие парапареза ног, нарушения чувствительности, тазовых расстройств.
Диагностика Лейкоза у детей:
При подозрении на лейкоз ребенка должен исследовать педиатр, а потом детский онкогематолог. Основной диагностики являются лабораторные методы: исследование периферической крови и костного мозга.
При остром лейкозе у ребенка выявляют в общем анализе крови типичные изменения:
— лейкоцитоз различной степени или лейкопения
— исчезновение базофилов и эозинофилов
Типичным признаком служит так называемый феномен «лейкемического провала»: между зрелыми и бластными клетками нет промежуточных форм.
Лейкоз диагностируют обязательно с проведением стернальной пункции и миелограммы. О болезни говорит содержание бластных клеток 30% и более. Если исследования костного мозга не дали четких результатов, ребенку делают трепанобиопсию. Чтобы определить вариант острого лейкоза, проводят такие исследования: иммунологические, цитохимические, цитогенетические.
Подтверждение диагноза проводится при участии детского офтальмолога и детского невролога. Также проводится в некоторых случаях рентгенография черепа, люмбальная пункция и исследование цереброспинальной жидкости, офтальмоскопия.
Вспомогательные методы диагностики лейкоза у детей:
Лейкоз при диагностике врачи отличаются от лейкозоподобной реакции, которая бывает при коклюше, тяжелых формах туберкулеза, цитомегаловирусной инфекции, инфекционном мононуклеозе, сепсисе. При таких заболеваниях проявления лейкоза могут иметь обратимый характер.
Как установить стадию лейкоза?
Лейкозы стадируются не так, как большинство случаев рака. С самого начала болезни поражена периферическая кровь и костный мозг. Нужно выявить проникновение клеток лейкоза в селезенку, печень, лимфоузлы, ЦНС, яички, яичники.
Если в центральной нервной системе лейкозные клетки есть в большом количестве, то их фиксируют при помощи исследования спинномозговой жидкости под микроскопом. Если клетки выявлены, ребенку нужно более интенсивное лечение.
Прогностические факторы при лейкозе (лейкемии) у детей:
Лечение Лейкоза у детей:
При обнаружении лейкоза ребенка нужно госпитализировать в специализированное учреждение онкогематологического профиля. Чтобы не возникли инфекционные осложнения, ребенка помещают в отдельный бокс, условия в котором максимально приближенны к стерильным. Рацион больного обязательно должен быть сбалансированным и полноценным.
Для лечения лейкозов необходима полихимиотерапия, направленная на полную эрадикацию лейкозного клона. При острых лимфобластных и миелобластных лейкозах необходима различная комбинация химиопрепаратов, дозы и способы введения.
Этапы лечения:
Химиотерапию в части случаев дополняют активной и пассивной иммунотерапией: вакцинами БЦЖ, введением лейкозных клеток, интерферонами, противооспенной вакциной и т.д. Сегодня исследуется эффективность методов трансплантации пуповинной крови, костного мозга, стволовых клеток.
Также необходимо симптоматическое лечении при лейкемии у детей:
Прогноз лейкоза у детей
Прогноз зависит от возраста ребенка, когда у него возник лейкоз, от стадии диагностирования и прочих факторов. Худший прогноз дают детям, у которых лейкоз возник в возрасте до 2-х лет и старше 10-ти лет; у детей с диагнозом гепатоспленомегалии и лимфаденопатии; с нейролейкозом на момент диагностирования лейкемии. Также плохой прогноз у детей с Т- и В-клеточными вариантами лейкоза, при бластном гиперлейкоцитозе.
Благоприятный прогноз при остром лимфобластном лейкозе L1 типа; в случаях раннего начала лечения, при быстром достижении ремиссии; у детей в возрасте 2-10 лет. У девочек с острым лимфобластным лейкозом вероятность излечение несколько выше, чем у мальчиков.
Профилактика Лейкоза у детей:
Необходимо снизить факторы риска, которые перечислялись выше. Дети с известным фактором риска развития лейкоза, например, при синдроме Ли-Фраумени или синдроме Дауна, должны находиться под тщательным периодическим наблюдением.
Нужно избегать изменения климатических условий и физиотерапевтического лечения, чтобы не спровоцировать рецидив лейкоза у детей. Вакцинопрофилактика проводится по индивидуальному календарю с учетом эпидемической ситуации.
К каким докторам следует обращаться если у Вас Лейкоз у детей:
Лейкозы у детей: симптомы, диагностика, лечение
Лейкозы относятся к большой группе злокачественных новообразований системы крови под названием «гемобластозы». Лейкоз (от греческого слова «leukos» — белый) — злокачественная опухоль, возникающая из ранних незрелых кроветворных клеток костного мозга и метастазирующая из костного мозга в кровь, лимфатические узлы, печень, селезенку, головной мозг, спинной мозг и другие органы и ткани.
Все лейкозы можно разделить на острые лимфобластые, острые миелоидные лейкозы (ОМЛ) и хронический миелолейкоз.
Острый лимфобластный лейкоз
Более 80% всех лейкозов у детей составляет острый лимфобластный лейкоз (ОЛЛ). Причиной его развития является химерный ген TEL/AML, формирование которого происходит внутриутробно, возможно, в результате спонтанных ошибок в процессе репликации и репарации ДНК. Накопление генетических аномалий в опухолевом клоне ведет к блоку нормальной клеточной дифференцировки и нарушениям в процессе пролиферации и апоптоза.
В соответствии с франко-американо-британской (FAB) классификацией выделяют три морфологических варианта: L1, L2, L3.
Клинические симптомы ОЛЛ обусловлены степенью инфильтрации костного мозга лимфобластами, а также наличием экстрамедуллярного распространения процесса. Нередко отмечаются общие симптомы опухолевой интоксикации, а именно, повышение температуры тела, снижение аппетита, слабость, вялость. В течение процесса выделяют несколько периодов: начальный, развернутый, период ремиссии.
Развернутый период характеризуется бурным началом, многообразием клинических симптомов. К симптомам общей интоксикации присоединяются костные боли вследствие лейкозной инфильтрацией костной ткани (чаще поражаются диафизы длинных трубчатых костей), артралгии, вызванные лейкемической инфильтрацией суставов. Кожные покровы и слизистые становятся бледными. К сожалению, нередко на них появляются кровоизлияния, обусловленные геморрагическим синдромом, а также кровотечения (носовые, желудочно-кишечные, почечные). Увеличение периферических лимфатических узлов (шейно-надключичных, подмышечных, паховых) является одним из основных симптомов заболевания. Практически у всех пациентов отмечается обусловленное пролиферацией лейкозных клеток увеличение печени и селезенки. В некоторых случаях у пациентов поражение кожи и слизистых оболочек проявляется в виде лейкемидов, некроза, гингивита и стоматита.
Таким образом, можно выделить несколько симптомокомплексов, характерных для ОЛЛ:
При диагностике оцениваются морфологические особенности бластов костного мозга и периферической крови. Помимо обнаружения опухолевых клеток лимфоидной линии кроветворения при окраске по Романовскому – Гимзе, проводятся следующие методы исследования:
Для подтверждения диагноза ОЛЛ необходимо комплексное обследование, в котором ведущая роль отводится морфологическому методу.
В настоящее время используются программы лечения BFM (БФМ: Берлин-Франкфурт-Мюнстер) и МВ (МБ: Москва-Берлин).
Все лечение можно разделить на базисное и сопроводительное. Базисная терапия представляет собой системную и локальную химиотерапию и, при необходимости, лучевую терапию. Сопроводительное лечение обязательно назначается для профилактики инфекционных осложнений и коррекции постцитостатических реакций. Выделяют следующие этапы в лечении злокачественных процессов: индукция ремиссии, консолидация ремиссии (как правило, несколько фаз), поддерживающее лечение.
Острый миелоидный лейкоз
Острый миелоидный лейкоз составляет 15% всех острых лейкозов у детей. Существующая FAB-классификация (Франко-Американо-Британская) позволяет разделить ОМЛ на следующие варианты:
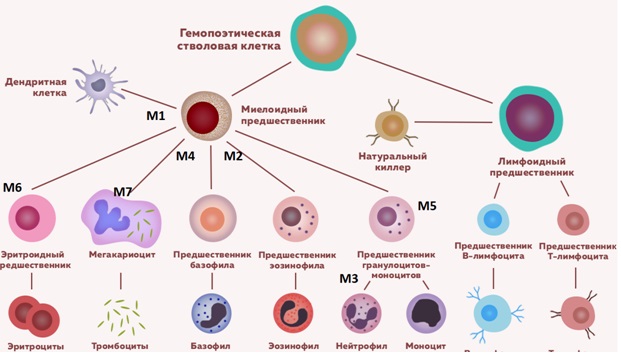
Схема гемопоэза с клетками предшественниками острого миелоидного лейкоза
Клиническая картина ОМЛ также складывается из анемического, геморрагического и токсического синдромов, которые являются следствием снижения продукции эритроцитов, тромбоцитов и гранулоцитов.
У 50% пациентов отмечается увеличение размеров печени (гепатомегалия) и селезенки (спленомегалия) вследствие инфильтрации органов опухолевыми клетками.
Внекостномозговые проявления заболевания связаны с лейкозной инфильтрацией центральной нервной системы и метастатическим поражением оболочек и вещества головного и спинного мозга (нейролейкемия). В этих ситуациях отмечается постоянная головная боль, возможна рвота, вялость, выявляется отек дисков зрительных нервов, могут быть нистагм, косоглазие, другие признаки поражения черепно-мозговых нервов, выявляются ригидность затылочных мышц, симптом Кернига.
Решающую роль в диагностике также имеет цитохимическое, иммунофенотипическое и морфологическое исследование бластов в костном мозге и периферической крови.
Ремиссию заболевания можно достичь посредством проведения высокодозной полихимиотерапии с последующей трансплантацией гемопоэтических стволовых клеток от HLA-геноидентичного родственного или альтернативного (неродственного, гаплоидентичного) донора у пациентов группы высокого риска рецидива. Благодаря адаптивным протоколам удается достичь ремиссии у 90% детей.
Хронические миелолейкоз
Хронический лейкоз – это вариант гемобластоза, субстратом которого являются созревающие клетки. У детей встречается только хронический миелолейкоз, который характеризуется пролиферацией гранулоцитарного ростка, гиперплазией миелоидной ткани, миелоидной метаплазией кроветворных органов, ассоциированной с хромосомной транслокацией t(9;22)(q34;q11), в результате которой образуется химерный онкоген BCR-ABL.
В течение хронического миелолейкоза выделяют три фазы:
В дебюте заболевание трудно диагностировать, поскольку основные симптомы обусловлены общим опухолевым симптомокомплексом и носят преходящий характер. Наиболее частые симптомы, присоединяющиеся позднее – гепатомегалия и спленомегалия. Нарастающая интоксикация приводит к появлению слабости, утомляемости, повышению температуры тела, болям в костях.
В периферической крови отмечается гиперлейкоцитоз (до 200 – 300 х 10 9 /л и более) с увеличением содержания гранулоцитов до 95% и преобладанием незрелых клеток гранулоцитарного ряда: промиелоцитов, миелоцитов, метамиелоцитов, миелобластов, базофилов (до 10%) и эозинофилов (до 5%). Характерна анемия и повышение СОЭ. Уровень тромбоцитов преимущественно в норме, однако может отмечаться гипертромбоцитоз (до 600 х 10 9 /л и более).
В пунктате костного мозга отмечается увеличение числа миелокариоцитов за счет пролиферирующего пула клеток гранулоцитарного ряда с увеличением базофилов и эозинофилов. Позднее отмечается угнетение эритронормобластического и мегакариоцитарного ростков кроветворения.
Основным средством терапии и стандартом лечения хронического миелолейкоза в настоящее время является применение ингибиторов тирозинкиназы (ИТК). Данные препараты имеют механизм таргетного (целенаправленного) воздействия на BCR-ABL-положительные опухолевые клетки и должны назначаться всем пациентам после подтверждения диагноза. Для оценки эффективности и переносимости терапии ИТК рекомендуется регулярный мониторинг гематологических, цитогенетических и молекулярно-генетических и других показателей у пациента.
Список литературы
Авторская публикация:
Кулева С.А.
Заведующая отделением, врач-детский онколог, ведущий научный сотрудник, профессор НМИЦ онкологии им. Н.Н. Петрова
Иванова Светлана Вячеславовна
Врач-детский онколог, научный сотрудник, кандидат наук НМИЦ онкологии им Н.Н. Петрова