что такое дериват хромосомы
Идентификация кольцевой и маркерной хромосом при типичных формах дисгенезии гонад
| Нарушения половой дифференцировки представляют собой обширную группу заболеваний с высокой клинической вариабельностью и генетической гетерогенностью. Характерными признаками этих заболеваний являются количественные и структурные аберрации половых хромосом, а также несоответствие фенотипа генетическому полу (набору половых хромосом) индивида. Наиболее распространенной патологией среди этой группы заболеваний является типичная форма дисгенезии гонад, или синдром Шерешевского-Тернера. Частота рождения больных детей составляет 1:1500 девочек [1]. |
Несмотря на разнообразие генотипов, подавляющее большинство больных с синдромом Шерешевского-Тернера причисляют к лицам женского пола, в связи с тем, что из всех больных, имеющих хромосому Y в кариотипе, женский пол присваивается в 60% [2].
Наличие хромосомы Y в кариотипе у таких «девочек» часто сопровождается малигнизацией гонад, что требует высокой онкологической настороженности. Установлено, что опухоли дисгенетичных гонад у этих больных до 16 лет выявляются в 10,2% случаев; во второй и третей декадах жизни процент этот возрастает до 30-35 [3]. Однако ряд авторов обнаружили возникновение гонадобластом и дисгермином в раннем детском возрасте, что свидетельствовало о перерождении гонад еще в период внутриутробного развития. В связи с этим обнаружение хромосомы Y в кариотипе имеет важное значение для лечения и прогноза заболевания.
По данным Saenger (1993) [цит. по 1], хромосома Y в кариотипе обнаруживается только у 6% больных с синдромом Шерешевского-Тернера при использовании дифференцированной окраски. В ряде случаев присутствие в кариотипе больных отдельных фрагментов хромосом не позволяет определить их принадлежность к хромосомам Х или Y. Поэтому в последнее время для идентификации этих фрагментов стали применять молекулярно цитогенетический метод FISH-анализа, в основе которого лежит гибридизация in situ.
В настоящей статье представлены два клинических наблюдения больных с типичной формой дисгенезии гонад и мозаичными вариантами кариотипа. В первом случае у пациентки в кариотипе был обнаружен клон с кольцевой хромосомой. В кариотипе второй пациентки присутствовала маркерная хромосома небольшого размера. Кольцевую и маркерную хромосому невозможно было идентифицировать цитогенетическим методом с применением дифференцированной окраски. У обеих больных в кариотипе доминирующим клеточным клоном был клон 45,Х.
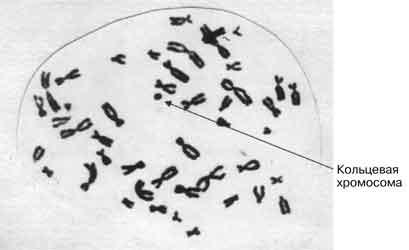 |
| Рис. 1. Кариотип пациентки (наблюдение 1) |
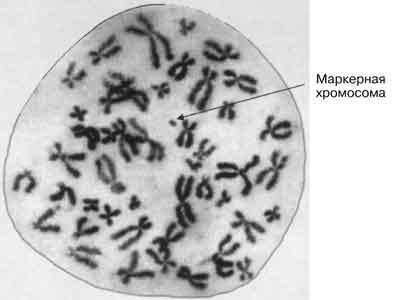 |
| Рис. 2. Кариотип пациентки (наблюдение 2) |
Для идентификации кольцевой и маркерной хромосом был использован метод флюоресцентной гибридизации in situ (FISH) модифицированный Ю.Б. Юровым и С.Г. Ворсановой [4].
Принцип метода основан на специфической гибридизации флюоресцентно меченных зондов с определенными участками хромосом (обычно это расположенные в районе центромеры хромосомоспецифические альфоидные повторы). По флюоресценции зондов можно быстро детектировать число копий хромосомы и структурные перестройки в интерфазных ядрах. Этот метод позволял избежать ошибок в определении пола при наличии маркерной хромосомы Y [5].
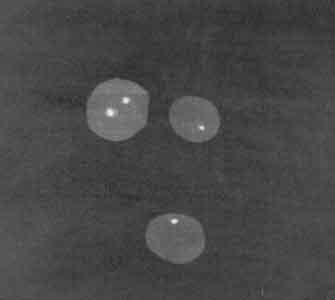 |
| Рис. 3. FISH-анализ лимфоцитов пациентки (наблюдение 1) |
Анализ результатов исследования лимфоцитов больной методом FISH показал, что кольцевая хромосома является дериватом хромосомы Х. Таким образом, кариотип больной был 45,Х/46,Хr(X).
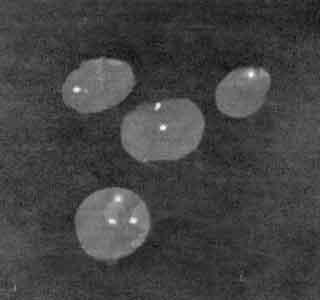 |
| Рис. 4. FISH-анализ лимфоцитов пациентки (наблюдение 2) |
Флюоресцентная гибридизация, позволяющая исследовать не только метафазные хромосомы, но и интерфазные ядра, является методом быстрой цитогенетической диагностики.
Использование флюоресцентной гибридизации при анализе кариотипа у больных с нарушением половой дифференцировки продемонстрировало преимущество метода, так как способствовало идентифицированию комплекса половых хромосом в клеточном клоне, где одна из хромосом была представлена мелким фрагментом.
Ж.И. Глинкина, И.Г. Дзенис, Б.В. Леонов, Г.И. Мушакова, В.А. Бахарев
Научный центр акушерства, гинекологии и перинатологии РАМН, Москва
Полный текст:
Аннотация
Ключевые слова
Об авторах
Список литературы
1. Захаров АФ, Бенюш ВА, Кулешов НП, Барановская ЛИ. Хромосомы человека (атлас). М.: Медицина. 1982; 263 с.
2. Goodpasture C, Bloom SE Visualization of nucleolar organizer regions. III. Mammalian chromosomes using silver staining. Chromosoma. 1975;53:37-50.
3. Баранов ВС, Кузнецова ТВ. Цитогенетика эмбрионального развития. СПб: Издательство Н-Л. 2007; 640 с.
4. Henegariu О, Heerema N, Wright l, Bray-Ward P et al. Improvements in cytogenetic slide preparation: controlled chromosome spreading, chemical aging and gradual denaturing. Cytometry. 2001;43:101-109.
5. Rubtsov N, Karamysheva T, Babochkina T et. al. A new simple version of chromosome microdissection tested by probe generation for 24-multi-color FISH, multi-color banding (MCB), ZOO-FISH and in clinical diagnostics. MedGen. 2000;12:65.
6. Карамышева ТВ, Матвеева ВГ, Шорина АР, Рубцов НБ. Клинический и молекулярно-цитогенетический анализ редкого случая мозаицизма по частичной моносомии 3p и частичной трисомии 10q у человека. Генетика. 2001;37(3):1-6.
7. Telenius H, Carter NP, Bebb CE. Degenerate oligonucleotide-primed PCR: general amplification of target DNA by single degenerate primer. Genomics. 1992;13:718-725.
8. Lichter P, Cremer T, Borden J, Manuelidis L, Ward DC. Delineation of individual human chromosomes in metaphase and interphase cells by in situ supression hybridization using recombinant DNA libraries. Hum Genet. 1988;80:224-234.
9. Shaffer LG, Slovak ML, Campbell LJ, editors. An International System for Human Cytogenetic Nomenclature: Recommendations of the International Standing Committee on Human Cytogenetic Nomenclature. Basel, Switzerland: Karger. 2009.
10. Ворсанова СГ, Юров ЮБ, Чернышов ВН. Медицинская цитогенетика. М: «Медпрактика-М». 2006;300 с.
11. Wilson MG, Towner JW, Coffin GS et al. Genetic and clinical studies in 13 patients with the Wolf-Hirschhorn syndrome del(4p). Hum. Genet. 1981;59:297-307.
13. Todd ES, Weinberg SM, Berry-Kravis EM et al. Facial Phenotype in Children and Young Adults with PHOX2B-Determined Congenital Central Hypoventilation Syndrome: Quantitative Pattern of Dys-morphology. Pediatric Research. 2006;59:39-45.
14. Nakayama T, Saitsu H, Endo W et al. RBPJ is disrupted in a case of proximal 4p deletion syndrome with epilepsy. Brain. Dev. 2014 Jun;36(6):532-536.
15. Mоller RS, Hansen CP, Jackson GD et al. Interstitial deletion of chromosome 4p associated with mild mental retardation, epilepsy and polymicrogyria of the left temporal lobe. Clinical Genetics. 2007;72(6):593-598.
16. Blennow E, Bui TH, Kristoffersson U et al. Swedish survey on extra structurally abnormal chromosomes in 39105 consecutive prenatal diagnoses: prevalence and characterization by fluorescence in situ hybridization. Prenat. Diagn. 1994;14(11):1019-1028.
17. Рубцов НБ, Карамышева ТВ, Гайнер ТА, Шкляева ОА. Анализ маркерных хромосом: ДНК пробы для оценки возможного клинического значения маркерной хромосомы. Медицинская генетика. 2003;2(12):520-527.
18. Wandstrat AE, Schwartz S. Isolation and molecular analysis of inv dup(15) and construction of a physical map of a common breakpoint in order to elucidate their mechanism of formation. Chromosoma. 2000;109(7):498-505.
19. Webb T, Hardy CA, King MA et al. A clinical, cytogenetic and molecular study of ten probands with supernumerary inv dup (15) marker chromosomes. Clin. Genet. 1998; 53(1):34-43.
20. Kariya S, Aoji K, Akagi H et al. A terminal deletion of the short arm of chromosome 3: karyotype 46, XY, del (3) (p25-pter); a case report and literature review. Int J Pediatr Otorhinolaryngol. 2000;56(1):71-8.
Для цитирования:
For citation:
Gayner T.A., Karamysheva T.V., Karimova O.G., Koren O.L., Shloma V.V., Shorina A.R., Bogomolov A.G., Rubtsov N.B. Сomprehensive chromosomal pathology diagnostic of derivative of the 4 chromosome and the small supernumerary marker chromosome. Medical Genetics. 2017;16(12):9-17. (In Russ.)
Хромосомные транслокации
Наша команда профессионалов ответит на ваши вопросы
Данная брошюра содержит информацию о том, что такое хромосомные транслокации, как они могут наследоваться и какие проблемы они могут вызывать. Данная брошюра не может заменить Ваше общение с врачом, однако она может помочь Вам при обсуждении интересующих Вас вопросов.
Что такое хромосомные транслокации?
Для того, чтобы понять, что такое хромосомные транслокации, вначале будет полезно узнать, что такое гены и хромосомы.
Что такое гены и хромосомы?
Наше тело состоит из миллионов клеток. Большинство клеток содержат полный набор генов. У человека тысячи генов. Гены можно сравнить с инструкциями, которые используются для контроля роста и согласованной работы всего организма. Гены отвечают за множество признаков нашего организма, например, за цвет глаз, группу крови или рост.
Гены расположены на нитевидных структурах, называемых хромосомами. Как правило, в большинстве клеток организма содержится по 46 хромосом. Хромосомы передаются нам от родителей – 23 от мамы, и 23 от папы, поэтому мы часто похожи на своих родителей. Таким образом, у нас два набора по 23 хромосомы, или 23 пары хромосом. Так как на хромосомах расположены гены, мы наследуем по две копии каждого гена, по одной копии от каждого из родителей. Хромосомы (следовательно, и гены) состоят из химического соединения, называемого ДНК.
Рисунок 1: Гены, хромосомы и ДНК
Рисунок 2: 23 пары хромосом, распределенные по размеру; хромосома под номером 1 – самая большая. Две последние хромосомы – половые.
Правильный хромосомный набор является очень важным для нормального развития человека. Это связано с тем, что гены, которые дают «инструкции к действиям» клеткам нашего организма, находятся на хромосомах. Любое изменение количества, размера или структуры наших хромосом может привести к трудностям в обучении, задержке развития и другим проблемам здоровья ребенка.
Что такое транслокация?
Транслокация означает, что существует какая-либо необычная структура хромосом. Причины для этого могут быть разные:
Существует два основных типа транслокаций: реципрокная транслокация и робертсоновская траслокация.
Реципрокные транслокации
Реципрокные транслокации возникают в том случае, если два фрагмента из двух разных хромосом отрываются и меняются местами
Рисунок 3: Как возникает реципрокная транслокация
две нормальные хромосом из пары части двух хромосом отрываются и снова прикрепляются к другим хромосомах
Робертсоновские транслокации
Робертсоновские транслокации возникают в том случае, когда одна хромосома соединяется с другой. На Рисунке 4 показана робертсоновская транслокация, в которую вовлечены две хромосомы
Рисунок 4: Как возникает робертсоновская транслокация
две нормальные хромосом из пары Робертсоновская транслокация: хромосома одной пары оказываются прикрепленной к хромосоме из другой пары
Почему возникают транслокации?
Несмотря на то, что транслокации встречаются довольно часто (примерно у 1 человека из 500), причины их возникновения остаются неясными. Мы знаем, что хромосомы, по-видимому, могут разрываться и восстанавливаться во время процесса созревания сперматозоида или яйцеклетки, или при оплодотворении, и лишь в некоторых случаях это приводит к проблемам. Мы не можем контролировать эти изменения.
Когда это может приводить к проблемам?
В обоих рассмотренных нами примерах хромосомные перестройки происходили таким образом, что общее количество хромосомного материала не менялось. Такие перестройки называются сбалансированными транслокациями.
Как правило, человек, имеющий сбалансированную транслокацию, не страдает от этого, и часто даже не подозревает, что в его (ее) хромосомах есть перестройка. И важным это может оказаться только в случае, когда у него (или у нее) появляется ребенок. Это связано с тем, что у ребенка может возникнуть несбалансированная транслокация.
Несбалансированные транслокации
Если один из родителей является носителем сбалансированной транслокации, существует вероятность, что у ребенка возникнет несбалансированная транслокация, при которой присутствует лишний фрагмент одной хромосомы и/или потеря части материала другой хромосомы.
Часто бывает так, что ребенок рождается с транслокацией, несмотря на то, что у обоих родителей нормальные хромосомы. Это называется «вновь возникшей» перестройкой, или перестройкой «de novo» (от латинского слова). В этом случае вероятность повторного рождения ребенка с транслокацией у этих родителей крайне мала.
Ребенок, имеющий несбалансированную транслокацию, может иметь трудности в обучении, задержку развития и другие проблемы со здоровьем. Выраженность проявлений зависит от того, какие участки хромосомы оказались вовлеченными в перестройку, и какой материал хромосомы присутствует в избытке, или отсутствует, так как некоторые районы хромосомы важнее других.
Если у родителя есть сбалансированная транслокация, всегда ли она передается ребенку?
Таким образом, у носителя сбалансированной транслокации могут рождаться здоровые дети, и во многих случаях происходит именно так. Однако, для носителя сбалансированной транслокации существует повышенный риск рождения ребенка с определенной степенью задержки развития, при этом тяжесть проявлений зависит от конкретного типа транслокации.
Диагностика хромосомных транслокаций
Возможно проведение генетического анализа для выявления носительства транслокации. Берется образец крови, и клетки крови исследуют в специализированной лаборатории для выявления хромосомных транслокаций. Такой анализ называется кариотипированием. Также возможно проведение теста во время беременности для выявления хромосомных транслокаций. Это называется пренатальной диагностикой, и этот вопрос следует обсудить с врачом-генетиком. Более подробная информация на эту тему представлена в брошюрах «Биопсия ворсин хориона» и «Амниоцентез».
Какое отношение это имеет к другим членам семьи?
Если у одного из членов семьи обнаружена транслокация, возможно, Вы захотите обсудить этот вопрос с другими членами семьи. Это даст возможность другим родственникам, при желании, пройти обследование (анализ хромосом в клетках крови) для определения носительства транслокации. Это может быть особенно важно для родственников, уже имеющих детей или планирующих беременность. Если они не являются носителями транслокации, они не могут передать ее своим детям. Если же они являются носителями, то им могут предложить пройти обследование во время беременности для анализа хромосом плода.
Некоторым людям сложно обсуждать проблемы, связанные с хромосомной перестройкой, с членами семьи. Они могут бояться причинить беспокойство членам семьи. В некоторых семьях люди из-за этого испытывают сложности в общении и теряют взаимопонимание с родственниками. Врачи-генетики, как правило, имеют большой опыт в решении подобных семейных ситуаций и могут помочь Вам в обсуждении проблемы с другими членами семьи.
Статьи
Классификация хромосомных болезней
Хромосомные болезни появляются вследствие повреждений ге¬нома, возникающих при созревании гамет, в процессе оплодотворе¬ния или на ранних стадиях дробления зиготы. Все хромосомные болезни могут быть разделены на 3 большие группы:
1) связанные с нарушением плоидности;
2) обусловленные нарушением числа хро¬мосом;
3) связанные сизменением структуры хромосом.
Аномалии хромосом, связанные с нарушением плоидности, пред¬ставлены триплоидией и тетраплоидией, которыевстречаются пре¬имущественно в материале спонтанных абортусов. Отмечены лишь единичные случаи рождения детей-триплоидов с тяжелыми МВПР, несовместимыми с нормальной жизнедеятельностью. Триплоидия может возникать каквследствие дигении (оплодотворение дипло¬идной яйцеклетки гаплоидным сперматозоидом), так и вследствие диандрии (обратный вариант) и диспермии (оплодотворение гап¬лоидной яйцеклетки двумя сперматозоидами).
Хромосомные болезни, связанные с нарушением структуры хро¬мосом, представляют большую группу синдромов частичных моно- или трисомии. Как правило, они возникают в результате структурных перестроек хромосом, имеющихся вполовых клетках родите¬лей, которые вследствие нарушения процессов рекомбинации в мейозе приводят к утрате или избытку фрагментов хромосом, вовлечен¬ных в перестройку. Частичные моно- или трисомии известны практи¬чески повсем хромосомам, но лишь некоторые из них формируют четко диагностируемые клинические синдромы. Фенотипические про-явления этих синдромов более полиморфны, чем синдромов целых моно- и трисомии. Отчасти этосвязано с тем, что размеры фрагмен¬тов хромосом и, следовательно, их генный состав, могут варьиро¬вать в каждом отдельном случае, а также тем, что при наличии хро¬мосомной транслокации у одного из родителей частичная трисомия поодной хромосоме у ребенка может сочетаться с частичной моно¬сомией по другой.
Клинико-цитогенетическая характеристика синдромов, связанных с числовыми аномалиями хромосом
Синдром трисомии хромосомы 8. Впервые описан в 1962 году. Популяционная частота 1 на 50000. Возникает врезультате нерас¬хождения хромосом на ранних стадиях бластулы, кроме редких слу¬чаев мутаций de novo в гаметогенезе. Цитогенетически выявляются как полные, так и мозаичные формы, которые составляют до 90% всех случаев. Различий поклинической картине таких форм нет. Не обнаружено корреляции между тяжестью заболевания и долей мо¬заичного клона.
Основными диагностическими признаками данного синдрома яв¬ляются: макроцефалия, микрогнатия, вывернутая нижняя губа, мас¬сивный выступающий лоб, широкая спинка носа, высокое акровидное небо, большие оттопыренные уши с выступающим противозавитком. Кроме того, имеются аномалии скелета, выражающиеся в добавочных ребрах и позвонках, закрытые спинномозговые грыжи в шейном и грудном отделах позвоночника, аплазия и гипоплазия надколенника, короткая шея. Имеются множественные контрактуры су¬ставов, клинодактилия, камптодактилия. Распространены пороки мо-чевой системы, особенно гидронефроз. Диагностируют пороки серд¬ца, особенно дефекты перегородок и крупных сосудов. Интеллект у больных снижен, отмечена задержка психомоторного и речевого раз-вития. Прогноз физического, психического развития и жизни небла¬гоприятный, хотя и отмечены пациенты в возрасте 17 лет.
Синдром трисомии хромосомы 9. Описан в 1970 году. В осно¬ве этиологии лежит нерасхождение хромосом на раннихстадиях бла¬стулы, кроме редких случаев мутаций de novo в гаметогенезе. Цито-генетически отмечены полные формытрисомии и мозаики (50%). Му¬тации de novo составляют 1/3 всех описанных случаев. Кроме полных аутосомных трисомийхромосомы 9 выявлены также делеции дистального участка ее длинного плеча. Транслокационные варианты встречаются редко.
Основными диагностическими признаками синдрома трисомий 9 являются: микроцефалия (долихоцефалия), глубокопосаженные гла¬за, высокий лоб, широкая переносица, бульбообразный нос, высо¬кое небо, часто с расщелиной, микроретрогнатия. Ушные раковины деформированы и низко посажены, отмечается короткая шея с низ¬кой линией роста волос. Наблюдаются аномалии развития опорно-двигательного аппарата, включающие дисплазию тазобедренного сустава, вывих локтевого или коленного суставов, аномалии ребер. У мальчиков выражен крипторхизм и микропенис. Из патологии внут¬ренних органов, в основном, отмечена патология сердечно-сосудис¬той системы, почек, комплексные порокижелудочно-кишечного трак¬та. Прогноз жизни неблагоприятный. Большинство больных погиба¬ют в первые 4 месяца жизни, особенно от респираторных инфекций.
Синдром Патау (трисомия по хромосоме 13). Впервые опи¬сан в 1960 году. Популяционная частота 1 на 7800. Цитогенетические варианты могут быть различны: целая трисомия 13 (нерасхождение хромосом в мейозе, в 80% случаев уматери), транслокационный ва¬риант (робертсоновские транслокации D/13 и G/13), мозаичные фор¬мы, дополнительная кольцевая хромосома 13, изохромосомы.
Для синдрома Патау характерны следующие диагностические при¬знаки: микроцефалия, расщелина верхней губы и неба, низко поса¬женные деформированные ушные раковины, микрогения, полидак-тилия, флексорное положение пальцев рук, выпуклые ногти, попе¬речная ладонная складка, стопа-качалка. Из пороков внутренних ор¬ганов отмечены врожденные пороки сердца (дефекты перегородок и крупных сосудов), незавершенный поворот кишечника, дивертикул Меккеля, поликистоз почек, удвоение мочеточника. Наблюдается крипторхизм, гипоплазия наружных половых органов, удвоениемат¬ки и влагалища. Глубокая идиотия. Дети, в основном, умирают в воз¬расте до 1 года, чаще в первые 2-3 месяца жизни.
Синдром трисомий хромосомы 14. Описан в 1975 году. Ос¬новными цитогенетическими формами являются мозаики. Кроме того, часто встречаются транслокационные варианты, включающие робертсоновские транслокации 14/14.
Основными диагностическими признаками синдрома являются: микроцефалия, асимметрия лица, высокий и выступающийлоб, нос короткий и бульбообразный, губы полные, высокое небо, часто с расщелинами, микроретрогнатия. Ушные раковины низко посажены, с маленькими мочками. Короткая шея, узкая и деформированная груд¬ная клетка, крипторхизм, гипогонадизм и маленький пенис. Из поро¬ков внутренних органов выражены пороки сердечно-сосудистой сис¬темы, смещение почки и почечная недостаточность, астма и дерма¬тозы. Прогноз жизни неблагоприятный, однако отмечены больные в возрасте 13,5 лет.
Синдром Эдвардса (трисомия по хромосоме 18). Описан в 1960 году. Популяционная частота составляет 1 на 6500. Цитогенетически в большинстве случаев представлен целой трисомиеи 18 (гаметическая мутация одного из родителей, чаще по материнской линии). Кроме того, встречаются и мозаичные формы, а транслокации наблюдаются очень редко. Критическим сегментом, ответственным за формирование основных признаков синдрома, является сег¬мент 18q11. Клинических различий между цитогенетическими фор¬мами не обнаружено.
Основными диагностическими признаками синдрома являются: типичное плоское лицо, монголоидный разрез глаз, эпикант, откры¬тый рот, макроглоссия и аномалии зубов, короткий нос и плоская пе-реносица, избыток кожи на шее, короткие конечности, поперечная четырех-пальцевая ладонная складка (обезьянья борозда). Из по¬роков внутренних органов часто отмечаются врожденные пороки сер¬дца и желудочно-кишечного тракта, которые и определяют продолжительность жизни больных. Умственная отсталость обычно сред¬ней степени тяжести. Дети с синдромом Дауна часто ласковые и при-вязчивые, послушные и внимательные.
Клинико-цитогенетическая характеристика синдромов, связанных с аномалиями половых хромосом
Синдром Шерешевского-Тернера (моносомия Х-хромосомы).
Это единственная форма моносомии у человека, которая может быть выявлена у живорожденных. Популяционная частота 1 на 3000 ново¬рожденных. Кроме простой моносомии по X хромосоме, составляю¬щей 50%, встречаются мозаичныеформы, делеции длинного и ко¬роткого плеча X хромосомы, изо-Х-хромосомы, а также кольцевые X хромосомы. Интересноотметить, что мозаицизм 45,X/46,XY состав¬ляет 2-5% от всех больных с этим синдромом и характеризуется широким диапазоном признаков: от типичного синдрома Шерешевс¬кого-Тернера до нормального мужского фенотипа Основными клиническими признаками заболевания являются: на¬низм, крыловидные кожные складки на шее, короткая шея с низкой линией роста волос, отеки кистей и стоп новорожденных, бочкооб¬разная грудная клетка, вальгусная девиация коленных и локтевых суставов. У больных выявляются первичная аменорея и половой ин¬фантилизм, бесплодие, гиперпигментациякожи, снижение зрения и слуха. Часто встречаются врожденные пороки сердца и почек. Ин¬теллектуальное развитие в пределах нормы.
Синдром Клайнфельтера. Описан в 1942 году. Популяционная частота 1 на 1000 мальчиков. Цитогенетические вариантысиндрома могут быть различны: 47.XXY; 48.XXYY; 48.XXXY; 49.XXXXY. Отме-чены как полные, так и мозаичные формы. Больные высокого роста с непропорционально длинными конечностями, выраженной гинеко¬мастией и оволосением поженскому типу. В детстве отличаются хруп¬ким телосложением, а после 40 лет страдают ожирением. Важными диагностическими признаками являются гипогонадизм и гипогенитализм. Характерно снижение полового влечения, импотенция и бес-плодие. Коэффициент интеллекта ниже 80.
Синдром полисомии Y-хромосомы. Популяционная частота 1 на 1000 мальчиков. Цитогенетически отмечены полные имозаичные формы. Большинство индивидов по физическому и умственному развитию не отличается от здоровых. Обычноони высокого роста и в 50% случаев могут иметь нормальное потомство. При данном синд¬роме имеются некоторые особенности поведения: склонность к аг¬рессии, асоциальному поведению, гомосексуализму.
Клинико-цитогенетическая характеристика синдромов, связанных со структурными перестройками хромосом
Синдром дупликации короткого плеча хромосомы 9 (синдром 9р+). Описан в 1970 году. Это наиболее частая формачастич¬ных трисомий у человека. Цитогенетика синдрома разнообразна: простые дупликации, изохромосомы 9р, несбалансированные транс¬локации, но во всех случаях имеется тройной набор генов части ко¬роткого плеча хромосомы 9. Диагностическими признаками заболе¬вания являются: микробрахицефалия, антимонголоидный разрез глаз, гипертелоризм, анофтальм, широкий и округлый кончик носа, выступающая верхняя губа и верхняя челюсть. Ушные раковины низко расположены с аномальным противозавитком и противокозелком, узкий слуховой канал. Кроме того имеется короткая шеяс низкой линией роста волос, поперечная ладонная складка, рентгенологи¬чески отмечается задержка костного возраста. Убольных обна¬руживают патологию почек. Олигофрения. Прогноз жизни благопри¬ятный, больные доживают до пожилого возраста 25%
Синдром трисомии длинного плеча 14-й хромосомы (синд¬ром 14q+). Описан в 1970 году. Цитогенетически проявляетсякак дупликация участка хромосомы 14, имеются транслокационные фор-мы и изохромосома 14 по длинному плечу. Типичными признаками заболевания являются: микроцефалия, луковицеобразный нос, тон¬кая верхняя губа, микростомия, опущенные углы рта, низкорасполо¬женные ротированные назад ушные раковины, короткая шея. Харак¬терно неправильное расположение пальцев на руке, клинодактилия, косолапость. Из внутренних пороков описана патология сердечно-¬сосудистой системы. Дети резко отстают в психомоторном и физи¬ческом развитии.
Синдром кольцевой хромосомы 18. Описан в 1962 году. Цито¬генетически представлен кольцевой хромосомой 18, возможны мо¬заичные варианты. Основные клинические признаки заболевания: микроцефалия, гипертелоризм, страбизм, птоз, нистагм, колобома радужной оболочки глаза, уплощенная спинка носа, рот «карпа», тон¬кая верхняя губа, высокое небо (часто с расщелиной). Патология внутренних органов встречается редко. Умственная отсталость как правило тяжелая ипроявляется у 100% больных.
Синдром моносомии короткого плеча 18 хромосомы (синд¬ром 18р-). Описан в 1963 году. Цитогенетически характеризуетсяде¬лециеи короткого плеча 18 хромосомы. Отмечается низкая масса тела при рождении. Основными диагностическими признаками синдрома являются: мышечная гипотония, умеренная микроцефалия, высокий лоб, гипертелоризм, эпикант, птоз, широкая уплощенная переноси¬ца, микрогения, широкий рот с опущенными уголками губ и выпячиванием верхней губы в виде «полицейской фуражки», аномалии зу¬бов, крупные деформированные ушные раковины. Часто встречают¬ся короткая шея, вдавленная грудная клетка, пупочная и паховая грыжы. Скелетные аномалии могут быть представленывывихом бед¬ра, деформацией локтевого сустава. Из пороков внутренних органов встречается ВПС. Выявляется также дефицит IgA. Все больные от¬стают в психомоторном развитии, во многих случаях отсутствует фразовая речь до 7-9 лет.
Синдром делеции длинного плеча 21 хромосомы (синдром 21 q-). Выделен в отдельную нозологическую группу в 1970 году. Ци¬тогенетически характеризуется частичной делециеи длинного плеча хромосомы 21, а также кольцевой хромосомой. Отмечены моза¬ичные формы этих хромосомных нарушений. Диагностическими при¬знаками заболевания являются: низкая масса тела при рождении, микроцефалия, антимонголоидный разрез глаз, эпикант, широкая переносица, большиенизко посаженные деформированные уши с расширенным слуховым каналом, микрогнатия. К основным призна¬камотносятся также сколиоз, клинодактилия, паховая грыжа, косо¬лапость и крипторхизм. Их пороков внутренних органов наблюдают¬ся пороки сердца и патология почек (гидронефроз, удвоение почеч¬ных лоханок). Отмечена задержка психомоторного развития. При грубых пороках развития дети умирают в первые недели жизни, хотя описаны больные в возрасте 50 лет.
Синдром кольцевой хромосомы 22. Выделен в самостоятель¬ный синдром в 1972 году. Цитогенетические варианты могутбыть раз¬личны: кольцевая хромосома 22, делеции длинного плеча этой хро¬мосомы и мозаичные варианты. В 90% случаев данные хромосом¬ные нарушения являются мутациями de novo. Основными диагнос¬тическими признаками заболеванияя вляются: микроцефалия, эпикант, гипертелоризм, крупные выступающие глаза («глаза лани»), расщелина язычка инеба, густые брови и ресницы. Кроме того, от¬мечается дисплазия тазобедренных суставов, клинодактилия и син-дактилия. Пороки внутренних органов не характерны. Умственная от¬сталость проявляется как легкой, так и выраженной олигофренией. Больные легко возбудимы, отмечается частая смена настроения, на-рушение координации, а также грубое недоразвитие речи, вплоть до ее отсутствия.
Клинико-цитогенетическая характеристика синдромов и злокачественных новообразований, вязанных с микроструктурными аномалиями хромосом
В последнее время клинико-цитогенетические исследования ста¬ли опираться на высокоразрешающие методыхромосомного анали¬за, позволившее подтвердить предположение о существовании мик-рохромосомных мутаций, выявление которых находится на грани воз¬можностей светового микроскопа. Используя стандартные цитогенетические методы можно достичь визуального разрешения хромосом с числом сегментов не более 400, а применение методов прометафазного анализа, предложенного Юнисом в 1976 году, удается полу¬чать хромосомы с числом сегментов до 550-850. Незначительные нарушения в структуре хромосом могут быть выявлены с помощью этихметодов хромосомного анализа не только среди больных с МВПР, но и при некоторых неизвестных менделирующих синдромах. Отли-чительная черта этих синдромов состоит в том, что клинически они были описаны задолго до того, как была выявлена их хромосомная этиология. Нет никаких сомнений в том, что еще некоторые синдро¬мы, рассматриваемые пока в группе синдромов с неясной этиологи¬ей, могут оказаться хромосомными. На сегодняшний день выяснена этиология около 20 нозологических форм, при которых выявлены мик-роструктурные хромосомные нарушения. Показано, что микрострук¬турные аномалии хромосом сопровождают не только синдромы МВПР, но и различные гиперпластические процессы, включая и зло-качественные образования. Большинство синдромов, связанных с микроаномалиями хромосом, встречается редко-1 случай на 50000-100000 новорожденных).
Синдром Лангера-Гидиона (трихо-рино-фалангиальный синдром). Особый интерес к этому синдрому проявился в 1980 году, когда была выяснена его хромосомная этиология, выражающаяся в микроделеции хромосомы длинного плеча хромосомы 8. Отмечены мозаичные формы синдрома.
Основными клиническими признаками заболевания являются: тонкие и редкие волосы, бульбообразныйнос, конические эпифизы фаланг пальцев, множественные хрящевые экзостозы. Кроме этих признаков больные имеют ряд микроаномалий: широкие редкие бро¬ви, глубоко посаженые глаза, макростомию, нарушение прорезыва¬ния и расположения зубов, микрогнатию, большие и низко располо¬женные ушные раковины. Множественные хрящевые экзостозы проявляются до 4-х лет и располагаются везде, где есть хрящи, причем их рост усиливается в периоды активного роста организма и прекра¬щается в возрасте 18-20 лет. У новорожденных бывает избыточная кожа. Отмечается умственная отсталость различной степени, задер¬жка речевого развития.
Синдром Видемана-Беквита. Цитогенетически характеризует¬ дупликацией участка короткого плеча 11 хромосомы-11р15. Основными диагностическими признаками заболевания являются: макроглоссия, макросомия с увеличением мышечной массы и подкожного жирового слоя, выступающий затылок и аномалии прикуса, связанные с гипоплазией верхней челюсти и относительной гиперплазией верхней. Характерным признаком является нали¬чие вертикальных бороздок на мочках ушей. Описана патология раз¬вития внутренних органов: дефекты межжелудочковых перегородок, добавочная селезенка, цитомегалия коры надпочечников, незавершенный поворот кишечника. Костный возраст опережает паспортный.
Психическое развитие соответствует возрасту, возможна умеренная умственная отсталость. В сегменте 11 р15 локализован ген «инсулиноподобного фактора роста II типа», при дупликации которого обра-зуются три его копии, что приводит к появлению таких признаков син¬дрома как большой вес, пупочная грыжа, увеличенный язык и т.д.
Синдром Прадера-Вилли. Описан в 1956 году. Популяционная частота 1 на 15 000. Встречается в основномспорадически, хотя описаны и семейные случаи с аутосомно-доминантным типом наследования. Основные диагностические признаки заболевания: слабое шевеление плода во II триместре беременности, мышечная гипотония, умственная отсталость, нанизм, ожирение, гипогонадотропный гипогонадизм, маленькие дистальные отделы конечностей (акромикрия).
Отмечаются также гипопигментация, страбизм, микрогнатия, доли¬хоцефалия, миндалевидный разрез глаз, крипторхизм игипоплазия полового члена у мальчиков.
Синдром Энгельмана (синдром «счастливой куклы»). Опи¬сан в 1965 году. Основными признаками заболевания являются: нео¬бычный и частый смех, специфичное лицо с гримасой улыбки, повторяющиеся кукольные стереотипные движения, отсутствие речи. Имеется выраженная умственная отсталость. Большинство больных имеют микроделецию 15q11-q13, но эта делеция всегда материнско¬го происхождения. Обнаружены также пациенты с типичным синдро¬мом Энгельмана безмикроделеции, у которых выявляется одноро¬дительская дисомия хромосомы 15 отцовскою происхождения.
Моногенные заболевания, проявляющиеся хромосомной нестабильностью



