что такое артерио венозная разница по кислороду
Что такое артерио венозная разница по кислороду
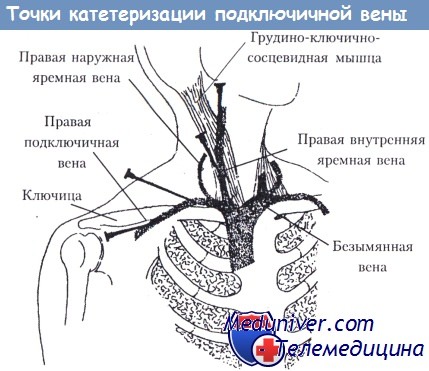
Советы по мониторингу центрального венозного давления (ЦВД)
1. Что такое центральное венозное давление (ЦВД)?
Центральное венозное давление, или давление в правом предсердии, — это давление, которое продвигает кровь в правый желудочек во время диастолы. Чем больше ЦВД, тем больше крови попадет в правый желудочек. Согласно закону Старлинга, при повышении конечного диастолического объема в систолу изгоняется большее количество крови. Следовательно, повышение ЦВД обычно сопровождается повышением сердечного выброса. В норме правый желудочек может адекватно наполняться при низком ЦВД (3-5 мм рт. ст.).
2. Каковы показания к установке центрального венозного катетера?
Более простое введение жидкостей или лекарственных препаратов, необходимость срочного ведения водителя ритма, отсутствие адекватной периферической вены, длительное введение гипертонических растворов (для полного парентерального питания) и антибиотиков.
3. Как измеряется ЦВД?
Катетер должен находиться в верхней полой вене или правом предсердии. Поскольку перепадом давления в верхней полой вене и правом предсердии можно пренебречь, оба положения катетера приемлемы (во всех внутригрудных венах давление почти одинаковое). Для проведения катетера в грудную клетку выполняется либо венесекция в локтевой ямке, либо чрескожная пункция подключичной или внутренней яремной вены. Для определения ЦВД (мм. вод. ст.) используется система передачи давления или система электронных датчиков.
4. Каковы противопоказания к чрескожной катетеризации подключичной или внутренней яремной вены?
Кровотечение и пневмоторакс. При катетеризации подключичной или внутренней яремной вены риск возникновения кровотечения достаточно низок, по все же существует. При нарушении свертывающей системы (любой этиологии) в сторону гипокоагуляции или при снижении количества тромбоцитов ниже 20 000 гораздо безопаснее катетеризировать центральную вену через веносекционпый доступ. При эмфизематозных легких, хронической обструктивной болезни легких и респираторном дистресс-синдроме больной может тяжело ответить на пневмоторакс.
При отсутствии нарушений со стороны свертывающей системы случайная пункция артерии переносится легко пациентами с нормальной коагуляцией.
5. В чем заключается методика чрескожной установки центрального венозного катетера или катетера Свана-Ганца?
1. Уложите больного в положение Тренделенбурга (со слегка опущенным головным концом).
2. Возьмите стерильный 10-мл шприц и “поисковую” 18G иглу. Введите иглу по среднеключичной линии в направлении надгрудинной ямки. Продвигайте иглу, придерживаясь нижней поверхности ключицы и осторожно подтягивая поршень па себя. Как только вы пунктируете вену, темная (не пульсирующая) кровь сразу попадет в шприц.
3. Проведите через иглу мягкий гибкий проводник.
4. Удалите иглу, оставив гибкий проводник в вене.
5. Проведите по проводнику в вену пластиковый расширитель. Удалите проводник.
6. Пластиковый катетер (или катетер Свана-Ганца) должен легко проходить внутри расширителя.
6. Как убедиться в правильном расположении центрального венозного катетера или катетера легочной артерии (Свана-Ганца)?
Нужно выполнить рентгенографию грудной клетки.
7. Для чего ставится катетер легочной артерии (Свана-Ганца)?
Для измерения: (1) давления (давления в левом желудочке); (2) потока (сердечного выброса) и (3) насыщения (системное потребление кислорода тканями).
8. На каких допусках основан мониторинг давления в легочной артерии?
1. Диастолическое давление в легочной артерии равно давлению заклинивания в легочных капиллярах.
2. Давление заклинивания в легочных капиллярах равно давлению в легочных венах.
3. Давление в легочных венах равно давлению в левом предсердии.
4. Давление в левом предсердии равно конечному диастолическому давлению в левом желудочке.
5. Конечное диастолическое давление в левом желудочке отражает конечный диастолический объем левого желудочка.
6. От конечного диастолического объема левого желудочка зависит ударный объем сердца.
7. Ударный объем сердца, умноженный на число сердечных сокращений, равен сердечному выбросу.
9. Велико ли количество этих допусков?
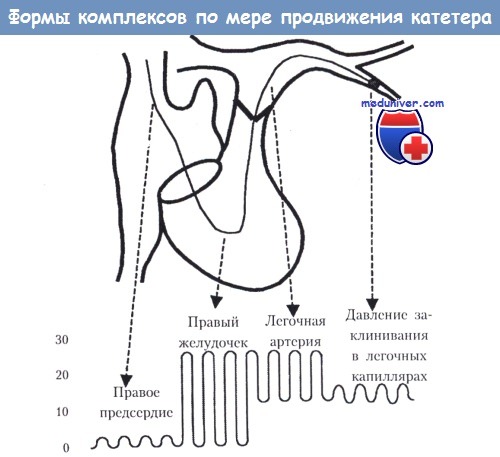
10. Как изменяется форма комплексов на кривой давления по мере продвижения катетера Свана-Ганца?
Характер комплексов, регистрируемых при измерении давления по мере продвижения катетера Свана-Ганца
11. Как определить величину сердечного выброса по термодилюции?
Введите 10 мл холодного (10°С) физиологического раствора в проксимальный порт катетера Свана-Ганца. Температурный зонд на конце катетера реагирует на протекающую мимо холодную кровь, а электроника преобразует полученный сигнал в величину кровяного потока (л/мин). Поскольку сердечный выброс меняется в зависимости от фазы дыхания, для стандартизации показателей инъекция должна совпадать с концом выдоха (функциональная остаточная емкость). Но даже в этом случае отклонение результатов ± 15%.
12. При каких обстоятельствах определение величины сердечного выброса но термодилюции может оказаться недостоверным?
Сброс крови слева направо увеличивает порцию холодного физиологического раствора и приводит к завышению величины сердечного выброса. Аналогично, завышение величины сердечного выброса наблюдается при недостаточности трикуспидального клапана. Чем выше сердечный выброс, тем менее достоверны электронные расчеты.
13. Как определить общее (периферическое) сосудистое сопротивление?
14. Какую информацию при шоке дает давление в правых или левых отделах сердца?
Периферическое сосудистое сопротивление — высокое. (При заболеваниях сердца ЦВД часто неправильно отражает давление в левом желудочке.) Диагноз подтверждается, если при увеличении объема циркулирующей крови и повышении давления в левом желудочке сердечный выброс увеличивается, артериальное давление нормализуется и периферическое сосудистое сопротивление снижается.
— Кардиогенный шок. Это шок, развивающийся, несмотря на адекватное давление в правых (ЦВД) и левых отделах сердца (ДЗЛК). Развивается при нормальном объеме циркулирующей крови и нарушении насосной функции сердца. Сердечный выброс — низкий. При высоком ОСС показано внутривенное введение добутамина со скоростью 5 мкг/кг/мипуту. Добутамин обладает положительным инотропным действием и снижает ОСС. При низком ОСС назначается адреналин со скоростью 0,05 мкг/кг/мипуту. Адреналин также обладает положительным ипотропным действием и повышает ОСС.
15. Что такое оксиметрический канал катетера Свана-Ганца?
Это капал с фиброоптическим датчиком па дистальном конце, непрерывно измеряющим HbО2 и насыщение кислородом [SО2 (%)]. При правильном расположении дистальный конец катетера находится в легочной артерии и определяет насыщение кислородом смешанной венозной крови (SvО2).
16. Каково значение сатурации (насыщения) кислородом смешанной венозной крови? В чем состоит различие между РаО2, сатурацией кислородом и общим содержанием кислорода в крови?
1. Общее содержание кислорода в артериальной крови (СаО2).
Это растворенный в крови кислород + кислород, связанный с гемоглобином. Растворенный кислород = 0,003 х РО2
Кислород, связанный с гемоглобином = 1,38 х Hb х SaО2
Например, если Hb = 12г%, РО2 = 60 мм рт. ст. и SaО2 = 90%, СаО2 = (0,003 х 60) + + (1,38 х 12 х0,90) = 15,08 мл О2/100 мл крови или 15,08 об.%. Обычно растворенный в крови кислород составляет лишь небольшую долю в СаО2 (в нашем примере 1%), поэтому его влияние на СаО2 в дальнейшем будет опускаться.
2. А-ВО2 (артериовенозная) разница по кислороду.
Знание того, как определяется содержание кислорода в крови, позволяет установить разницу содержания кислорода в артериальной (СаО2) и смешанной венозной крови (СвО2), или артериовенозную разницу по кислороду. Если известно насыщение HbО2 (SaО2), то арифметика становится элементарной:
Другими словами, каждые 100 мл крови за один цикл кровообращения доставляют тканям до 4,35 мл кислорода. В норме артериовенозная разница по кислороду составляет 3-5%.
Экспериментально доказано, что в покое организм поглощает кислород со скоростью 125 мл/мин/м2. Это позволяет с определенными допусками рассчитать потребление кислорода в минуту. По А-ВО2 можно определить вклад каждых 100 мл крови в общее потребление кислорода в минуту (ПО2). Таким образом, у мужчин с площадью поверхности тела 2 м2, минутное потребление кислорода (ПО2) составляет 250 мл. Если А-ВО2 = 4,35 мл (как в нашем примере), можно сказать, что каждую минуту 100 мл крови отдают 4,35 мл кислорода, чтобы удовлетворить П02 (250 мл).
Таким образом, для удовлетворения потребностей в кислороде 4,75 л крови должны совершить полный цикл кровообращения за 1 минуту. Приняв значение ПО2 за истинное и измерив А-ВО2, можно рассчитать величину сердечного выброса:
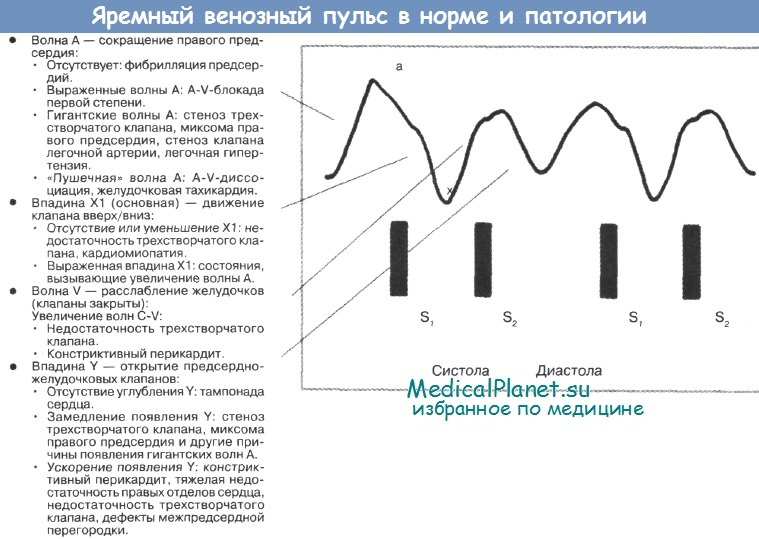
17. Каково значение насыщения кислородом смешанной венозной крови (SvО2)?
Если ваша голова еще не переполнена многочисленными допусками, давайте условимся еще о нескольких:
1. Допустим, что общее потребление кислорода (ПО2) стабильно (верно на коротких промежутках времени).
2. Допустим, что общее содержание кислорода в артериальной крови (СаО2) также стабильно (верно на коротких промежутках времени).
Когда сердечный выброс повышается (доставляя больше кислорода тканям при неизменных потребностях), на периферии поглощается меньшее количество кислорода, и объемное содержание кислорода в смешанной венозной крови повышается. Напротив, когда сердечный выброс уменьшается (доставляя па периферию меньше кислорода при неизменных потребностях), потребление кислорода тканями повышается, и насыщение кислородом смешанной венозной крови снижается.
Поэтому можно допустить (для короткого промежутка времени), что па насыщение кислородом смешанной венозной крови (SvО2) влияет только сердечный выброс. Для коротких промежутков времени также верны следующие выводы: зеленая зона SvO (стабильное состояние) = 75% или выше, желтая зона SvO (тяжелое состояние) = 55% или выше, красная зона SvO (критическое состояние) = 55% или ниже.
18. Когда оксиметрический катетер Свана-Ганца дает неточные показания?
Если катетер находится в легочной артерии достаточно долго (24-72 часа), его фиброоптический датчик может покрываться фибрином. В этих случаях интенсивность передачи света снижается, и результаты исследования становятся недостоверными. Современные оксимегрические катетеры Свана-Ганца определяют степень интенсивности света и подают сигнал тревоги, если оптика покрывается фибрином. При снижении гематокрига значение SvО2 также снижается, но эго явление нельзя считать артефактным (поскольку доставка кислорода действительно уменьшается).
Если А-ВО2 составляет 5 об%, а гемоглобин — 15 г%, то SvО2 = 75%. Однако при гемоглобине 7,5 г%, SvО2 = 50%. При стабильном сердечном выбросе величина SvО2 зависит только от концентрации гемоглобина в крови.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Артерио-венозные мальформации
Происхождение сосудистых мальформаций
Артериовенозные соустья часто бывают множественными, имеют разнообразный калибр и форму. В зависимости от диаметра различают макрофистулы, заметные невооруженным глазом, и микрофистулы, которые выявляются только при микроскопическом исследовании тканей конечности.
Окончательно причины развития синдрома Паркса-Вебера-Рубашова не установлены. Ряд авторов рассматривают его как результат мутаций в гене RASA1, который кодирует белок p120-RasGAP, участвующий в передаче химических сигналов из внеклеточного пространства к ядру клетки. Вместе с тем, каким именно образом эти изменения приводят к специфическим сосудистым аномалиям у лиц с синдромом Паркса Вебера-Рубашова, не установлено.
Патологические соустья чаще располагаются в зоне бедренной, ветвей подколенной артерии, а также по ходу большеберцовых артерий. Интенсивный сброс артериальной крови через артерио-венозные свищи ведет к повышению давления крови в венах.
Из-за повышенной функциональной нагрузки изменяется гистологическая структура венозной стенки. Происходит утолщение ее мышечной оболочки и формирование внутренней эластической мембраны («артериализация» вены).
Значительная часть артериальной крови при наличии свищей поступает в венозное русло, минуя капиллярную сеть, поэтому возникает тяжелое кислородное голодание в тканях и нарушаются обменные процессы. Из-за венозной гипертензии усиливается нагрузка на сердце, что постепенно приводит к расширению его границ и сердечной декомпенсации.
Основные симптомы
Преимущества лечения в клинике
Диагностика

Клиническая симптоматика обусловлена нарушениями регионарного кровообращения и центральной гемодинамики. Конечность удлинена на 3-8 см, мягкие ткани ее гипертрофированы. Удлинение конечности обусловлено продуктивной перестройкой костной ткани из-за усиленной васкуляризации эпифизарных линий.
Характерно наличие варикозно расширенных поверхностных вен на нижней или верхней конечности. Их появление связано с высокой венозной гипертензией вследствие заброса крови из артерии. Стенки вен плотноэластической консистенции, с трудом сжимаемые. Расширенные вены не исчезают после придания конечности возвышенного положения. Иногда при осмотре над ними определяется пульсация.
Рука, приложенная к месту проекции артериовенозного соустья, ощущает вибрацию (симптом «кошачьего мурлыкания»). При аускультации в этой области выслушивают непрерывный систоло-диастолический шум, усиливающийся в момент систолы.
Нарушения микроциркуляции, связанные с регионарными гемодинамическими расстройствами, в ряде случаев приводят к образованию язв и некрозов дистальных отделов конечностей. Из язв часто возникают повторные обильные кровотечения, приводящие к тяжелой анемии. Нередко бывает гипертрихоз и гипергидроз.
Ряд клинических симптомов связан с изменениями центральной гемодинамики. При значительной венозной гипертензии увеличивается нагрузка на правые отделы сердца, следствием ее являются гипертрофия сердечной мышцы, увеличение ударного и минутного объема сердца Однако по мере прогрессирования заболевания сократительная функция сердца начинает ослабевать, происходит миогенная дилатация сердца с расширением его полостей Развивается сердечная недостаточность, проявляющаяся одышкой, сердцебиениями, отеками, застойной печенью, асцитом, анасаркой. Для врожденных артериовенозных свищей характерно урежение пульса, наступающее после пережатия приводящей артерии.
Реографическая кривая, записанная с сегмента конечности, где расположены артериовенозные соустья, характеризуется высокой амплитудой, отсутствием дополнительных зубцов на катакроте, увеличением реографического индекса. В дистальных сегментах конечности амплитуда кривой, напротив, снижена. Артериализация венозной крови ведет к увеличению насыщения ее кислородом, содержание которого в расширенных венах увеличивается на 20-30%.
Наиболее важным методом диагностики врожденных артериовенозных свищей является ангиография. Различают прямые и косвенные ангиографические признаки артериовенозных свищей Наличие на ангиограммах контрастированного соустья или сосудистой полости, сообщающейся с артерией и веной, относят к прямым признакам. Косвенно о наличии свища свидетельствуют одновременное контрастирование артерий и вен, расширение просвета приводящей артерии, обеднение сосудистого рисунка дистальнее расположения артериовенозного свища.
Артерио-венозная разница параметров гемостаза у реанимационных больных с различными типами энергодефицита
Полный текст:
Аннотация
Об авторах
Список литературы
1. Неговский В.А., Гурвич А.М., Золотокрылина Е.С.
2. Ефуни С.Н., Шпектор ВА.Гипоксические состояния и их классификация.Анестезиология и реаниматология.1986; 2: 3—1
3. Шапошников С.А., Синьков С.В., Иванов К.Ф., Заболотских И.Б.Закономерности развития нарушений гемостаза после резекции печени в зависимости от типа энергодефицита.Общая реаниматология.2010; 6 (5): 21—2
4. Синьков С.В., Шапошников С.А., Величко Д.С., Заболотских И.Б.Характеристика гемостаза с позиции энергодефицитных состояний.Кубанский науч. мед. вестн.2012; 3: 132—137.
5. Величко Д.С., Шапошников С.А., Синьков С.В.Коррекция нарушений системы гемостаза с позиции энергодефицитных состояний.Современные проблемы науки и образования.2012; 6: 184.
6. Гаврилов О.К.Проблемы и гипотезы в учении о свертывании крови. М.: Медицина; 1981.
7. Kitchens C.S., Alving B.M., Kessler C.M.Consultative hemostasis and thrombosis. W.B. Saunders Company; 2004: 768.
8. Гологорский В.А., Багдатьев В.Е., Гельфанд Б.Р.Изменение метаболической функции легких и содержание биологически активных веществ в крови больных с респираторным дистресс-синдромом.Анестезиология и реаниматология.1992; 1: 20—22.
9. Багдатьев В.Е., Гологорский ВА., Гельфанд Б.Р.Нарушения фибри-нолитической функции легких при респираторном дистресс-синдроме у больных перитонитом.Анестезиология и реаниматология.1991; 5: 9—12.
10. Заболотских И.Б., Зыбин К.Д., Курзанов А.Н., Мусаева Т.С.Сверхмедленные биопотенциалы как способ экспресс-диагностики типа энергодефицита у реанимационных больных.Кубанский науч. мед вестн.2009; 1: 37—42.
11. Синьков С.В., Заболотских И.Б., Шапошников С.А.Приобретенные коагулопатии: современные подходы к дифференциальной диагностике и интенсивной терапии с позиции доказательной медицины.Общая реаниматология.2007; 3 (5—6): 192—198.
12. Гаврилов О.К.Мозаичность гемостатических потенциалов и патология РАСК. В кн.: Проблемы и гипотезы в учении о свертывании крови. М.: Медицина; 1981: 11—25.
13. Kalfarentzos F., KehagiasJ., MeadN., Kokkinis K., Gogos CA.Enteral nutrition is superior to parenteral nutrition in severe acute pancreatitis: results of randomised prospective trial.Br. J. Surg.1997; 84 (12): 1665—1669.
14. Tesinsky P.Nutritional care of pancreatitis and itscomplications.Curr. Opin. Clin. Nutr. Metab. Care.1999; 2 (5): 395—398.
15. Moore F.D.Metabolism in trauma: the reaction of survival.Metabolism.1959; 8: 783—786.
16. Голубев А.М., Мороз В.В., Сундуков Д.В.Патогенез острого респираторного дистресс-синдрома.Общая реаниматология.2012; 8 (4): 13—21.
17. Мороз В.В., Власенко А.В., Голубев А.М., Яковлев В.Н., Алексеев В.Г., Булатов Н.Н., Смелая Т.В.Патогенез и дифференциальная диагностика острого респираторного дистресс-синдрома, обусловленного прямыми и непрямыми этиологическими факторами.Общая реаниматология.2011; 7 (3): 5—13.
18. Синьков С.В., Заболотских И.Б., Шапошников С.А., Федоренко А.А.Вклад острого повреждения легких в патогенез развития нарушений системы гемостаза.Общая реаниматология.2008; 4 (3): 6—9.
19. Мороз В.В., Кармен Н.Б., Маевский Е.И.Механизмы вторичного повреждения нейронов при тяжелой черепно-мозговой травме (часть 2).Общая реаниматология.2011; 7 (5): 42—45.
20. Данилов И.А., Овечкин А.М.Полиорганная недостаточность: состояние проблемы и современные методы лечения с использованием низкопоточных мембранных технологий.Общая реаниматология.2011; 7 (6): 66—71.
21. Лихванцев В.В., Мороз В.В., Гребенчиков О.А., Гороховатский Ю.И., Заржецкий Ю.В., Тимошин С.С., Левиков Д.И., Шайбакова В.Л.Ише-мическое и фармакологическое прекондиционирование.Общая реаниматология.2011; 7 (6): 59—65.
Для цитирования:
For citation:
Что такое артерио венозная разница по кислороду
Введение
Согласно данным ряда исследований [1-4; 7; 8], величина потребления кислорода организмом, особенно в условиях максимальных физических нагрузок, определяется особенностями реакции каждого из звеньев газотранспортной системы, что определяет ту или иную степень экономичности и эффективности КРО.
Цель: исследование особенностей кислородных режимов в покое и при максимальной нагрузке у лиц с различным уровнем аэробных возможностей по уровню максимального потребления кислорода (МПК).
Материалы и методы
В исследовании приняли участие мужчины в возрасте 18–24 лет, из которых было сформировано 5 групп по уровням МПК согласно классификации Астранда [6].
Низкое потребление кислорода ≤ 38мл/мин/кг.
Умеренное потребление кислорода 39-43 мл/мин/кг.
Среднее потребление кислорода 44-51мл/мин/кг.
Хорошее потребление кислорода 52-56мл/мин/кг.
Высокое потребление кислорода ≥ 57 мл/мин/кг.
Скорость транспорта поступления кислорода в лёгкие (мл/мин) рассчитывали по формуле:
где FIO2 – содержание кислорода во вдыхаемом воздухе (%).
Скорость транспорта кислорода артериальной кровью (об.%/ мин) рассчитывали по формуле:
где CaO2 – содержание кислорода в артериальной крови (об%).
Скорость транспорта кислорода смешанной венозной кровью (об.%/мин) рассчитывали по формуле:
Артерио-венозная разница по кислороду (об.%) рассчитывалась по формуле Фика:
Экономичность КРО оценивалась по вентиляционному эквиваленту (VE), коэффициенту использования кислорода в лёгких (КИO2), кислородному эффекту дыхательного цикла (Q2rc, мл), гемодинамическому эквиваленту (HE), кислородному эффекту сердечного цикла ( Q2cc, мл)
Результаты
Соотношение приростов показателей qIO2, МОД и ЧД позволяет говорить о наиболее выраженной реакции звена внешнего дыхания в группе со средним уровнем МПК.
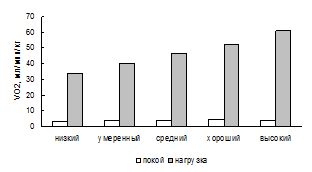
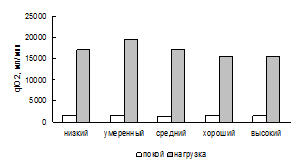
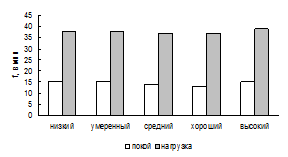
Рис. 1. VO2 при различных уровнях МПК. Рис. 2. qIO2 при различных уровнях МПК.
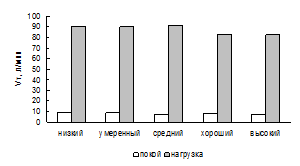
Рис. 3. МОД при различных уровнях МПК. Рис. 4. ЧД при различных уровнях МПК.
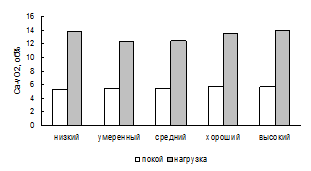
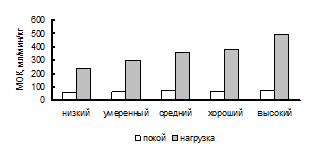
Рис. 5. Ca-vO2 при различных уровнях МПК. Рис. 6. МОК при различных уровнях МПК.
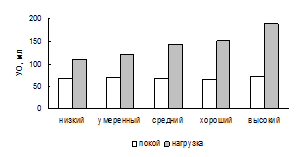
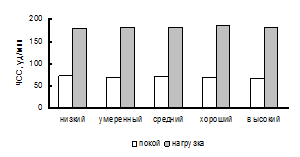
Рис. 7. УО при различных уровнях МПК. Рис. 8. ЧСС при различных уровнях МПК.
Параметры газообмена в покое и при максимальной нагрузке у лиц с различными уровнями МПК
Параметры газообмена в покое и при максимальной нагрузке у лиц с различными уровнями МПК
Основные патогенетические аспекты острой кровопотери
Учитывая, что диагностика кровопотери и интенсивная заместительная терапия при кровотечениях, в том числе и язвенной природы, должна быть основана не на механическом исполнении малоконкретных и часто противоречивых инструкций, а на четком понимании механизмов нарушения гомеостаза и их клинических проявлений, мы считаем обязательным остановиться на современной концепции патофизиологии острой кровопотери.
В патогенезе развития синдрома острой кровопотери традиционно выделяют три основных фактора: уменьшение объема циркулирующей крови (ОЦК), изменение сосудистого тонуса, снижение сердечного выброса. В ответ на острую кровопотерю в организме больного развивается комплекс ответных компенсаторно-защитных реакций, имеющих универсальный характер. Известно, что острая кровопотеря приводит к выбросу надпочечниками катехоламинов, вызывающих спазм артериол и прекапиллярных сфинктеров с редукцией перфузии микроциркуляторного русла. Ограничение перфузии микроциркуляторного компартмента сосудистой системы имеет несколько последствий. Сам по себе сброс крови в венозное русло по артериовенозным шунтам и соответствующее объему микроциркуляторного русла (7-14%) увеличение объема всего функционирующего в данный момент сосудистого русла может частично компенсировать возникший дефицит ОЦК. Централизация кровообращения при этом позволяет, во-первых, поддерживать адекватный сердечный выброс за счет сохранения преднагрузки и, во-вторых, обеспечить перфузию жизненно важных тканей (нервная ткань, миокард, легочная ткань) и тем самым обеспечить поддержание жизни в критических ситуациях. Принято считать, что поддержание адекватного внутрисосудистого объема и связанной с ним преднагрузки желудочков – это основа нормальной насосной функции сердца. Принципы, высказанные Э. Старлингом и О. Франком в начале двадцатого столетия, до сих пор формируют наше понимание физиологии кровообращения, патофизиологических механизмов и способов ее коррекции. Состояние сократимости миокарда при различных условиях, таких как гипокинезия – недостаточность кровообращения при острой кровопотере, или гиперкинезия – ранняя фаза септического шока, являются примерами ситуаций, где закон Франка-Старлинга действует относительно безупречно.
Компенсаторный механизм, являющийся при кровопотере до 15% ОЦК самодостаточным, при большей величине кровопотери может оказаться несостоятельным для предотвращения прогрессирующей гипотонии и, кроме того, является причиной развития тяжелых расстройств микроциркуляции даже после видимой нормализации гемодинамики. Длительный спазм периферических сосудов вызывает серьезные прогрессирующие расстройства кровообращения в микроциркулярном русле, вплоть до полного прекращения почечного, печеночного, мезентериального кровотока, перфузии мышц и покровных тканей. Это, в свою очередь, приводит к возникновению дефицита в транспорте кислорода (гипоксемия), развитию гипоксии органов, переходу клеток органов на анаэробный путь расщепления глюкозы, накоплению недоокисленных продуктов метаболизма, развитию тканевого ацидоза, что определяет возникновение синдрома полиорганной недостаточности. Как метко замечено, при шоке арена катастрофы – в системе макроциркуляции, а ее судьба – в системе микроциркуляции.
По мнению современных авторов, состояние острой артериальной гипотензии и гипоперфузии тканей, закономерно возникающих в результате острой потери части ОЦК, не является всеобъемлющим отражением сущности геморрагического шока, поскольку перфузия тканей насыщенной кислородом кровью, а тем более, артериальное давление, являются не целью для организма, но всего лишь средством осуществления энергообеспечения тканей. Данное положение является иллюстрацией принципа постоянства гомеостаза, основанного на теории функциональных систем П. К. Анохина и утверждающего, что именно конечный приспособительный результат, биологическая константа (в данном случае – доставка кислорода соответственно метаболическим потребностям тканей) является системообразующим фактором и определяет взаиморегуляцию звеньев системы.