что такое аффинность антител
аффинность антител
АФФИННОСТЬ — антител (от лат. affinis родственный), прочность связывания активных центров молекулы антитела с детерминантными (реакционно способными) группами антигена; осн. характеристика специфичности антител. Зависит от взаимной пространственной… … Биологический энциклопедический словарь
Аффинность — (лат. affinitas родственность) термодинамическая характеристика, количественно описывающая силу взаимодействия веществ (например, антигена и антитела).[1] Аффинность можно определить по закону действующих масс как отношение… … Википедия
Антитела — I Антитела белки сыворотки крови и других биологических жидкостей, которые синтезируются в ответ на введение антигена и обладают способностью специфически взаимодействовать с антигеном, вызвавшим их образование, или с изолированной детерминантной … Медицинская энциклопедия
antibody affinity — antibody affinity. См. аффинность антител. (Источник: «Англо русский толковый словарь генетических терминов». Арефьев В.А., Лисовенко Л.А., Москва: Изд во ВНИРО, 1995 г.) … Молекулярная биология и генетика. Толковый словарь.
Антитела — Эта статья об иммунологии. Об украинской поп рок группе см. Антитела (группа); о фильме см. Антитела (фильм, 2005). Антитела (иммуноглобулины, ИГ, Ig) это особый класс гликопротеинов, присутствующих на… … Википедия
Авидность — антител характеристика общей стабильности комплекса антигена и антитела. Авидность определяется аффинностью антитела к антигену, количеством антигенсвязывающих центров в молекуле антитела и особенностями пространственной структуры антигена … Википедия
Белки — У этого термина существуют и другие значения, см. Белки (значения). Белки (протеины, полипептиды[1]) высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью альфа аминокислот. В живых организмах… … Википедия
Артериола — Артериолы мелкие артерии, по току крови непосредственно предшествующие капиллярам. Характерная их особенность преобладание в сосудистой стенке гладкомышечного слоя, благодаря которому арте … Википедия
Общее периферическое сосудистое сопротивление — Артериолы мелкие артерии, по току крови непосредственно предшествующие капиллярам. Характерная их особенность преобладание в сосудистой стенке гладкомышечного слоя, благодаря которому артериолы могут активно менять величину своего просвета и,… … Википедия
Биотехнология антител
Автор
Редакторы
Первые статьи спецпроекта о терапевтических антителах были посвящены истории открытия и применения антител, их структуре и разнообразию. В этом тексте мы затронем то, как ученые научились производить антитела для лекарственного применения, а также модифицировать их. Поскольку антитело — очень сложная молекула, обладающая пространственной структурой, определяющей ее функцию, — антитело нельзя синтезировать химически, а нужно обязательно использовать для этого биологические системы, например, клеточные культуры животных, в которые заложены все необходимые средства для производства таких сложных белков. В этой статье мы рассмотрим современные подходы в биоинженерии антител.
Терапевтические антитела
Спецпроект об антителах, истории их изучения, методах работы с ними, а также о применении антител в современной медицине и биотехнологии.
Партнер спецпроекта — Департамент вычислительной биологии одной из крупнейших российских биотехнологических компаний — BIOCAD. BIOCAD заслужил серьезные позиции на мировом фармацевтическом рынке благодаря выпуску лекарственных препаратов на основе антител.
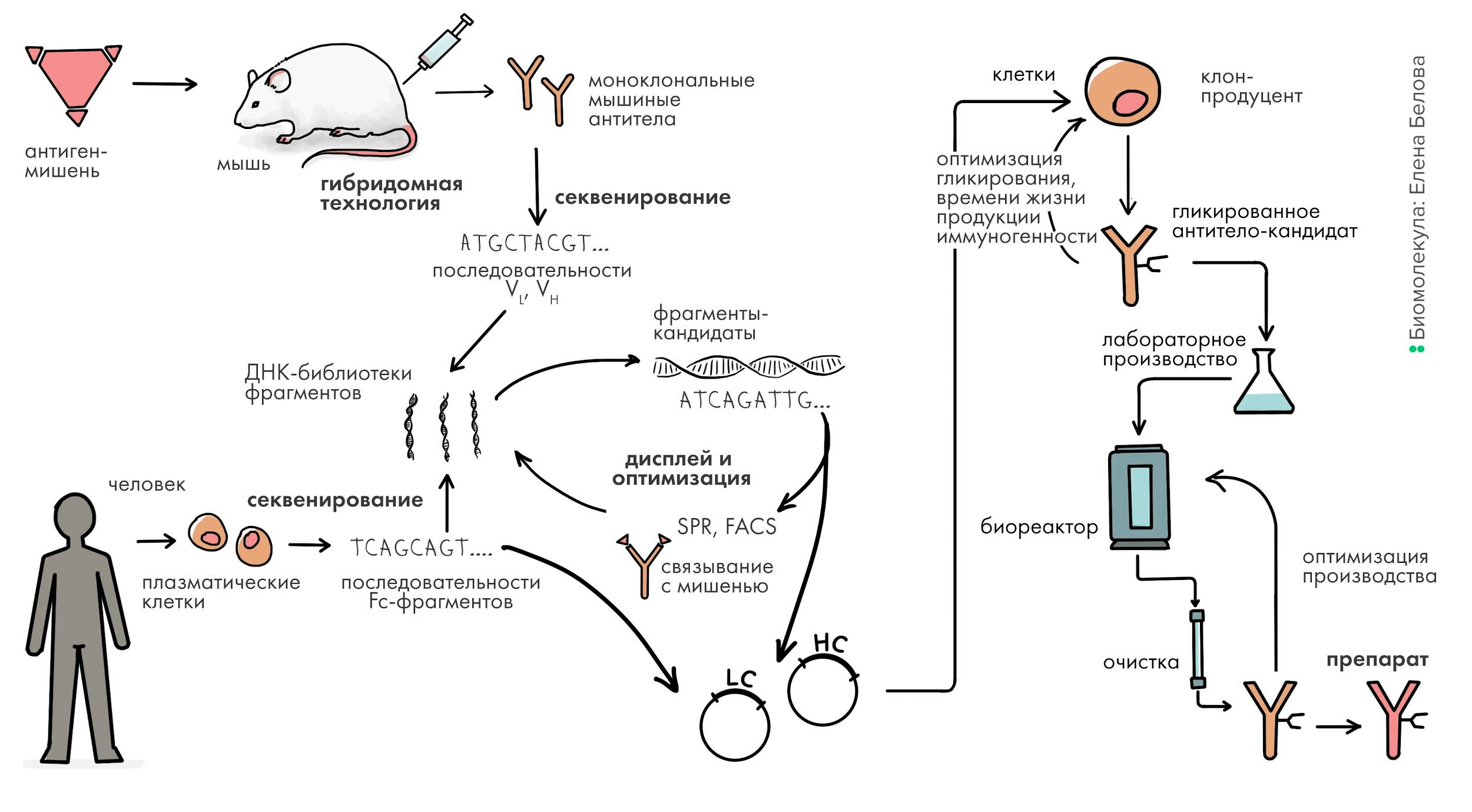
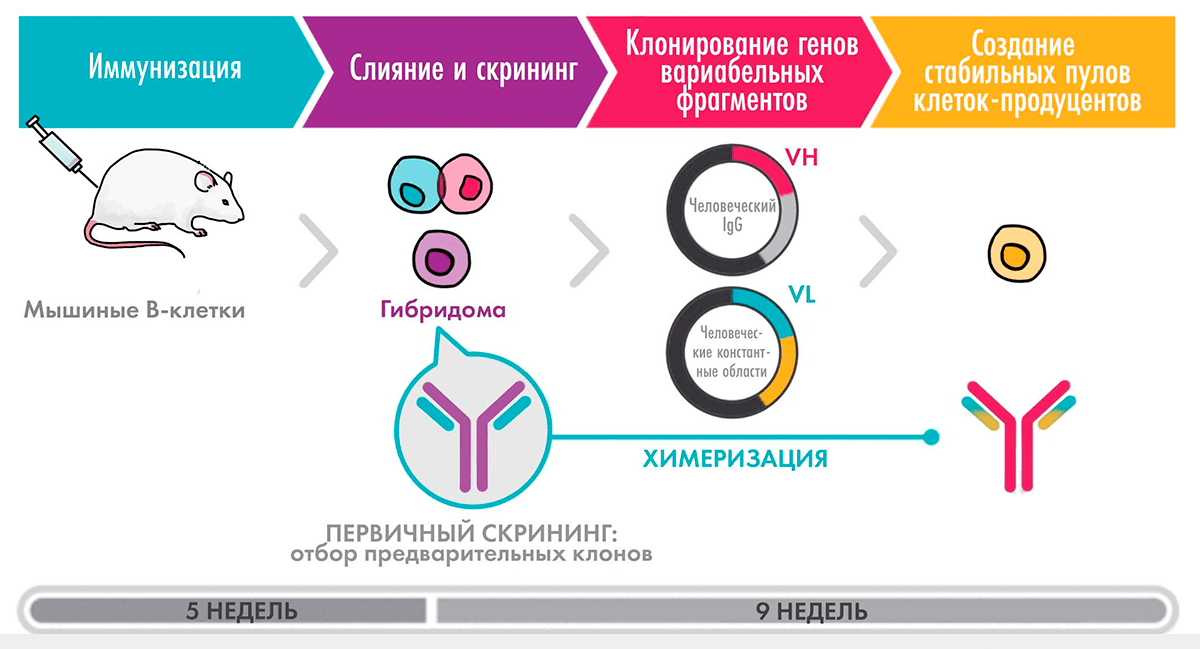
В первой статье спецпроекта — «Краткая история открытия и применения антител» [1] — рассказывается о том, как: были открыты антитела; возникла идея их использования в диагностике и терапии; были разработаны методы получения высокоочищенных моноклональных антител; антитела применяются в лабораторной и медицинской диагностике; а также о наиболее успешных терапевтических антителах. Вторая статья — «Антитело: лучший способ распознать чужого» [2] — посвящена устройству антител и механизму их образования в организме. В третьей статье цикла мы расскажем о том, как биотехнологи создают антитела к нужным мишеням: о генной инженерии антител, создании их «с нуля», оптимизации структуры и производстве в клеточных культурах животных (рис. 1).
Рисунок 1. Общая схема разработки антитела
Для того чтобы клетка производила антитело, необходимо ввести в нее гены, кодирующие его тяжелые и легкие цепи. Также нужно, чтобы генетическая конструкция, которая вводится в клетку (ее называют вектором), содержала ряд вспомогательных элементов, обеспечивающих наиболее эффективную транскрипцию и трансляцию гена в клетке (рис. 2). Уже на данном этапе необходимо продумать весь путь разработки антитела вплоть до выхода на рынок. Для этого еще на стадии конструирования антитела создают Target product profile — документ, который со временем превратится в инструкцию к препарату. Именно он определяет, каким пациентам будет показано антитело, с какой частотой оно будет вводиться, а значит, каков должен быть его формат и другие параметры, о которых мы расскажем ниже.
Технологическая платформа MabNext компании BIOCAD
В компании BIOCAD создана технологическая платформа MabNext для ускорения разработки моноклональных антител. Компания открыла собственный центр обработки данных (ЦОД), чтобы как можно более эффективно предсказывать свойства антител и оптимизировать их структуру на собственных вычислительных мощностях. Так, если раньше на сбор информации и краткое описание аминокислотной последовательности целевых антител для лечения заболеваний уходило более двух недель, то теперь с помощью новых вычислительных мощностей на это будет тратиться всего несколько десятков минут.
В разработке компании более 30 препаратов — моноклональных антител для терапии онкологических и аутоиммунных заболеваний. Среди них российские антитела, успешно прошедшие первые клинические испытания, в том числе PD-1 (фаза 2), IL-17 (фаза 3), IL-6R (фаза 2), CTLA-4 (фаза 1), и антитела на более ранних фазах исследований — биспецифические PDL1/CD47, cMET/EGFR, PCSK9 (доклинические исследования), IL-5R.
Материал предоставлен партнёром — Департаментом вычислительной биологии компании BIOCAD
Путем изменения генетических конструкций, кодирующих антитело, можно влиять на такие его характеристики, как способ действия (будет оно убивать клетку-мишень или только препятствовать проведению сигнала), селективность к мишени, время выведения из организма и др. Если необходимо модифицировать специфичность или селективность антитела (выделенные жирным термины см. в «Словарике»), то изменению подлежат вариабельные фрагменты антител, отвечающие за связывание с антигеном (Fab-фрагменты). Если же нужно изменить другие параметры — время полужизни антитела, его механизм действия, — модифицируют константные участки (Fc-фрагмент).
Генная инженерия антител
Обычно создание генно-инженерной конструкции для экспрессии антитела начинается с выбора системы экспрессии, вектора и оптимизации нуклеотидной последовательности, кодирующей антитело. Необходимо откорректировать состав кодонов таким образом, чтобы экспрессия антитела была максимальной. Аминокислотный состав белка оптимизируют для снижения вероятности выпадения в осадок, агрегации, а также иммуногенности, о чем мы подробнее расскажем далее. Кроме того, важно обеспечить правильное сворачивание (фолдирование, упаковку) цепей и их соединение между собой. Сейчас существуют программы, позволяющие оптимизировать нуклеотидную последовательность генно-инженерных конструкций для продукции антител in silico, хотя, конечно, последнее слово остается за экспериментальными данными.
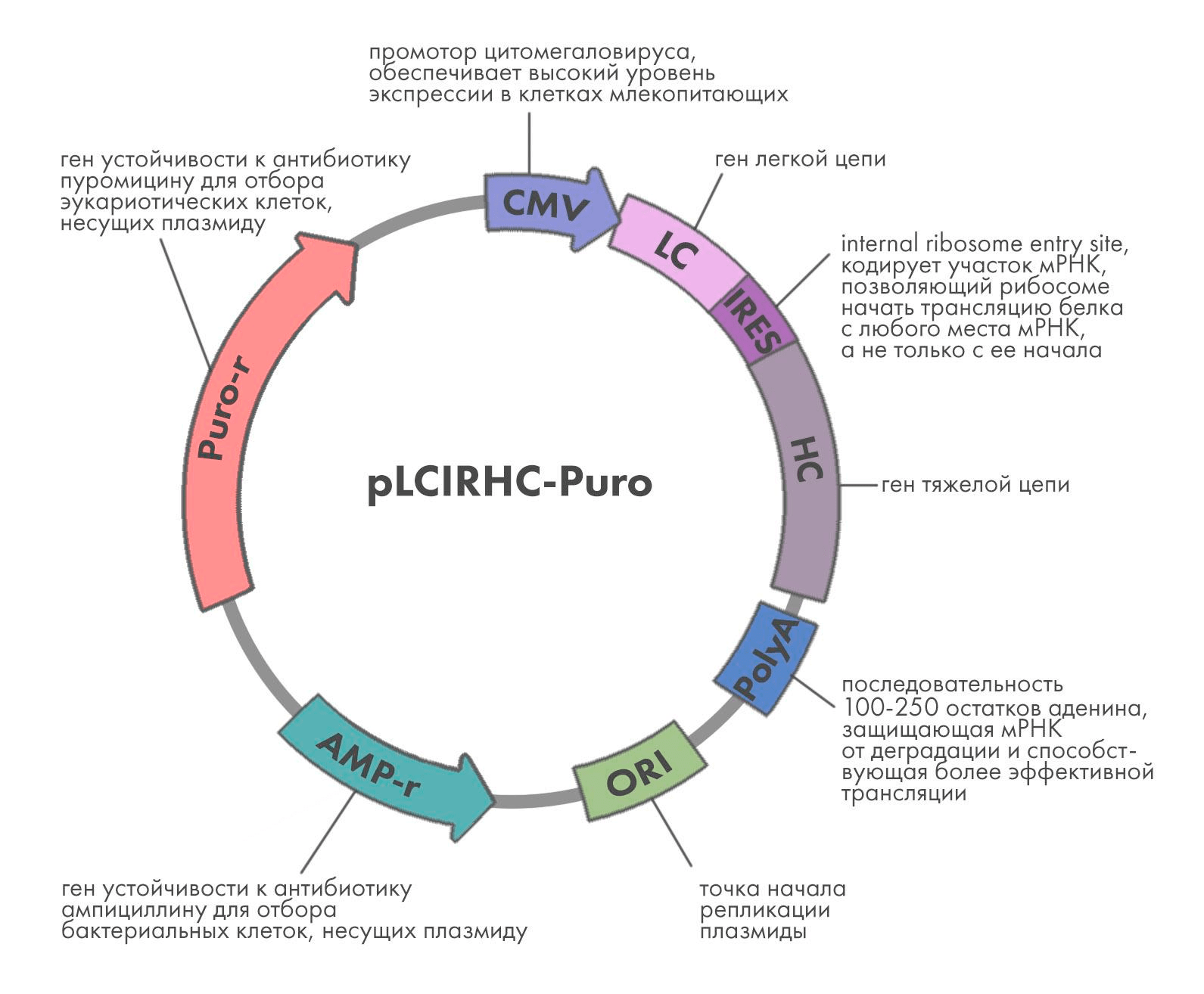
В качестве вектора используют плазмиды — кольцевые ДНК, кодирующие как сам ген белка, так и вспомогательные элементы. Так, для экспрессии в эукариотических клетках используют промотор цитомегаловируса (CMV), обеспечивающий высокую эффективность транскрипции.
Поскольку антитело состоит из двух полипептидных цепей — легкой и тяжелой, — используют либо двухплазмидную систему экспрессии, либо один вектор, содержащий оба гена. Последний вариант предпочтительнее, так как позволяет точнее контролировать соотношение продукции легких и тяжелых цепей. Было показано, что в природных условиях в B-клетках легкие цепи синтезируются в бóльшем количестве, чем тяжелые, и такое соотношение скоростей синтеза наиболее благоприятно для продукции антител [3].
О том, как и зачем ученые работают с клеточными культурами, мы рассказывали в статье «12 методов в картинках: клеточные технологии» [4]. — Ред.
Рисунок 2. Схема плазмиды для экспрессии антител в клетках млекопитающих
Получение вариабельных фрагментов антител
Перейдем к тому, как получаются последовательности вариабельных фрагментов антител, которые и определяют их специфичность и селективность.
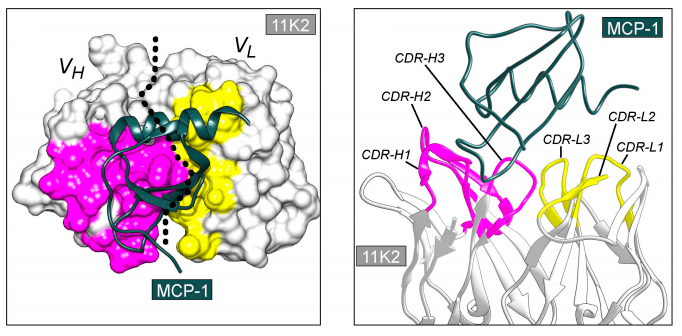
Исследователи пока не могут предсказать, какая именно последовательность вариабельного фрагмента антитела будет оптимальной для связывания антигена. Антиген, как правило, представляет собой белковую молекулу, и площадь поверхности контакта антитела с антигеном слишком велика для моделирования in silico (рис. 3), которое также осложняется наличием молекул воды. Поэтому приходится использовать биологические объекты, у которых есть способность очень тонко настраивать последовательность аминокислот антитела для обеспечения высочайшей аффинности к антигену.
Биологические процессы настолько сложны, что порой их намного удобнее смоделировать на компьютере, нежели пытаться повторить в пробирке. О том, как устроена работа биоинформатика, мы уже писали в статьях «12 методов в картинках: сухая биология» [5], «Вычислительное будущее биологии» [6] и в других [7–9]. — Ред.
Рисунок 3. Кристаллическая структура комплекса антитела 11К2 (серый, розовый и желтый цвета) и антигена MCP-1 (зеленый цвет) в двух проекциях. Структура иллюстрирует сложность поверхности контакта антитело—антиген.
Методы получения антител подразделяются на гибридомные и дисплейные. Гибридомный метод, более подробно описанный в статьях «Краткая история открытия и применения антител» [1] и «Моноклональные антитела» [10], использует для получения антител организм млекопитающего, который после иммунизации (введения антигена) вырабатывает антитела с высокой аффинностью и селективностью. В дальнейшем эти антитела или их гены можно выделить, отсеквенировать [11] и модифицировать с целью придания им нужных фармакологических свойств.
Дисплейные методы
Дисплейные методы используют в качестве исходного материала широкий репертуар генов, кодирующих антитела. Самым распространенным методом является фаговый дисплей [12], [13]. Метод представления (отсюда название — «дисплейный») пептида на поверхности бактериофага М13 был изобретен в 1985 году. В 1989 г. научились клонировать гены иммуноглобулинов, что позволило обойтись без гибридомной технологии для получения антител. Первоначально в бактериях синтезировали Fab или scFv фрагменты антител, создавая библиотеки клонов, и проводили вручную отбор наиболее аффинных клонов с помощью радиоактивно-меченного антигена. Однако это была очень трудоемкая и неэффективная процедура. В 1990 году впервые использовали дисплейную технологию представления фрагментов антител на поверхности фагов, а в 1991 создали первую библиотеку вариабельных фрагментов. Первым антителом, созданным с помощью технологии фагового дисплея, стала «Хумира» (адалимумаб компании Abbott) против мишени TNF для лечения ревматоидного артрита [14] и болезни Крона. «Хумира» зарегистрирована в 2002 году, и уже долгое время возглавляет список лекарств — лидер ов продаж.
Получение антитела дисплейным методом in vitro схематически подражает эволюционному процессу формирования антител в организме [15]:
Таким образом, в процессе присутствуют все составляющие эволюции — наследственность, изменчивость и отбор. Рассмотрим эти шаги подробнее.
Качество получаемой библиотеки фрагментов зависит от способности получить широкий репертуар разнообразных и при этом качественных антител [16]. Существует два принципиально разных подхода к получению библиотек: естественный (наивный) и синтетический.
Естественные библиотеки вариабельных доменов антител получают методом полимеразной цепной реакции природных генов с обратной транскрипцией (RT-PCR) [17] из лимфоидных тканей или периферической крови людей, а также других животных. Преимущество этого метода в том, что полученные антитела будут в правильной конформации, так как их гены кодируют функциональные антитела. Однако недостаток в том, что разнообразие последовательностей ограничено охватом естественной иммунной системы, в которой существует определенная неравномерность использования тех или иных последовательностей. Также фрагменты из природных библиотек сильно отличаются по качеству и непредсказуемы по составу; многие из них могут оказаться недостаточно стабильными или неподходящими по другим причинам. Репертуар естественных библиотек составляет 10 7 –10 11 фрагментов [18].
Синтетические библиотеки создают путем встраивания искусственно синтезированной ДНК в последовательности, кодирующие вариабельные домены. ДНК синтезируется таким образом, чтобы вносить совершенно случайные (рандомизированные) мутации в получающиеся фрагменты антител и тем самым расширять разнообразие определяющего комплементарность сайта (complementarity-determining region, CDR). Синтетические библиотеки позволяют использовать определенную коровую (germline) структуру вариабельного домена, про которую известно, что она наиболее представлена в каждом индивидууме, неиммуногенна и стабильна. Однако введение полностью синтетических участков CDR может привести к неправильному сворачиванию и агрегации белка. Потребовалось время для отработки подходов к определению того, какие CDR лучше использовать. Репертуар синтетических библиотек, как правило, доходит до 10 9 –10 11 фрагментов.
Далее начинается самое интересное: как дисплейная технология позволяет связать генотип с фенотипом и отобрать клоны с нужными свойствами. Гены всех фрагментов антител вставляют в геном бактериофага в одно и то же положение — внутрь гена, кодирующего белок оболочки фага. Потом гены переносят в кишечную палочку Escherichia coli (это называется трансдукцией) и заражают вспомогательным фагом, который вызывает сборку бактериофага, содержащего на поверхности фрагмент антитела. В результате получается библиотека бактериофагов, у каждого из которых на поверхности экспрессируется фрагмент антитела, соответствующий гену, который попал в данного бактериофага. Препарат библиотеки добавляют к иммобилизованному на поверхности пластиковой пробирки антигену, против которого надо создать антитела, и проводят отмывку. На поверхности остаются только бактериофаги, содержащие вставку гена фрагмента антитела с высоким сродством к антигену. Чтобы отобрать самые высокоаффинные клоны, связавшиеся с антигеном, фаги снимают с поверхности и снова заражают ими E. coli (рис. 4). После нескольких этапов отбора ДНК полученных фагов секвенируют и узнают последовательность, кодирующую самые аффинные фрагменты [19].
Рисунок 4. Процесс селекции нужных генотипов в соответствии с аффинностью к антигену. а — Бактериофаг, обеспечивающий связь генотип—фенотип. Ген фрагмента антитела (розовый) вставляется в фаговую ДНК, что приводит к экспрессии на поверхности фага белка — фрагмента антитела. б — Схема фагового дисплея. 1. Фаговую библиотеку, состоящую из 10 6 –10 11 клонов, инкубируют с иммобилизованным антигеном. 2. Не связавшиеся фаги удаляют промывкой. 3. Связавшиеся фаги снимают с поверхности. 4. E. coli заражают фагом для амплификации полученных кандидатов. 5. Клетки высевают на среду с антибиотиком и амплифицируют. Процесс повторяют 2–3 раза для обогащения популяции антительными фрагментами, специфичными к антигену.
Важное преимущество использования дисплейных методов по сравнению с гибридомными — возможность отбирать только те антитела, которые НЕ связываются с ненужными белками, например, с близкими к мишени, но которые не надо блокировать, чтобы не вызывать токсичность. Для этого достаточно иммобилизовать теперь уже нежелательный белок и отбирать те фаги, которые не связались с ним.
Также бывает полезно создать антитело, которое бы хорошо связывалось и с мышиным, и с обезьяньим, и с человеческим вариантами мишени — это обеспечивает быстрое успешное прохождение доклинических исследований и контроль безопасности до выведения потенциального лекарственного кандидата в клинические испытания.
Существуют и другие типы дисплеев, помимо фагового, например, рибосомный или дрожжевой [20]. Здесь я не буду подробно на них останавливаться, так как принцип у них тот же: они обеспечивают связь гена, кодирующего фрагмент антитела, с его аффинностью к мишени, то есть с фенотипом, и позволяют производить отбор по заданным свойствам из огромного количества вариантов в библиотеке.
Созревание аффинности антител
После получения фрагментов-кандидатов разработчики приступают к более сфокусированной настройке аффинности, которая носит название созревание аффинности. В иммунной системе созревание аффинности происходит путем последовательного внесения мутаций в участки, кодирующие CDR, и селективного давления отбора в сторону бóльшей аффинности. In vitro процесс примерно такой же. Разработчики берут ген лидер ного кандидата, вносят мутации в положениях соответствующих CDR и проводят скрининг на аффинность. Индивидуальные мутации, усиливающие аффинность, затем объединяют в одном клоне. Рибосомный дисплей позволяет довольно быстро проскринировать миллионы клонов, а использование нескольких раундов отбора имитирует естественный процесс созревания аффинности. В результате получаются антитела с аффинностью даже выше, чем у природных.
Полученная генетическая последовательность фрагмента антитела, содержащая вариабельные домены, объединяется с последовательностью, кодирующей константные участки тяжелой и легкой цепей (Fc-фрагмент). Если оптимизация вариабельного фрагмента касается аффинности и селективности антитела, то Fc-фрагмент отвечает за фармакокинетику и эффекторные функции антитела, о чем я более подробно расскажу далее.
Так выглядит простейшая схема получения антитела, однако на практике разработчики прибегают к модификации и совмещению различных подходов. Расскажу для примера, как была получена молекула уже упомянутой «Хумиры»: за основу взяли тяжелую цепь мышиного антитела против TNF, ее ген скомбинировали с библиотекой человеческих легких цепей и провели селекцию на связывание с человеческим TNF (hTNF). Полученное антитело-кандидат имело аффинность около 15 нМ. Далее провели созревание аффинности, которое позволило добиться аффинности на уровне 300 пМ [21].
Эпитопная специфичность
Если оптимизация аффинности — относительно простая задача, то инженерия эпитопной специфичности может оказаться достаточно трудным делом. От того, с каким участком мишени свяжется антитело, часто зависит итоговый эффект. Особенно это существенно в случае активирующих антител. Однако и для блокирующих антител это тоже важно: например, антитело с тщательно подобранной эпитопной специфичностью может предотвратить связывание мишени с одним из лигандов, не влияя на связывание с другими.
Один из самых ярких примеров важности определенной эпитопной специфичности — антитела против рецептора HER2, который часто повышенно экспрессируется в клетках рака молочной железы и выставляется на их поверхности. Антитело «Герцептин» (трастузумаб компании Roche/Genentech), одобренное в качестве первой линии терапии метастатического рака молочной железы с повышенной экспрессией HER2, связывается с С-концевым доменом HER2 [22], который отвечает за связывание с другим рецептором, HER3, и препятствует активации последнего. Трастузумаб работает только у пациенток с высокой экспрессией HER2, и у большинства впоследствии развивается резистентность к препарату, то есть опухоль снова начинает расти. Компания Roche разработала антитело «Перджета» (пертузумаб), которое связывается с другим эпитопом HER2, отвечающим за его связывание с рядом рецепторов [23]. Пертузумаб предотвращает активацию самого HER2, тем самым позволяя преодолеть резистентность к трастузумабу.
Один из методов создания антител к выбранному эпитопу состоит из двух этапов [24]. На первом этапе проводится скрининг исходной библиотеки антительных фрагментов на связывание с выбранной мишенью, как описано выше. После того, как получены высокоаффинные фрагменты, проводится их скрининг с мутантной мишенью, у которой аминокислотные остатки в области эпитопа заменены на другие, препятствующие связыванию с ним. В ходе скрининга отбираются те антитела, которые НЕ связываются с мутантной мишенью. Это и будут антитела, специфичные к нужному эпитопу.
Антитело против c-Met для терапии эпителиальных опухолей
В компании BIOCAD сочетанием методов иммунизации, фагового дисплея и точечного мутагенеза получено антагонистическое антитело против с-Met. с-Met — рецептор фактора роста гепатоцитов HGF. Нарушение регуляции с-Met обнаружено при многих злокачественных заболеваниях, оно запускает рост опухоли, инвазию и метастазирование. Полученное в компании BIOCAD гуманизированное анти-c-Met антитело BCD-088 обладает минимальной агонистической активностью, не вызывает аутофосфорилирование рецептора, обладает ADCC и вызывает интернализацию и последующую деградацию c-Met. Сейчас BCD-088 находится в доклинических исследованиях и уже показало эффективность в ряде мышиных моделей онкологических заболеваний.
Материал предоставлен партнёром — Департаментом вычислительной биологии компании BIOCAD
Выбор системы экспрессии
Выше было сказано, что систему экспрессии, то есть тип клеток, в котором будет происходить производство антитела, выбирают на раннем этапе, и ее выбор влияет на то, как должна выглядеть генетическая конструкция и как будут происходить дальнейшее масштабирование и оптимизация экспрессии. Наиболее распространенный во всем мире промышленный вариант системы экспрессии — клетки яичника китайского хомячка CHO (chinese hamster ovary). Клетки СНО дают хорошие выходы белка (как правило, 1–2 г с литра культуры, иногда до 10 г/л), обеспечивают правильное сворачивание и гликозилирование антител, способны к суспензионному росту (то есть в объеме, а не на поверхности) и хорошо адаптируются к изменению условий культивирования, что позволяет масштабировать процесс в различных объемах и использовать их в биореакторах. Другие клеточные линии включают NS0, Sp2/0 (обе — мышиной миеломы), HEK293 (клетки почки человеческого эмбриона) и PER.C6 (получены из человеческих фетальных ретинобластов). Также предпринимаются попытки производства антител в трансгенных растениях и животных, но они пока не дошли до коммерческого использования [25].
Оптимизация вариабельной части антитела — гуманизация
В случае классической гибридомной технологии антиген вводится, как правило, мыши, и в ходе естественного иммунного ответа вырабатываются антитела нужной специфичности. Помимо того, что естественная иммунизация не позволяет контролировать аффинность и селективность антитела, потому что мы не можем проконтролировать представление антигена в иммунной системе и последующий процесс продукции антител, есть еще более важная проблема: при гибридомной технологии мышиное антитело получается чужеродным по отношению к человеку из-за наличия других аминокислотных остатков по сравнению с антителами человека в определенных позициях константной части. Поэтому первое же коммерческое антитело против CD3 — OKT3 — вызывало у многих пациентов антительный ответ.
Такие антитела получили название HAMA — human anti-mouse antibodies, то есть «человеческие противомышиные антитела». Антительный ответ на введенное лекарство сильно снижает его эффективность, потому что приводит к выведению лекарства из организма и делает бессмысленным повторное введение препарата, так как во второй раз антительный ответ гораздо сильнее, и никакой пользы от лекарства точно не будет. Кроме того, антительный ответ может привести к серьезным аллергическим реакциям. Еще одна проблема не полностью человеческих антител — слабое взаимодействие мышиных антител с рецепторами человеческих клеток, которые обеспечивают некоторые из механизмов действия антител и длительность их пребывания в организме. Поэтому перед исследователями встала задача поиска технологий гуманизации антител, то есть приближения их к естественным человеческим аналогам [26].
Химерные антитела
Первым типом антител, приближенных к человеческим, стали химерные (рис. 5). В 1997 году был одобрен ритуксимаб — антитело против белка CD20 на поверхности В-лимфоцитов, предназначенное для лечения В-клеточных лимфом. Для его генерации полученные гибридомным методом вариабельные фрагменты объединили с человеческими константными доменами и таким образом достигли содержания человеческих участков более 70%. Включение ритуксимаба в схемы лечения лимфом произвело революцию, позволив не только увеличить время до прогрессирования заболевания, но и повысить общую выживаемость.
Рисунок 5. Схема получения химерного антитела
Рассмотрим более подробно процесс получения химерного антитела на примере инфликсимаба — препарата против TNF, который, как и рассмотренный выше адалимумаб, применяется для лечения ревматоидного артрита и болезни Крона. Вначале мышь иммунизировали человеческим TNF (hTNF) в сочетании с адъювантом — веществом, усиливающим иммунный ответ, — выделяли спленоциты и сливали их с клетками миеломы. Для отбора клонов клеток, экспрессирующих нужные антитела, использовали радиоиммунный метод с иммобилизованным hTNF. Затем после построения геномных библиотек с использованием фаговых векторов и скрининга путем саузерн-блоттинга [27] выделяли гены, кодирующие легкие и тяжелые цепи антитела. После этого получали плазмиду, содержащую гены мышиных вариабельных участков, объединяли с генами человеческих константных областей (полученных ранее секвенированием генов В-клеток человека) и вводили ее в клетки мышиной миеломы для продукции химерного антитела [28].
Гуманизированные антитела
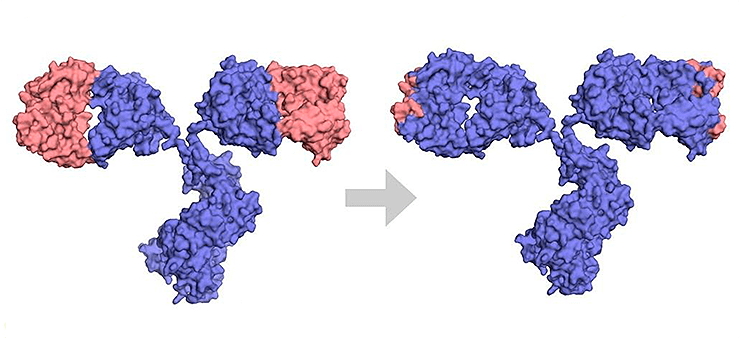
Хотя химерные антитела оказались более эффективными и менее иммуногенными, чем полностью мышиные, они все же вызывают HACA-ответ — образование human anti-chimeric antibody, то есть человеческих антител против химер. Поэтому с 1980-х годов начали разработку гуманизированных антител, у которых чужеродны человеку только CDR и отдельные позиции FR-регионов вариабельных доменов, а остальные части, включая каркас, почти полностью человеческие (рис. 6). Первым таким антителом в разработке стал алемтузумаб против антигена лимфоцитов CD52. Это лекарство применяется для лечения некоторых гемобластозов и рассеянного склероза [29]. Оно было получено на основе крысиного антитела, чьи CDR перенесли в человеческие домены VH и VL уже существующего человеческого антитела [26].
Рисунок 6. Разница между химерным и гуманизированным антителами. Синим показаны человеческие последовательности, оранжевым — мышиные.
Другой подход применили при разработке антитела даклизумаб против рецептора CD25 на Т-лимфоцитах, которое стало первым гуманизированным антителом на рынке (оно использовалось для лечения рассеянного склероза, но уступило конкурентам и было выведено с рынка). Даклизумаб также был получен включением мышиных CDR в человеческий каркас, но на этот раз человеческие участки антитела подобрали компьютерными методами так, чтобы максимизировать сходство с мышиным антителом, откуда взяты CDR. Кроме того, построили компьютерную модель мышиного антитела, и те аминокислотные остатки каркаса, которые контактировали с CDR, перенесли в каркас человеческого антитела, что позволило улучшить аффинность [26].
Хотя гуманизированные антитела включают повышенное количество человеческих последовательностей по сравнению с химерными, вероятность выработки антител против них остается — они называются HAHA (human anti-human antibody, человеческие анти-человеческие антитела).
HAMA-ответ может быть направлен на все антитело, HACA — против вариабельных областей, а HAHA-ответ еще более фокусный — только против CDR. Некоторые компании предприняли попытки заменить CDR-последовательности, чужеродные для человека, на человеческие. Таким образом удается повысить количество полностью человеческих последовательностей на 17–29% и получать с помощью гибридомной технологии почти полностью человеческие антитела [26].
Полностью человеческие антитела
Существует две группы технологий получения полностью человеческих антител. Одна из них подробно описана выше — это технологии дисплея, в первую очередь, фагового. Вторая — технология использования трансгенных животных, экспрессирующих человеческий репертуар антител. У метода трансгенных животных есть два важных преимущества перед дисплейными: антитела получаются быстрее и, поскольку отбор идет in vivo, а не in vitro, исключено образование антител с плохой растворимостью и другими проблемами в дальнейшей разработке.
Этим методом было получено одно из самых известных сейчас антител ниволумаб против мишени PD-1 на активированных T-лимфоцитах [30], которое вместе с другими антителами класса ингибиторов иммунологических чекпойнтов произвело революцию в лечении метастатических злокачественных заболеваний: меланомы, рака легкого, рака мочевого пузыря, дав впервые в истории надежду на полное выздоровление части пациентов. Ниволумаб был разработан по технологии компании Medarex, которая в 1993 году получила линию мышей, экспрессирующих человеческие IgM, IgG и Igκ и не экспрессирующих мышиные IgM и Igκ. Мыши оказались способными к производству полноценных В-клеток, в которых происходит V(D)J-рекомбинация человеческих трансгенных участков, а после введения антигенов — переключение класса тяжелой цепи и соматический мутагенез. Далее из этих мышей по обычной гибридомной технологии получают человеческие антитела [31].
Так, для получения ниволумаба трансгенных мышей иммунизировали рекомбинантным человеческим белком PD-1-Fc, состоящим из внеклеточного домена PD-1 и Fc-фрагмента IgG. Одновременно мышам ввели клетки яичников китайского хомячка CHO, экспрессирующие на поверхности PD-1. Спленоциты мышей слили с клетками миеломы SP2/0 и отобрали гибридомы, производящие антитела, реактивные против PD-1-Fc, с помощью ELISA. Связывание ниволумаба с CD4+ лимфоцитами определяли методом проточной цитофлуориметрии [32], а кинетику связывания с мишенью — методом плазмонного резонанса [33] (см. раздел «Методы изучения свойств антител»).
Несмотря на то, что у мышей технология Medarex порождает довольно ограниченный репертуар генов, кодирующих человеческие VH и VL, даже его хватает для генерации антител с высокой аффинностью, правда, не во всех случаях. Если антиген, к которому надо получить антитела, высокогомологичен с мышиным аналогом, сделать это не удастся. Здесь на помощь могут прийти трансгенные крысы, куры или дисплейные технологии. Также дисплейные технологии являются единственным выходом, если мишень токсична в концентрациях, необходимых для иммунизации животного [26], например, при разработке нейтрализующих антител против природных токсинов.
Первое оригинальное антитело, созданное в России для иммуноонкологии — BCD-100
В компании BIOCAD с помощью фагового дисплея библиотеки донорских антител человека MeganLib и последующего мутагенеза создано полностью человеческое антагонистическое антитело против рецептора PD-1 — BCD-100 (видео 1). В сравнительных клеточных тестах BCD-100 превзошел препараты коммерческих антител ниволумаб и пембролизумаб. Оптимизация свойств молекулы позволила добиться высокого уровня продукции белка в культуре СНО (более 2 г/л), а также повышенной агрегационной стабильности, что должно обеспечить минимальную иммуногенность препарата и улучшенные фармакокинетические и фармакодинамические свойства. BCD-100 находится на стадии подготовки к клиническим исследованиям III фазы.
Видео 1. Механизм действия BCD-100
Материал предоставлен партнёром — Департаментом вычислительной биологии компании BIOCAD
Оптимизация константной части антитела
До сих пор речь шла в основном о том, как получить правильные последовательности CDR, которые определяют взаимодействие антитела с мишенью, его аффинность и отчасти иммуногенность. Теперь пришла пора поговорить о другой части антитела — Fc-фрагменте, структура которого определяет изотип антитела и такие важные его характеристики, как механизм действия (так называемые эффекторные функции), фармакокинетику и взаимодействие с остальными молекулами организма, помимо мишени.
Выбор подкласса IgG
Более подробно строение антител и особенности различных изотипов описаны во второй статье цикла — «Антитело: лучший способ распознать чужого» [2].
Механизмы действия антител
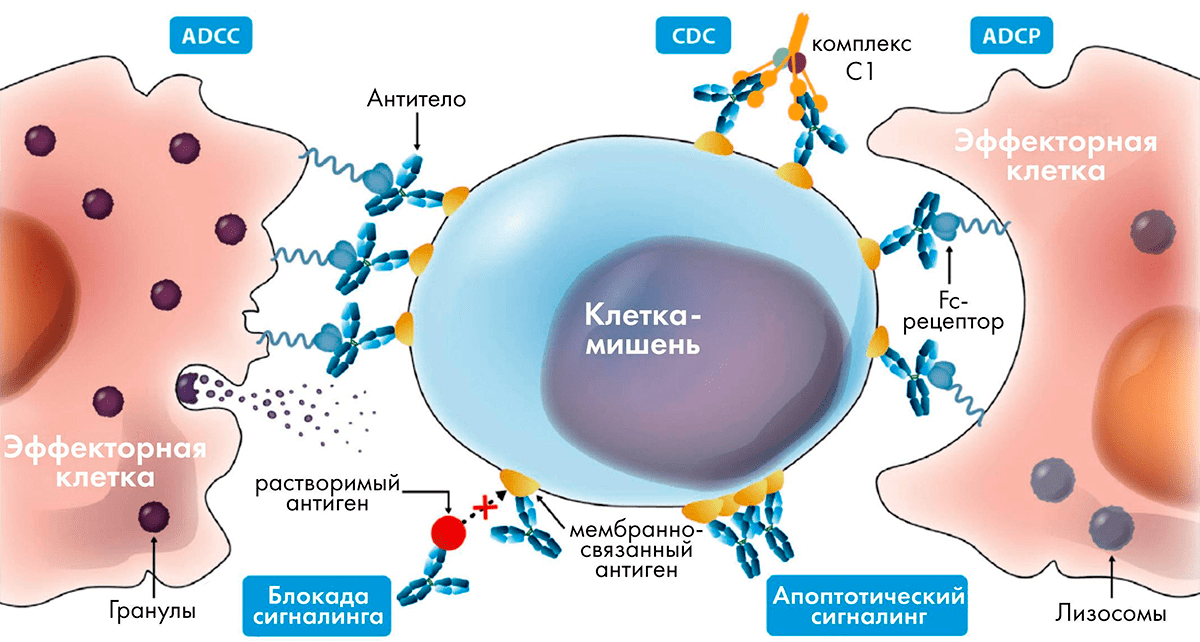
Клетки иммунной системы экспрессируют на поверхности семейство Fcγ-рецепторов, связывающихся с Fc-фрагментом антител подкласса IgG с разным сродством. Когда антитело связывается со своим антигеном, например, с рецептором на поверхности опухолевой клетки, конформация Fc-фрагмента немного меняется, и сродство к Fcγ-рецептору повышается. Клетка-эффектор с Fcγ-рецептором на поверхности присоединяется к антителу, и каскад событий внутри нее приводит к высвобождению цитотоксических гранул, которые убивают раковую клетку (рис. 7). Этот процесс носит название ADCC (antibody-dependent cytotoxicity — «антителозависимая цитотоксичность»). Наиболее активны в отношении ADCC натуральные киллеры (NK-клетки), несущие на поверхности рецептор FcγRIIIa [35]. Помимо цитотоксических гранул, содержащих гранзим и перфорин, NK-клетки также выбрасывают цитокины IFNγ и TNF, создающие воспалительную среду и привлекающие другие клетки иммунной системы.
Рисунок 7. Различные механизмы действия антител
Показано, что ADCC играет важную роль в механизме действия многих антител против поверхностных мишеней, например, ритуксимаба (анти-CD20), трастузумаба (анти-HER2) и цетуксимаба (анти-EGFR). Наибольшее сродство к Fcγ-рецепторам имеет подкласс IgG1, поэтому, если необходимо, чтобы введение антитела приводило к уничтожению клеток, экспрессирующих мишень на поверхности, используют именно этот подкласс.
Сходный механизм — ADCP (antibody-dependent phagocytosis — антителозависимый фагоцитоз), при котором макрофаг после связывания Fc-фрагмента антитела с Fcγ-рецептором поглощает целиком и раковую клетку, и связавшееся с ней антитело [26].
Другой механизм уничтожения клеток, несущих мишень на поверхности, — CDC (complement-dependent cytotoxicity — комплемент-зависимая цитотоксичность). В этом случае с Fc-фрагментом связывается белок С1q системы комплемента, и запускается каскад событий, приводящий к образованию на поверхности клетки MAC-комплекса. MAC (membrane-associated complex) — это белки, которые формируют в мембране раковой клетки канал, что приводит к ее гибели [26].
Мутации в Fc-фрагменте IgG могут как увеличивать эффекторные функции — ADCC, ADCP и CDC, — так и снижать их. Так, оказалось, что ADCC антитела трастузумаб зависит от того, какой у пациента вариант рецептора FcγRIIIa. У пациентов с определенной мутацией в этом рецепторе антитело оказывается недостаточно эффективным. Введение мутаций в Fc-фрагмент трастузумаба повысило ADCC, что, возможно, позволит создать препарат, подходящий всем пациентам независимо от варианта FcγRIIIa [26].
В некоторых случаях необходимо только заблокировать мишень, например растворимые лиганды, при этом нет необходимости в гибели клеток. Тогда либо используют антитело другого подкласса — IgG2 или IgG4, которые почти не проявляют ADCC-активности, — либо вводят в Fc-фрагмент мутации, снижающие эффекторные функции. Так, для ниволумаба был выбран подкласс IgG4, потому что его мишень PD-1 экспрессируется в нормальных клетках иммунной системы, и было бы нежелательно их уничтожать. Вместо этого ниволумаб, не проявляя ADCC и CDC, блокирует взаимодействие PD-1 на Т-лимфоците с лигандом PD-L1 на поверхности раковой клетки и тем самым не дает раковой клетке снизить активность лимфоцита [26].
Гликозилирование
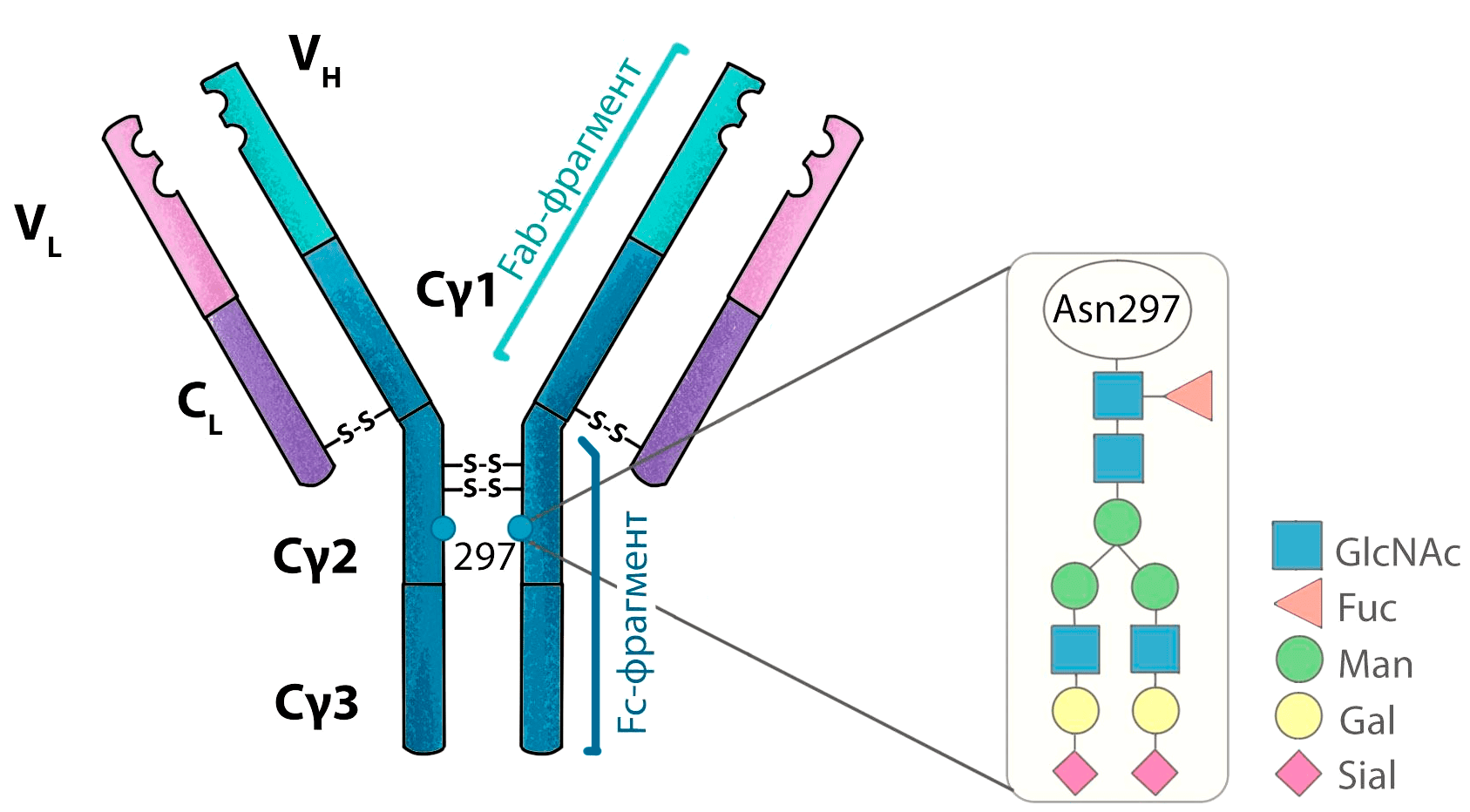
У молекул IgG в домене CH2 находится сайт N-гликозилирования, то есть присоединения остатков сахаров по атому азота (рис. 8). Модификация остатков сахаров, связанных с антителом, позволяет модулировать некоторые эффекторные функции.
Рисунок 8. Структура гликана IgG. Гликозилирование антител происходит всегда в одном месте — по остатку аспарагина-297.
Гликозилирование абсолютно необходимо для взаимодействия антитела с Fcγ-рецепторами, поэтому удаление остатков сахаров приводит к тому, что CH2-домен изменяет свою конформацию, и антитело теряет все эффекторные свойства.
Модуляция состава сахаров, присоединенных к аспарагину-297, также позволяет увеличивать ADCC. К примеру, удаление остатка фукозы (дефукозилирование) приводит к росту ADCC. Чтобы добиться дефукозилирования, для производства антитела используют клеточную линию, в которой выключен фермент, отвечающий за добавление фукозы — фукозилтрансфераза.
Фармакокинетика
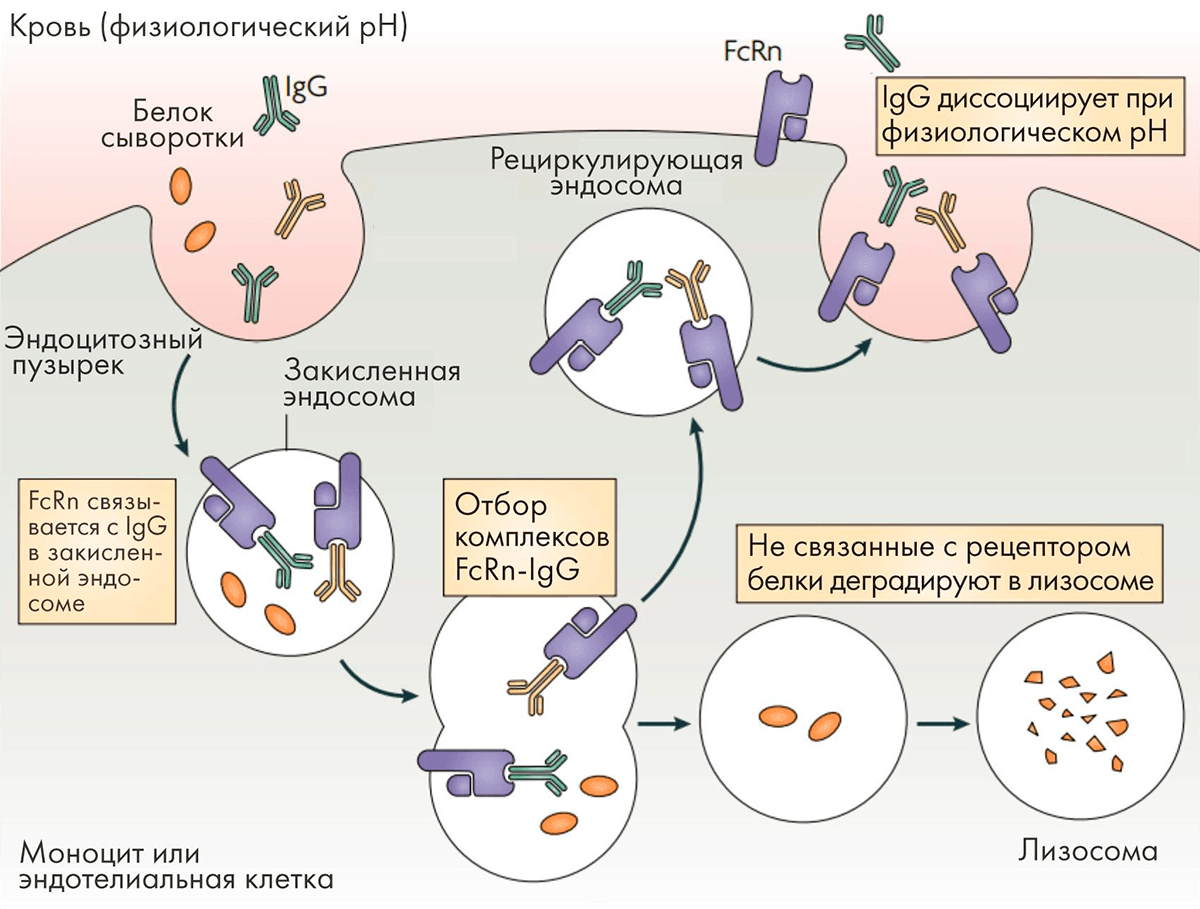
Специфические последовательности, расположенные в районе соединения доменов CH2 и CH3 молекулы IgG, отвечают за ее связывание с рецептором FcRn, которое в значительной мере определяет период полувыведения антитела. Этот удивительный рецептор экспрессируется на многих эндотелиальных и эпителиальных клетках и отвечает за транспорт антител через клеточные барьеры, а также за их возврат в кровоток [36]. Связывание Fc-фрагмента антитела с FcRn в кровотоке при рН 7,4 незначительно, тогда как в кислой среде в эндосомах (pH
Рисунок 9. Взаимодействие антител с рецептором FcRn
Именно поэтому антитела подклассов IgG1, IgG2 и IgG4, обладающие высоким сродством к FcRn, имеют период полувыведения из организма 21 день, а антитела подкласса IgG3 с более низким сродством к нему — всего 5–7,5 дней. Были найдены мутации, усиливающие связывание IgG1 с FcRn, что позволило еще больше продлить период полувыведения.
Иногда, наоборот, нужно ускорить выведение антитела из организма, например, если оно потенциально токсично. В таких случаях вводят мутации, снижающие сродство к FcRn [26].
Методы изучения свойств антител
Плазмонный резонанс
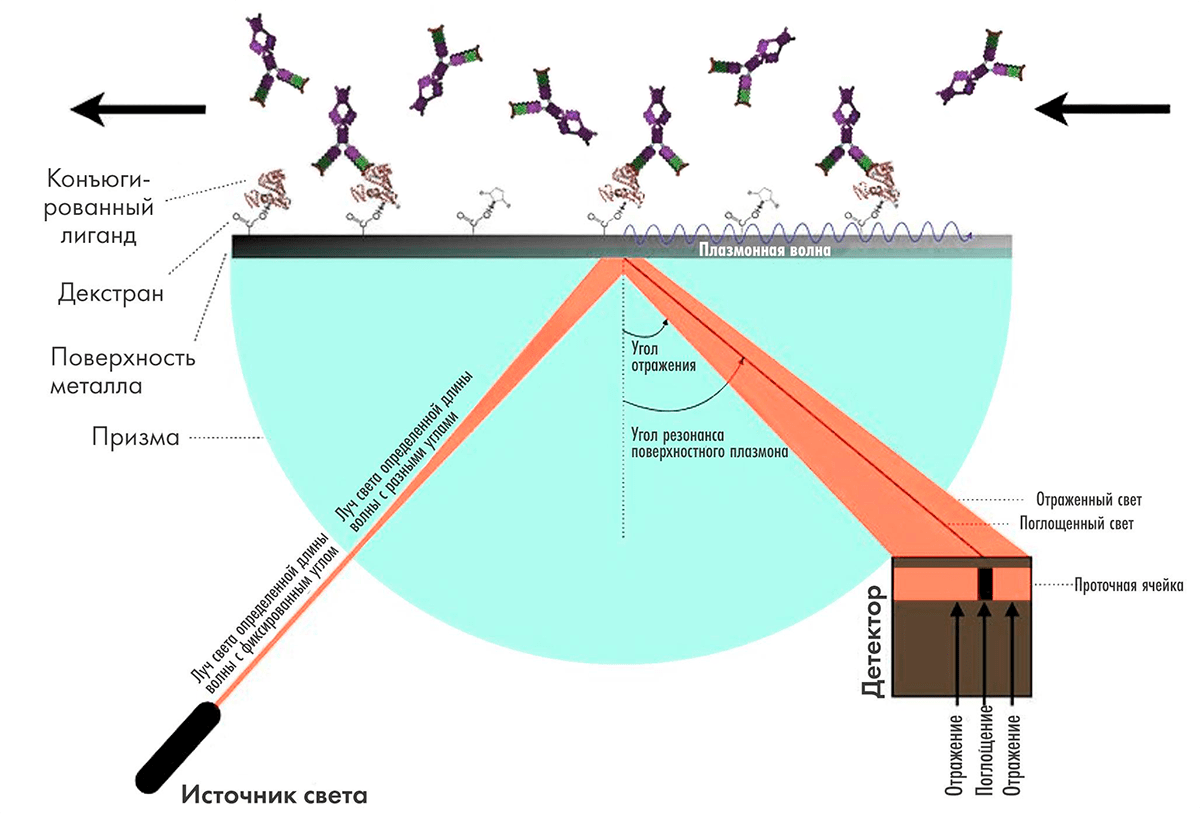
Основной метод изучения кинетики и аффинности связывания антигена с антителом — поверхностный плазмонный резонанс (surface plasmon resonance, SPR). Метод основан на том, что на поверхности металлов при возбуждении источником света под определенным углом возникает плазмон — электромагнитная волна, распространяющаяся вдоль поверхности. Угол, при котором он возникает, зависит от свойств среды в непосредственной близи от поверхности, поэтому адсорбция веществ на поверхности металла приводит к изменению этого угла, и таким образом ее можно измерять (рис. 10) [37].
Рисунок 10. Схема работы прибора на принципе поверхностного плазмонного резонанса. Излучение от источника с длиной волны 760 нм отражается от металлической подложки, на противоположной поверхности которой закреплена одна из двух взаимодействующих молекул. Один из углов отражения является резонансным, и явление поверхностного плазмонного резонанса приводит к снижению интенсивности отраженного под этим углом света. При связывании антитела с конъюгированным лигандом меняется показатель преломления среды вблизи поверхности, резонансный угол отражения изменяется, что регистрируется фотоэлементом.
Наилучшие параметры метода, которые используются в наиболее популярных приборах для плазмонного резонанса Biacore, достигаются при применении в качестве поверхности золотых пластинок толщиной 50 нм [37]. К слою золота ковалентно присоединяется декстрановая матрица, и молекула мишени иммобилизуется в декстране (разветвленном полимере глюкозы).
Использование метода решает следующие основные задачи:
Изучение плазмонного резонанса идеально подходит для скрининга, поскольку он не требует химических модификаций метками для измеряемых биологических молекул в растворе и хорошо автоматизируется.
На измерения также может повлиять скорость переноса антитела из подвижной фазы (буфера) в неподвижную (декстрановую матрицу), поэтому для подтверждения результата рекомендуется пользоваться независимым методом, например, KinExA, в котором измеряется взаимодействие антитела не с иммобилизованным антигеном, а со свободным [38–41].
Вторая проблема заключается в том, что свойства антитела и антигена в растворе и на поверхности отличаются от соответствующих свойств в организме, однако это фундаментальное затруднение характерно для всех аналитических методов in vitro.
Проточная цитофлуориметрия
Другой метод, который рутинно используют при разработке антител — FACS (fluorescence-activated cell-sorting — сортировка клеток с активацией флуоресценции или, по-другому, проточная цитофлуориметрия [32]). В случае антител с помощью FACS можно определить аффинность связывания с поверхностным рецептором клетки прямо на клеточной поверхности, не выделяя рецептор [40]. Это очень полезная особенность, так как поверхностные рецепторы являются мембранными белками, и манипуляции с ними in vitro сопряжены со множеством трудностей: для них требуется создавать особые условия, иначе они не сохраняют свою конформацию и агрегируют.
Для определения аффинности постоянное количество клеток, несущих рецептор, титруется возрастающей концентрацией антитела, при этом каждый раз устанавливается равновесие. Антитела, связавшиеся с клетками, детектируют с помощью других антител, меченых флуоресцентной меткой.
В связи с хорошей автоматизируемостью и высокой производительностью метода он хорошо подходит для скрининга библиотек клонов антител (см. раздел «Дисплейные методы»). Один и тот же клон проверяют на связывание с клетками, экспрессирующими и не экспрессирующими рецептор. Если отношение связывания больше определенного порога, клон отбирают для дальнейшей работы [41].
Методы in silico
После того, как методом дисплея получены фрагменты антител с высокой аффинностью к мишени, важно провести картирование эпитопов, то есть определение того, с каким участком мишени связываются антитела-кандидаты. Кандидаты, связывающиеся с разными участками мишени, лучше подходят для дальнейшего тестирования, так как в случае неудачи одного из кандидатов больше шансов, что другой кандидат будет успешен [42].
Экспериментальное картирование, например, с помощью мутагенеза или рентгено-структурного анализа — долгий и трудоемкий процесс, который не подходит для анализа кандидатов на начальном этапе. Поэтому прибегают к картированию эпитопов in silico — то есть компьютерному расчету эпитопов исходя из аминокислотной последовательности мишени, антиген-связывающего фрагмента антитела и сведений, содержащихся в базах данных эпитопов [43]. Алгоритмы на основе машинного обучения и больших баз данных белковых последовательностей и трехмерных моделей способны предсказывать как линейные, так и конформационные эпитопы. Точность таких предсказаний не стопроцентна, но для грубого отбора фрагментов-кандидатов она вполне достаточна.
Методы in silico применяют и на других стадиях разработки антител. Так, для поиска аминокислотных остатков, предположительно обусловливающих агрегацию антител, используют метод SAP (spatial aggregation propensity — пространственную склонность к агрегации). По этой технологии каждой аминокислоте в антителе присваивается величина SAP в зависимости от ее гидрофобности, степени доступности на поверхности, вкладов гидрофобных взаимодействий с другими аминокислотами в пределах заданного радиуса. Затем для антитела строится цветовая карта, из которой сразу видно, какие области молекулы отвечают за агрегацию. Экспериментально показано, что замена аминокислот в таких участках на более гидрофильные позволяет снизить агрегацию белка и тем самым улучшить его фармакологические свойства [44].
Для разработки стратегии гуманизации антитела также используют методы in silico. При вставке мышиной вариабельной последовательности в человеческий каркас аффинность антитела к антигену может быть снижена. В этом случае применяют «обратное» введение мутаций, отвечающих за более сильное связывание с антигеном. Такие мутации, в частности, можно выбирать путем статистического анализа последовательностей известных комплексов антитело—антиген [45].
Методы молекулярного моделирования с использованием расчета свободной энергии связывания антител с антигенами иногда используют на этапе созревания аффинности для поиска мутаций, обеспечивающих более высокую аффинность [46]. Эти методы предполагают применение энергетических функций, отражающих взаимодействия атомов антигена и антитела между собой. Такие функции могут быть или основаны на физических параметрах взаимодействия атомов, или рассчитаны исходя из статистических данных — как правило, извлеченных из трехмерных структур комплексов антиген—антитело [47]. Однако из-за сложности объекта моделирования и неизбежности многих допущений успехи в этой области пока не так велики, как хотелось бы.
Производство антител
Итак, мы получили генетическую конструкцию, кодирующую антитело с нужными нам свойствами, ввели ее в клетку-продуцент, получили в лаборатории нужные антитела и охарактеризовали их. Что же дальше? Теперь необходимо масштабировать производство и очистку антитела, чтобы получить его в достаточных количествах для последующих исследований, а потом, если все пойдет хорошо, и для продажи. Причем если в случае лабораторных процессов исследователи сами следят за их качеством, то как только лекарственный препарат доходит до стадии исследования токсичности на животных, он попадает под действие законодательства: регуляторные органы (FDA в США, Минздрав в РФ, EMA — Европейское медицинское агентство — в Евросоюзе и т. д.) принимают только такие исследования, которые соответствуют строгому набору правил. В частности, препарат должен быть произведен в соответствии с правилами GMP — Good manufacturing practice («Надлежащей производственной практики»). GMP регламентирует все аспекты производства, начиная от требований к устройству помещений и заканчивая контролем качества продукции. Регулятор имеет право в любой момент проверить соблюдение правил GMP производителем лекарства.
При производстве антител разработчики должны учитывать следующие критерии:
Более подробно об устройстве процесса производства рекомбинантных белков можно прочесть в статье на «Биомолекуле», посвященной Опытному биотехнологическому производству ИБХ [48].
Получение клона-продуцента
Для получения стабильного клона-продуцента антител разработчикам нужно добиться правильного встраивания вектора в геном клетки, модифицировать, если необходимо, аппарат трансляции и посттрансляционных модификаций (про модуляцию гликозилирования см. раздел «Гликозилирование»), добиться высокой жизнеспособности продуцента. В клетках CHO с этой целью снижали экспрессию про-апоптотических факторов и повышали экспрессию анти-апоптотических (например Bcl-2). Трансляцию белка увеличивали, сверхэкспрессируя шапероны, чтобы защитить клетку от апоптоза под воздействием стресса и обеспечить более правильное сворачивание антител [25]. Кроме того, в геном клетки-продуцента вносят модификации, обеспечивающие желаемый профиль гликозилирования.
После создания клеточной линии начинается подбор и оптимизация процесса культивирования, сначала в 96-луночных планшетах, затем в колбах и настольных биореакторах объемом 1–5 л. В результате скрининга сотен и тысяч клонов выбирают клон-продуцент с наилучшими характеристиками и переходят к пилотному культивированию в реакторах объемом 10–25 л, а затем масштабируют процесс до бóльших размеров (рис. 11) [49].
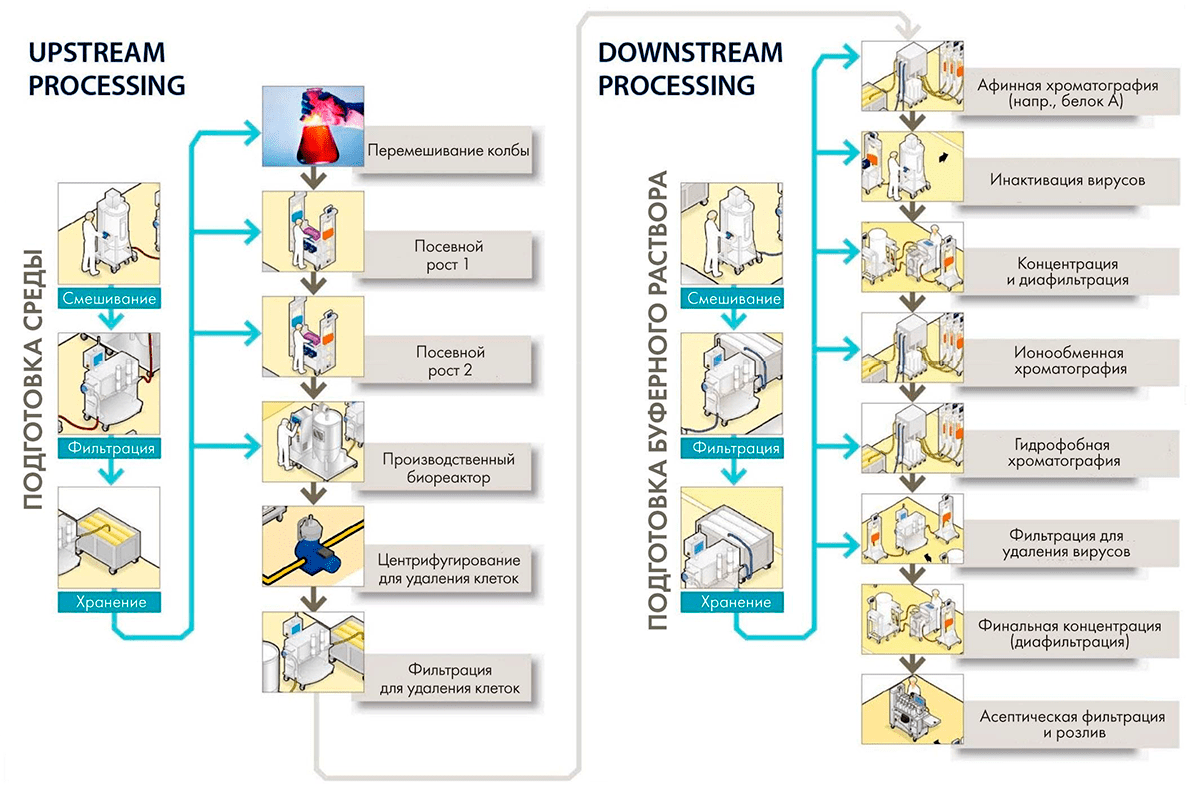
Рисунок 11. Производство антител и других рекомбинантных белков делится на две большие стадии: upstream process (USP), включающий все стадии от размораживания пробирки с клоном-продуцентом до сбора среды культивирования, и downstream process (DSP) — процесс выделения и очистки продукта.
Культивирование
Обычно клетки, производящие антитела, культивируют в биореакторах-ферментёрах объемом от 100 до 25 000 л (рис. 12). Традиционным способом культивирования являются процессы batch и fed-batch. В первом случае все компоненты среды и клон-продуцент загружают в реактор на несколько дней, после чего собирают культуральную среду для выделения белка. Во втором случае в среду периодически добавляют питательные вещества.
Рисунок 12. Внешний вид биореактора
Важнейшим фактором обеспечения высоких выходов белка является культуральная среда. Причем прогресс в этой области продолжается, и если в 1990-х годах выходы составляли 0,1 г/л, в 2007 — до 5 г/л, то сейчас удается достигать 10 и более г/л. Такие успехи стали возможны благодаря переходу от сред, содержащих сыворотку животных к бессывороточным: сначала использовались гидролизаты белков, а сейчас — полностью химические среды с четко определенным составом. Дело в том, что вариабельность состава ухудшает параметры культивирования. Также оказалось плодотворным изменение состава среды в зависимости от стадии культивирования: применяются разные среды в фазе роста и в фазе накопления продукта.
Для повышения продуктивности применяют также тонкую настройку параметров среды с обратной связью: температуры, рН, солевого состава, уровней O2 и CO2, что позволяет добиться снижения концентрации токсичных побочных продуктов (молочной кислоты, аммиака) и более плавного расхода питательных веществ.
В настоящее время наблюдается тенденция к переходу на непрерывные процессы: на так называемое перфузионное культивирование, при котором свежая среда непрерывно добавляется к клеточной культуре, а продукт удаляется из нее. Такой подход лучше автоматизируется, дает продукт более высокого качества и с увеличенными выходами. Также разработчики переходят от стальных биореакторов к одноразовым контейнерам, так как у последних есть ряд преимуществ:
Выделение и очистка антител
Антитела секретируются клетками-продуцентами в окружающую среду, и для получения чистого препарата требуется многоступенчатый процесс отделения антитела от всех ненужных и потенциально опасных примесей (рис. 11). Основными стадиями здесь являются различные виды хроматографии [50], диафильтрация и инактивация вирусов. Одна из особенностей очистки антител по сравнению с другими белками — использование хроматографии с белком А. Это белок клеточной стенки золотистого стафилококка, который сильно и селективно связывается с антителами при нормальном рН и слабо — при пониженном. Благодаря высоким выходам и чистоте получающегося продукта это предпочтительный метод на первом этапе очистки антител.
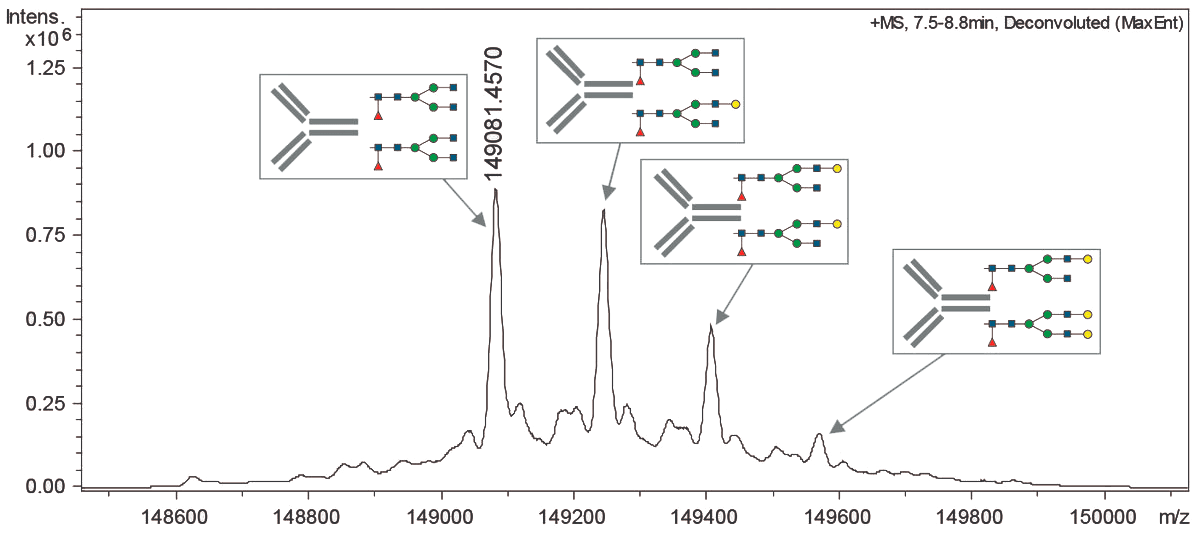
Важнейшим требованием и на стадии производства, и на стадии очистки антитела является постоянство состава продукта. Поскольку антитело — сложный объект и производится в биологической системе (в клетках), молекулы получаются не одинаковые, а с вариациями (рис. 13). Цель разработки процесса производства и очистки — добиться того, чтобы эти вариации не влияли на фармакологические характеристики продукта, его стабильность, и не слишком менялись от одной партии продукта к другой. Для этого проводится валидация процесса производства — экспериментальное подтверждение того, что процесс обеспечивает получение продукта с надлежащими характеристиками.
Рисунок 13. Профиль гликозилирования определяют методом масс-спектрометрии. На этом спектре видна типичная картина гетерогенности препарата антитела.
На некоторых промежуточных и на финальном этапе состав продукта контролируют аналитическими методами. Обязательно следят за:
Часть этих показателей входит в спецификацию на субстанцию, из которой затем получают лекарственный препарат.
Тем не менее описанные в этой статье технологии уже позволили создать десятки лекарственных препаратов, которые помогают миллионам людей — о чем подробно будет рассказано в следующей статье цикла.
Департамент вычислительной биологии компании BIOCAD — спонсор спецпроекта
BIOCAD — международная биотехнологическая компания, которая создала умную технологическую платформу, объединившую в себе компьютерное моделирование и современные принципы синтеза генов de novo.
В компании реализован полный цикл выпуска лекарственных препаратов: от поиска лекарственной молекулы до массового производства и маркетинговой поддержки.
Компания ведет два масштабных проекта:
Для разработки лекарственных препаратов BIOCAD применяет технологию structure-based drug design, использующую методы компьютерного моделирования. Это позволяет сделать поиск молекул направленным. С помощью математического моделирования отобранная молекула оптимизируется под конкретную мишень, а затем воспроизводится в реальной лаборатории.
В основе большинства разработок компании лежит математическое моделирование. То, что раньше было возможно осуществить исключительно in vitro в стенах лабораторий, по мнению исследователей BIOCAD, сегодня может быть воплощено in silico силой чистого разума.
Здесь собрали одну из лучших команд биоинформатиков в стране, которая занимается научными исследованиями, разрабатывает и внедряет новейшие методы интеллектуального анализа данных. В ее распоряжении один из мощнейших вычислительных кластеров, и если еще 2–3 года назад можно было только мечтать о решении задач направленного дизайна белковых молекул, то сейчас это одно из направлений работ Департамента вычислительной биологии.
Материал предоставлен партнёром — Департаментом вычислительной биологии компании BIOCAD