Чего больше протонов или нейтронов в атоме
15 самых интригующих фактов об атомах
Все во Вселенной — от ядра Земли до самых дальних галактик — состоит из атомов. Это фундаментальная единица элемента.
К настоящему времени было идентифицировано 118 элементов (все они перечислены в периодической таблице).
Слово «атом», означающее «неделимый», происходит от древнегреческого слова «ἄτομος». Древнегреческие философы считали, что атом невозможно разделить на что-то меньшее. Однако ученые доказали этот факт неправильно в начале 20 века, когда они открыли субатомные частицы (электроны, протоны, нейтроны).
Ниже мы перечислили некоторые из наиболее интригующих фактов об атомах, которые только сделают вас умнее. Так что давайте начнем с самого короткого и простого.
1. Состав атомов
Каждый атом содержит одно ядро [в центре] и один или несколько электронов. Ядро обычно состоит из равного числа протонов и нейтронов, вместе называемых нуклонами.
2. Ядро содержит почти всю массу
Ядро, расположенное в центре атома, составляет более 99,9 % его массы, но занимает лишь одну триллионную его общего объема. Таким образом, большая часть пространства внутри атома пуста.
3. Электроны чрезвычайно малы
Электрон является наиболее активным компонентом атома, но он почти ничего не вносит в массу атома. Например, в атоме водорода масса электрона составляет всего 0,0005 массы ядра.
4. Атом может иметь электрический заряд
Электроны несут отрицательный заряд, протоны несут положительный заряд, а нейтроны не имеют электрического заряда. Атом электрически нейтрален, если он имеет одинаковое количество электронов и протонов.
Однако, если атом имеет меньше или больше протонов, чем электронов, он имеет общий положительный или отрицательный заряд (известный как Ион).
5. Что удерживает протоны и нейтроны вместе?
Ядерная сила удерживает протоны и нейтроны вместе в ядре атома. Электроны притягиваются к протонам другой силой, называемой электромагнитной силой, которая слабее ядерной силы.
6. 94 Атома естественного происхождения на Земле
Из 118 известных атомов 94 встречаются в природе, хотя некоторые встречаются в незначительных количествах. Остальные 24 были синтезированы только в лабораториях или ядерных реакторах.
7. Каждый атом уникален
Каждый атом содержит определенное количество протонов в ядре. Например, все атомы натрия содержат 11 протонов, а все атомы серебра содержат 47 протонов.
Изотоп элемента определяется числом нейтронов, а магнитные характеристики зависят от количества электронов в атоме.
8. Самый большой и самый маленький атом
Самым большим элементом (по размеру) является Франций, но поскольку он крайне нестабилен, предпочтение отдается Цезию. У него большая валентная оболочка и относительно менее эффективный заряд ядра.
Иллюстрация атома гелия | Предоставлено: Викимедиа.
9. Самый тяжелый и легкий атом
Оганессон, однако, является самым тяжелым синтетическим химическим элементом. Самым тяжелым природным элементом является Уран с атомным весом 238,029.
Элемент, который имеет самый легкий атом-это водород. У него есть только один протон, обращающийся вокруг одного электрона. Его самый распространенный изотоп, известный как Протий, состоит из одного протона и нулевых нейтронов.
10. Возможно ли преобразовать один элемент в другой?
В некоторых экстремальных условиях электромагнитная сила (которая отталкивает электроны и протоны) преодолевает сильную ядерную силу, выбрасывая нуклоны из атомного ядра и оставляя после себя совершенно другой элемент. Это именно то, что происходит при делении ядер.
Однако этот процесс [распада] является дорогостоящим и опасным. Ученые пока не смогли безопасно генерировать энергию с помощью ядерного деления.
11. Атомы в человеческом теле
Тело человека весом 70 кг состоит из 7 × 10 27 атомов. Три атома (водород, кислород и углерод) составляют до 99 процентов от общего количества.
12. Сколько атомов существует во Вселенной?
Наблюдаемая вселенная огромна: она охватывает приблизительно 93 миллиарда световых лет. Согласно теоретической оценке, в нашей вселенной насчитывается от 10 78 до 10 82 атомов.
Это не какой-то выдуманный номер. Расчеты основаны на достоверных данных (что мы знаем о вселенной). Однако между этими оценками существует огромная разница, что говорит о значительной степени ошибки. Более точные цифры будут доступны, когда мы узнаем больше о космосе.
13. Радиоактивные атомы
В нестабильном атоме силы неуравновешенны. В этом случае атомное ядро содержит избыток либо протонов, либо нейтронов. Атом пытается достичь стабильного состояния, выбрасывая свои дополнительные частицы или высвобождая энергию в других формах. Элементы, содержащие такие нестабильные ядра, называются радиоактивными.
Фермий, например, является радиоактивным элементом: его самый стабильный изотоп (Fm-257) имеет период полураспада 100,5 суток.
14. Видя атомы
Поскольку атомы невероятно малы по сравнению с длиной волны видимого света, их нельзя наблюдать даже с самым мощным в мире оптическим микроскопом.
Сканирующий туннельный микроскоп захватывает атомы кремния на поверхности кристаллического карбида кремния
Вот почему ученые используют микроскоп другого типа, известный как сканирующий туннельный микроскоп. Он может обеспечить боковое разрешение 0,1 нм и разрешение по глубине 0,01 нм, что достаточно для изображения отдельных атомов в материалах.
15. Квантовая природа атомных свойств
Поскольку атомы чрезвычайно малы по размеру, они проявляют квантовые свойства, поэтому предсказание их поведения с применением классической физики всегда приведет к неверным результатам.
Когда электрон прыгает с одного энергетического уровня (орбиты) на другой, он не перемещается в пространстве между ними. Вместо этого он исчезает с одной орбиты, а затем сразу же появляется на другой орбите.
Чтобы лучше описать и оценить их поведение, несколько атомных моделей включили в себя законы квантовой физики.
Протоны и нейтроны: столпотворение внутри материи
В центре каждого атома находится ядро, крохотный набор частиц под названием протоны и нейтроны. В этой статье мы изучим природу протонов и нейтронов, состоящих из частиц ещё мельче размером – кварков, глюонов и антикварков. (Глюоны, как и фотоны, являются античастицами сами себе). Кварки и глюоны, насколько нам известно, могут быть по-настоящему элементарными (неделимыми и не состоящими из чего-то мельче размером). Но к ним позже.
Как ни удивительно, у протонов и нейтронов масса почти одинаковая – с точностью до процента:
Поскольку они так похожи, и поскольку из этих частиц состоят ядра, протоны и нейтроны часто называют нуклонами.
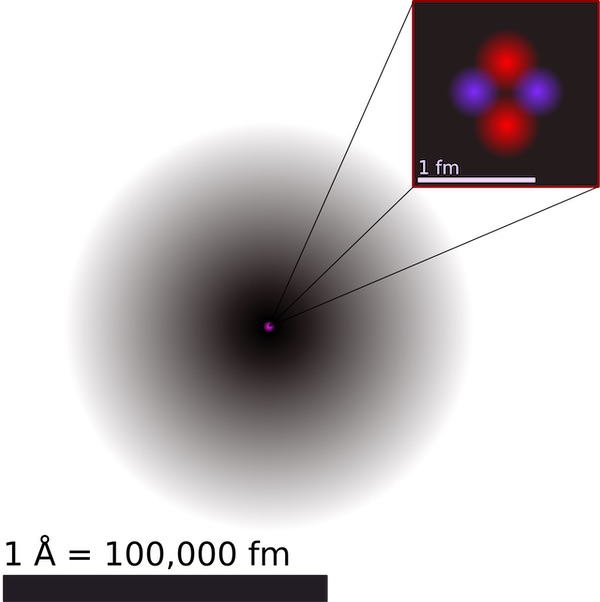
Протоны идентифицировали и описали примерно в 1920 году (хотя открыты они были раньше; ядро атома водорода – это просто отдельный протон), а нейтроны нашли где-то в 1933-м. То, что протоны и нейтроны так похожи друг на друга, поняли почти сразу. Но то, что у них есть измеримый размер, сравнимый с размером ядра (примерно в 100 000 раз меньше атома по радиусу), не знали до 1954-го. То, что они состоит из кварков, антикварков и глюонов, постепенно понимали с середины 1960-х до середины 1970-х. К концу 70-х и началу 80-х наше понимание протонов, нейтронов, и того, из чего они состоят, по большей части устаканилось, и с тех пор остаётся неизменным.
Нуклоны описать гораздо труднее, чем атомы или ядра. Не сказать, что атомы в принципе простые, но по крайней мере, можно сказать, не раздумывая, что атом гелия состоит из двух электронов, находящихся на орбите вокруг крохотного ядра гелия; а ядро гелия – достаточно простая группа из двух нейтронов и двух протонов. А вот с нуклонами всё уже не так просто. Я уже писал в статье «Что такое протон, и что у него внутри?», что атом похож на элегантный менуэт, а нуклон – на дикую вечеринку.
Сложность протона и нейтрона, судя по всему, всамделишные, и не проистекают из неполных физических знаний. У нас есть уравнения, используемые для описания кварков, антикварков и глюонов, а также сильных ядерных взаимодействий, происходящих между ними. Эти уравнения называются КХД, от «квантовая хромодинамика». Точность уравнений можно проверять различными способами, включая измерение количества появляющихся на Большом адронном коллайдере частиц. Подставляя уравнения КХД в компьютер и запуская вычисления свойств протонов и нейтронов, и других сходных частиц (с общим названием «адроны»), мы получаем предсказания свойств этих частиц, хорошо приближающиеся к наблюдениям, сделанным в реальном мире. Поэтому у нас есть основания полагать, что уравнения КХД не врут, и что наше знание протона и нейтрона основано на верных уравнениях. Но просто иметь правильные уравнения недостаточно, ибо:
Из-за внутренней сложности нуклонов вам, читатель, придётся сделать выбор: как много вы хотите узнать по поводу описанной сложности? Неважно, как далеко вы зайдёте, удовлетворения это вам, скорее всего, не принесёт: чем больше вы будете узнавать, тем понятнее вам будет становиться тема, но итоговый ответ останется тем же – протон и нейтрон очень сложны. Я могу предложить вам три уровня понимания, с увеличением детализации; вы же можете остановиться после любого уровня и перейти на другие темы, или можете погружаться до последнего. По поводу каждого уровня возникают вопросы, ответы на которые я могу частично дать в следующем, но новые ответы вызывают новые вопросы. В итоге – как я делаю в профессиональных обсуждениях с коллегами и продвинутыми студентами – я могу лишь отослать вас к данным полученным в реальных экспериментах, к различным влиятельным теоретическим аргументам, и компьютерным симуляциям.
Первый уровень понимания
Из чего состоят протоны и нейтроны?

Рис. 1: чрезмерно упрощённая версия протонов, состоящих только из двух верхних кварков и одного нижнего, и нейтронов, состоящих только из двух нижних кварков и одного верхнего
Чтобы упростить дело, во многих книгах, статьях и на сайтах указано, что протоны состоят из трёх кварков (двух верхних и одно нижнего) и рисуют нечто вроде рис. 1. Нейтрон такой же, только состоящий из одного верхнего и двух нижних кварков. Это простое изображение иллюстрирует то, во что верили некоторые учёные, в основном в 1960-х. Но вскоре стало понятно, что эта точка зрения чрезмерно упрощена до такой степени, что уже не является корректной.
Из более искушённых источников информации вы узнаете, что протоны состоит из трёх кварков (двух верхних и одного нижнего), удерживаемых вместе глюонами – и там может появиться картинка, похожая на рис. 2, где глюоны нарисованы в виде пружинок или ниток, удерживающих кварки. Нейтроны такие же, только с одним верхним кварком и двумя нижними.

Рис. 2: улучшение рис. 1 за счёт акцента на важной роли сильного ядерного взаимодействия, удерживающего кварки в протоне
Не такой уж плохой способ описания нуклонов, поскольку он делает акцент на важной роли сильного ядерного взаимодействия, удерживающего кварки в протоне за счёт глюонов (точно так же, как с электромагнитным взаимодействием связан фотон, частица, из которых состоит свет). Но это тоже сбивает с толку, поскольку на самом деле не объясняет, что такое глюоны и что они делают.
Есть причины двигаться дальше и описывать вещи так, как я делал в других статьях: протон состоит из трёх кварков (двух верхних и одного нижнего), кучи глюонов и горы пар кварк-антикварк (в основном это верхние и нижние кварки, но есть и несколько странных). Все они летают туда и сюда с очень большой скоростью (приближаясь к скорости света); весь этот набор удерживается при помощи сильного ядерного взаимодействия. Я продемонстрировал это на рис. 3. Нейтроны опять такие же, но с одним верхним и двумя нижними кварками; изменивший принадлежность кварк указан стрелкой.

Рис. 3: более реалистичное, хотя всё равно неидеальное изображение протонов и нейтронов
Эти кварки, антикварки и глюоны не только бешено носятся туда-сюда, но и сталкиваются друг с другом, и превращаются друг в друга через такие процессы, как аннигиляция частиц (в которой кварк и антикварк одного типа превращаются в два глюона, или наоборот) или поглощение и испускание глюона (в котором могут столкнуться кварк и глюон и породить кварк и два глюона, или наоборот).
Что у этих трёх описаний общего:
В некотором смысле рис. 2 пытается устранить разницу между рис. 1 и рис. 3. Он упрощает рис. 3, удаляя множество пар кварк-антикварк, которые, в принципе, можно назвать эфемерными, поскольку они постоянно возникают и исчезают, и не являются необходимыми. Но она производит впечатление того, что глюоны в нуклонах являются непосредственной частью сильного ядерного взаимодействия, удерживающего протоны. И она не объясняет, откуда берётся масса протона.
У рис. 1 есть другой недостаток, кроме узких рамок протона и нейтрона. Она не объясняет некоторые свойства других адронов, к примеру, пиона и ро-мезона. Те же проблемы есть и у рис. 2.
Эти ограничения и привели к тому, что своим студентам и на моём сайте, я даю картинку с рис. 3. Но хочу предупредить, что и у неё есть множество ограничений, которые я рассмотрю позже.
Масса протона и масса нейтрона
Поскольку массы протона и нейтрона так похожи, и поскольку протон и нейтрон отличаются только заменой верхнего кварка нижним, кажется вероятным, что их массы обеспечиваются одним и тем же способом, исходят из одного источника, и их разница заключается в небольшом отличии между верхним и нижним кварками. Но три приведённых рисунка говорят о наличии трёх очень разных взглядов на происхождение массы протона.
Рис. 2 менее понятен. Какая часть массы протона существует благодаря глюонам? Но, в принципе, из рисунка следует, что большая часть массы протона всё равно происходит от массы кварков, как на рис. 1.
Рис. 3 отражает более тонкий подход к тому, как на самом деле появляется масса протона (как мы можем проверить напрямую через компьютерные вычисления протона, и не напрямую с использованием других математических методов). Он сильно отличается от идей, представленных на рис. 1 и 2, и оказывается не таким простым.
Полезно классифицировать взносы в энергию массы протона по трём группам:
А) Энергия массы (энергия покоя) содержащихся в нём кварков и антикварков (глюоны, безмассовые частицы, никакого вклада не делают).
Б) Энергия движения (кинетическая энергия) кварков, антикварков и глюонов.
В) Энергия взаимодействия (энергия связи или потенциальная энергия), хранящаяся в сильном ядерном взаимодействии (точнее, в глюонных полях), удерживающих протон.
Рис. 3 говорит о том, что частицы внутри протона двигаются с большой скоростью, и что в нём полно безмассовых глюонов, поэтому вклад Б) больше А). Обычно, в большинстве физических систем Б) и В) оказываются сравнимыми, при этом В) часто отрицательно. Так что энергия массы протона (и нейтрона) в основном получается из комбинации Б) и В), а А) вносит малую долю. Поэтому массы протона и нейтрона появляются в основном не из-за масс содержащихся в них частиц, а из-за энергий движения этих частиц и энергии их взаимодействия, связанной с глюонными полями, порождающими силы, удерживающие протон. В большинстве других знакомых нам систем баланс энергий распределён по-другому. К примеру, в атомах и в Солнечной системе доминирует А), а Б) и В) получаются гораздо меньше, и сравнимы по величине.
Подводя итоги, укажем, что:
Обратите внимание, что это означает (противореча рис. 1), что отношение массы нижнего кварка к верхнему не приближается к единице! Масса нижнего кварка как минимум в два раза превышает массу верхнего. Причина того, что массы нейтрона и протона так похожи, не в том, что похожи массы верхнего и нижнего кварков, а в том, что массы верхнего и нижнего кварков очень малы – и разница между ними мала, по отношению к массам протона и нейтрона. Вспомните, что для превращения протона в нейтрон, вам нужно просто заменить один из его верхних кварков на нижний (рис. 3). Этой замены достаточно для того, чтобы сделать нейтрон немного тяжелее протона, и поменять его заряд с +е на 0.
Кстати, тот факт, что различные частицы внутри протона сталкиваются друг с другом, и постоянно появляются и исчезают, не влияет на обсуждаемые нами вещи – энергия сохраняется в любом столкновении. Энергия массы и энергия движения кварков и глюонов может меняться, как и энергия их взаимодействия, но общая энергия протона не меняется, хотя всё внутри него постоянно меняется. Так что масса протона остаётся постоянной, несмотря на его внутренний вихрь.
На этом моменте можно остановиться и впитать полученную информацию. Поразительно! Практически вся масса, содержащаяся в обычной материи, происходит из массы нуклонов в атомах. И большая часть этой массы происходит из хаоса, присущего протону и нейтрону – из энергии движения кварков, глюонов и антикварков в нуклонах, и из энергии работы сильных ядерных взаимодействий, удерживающих нуклон в целом состоянии. Да: наша планета, наши тела, наше дыхание являются результатом такого тихого, и, до недавнего времени, невообразимого столпотворения.
Строение атома
История открытия. Демокрит. Начала атомистики
Уже в древности философы задумывались, из чего же состоит природа вокруг них. Демокрит первым из античных ученых предположил, что все в мире состоит из крошечных неделимых частиц. Эту частицу он назвал атом, что в переводе с греческого означает «неделимый».
К сожалению, возможности ученых в те времена были весьма ограничены. Каких-либо приборов, позволяющих исследовать строение вещества, у них не было. Но значение Демокрита в зарождении атомистики невозможно сбросить со счетов истории.
Атомно-молекулярное учение. Строение атома
Практически до середины XVIII века, пока М.В. Ломоносов не принес в химию количественные эксперименты, учение об атомах оставалось лишь прерогативой философских размышлений. Михаил Васильевич считал, что лишь знание физических законов поможет правильно истолковать результаты химических опытов.
В своих исследованиях ученый выделил в веществе крупные частицы — «корпускулы», и мелкие — «элементы», или как мы называем их сейчас — атомы.
Ломоносов считал, что каждая молекула по своему составу идентична всему веществу, а также, что различные по химическому строению элементы имеют и разные по составу молекулы. Ученый предполагал, что вещества имеют особенности не только из-за отличий в составе молекул, но и благодаря различному расположению атомов в молекуле.
Следующий шаг в изучении атомов сделал английский естествоиспытатель Джон Дальтон. Проводя различные эксперименты с растворением газов в жидкостях, ученый открыл главное физическое качество атомов: эти мельчайшие частицы имеют вес. Но поскольку атом до сих пор никто не видел, Дальтон назвал вес частицы относительным. Он установил, что самым легким элементом является водород и предложил его вес принять за единицу.
Открытие Дальтона стало прорывом в химии. Ведь теперь к любому химическому соединению можно было подойти с измерительным прибором. Это исследование позволило приблизиться к современной записи химических формул и уравнений. И именно Дальтон придумал первые обозначения для известных химических элементов.
До конца XIX века, несмотря на все старания ученых, химическое строение атома по-прежнему оставалось лишь гипотезой.Ученым не хватало оборудования, чтобы постичь тайну мельчайшей частицы.
Открытие Дальтона дало толчок дальнейшим опытам, в ходе которых ученые вычислили относительную атомную массу разнообразных химических элементов, что позволило их классифицировать, а Д.И.Менделееву – сформулировать периодический закон и представить научному миру Периодическую систему химических элементов.
Протоны и нейтроны
Обнаружение катодных лучей немецким ученым-физиком Юлиусом Плюккером в 1859 году и создание прототипа электронной трубки Ульямом Круксом в 1879 году положили новый виток исследованиям в атомистике.
Однако потребовалось еще несколько десятков лет, чтобы строение атомов химических элементов приоткрыло свои тайны. на заре XX века в одном журнале появились две публикации, которые пытались объяснить структуру атома. Одна из публикаций принадлежала английскому ученому Д.Д. Томсону, автором другой был японский физик Хантаро Нагаока.
При создании своей атомной структуры Нагаока использовал разработанную Максвеллом в 1856 году теорию устойчивости колец Сатурна. Японский ученый был убежден, что опираясь на «сатурнианскую» модель ядра в будущих исследованиях, можно прояснить все основные свойства материи.
Исследователь ошибся, однако два постулата его теории впоследствии подтвердились:
Томсон выдвинул гипотезу о том, что атом напоминает шарообразную, электронейтральную сферу диаметром около 10 –10 м, где положительный заряд равномерно распределен по всей структуре атома, а электроны хаотично расположены в этом поле. Поэтому, можно сказать, что атом напоминает микроскопическую булочку с изюмом.
Опыты продолжались в разных странах. В лаборатории Резерфорда проходили испытания, которые смогли доказать, что в центре атома расположено крупное ядро с диаметром около —10 —15 м, в котором содержится более 99,95 % его массы, а заряд его положительный.
В 1932 году и Джеймс Чедвик обнаружил нейтрон — третий недостающий элемент атома.
Атомное взаимодействие обеспечивает тесную связь протонам и нейтронам в ядре атома. Протоны и нейтроны имеют общее название — нуклоны. Ученые считают, что их характеристики достаточно подобны, чтобы отнести эти частицы к одному семейству, как биологи относят в один вид собак и волков.
Казалось бы, вот оно – тайна ядра разгадана. Но нет, в современной физике считается, что нуклоны состоят из еще более мелких частиц, которые называют кварками, и кварковая модель является ведущей в современной науке.
Эксперименты по исследованию атома и его ядра не прекращаются, и в 2010 году международная группа физиков при исследовании протонов в мюонном водороде установила, что размер радиуса протона меньше на 4%, чем считалось до этого.
Так в фундаментальную физику ворвалась загадка протонного радиуса, почему измерение одной и той же величины в обычном и в мюонном водороде дает разные результаты — и, несмотря на усилия сотен специалистов, она до сих пор не решена.
Изотопы
Работая в лаборатории Резерфорда, Фредерик Содди экспериментально установил, что встречаются атомы одного химического элемента с различной атомной массой. А поскольку к этому времени уже было известно, что количество протонов для ядра постоянно, соответственно, отличались они количеством нейтронов.
Содди предложил термин изотоп (от греческих слов изос — «равный» и топос — «место») для обозначения веществ, идентичных по химическим свойствам, но отличающихся атомной массой и определенными физическими свойствами.
При графической записи изотоп выглядит как знак химического элемента, которому он соответствует. А что бы обозначить разницу, в массовом числе используют индекс слева вверху: ( 12 C, 222 Rn)
Протий, дейтерий, и тритий — исторические собственные названия изотопов водорода.
Электронное строение атома
Исследование таинственного микромира продолжается. Изучение движения электронов и внутриатомных взаимодействий выделилось в отдельную область физики — квантовую механику. Главный постулат квантовой механики — все волны обладают свойствами частиц, а микрочастицы имеют волновую природу.
В макромире физическое тело всегда находится в какой-то конкретной точке пространства. Даже если вы сфотографируете летящую муху и на фотографии она будет в виде черной полосы, вы все равно будете уверены, что в конкретный момент времени она была в определенном месте.
В мире атома все иначе. Легкий подвижный электрон находится одновременно во всех точках околоядерного пространства. Если провести аналогию с макромиром, больше всего это напомнит неплотный клубок мягкой пушистой шерсти.
И именно эта зона пространства, где существует вероятность встретить электрон, называется электронным облаком. Плотность электронного облака неравномерна.
В электронном облаке выделяют зону, где вероятность встречи с электроном более 90% — эта область обозначена как атомная или электронная орбиталь.
Все электроны в атоме обладают определенной энергией. Чтобы описать состояние электрона, ученые используют квантовые числа. Всего их четыре. Целое число n, которое определяет энергию электронов на конкретном энергетическом уровне, называют главным квантовым числом.
На одной электронной оболочке находятся атомные орбитали с единым значением главного квантового числа n.
У невозбужденного атома электроны расположены на орбиталях 4-х видов: s, p, d и f.
Но почему нельзя было обозначить буквами по алфавиту a, b, c? Все не так просто, для обозначения атомных орбиталей ученые решили использовать начальные буквы от прилагательных, описывающих спектральные линии в атомных спектрах:
Чтобы графически представить расположение электронов на уровнях и подуровнях атомной оболочки, ученые ввели электронные формулы. Это такие численно-буквенные комбинации, где подуровень обозначен строчной латинской литерой, а цифровой индекс вверху справа обозначает количество электронов на подуровне.
Несмотря на свои способности быть одновременно в любой точке пространства, электроны при заполнении орбиталей соблюдают определенный порядок:
У этого правила есть еще одно мнемоническое название — правило троллейбуса. Расположение электронов напоминает рассадку в общественном транспорте. Если есть свободные места и человек входит один, он сядет на свободное сиденье, и только если нет свободных сидений, подсядет к кому-то на свободное место.
Итак, подведем выводы, на которые ученым понадобилось более сотни лет опытов, исследований, научных дискуссий и даже трагедий.
Чтобы проверить насколько хорошо усвоен материал, предлагаем вашему вниманию тест на тему «Строение атома» для 8-11 классов: