Чего больше органических или неорганических веществ
Органические и неорганические вещества – что это и отличия
Органические и неорганические вещества – эти термины знакомы каждому человеку из школьной программы по биологии или химии. Также о них слышали садоводы. Что представляют собой и чем отличаются подобные вещества, способны объяснить не все. Для того чтобы лучше разобраться в особенностях и понять нюансы, рекомендуется сначала дать определение для каждого из рассматриваемых понятий, а затем провести сравнение по ключевым характеристикам.
Определение понятий
Органические вещества – соединения, которые имеют сложную химическую структуру (молекулярное строение). Они имеют невысокую температуру плавления, при воздействии высоких температур распадаются на несколько простых компонентов. Реакция протекает с выделением углекислого газа и воды. В молекулах присутствуют углерод и водород. Происхождение природное.
Неорганические вещества – химические соединения, имеющие простое молекулярное строение и небольшую массу. Температуры плавления высокие. Разложение происходит длительное время. Природа происхождения как биологическая, так и искусственная (промышленность).
Сравнение
Некоторые отличия между органикой и неорганическими веществами стала понятна из приведенных определений, но для более подробного разбора и выявления отличий, следует провести сравнение. Органика распадается за короткий промежуток времени на простые составные элементы – белки, углеводы, липиды. Разнообразие органики – результат наличия в ее молекулах углерода. Органические вещества способны к процессу изометрии. В результате образуются соединения, которые имеют одинаковый набор атомов в молекулах. Достичь разнообразия в этом случае позволяет различное положение атомов в молекулах образовавшихся веществ. Самыми распространенными являются такие соединения, как фруктоза и глюкоза. В них находится одинаковый набор атомов, но расположение отличается, поэтому свойства этих компонентов и их работа в химических реакциях различаются.
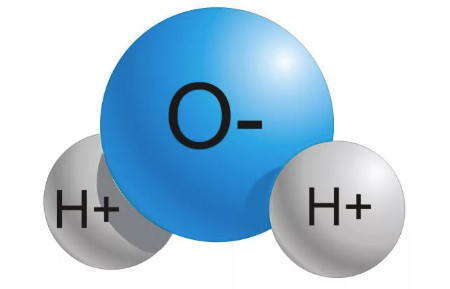
Неорганические вещества, самым распространенным из которых является вода, обладают небольшой молекулярной массой. Неорганики по современной классификации насчитывается всего около 100 тысяч, против органических соединений, которых представлено более 18 млн. Неорганические составляющие не способы к процессам изометрии. К неорганике также относятся различные металлы, соли, оксиды, различные смеси и простые вещества.
Выводы
Проведя сравнение, можно с уверенностью сказать, что различия между органическими и неорганическими веществами выражены в особенностях молекулярной структуры. Температура плавления и скорость разложения также являются факторами, указывающими на различия между рассматриваемыми понятиями. Наличие таких составляющих как водород и углерод характерны для органических соединений. Происхождение неорганики не всегда природное, многие компоненты являются плодом технических, производственных и научных изысканий. Общее количество неорганических веществ составляет по современной классификации 100 тысяч. Органика же превосходит числом, таких элементов в классификации представлено более чем в 10 раз больше. Органика имеет сложную структуру молекулярной сетки, неорганика — простую. Для того чтобы запустить процессы разложения в первом случае не требуется нагрева до высоких температур (например, мясо портиться при комнатной температуре, а для плавления металлов требуется длительный нагрев).
В состав молекул всех органических веществ входит углерод, но нужно учитывать и особенности этой группы компонентов. Так в карбидах или цианидах нет этого элемента. Уникальным свойством углерода является способность образовывать цепочки из атомов. Благодаря подобной способности соединений из одного и того же атомного набора может появляться очень много.
Разнообразие веществ. Простые и сложные, неорганические и органические вещества
Веществ существует очень много. Если химических элементов более ста, то веществ — более 10000000! Чтобы облегчить изучение и использование веществ, их разделяют на группы (классифицируют).
Какие вещества относятся к простым?
Вещества разделяют на простые и сложные. Рассмотрим примеры таких веществ: углерод, железо, кислород. Углерод образован атомами углерода. Из него изготавливают графитовые стержни карандашей. Железо, из которого сделано гвоздь, состоит из атомов железа. Эти тела, а следовательно, и вещества, из которых они образованы, вы видели не раз. Кислород мы не видим, но его недостаток чувствуем сразу. Это вещество состоит из молекул кислорода, образованных атомами кислорода.
Каждое из рассмотренных веществ образовано атомами одного химического элемента. Графит образуют атомы углерода, железо — атомы железа, кислород — атомы кислорода. Такие вещества называют простыми.
Молекулы некоторых простых веществ состоят из нескольких атомов. Например, молекула водорода состоит из двух атомов водорода, молекула кислорода — из двух атомов кислорода. Но несмотря на это, они остаются простыми веществами, так как их молекулы образовали атомы одного химического элемента.
Сложные вещества
Вещества, образованные из атомов двух и более химических элементов, называют сложными. Например, каждая молекула воды содержит два атома водорода и один атом кислорода. Ее состав обозначают записью H2O, который читается «аш-два-о».
Другим примером сложных веществ является углекислый газ. Его выдыхают все живые организмы, а растениям он нужен для питания. Молекула углекислого газа образована одним атомом углерода и двумя атомами кислорода. Этот состав молекулы отражают записью СО2, который читается «це о два».
Почему сложных веществ больше, чем простых?
Ученые доказали, что атомы различных химических элементов способны соединяться друг с другом в разном количестве и последовательности. Подобно тому, как в языке сочетанием букв образуется разнообразие слов, сочетанием различных атомов и в разном количестве образовалось более 10000000 веществ. Так что неудивительно, что сложных веществ существует гораздо больше, чем простых.
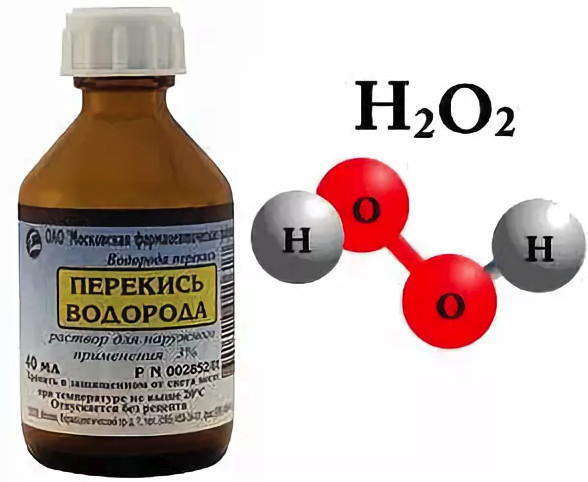
Рассмотрим еще раз рисунок и увидим, что молекула воды состоит из двух атомов водорода и одного атома кислорода. Из таких же атомов состоит и вещество водород пероксида, однако она имеет совсем другие свойства, чем вода. Например, водород пероксида имеет температуру кипения выше на 50°С, обладает обеззараживающими свойствами. Ни одна аптечка не обходится без него, ведь раствором этого вещества под названием «перекись водорода» обрабатывают раны, чтобы они быстрее заживали. Такие отличные от воды свойства перекиси водорода обусловленные различиями в строении его молекулы. Ведь молекула этого вещества состоит из двух атомов водорода и двух атомов кислорода.
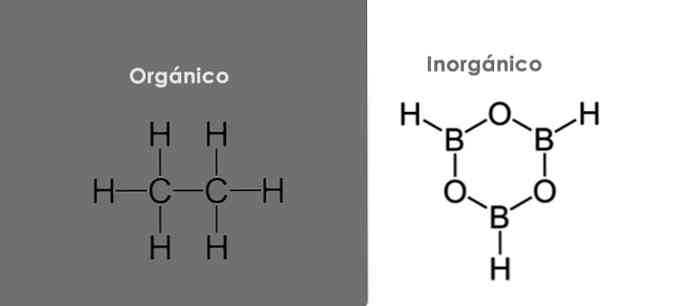
Органические и неорганические вещества
Вещества разделяют также на органические и неорганические. В состав всех органических веществ входят атомы углерода и, чаще всего, водорода. Так, из них образованы природный газ, вещества в составе нефти. В составе многих органических веществ содержатся еще и атомы кислорода. Это жиры, крахмал, сахар, уксус и другие. В состав важных для живых существ белков, кроме упомянутых элементов, обязательно входит азот.
Откуда такое название — органические вещества? Все очень просто. Первые из этих веществ ученые обнаружили в организмах — телах живой природы.
Есть и исключения. Некоторые вещества, содержащие атомы углерода, относят к неорганическим. Примерами являются углекислый газ, сода и еще несколько веществ.
Все тела природы, за исключением горных пород, воздуха и воды, состоят из органических веществ. Среди них больше всего углеводов (например, глюкозы и сахарозы), жиров (например, масла), белков (например, белок куриного яйца).
Многие органические вещества человек создал сам, например пластмассы, резину, полиэтилен. Они широко используются в машино- и самолетостроении, при сооружении зданий и мостов, а также в быту.
Без атомов углерода не существует никакой органического вещества. Так, атомы углерода вместе с атомами водорода и кислорода входят в состав органического вещества сахара, или сахарозы. Причем 1 молекула сахарозы состоит из 45 атомов. Среди них 12 атомов углерода, 22 атома водорода и 11 атомов кислорода. В том, что в составе сахара содержатся атомы углерода, убеждает черный цвет при сгорания кусочка сахара. Картофель или мясо, под действием высоких температур также обугливаются, приобретая черный цвет. Это является доказательством наличия углерода в составе органических веществ продуктов питания.
Заключение
Вещества разделяют на простые и сложные. Простые вещества образуются из атомов одного химического элемента. Сложные вещества образуются из атомов различных химических элементов.
Одной из классификаций веществ является разделение их на органические и неорганические. Органические вещества обязательно содержат атомы углерода.
Белки, жиры, углеводы — жизненно необходимые человеку органические вещества.
Различия между органическими и неорганическими соединениями
Основное различие между органическими и неорганическими соединениями это присутствие атома углерода.
Органические соединения содержат атом углерода и обычно также имеют атом водорода с образованием углеводородов. Со своей стороны, почти ни одно из неорганических соединений не содержит атомов углерода и / или водорода..
Основные различия между органическими и неорганическими соединениями
Хотя подавляющее большинство неорганических соединений не содержат углерода, есть некоторые исключения. Например, окись углерода и двуокись углерода содержат атомы углерода.
Однако этого количества недостаточно для образования прочных связей с кислородом, присутствующим в молекуле. Из-за этого ученые всегда считали эти соединения неорганическими. Поэтому, даже если соединение содержит уголь, оно не обязательно считается органическим.
Со своей стороны, неорганические соединения включают такие элементы, как соли, металлы и другие необходимые компоненты. Вещества, изготовленные из отдельных элементов, и любое соединение, которое не имеет атомов углерода, связанных с атомами водорода, также считаются неорганическими.
Несмотря на эти характеристики, химики-органики не достигли окончательного согласия между разницей между органическими и неорганическими соединениями. Будучи спорным вопросом, они называют присутствие углерода в молекуле наиболее приемлемым методом идентификации..
Органические соединения
В этих соединениях один или несколько атомов углерода присоединены к атомам других элементов. Наиболее распространенными элементами, к которым они присоединены, обычно являются водород, кислород и азот. Те немногие соединения, которые содержат углерод и не считаются органическими, представляют собой цианиды, карбонаты и карбиды..
Традиционно считается, что органические соединения имеют большое значение, поскольку вся известная жизнь основана на органических соединениях. Самые основные нефтехимические вещества рассматриваются в качестве основы органической химии.
Есть несколько соединений, которые считаются органическими, хотя они не имеют связи водорода и углерода. К ним относятся бензолексол, мезоксалевая кислота и четыреххлористый углерод.
Органические соединения можно классифицировать на природные и синтетические соединения..
Природные соединения
Они относятся к тем соединениям, которые вырабатываются растениями и животными. Многие из этих соединений извлекаются из природных источников, потому что было бы очень дорого производить их искусственно.
Наиболее распространенными являются сахара, некоторые алкалоиды и питательные вещества, такие как витамин B12. Как правило, все они представляют собой соединения, которые имеют большие или сложные молекулы и которые можно найти в разумных количествах в живых организмах..
Синтетические соединения
Соединения, которые получают реакцией других соединений, считаются синтетическими. Это могут быть соединения, встречающиеся в природе, или соединения, которые не встречаются в природе..
Большинство полимеров, таких как пластмассы и резина, являются полусинтетическими органическими соединениями..
биотехнология
Многие органические соединения, такие как этанол и инсулин, производятся в промышленности с использованием организмов из бактерий и дрожжей. Обычно ДНК организма изменяется, чтобы выразить соединения, которые обычно не вырабатываются в организме..
Многие соединения, полученные биотехнологией, ранее не существовали в природе..
Неорганические соединения
Соединение может считаться неорганическим, если оно не содержит в своем составе связи между углеродом и водородом, называемой в химическом цикле C-H. Кроме того, неорганические соединения, как правило, представляют собой минералы или соединения, основанные на геологии, которые не содержат углерод, связанный с молекулами водорода. Вот почему многие из неорганических соединений являются металлами.
Можно сказать, что соединение считается неорганическим, если оно соответствует одному из следующих критериев:
В настоящее время неорганические соединения также могут быть определены как любое соединение, которое не имеет органической природы..
По этой причине некоторые простые соединения, содержащие углерод, называются неорганическими. Некоторые из этих соединений включают монооксид углерода, диоксид углерода, бикарбонат натрия, карбиды, карбонаты и цианиды..
Многие из этих соединений являются нормальными частями многих в основном органических систем, в том числе организмов. Это означает, что химическое вещество может быть описано как неорганическое, но это не означает, что оно не присутствует в живых организмах..
Минералы в основном оксиды и сульфаты, которые являются строго неорганическими, хотя они имеют биологическое происхождение. На самом деле, большая часть планеты Земля неорганическая.
Хотя компоненты слоев Земли хорошо изучены, процесс минерализации и состав глубокого слоя остаются активными областями в исследованиях..
Правда заключается в том, что большинство соединений во вселенной неорганического характера. По этой причине неорганические соединения имеют большое применение и много практического применения в повседневной жизни. Поскольку многие из соединений в мире неорганические, эти соединения могут иметь много различных форм и могут иметь очень разные характеристики.
Например, поскольку многие металлы, они могут передавать электричество. Они также имеют тенденцию иметь высокие точки кипения, а также очень яркие и яркие цвета. Обычно они очень хорошо растворяются в воде, и многие из них обладают способностью образовывать кристаллы..
Органические и неорганические вещества
Органические и неорганические вещества или соединения.
Органические и неорганические вещества или соединения – это две большие химические группы, которые в основном отличаются наличием или отсутствием углеводородов и их производных.
Органические вещества:
Органические вещества включают в себя химические соединения с содержанием углерода и водорода. По составу их можно разделить на: углеводороды, кислородосодержащие и азотосодержащие вещества.
Органические вещества характеризуются в основном своей легкой плавкостью, ковалентной связью, соединениями (у которых похожий состав и молекулярная масса, но при этом разные физико-механические свойства), горючестью и явлением гомологии.
Органические соединения между собой отличаются строением углеродной цепи, и могут быть построены, как с открытой цепью атомов, так и с замкнутой. Те, что имеют строение с замкнутой цепью, относят к циклическим соединениям, которое подразделяются на предельные и непредельные, другие – к ациклическим, которые в свою очередь могут быть карбоциклическими и гетероциклическими.
Циклические соединения характеризуются кольцеобразной формой, при связи трех или более атомов. Ациклические соединения отличаются от циклических тем, что атомы углерода в них выстроены в прямые или разветвленные цепи.
Для того чтобы понять, к какому классу отнести то или иное органическое соединение, ориентируются на старшую функциональную группу – структурный фрагмент органической молекулы, который способствует определению химического состава данной молекулы.
В зависимости от типа функциональной группы они подразделяются на классы соединений: углеводороды, галогеноводороды, спирты, фенолы, простые эфиры, амины, нитросоединения, альдегиды, кетоны, карбоновые кислоты, сложные эфиры, амиды карбоновых кислот, тиолы и сульфоновые кислоты.
Неорганические вещества:
Неорганические вещества в основном в своем составе не имеют углеродного строения, как органические, но исключением являются вещества, содержащие углерод, которые традиционно относят к неорганическим: карбиды, карбонаты, некоторые оксиды углерода, цианиды и другие.
Неорганические вещества в большей своей массе характеризуются высокими температурами плавления, ионной связью, сложным разложением, отсутствием углеродного скелета и небольшой молекулярной массой.
Неорганические соединения делятся на простые вещества, которые в своем составе имеют атомы одного элемента и сложные вещества, состоящие из атомов двух или более элементов.
К группе простых веществ относятся: металлы, неметаллы, аморфные простые вещества и благородные газы. Кстати, периодическая таблица Менделеева позволяет быстро сориентироваться по веществам, относящимся к металлам и неметаллам.
Группа сложных веществ включает в себя: оксиды, гидроксиды, соли и бинарные соединения. Они в свою очередь имеют подразделение:
Химическая промышленность:
Отрасли химической промышленности могут в себя включать обработку, как органических, так и неорганических химических соединений.
Химическая промышленность в целом подразделяется на: горно-химическую промышленность, основную химию, химию органического синтеза, химико-фармацевтическую промышленность и бытовую химию.
В чем отличия между органическими веществами и неорганическими соединениями
В химии все соединения традиционно делят на 2 основных типа – органические и неорганические. Каждая из категорий отличается своей спецификой. Тем чем конкретно отличаются органические вещества от неорганических? Главная разница кроется в том, что в органических средствах всегда имеется углеродные компоненты. Причем, для неорганики это не характерно. Еще одной особенностью органики считается наличие углерод-водородных или СН-связей.
Что представляют собой органические вещества?
Такими элементами называют класс химических соединений, которые включают углерод. Исключением считаются карбиды, карбонаты, угольная кислота.
Для органики характерно следующее:
К распространенным элементам относятся белки, липиды, углеводы. В общей сложности современная химическая наука выделяет около 18 миллионов таких соединений. Исследователи считают, что такое разнообразие элементов связано с наличием углерода. Это вещество способно формировать очень широкий спектр связей с другими веществами.


Исключительно для органики характерна изомерия. Под этим термином понимают образование составов с одним и тем же набором атомов в молекулах, но разным их расположением. В результате формируются разные элементы с точки зрения химических и физических свойств.
Примеры соединений или молекул
Органикой называются молекулы, которые связаны с живыми организмами. К ним относятся жиры, нуклеиновые кислоты, белки, сахара. Также в эту группу входят ферменты и углеводородное топливо. Перечисленные молекулы включают углерод. Практически все они содержат водород. К тому же многие включают кислород.
К примерам таких составов стоит отнести следующее:
Соединения без связей CH
В отдельных органических составах нет углерод-водородных связей. В качестве примера стоит привести следующее:
Что представляют собой неорганические вещества?
Неорганические соединения представляют собой химические элементы, которые нельзя отнести к органике. Это означает, что они не включают углеродных компонентов. Для неорганики характерны следующие особенности:


Углерод и водород имеются далеко не во всех разновидностях неорганики. Не всегда такие составы характеризуются биологической природой. Неорганических элементов в современной химии существует намного меньше, чем органических, – около 100 тысяч. Для них не характерна изомерия.
Примеры неорганических соединений
В качестве примеров таких составов стоит привести металлы, соли и другие. При этом стоит отметить, что некоторые виды неорганики включают это вещество. В качестве примера таких соединений стоит привести следующее:
Почему углекислый газ не считается органическим соединением
Формирование углекислого газа носит естественный характер. Это вещество образуется вследствие процессов, которые нельзя считать органическими. Он выделяется из вулканов, минералов и прочих неживых объектов.
Чем отличаются
К главным отличиям относят следующее:


Сравнительная таблица
Главные особенности рассматриваемых понятий представлены в таблице:
| Органические составы | Неорганические элементы |
| Отличаются сравнительно сложной структурой. | Характеризуются относительно простым строением. |
| Характеризуются небольшой температурой плавления и разложения. | Плавятся и разлагаются при высоких температурах. |
| Отличаются значительной молекулярной массой. | Имеют небольшую массу. |
| Обычно включают углеродные компоненты и водород. | Могут не содержать водород и углерод в структуре молекул. |
| Обычно обладают природным происхождением. | Не всегда отличаются природным происхождением. |
Итоги
Рассматриваемые понятия характеризуются целым рядом отличий. Разница касается структуры, состава молекул, типа кристаллической решетки. Также вещества отличаются по распространенности на планете.